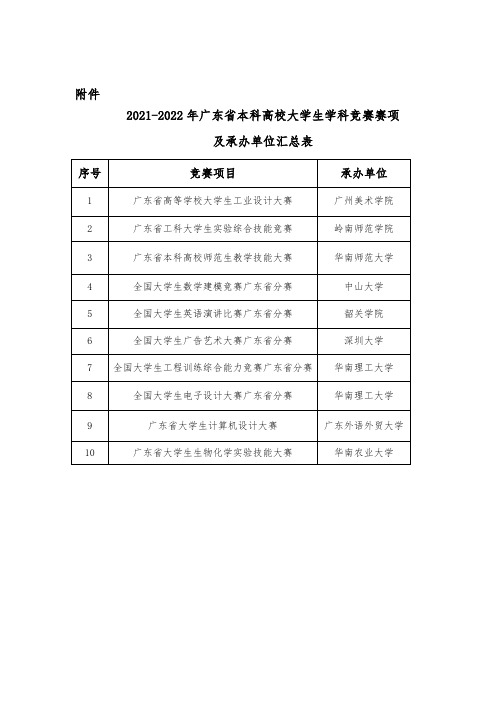
高中参考资料学科竞赛汇总表
- 格式:docx
- 大小:11.98 KB
- 文档页数:3

2024年中学高一年级学科竞赛活动方案一、活动背景与目的中学高一年级学科竞赛是一项旨在提高学生学科素养和综合能力的竞赛活动。
通过参与此次竞赛,学生将增强自主学习能力、合作意识和创新思维,为今后的学习和发展打下坚实的基础。
为此,我们制定了2024年学科竞赛活动方案。
二、活动时间和地点本次学科竞赛活动将于2024年5月中旬在学校举行。
各学科竞赛项目将在不同的时间分别进行,活动地点将在学校的教室、实验室和图书馆等地进行。
三、竞赛项目及内容1. 数学竞赛数学竞赛是本次学科竞赛的重要组成部分。
竞赛内容包括数学基础知识、问题求解和证明能力的考察。
参赛学生将通过开展一系列的数学知识竞赛、解题比赛等活动来展示自己的数学能力。
2. 语文竞赛语文竞赛旨在提高学生的语言表达能力和阅读理解能力。
竞赛内容包括语文知识点的考察、作文和阅读理解题目的解答。
参赛选手将在竞赛中展示自己的文字表达和阅读理解能力。
3. 英语竞赛英语竞赛是培养学生英语交流和应用能力的重要途径。
竞赛内容包括听力、口语、阅读和写作等方面的考察。
参赛选手将通过一系列的英语口语演讲、听力理解和写作比赛来展示自己的英语能力。
4. 物理竞赛物理竞赛旨在培养学生科学思维和实验操作能力。
竞赛内容包括物理知识的考察、实验设计和数据分析等。
参赛选手将通过一系列的物理实验、理论知识测试和实践能力考察来展示自己的物理学习成果。
5. 化学竞赛化学竞赛是培养学生实验技能和科学素养的重要途径。
竞赛内容包括化学知识的考察、实验设计和实验操作等。
参赛选手将通过一系列的化学实验、理论知识测试和实践能力考察来展示自己的化学学习成果。
6. 生物竞赛生物竞赛旨在培养学生生命科学的兴趣和实践能力。
竞赛内容包括生物知识的考察、实验设计和实验操作等。
参赛选手将通过一系列的生物实验、理论知识测试和实践能力考察来展示自己的生物学习成果。
四、竞赛形式和规则1. 各学科竞赛项目将采取笔试、实验、口试等多种形式进行。

高中生可能的专长及奖项:
1.学术类:数学、物理、化学、生物、信息学等奥赛及全国性学科竞赛,
以及科技创新大赛、机器人竞赛等。
2.艺术类:音乐、舞蹈、美术等比赛,如“青少年音乐大赛”、“青少年
舞蹈大赛”、“青少年美术大赛”等。
3.体育类:田径、乒乓球、羽毛球等比赛,如“全国青少年田径锦标赛”、
“全国青少年乒乓球锦标赛”、“全国青少年羽毛球锦标赛”等。
此外,还有一些非竞赛类奖项,如三好学生、优秀学生干部、优秀共青团员等荣誉称号。
需要注意的是,这些专长和奖项并不是绝对的,每个学生的情况都不同。
同时,这些奖项和荣誉也并不代表一个人的全部价值和能力,更重要的还是看一个人的综合素质和品德修养。

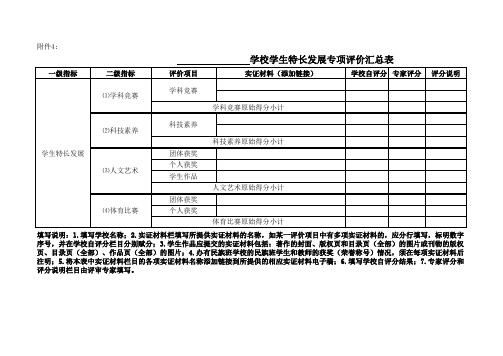
附件4:
学校学生特长发展专项评价汇总表
填写说明:1.填写学校名称;2.实证材料栏填写所提供实证材料的名称,如某一评价项目中有多项实证材料的,应分行填写,标明数字序号,并在学校自评分栏目分别赋分;3.学生作品应提交的实证材料包括:著作的封面、版权页和目录页(全部)的图片或刊物的版权页、目录页(全部)、作品页(全部)的图片;4.办有民族班学校的民族班学生和教师的获奖(荣誉称号)情况,须在每项实证材料后注明;5.将本表中实证材料栏目的各项实证材料名称添加链接到所提供的相应实证材料电子稿;6.填写学校自评分结果;7.专家评分和评分说明栏目由评审专家填写。

大学生可以参加的竞赛文案大全文案大全文案大全注:加黑赛事为教育部资助的九大赛事,上面共有八个,还有一个是全国大学生英语竞赛。
文案大全文案大全重庆大学大学生课外科技创新实践活动一览表文案大全文案大全注:1 含(*)赛事为教育部资助的九大赛事,上面共有 6个,还有“挑战杯”大学生课外学术科技作品竞赛、中国MEMS传感器应用大赛、全国大学生物流设计大赛。
2 加黑赛事为在机械学子关注较多、有广泛参与度的比赛。
重点项目竞赛的介绍及获奖情况主要分为三类,一.实践类1.国家大学生创新训练项目该项目隶属于国家大学生创新创业训练计划(原名“国家大学生创新性实验计划”)。
国家大学生创新训练项目是教育部为推动创新性人才培养工作的一项重要举措,是国家直接面向大学生组织开展的自主性、探索性、过程性、协作性和学科性的创新训练项目。
该计划项目的开展旨在探索并建立以问题和课题为核心的教学模式,倡导以本科学生为主体的创新性实验教学改革,调动学生的主动性、积极性和创造性,激发学生的创新思维和创新意识,掌握分析问题、解决问题的方法,培养学生从事科学研究和创造发明的素质,提高其创新实践的能力。
文案大全学生以个人或团队形式开展项目申请,每队人数最多不超过3人。
项目申报对象主要为学习成绩优良(或个别有特长)、学有余力、项目开展期间为2、3年级(五年制本科为2-4年级)的在校本科学生,申报项目的学生必须符合以下条件之一:(1)、弘深学院学生;(2)、课程成绩平均分值≥ 70 ,平均学年重修课程数不得多于 1 门,学有余力的学生;(3)、不满足1、2条中任何一条,但个别有特长的学生,经审查批准后可参加申报。
目前我校已连续开展六届,立项项目近400项,参与学生1100余人。
2.大学生科研训练计划“重庆大学大学生科研训练计划”( students research training program ,简称 SRTP ),是学校面向全校本科生开展的一项创新教育计划,是学校创新体系的重要组成部分。
高中竞赛奖项设置
一、学术类奖项
1. 卓越成就奖 - 颁发给在学术领域展现出杰出成就的学生,包括但不限于科研项目、作品创作、学术竞赛等。
2. 学科之星奖 - 颁发给在特定学科领域表现卓越的学生,包括但不限于数学、物理、化学、生物、语言学等。
3. 创新实践奖 - 颁发给在各类实验、发明创造、社会实践等方面展现出创新精神和
实践能力的学生。
二、艺术类奖项
1. 优秀艺术家奖 - 颁发给在音乐、舞蹈、戏剧、美术等艺术领域表现卓越的学生。
2. 创意设计奖 - 颁发给在平面设计、产品设计、时尚设计等方面展现出创造力和设
计才能的学生。
3. 摄影风景奖 - 颁发给在摄影作品中展现出独特视角和出色技巧的学生。
三、体育类奖项
1. 优秀运动员奖 - 颁发给在各类体育项目中展现出卓越运动技能和体育精神的学
生。
2. 球类冠军奖 - 颁发给在足球、篮球、排球等球类运动项目中获得冠军的学生。
3. 田径冠军奖 - 颁发给在田径、跳高、跳远、短跑等项目中获得冠军的学生。
四、团队合作类奖项
1. 协作达人奖 - 颁发给在团队合作中表现出良好领导能力和团结协作精神的学生。
2. 创业创意奖 - 颁发给在团队创业、社团活动及各类团队项目中展现出创新思维和
实践能力的学生。
五、社会公益类奖项
1. 公益先锋奖 - 颁发给在社会公益项目中表现出出色贡献和影响力的学生。
2. 社区服务奖 - 颁发给在社区服务、志愿者工作等方面展现出卓越贡献和责任感的
学生。
请注意:以上为示例奖项,具体设置和命名应根据实际情况进行调整和创新。
1
高中竞赛汇总表
数学类: 全国高中数学联赛
中国数学奥林匹克
(CMO)
国际数学奥林匹克 (IMO)
物理类:
全国中学生物理竞赛
(CPHO)
国际物理学奥林匹克 竞赛 (IPHO) 亚洲物理学奥林匹克 竞赛
(APHO)
化学类:
全国高中化学竞赛
(CCHO)
国际奥林匹克化学 竞赛
(ICHO)
生物类:
全国生物学联赛 和竞
赛
全国生物学联赛
(CNBO)
国际生物学奥林匹克 竞赛
(IBO)
信息学:
全国青少年信息学 奥
林匹克竞赛
全国青少年信息学
奥林匹克联赛 (NOIP)
亚洲与太平洋地区信息学
奥赛 (APIO)
国际信息学奥林匹克
竞赛 (IOI)
全国高中 数学
联赛
自 2010 年起,全国高中数学联赛 试题 新规则如下 : 联赛分为一试、加试
(即俗称的 “二试 ”)。一试和加试均在每年 10 月 中旬的第一个周日举行。
·一试考试时间为上午 8 :00-9 :20 ,共 80 分钟。 试题分填空题和解答题
两部分, 满分 120 分。其中填空题 8 道,每题 8 分;解答题 3 道,分别为 16
分、 20 分、 20 分。
·加试(二试)考试时间为 9 : 40-12 :10 ,共 150 分钟。 试题为四道解答
题,前两道每题 40 分,后两道每题 50 分,满分 180 分。试题内容涵盖平面几何
代数、数论、组合数学等。
中国数学 奥林
匹克 (CMO)
全国中学生数学冬令营是在全国高中数学联赛的基础上进行的一次较高 层次的
数学竞赛。 1985 年,由北京大学、南开大学、复旦大学和中国科技 大学四所大
学倡议,中国数学会决定,自 1986 年起每年一月份举行全国 中学生数学冬令
营,后又名中国数学奥林匹克( Chinese Mathematical?
Olympiad ,简称 CMO )。
国际数学 奥林
匹克 (IMO)
中国数学奥林匹克( CMO ):省一和国家一二三等奖有保送高校资格。省 二有自
主招生资格,通过自主招生后自动保送。
其它数学类 竞
赛介绍
女子
奥数
迄今为止,有两名女同学(陈卓、张 敏)
通过该竞赛入选国际数学奥林匹 克,并
夺得金牌。通常每队至多有四 名参赛选
手,两名领队,领队中至少 有一名女教
师。
西部
奥数
2009 年第 51 届国际数学奥林匹克金 牌
选手黄骄阳就是通过中国西部数学 奥林
匹克的选拔进入国家集训队的。
东南
奥数
参赛者为高一学生。参赛队伍主要是 来
自闽浙赣三省中学的代表队,也有 上
海、广东、香港等地的代表队。每 队由
4 名高一学生组成。
美国
奥数
学生需要通过美国数学竞赛
(AMC )和美国数学邀请赛( AIME )
2
的两层选拔,最终可以进入美国数学
奥林匹克( USAMO )的角逐。
俄罗斯 奥数
俄罗斯数学奥林匹克的特点是分 年级进
行。 高年级的优胜者可被免试 推荐进入
大学。现在,俄罗斯的数学 短期活动已
发展到包括小学生,中学 生和大学生在
内的各级各类数学奥林 匹克。
全国中学生 物
理竞赛
(CPHO)
预赛、复赛、决赛:笔试 + 实验 =140 分 +60 分。各考 3 小时。 预赛由全
国竞赛委员会统一命题, 采取笔试的形式, 所有在校的中学生都可 以报名参
加。全国奖取消保送资格,只有全国一等奖可以拥有保送资格。
亚洲物理学 奥
林匹克竞赛
(APHO)
组织国际性中学生物理竞赛, 宣传物理学科的重要性。 推动亚洲各国在 物理
学教育方面的交流与合作。 增进亚洲各国青少年间的联系与理解,激 励有才华的
青少年脱颖而出。
国际物理学 奥
林匹克竞赛
(IPHO)
IPhO 每年在不同的国家举行,已发展成为世界上最大的学科竞赛之一。 当今世界
上颇具有影响的青年智力大赛之一。 参赛国也由最的五个国家发 展到有 40 多个
国家参加,影响遍及世界五大洲。
全国高中
化学 竞赛
(CCHO)
参
参
加全国高中学生化学竞赛初赛的选手为普通高中学生。 年龄在来年国际竞赛 前小
于 20 岁。决赛选手名额为每个省、市、自治区 5 名。
加全国高中学生化学竞赛 ( 省级赛区 )获一等奖的学生不超过总人数的 1% , 可获
得大学保送生资格。
国际奥林
匹克
化学竞赛
(ICHO)
竞赛
一
参
共两天,理论部分 4 ~ 5 小时,隔一天后再进行实验部分竞赛,约 4 小时。 赛
者最高分 100 分,理论部分 60 分,实验部分 40 分。根据所得分数,通 常有
3 ~5 个一等奖,较多的二等奖和三等奖。
全国生物学
联赛和竞赛
全国生物学联赛、全国生物学竞赛目的是为加强中学生物学教学,提高 生物学
教学水平 ; 促进中学生生物学课外活动。
全国生物学 联
赛 (CNBO)
全国生物学竞赛一等奖获得者可参加全国中学生生物学冬令营,人数限 制在
18 人,第十八名总成绩若出现并列,以实验分高者为先。
国际生物学 奥
林匹克竞赛
(IBO)
国际生物学奥林匹克竞赛是针对中学生的竞赛。竞赛测试他们解决生物
问题,进行生物实验的能力。 除了对生物学感兴趣, 创造性, 创新性和毅力。
全国青少年 信
息学奥林匹 克
竞赛 (NOI)
全国青少年信息学奥林匹克竞赛 (NOI) 是国内包括港澳在内的省级代表 队最高水
平的大赛,自 1984 年至今,在国内包括香港、澳门组织竞赛活 动。每年经各省
选拔产生 5 名选手。
全国青少年 信
息学奥林匹 克
联赛 (NOIP)
国际生物学奥林匹克竞赛是针对中学生的竞赛。竞赛测试他们解决生物
问题,进行生物实验的能力。 除了对生物学感兴趣, 创造性, 创新性和毅力。
亚洲与太平洋
地区信息学奥
赛(APIO)
该竞赛为区域性的网上准同步赛,是亚洲和太平洋地区每年一次的国际 性赛
事,旨在给青少年提供更多的赛事机会,推动亚太地区的信息学。
3
国际信息学 奥
林匹克竞赛
(IOI)
由中国计算机学会组织代表队,代表中国参加国际每年一次的 IOI 。中 国是 IOI
创始国之一。 IOI2000 由中国主办, CCF 承办。