博纳吐单抗中文说明书
- 格式:doc
- 大小:27.50 KB
- 文档页数:6


核准日期:2021年1月5日修改日期:布罗索尤单抗注射液说明书本品为附条件批准上市,请仔细阅读说明书并在医师指导下使用。
【药品名称】通用名称:布罗索尤单抗注射液商品名称:麟平,Crysvita英文名称:Burosumab Injection汉语拼音:Buluosuoyou Dankang Zhusheye【成份】主要成份:布罗索尤单抗布罗索尤单抗系采用中国仓鼠卵巢细胞(CHO)表达制备的全人源抗成纤维细胞生长因子23(FGF23)单克隆抗体(IgG1)。
辅料:L-组氨酸、D-山梨醇、聚山梨酯80、L-蛋氨酸、盐酸10%、注射用水。
【性状】本品为澄清至浅乳白色以及无色至浅棕黄色溶液。
【适应症】用于成人和1岁及以上儿童患者的X连锁低磷血症(XLH)。
用于成人无法根治性切除或定位的磷酸盐尿性间充质肿瘤相关的肿瘤性骨软化症(TIO)中的FGF23相关性低磷血症。
【规格】西林瓶装:10mg(1ml)/瓶、20 mg(1ml)/瓶、30 mg(1ml)/瓶。
【用法用量】本品皮下注射,应由医务人员操作。
在开始本品治疗前1周应停用口服磷酸盐和活性维生素D类似物。
开始治疗前,空腹血磷浓度应低于各年龄段的参考值下限。
不应在本品治疗期间给予口服磷酸盐和活性维生素D类似物。
皮下注射给药一般注意事项应轮换注射部位(上臂、大腿上部、臀部或腹部的任何部位),每次在与前一次注射不同的解剖部位注射给药。
请勿在痣、疤痕或脆弱、瘀血、发红、硬皮或不完整的皮肤区域注射给药。
每次注射的最大容积为1.5 ml。
若需要多次注射,应在不同注射部位进行注射。
在给药之前,应目测检查本品中是否存在颗粒物质以及出现变色的情况。
本品是一种皮下注射用无菌、不含防腐剂、澄清至浅乳白色以及无色至浅棕黄色溶液。
如果溶液变色或混浊或溶液中含有任何颗粒或异物,请勿使用。
XLH儿童患者(1岁至18岁以下)推荐的起始剂量方案是0.8 mg/kg,四舍五入至最接近的10 mg,每2周一次。

纳武利尤单抗注射液Nivolumab 英文名:Nivolumab Injection汉语拼音:Na Wu Li You Dan Kang Zhu She Ye【成份】活性成份:纳武利尤单抗(Nivolumab),一种针对程序性死亡1(PD-1)受体的人源化单克隆抗体(IgG4亚型)。
辅料:枸橼酸钠二水合物、氯化钠、甘露醇、喷替酸、聚山梨酯80、盐酸、氢氧化钠、注射用水。
【性状】澄清至乳光,无色至淡黄色液体,可能存在少量(极少)颗粒。
【适应症】非小细胞肺癌(NSCLC):本品单药适用于治疗表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性、既往接受过含铂方案化疗后疾病进展或不可耐受的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。
颈部鳞状细胞癌(SCCHN):适用于治疗接受含铂类方案治疗期间或之后出现疾病进展且肿瘤PD-L1表达阳性(表达PD-L1的肿瘤细胞≥1%)的复发性或转移性头颈部鱗癌患者。
胃腺癌和胃食道连接部腺癌:用于接受过两种或两种以上全身治疗方案后的晚期或复发性胃腺癌和胃食道连接部腺癌。
【规格】40 mg/4ml(10 mg/ml)。
100 mg/10 ml(10 mg/ml)。
【用法用量】患者选择:头颈部鳞状细胞癌患者使用本品前,必须获得经充分验证的检测方法证实的PD-L1阳性评估结果。
推荐剂量:本品推荐剂量为3mg/kg或240mg固定剂量,静脉注射每2周一次,直至出现疾病进展或产生不可接受的毒性。
推荐剂量和输注时间视适应症而定,如表1所示。
表1:本品单药治疗的推荐剂量和输注时间只要观察到临床获益,应继续本品治疗,直至患者不能耐受。
有可能观察到非典型反应(例如最初几个月内肿瘤暂时增大或出现新的小病灶,随后肿瘤缩小)。
如果患者临床症状稳定或持续减轻,即使有疾病进展的初步证据,基于总体临床获益的判断,可考虑继续应用本品治疗,直至证实疾病进展。
根据个体患者的安全性和耐受性,可能需要暂停给药或停药。

一文搞懂不同等级致吐风险药物及止吐方案原创:热那恶心、呕吐是肿瘤药物治疗的常见不良反应。
严重的恶心、呕吐还可能导致脱水、电解质紊乱、自理能力下降、功能性活动受限、营养缺乏、焦虑、体力状况评分降低、伤口裂开、食管黏膜撕裂、治疗耐受性降低等严重后果,因此肿瘤药物治疗所致恶心呕吐的预防及治疗及其重要。
目前肿瘤药物治疗所致恶心呕吐的治疗中,预防为主,注重全程与个体化管理止吐治疗应先于抗肿瘤治疗,根据拟行抗肿瘤治疗方案的致吐风险、患者自身的高危因素、既往发生恶心呕吐的严重程度,制订个体化的防治方案。
化疗药物诱导的呕吐反应的发生率主要与所使用化疗药物的致吐性相关。
临床普遍采用的是4分级法,该分级将化疗药物按照未进行预防处理时发生急性呕吐的风险比率分为高度、中度、低度和轻微4个致吐风险等级,分别对应的急性呕吐发生率为>90%、30%~90%、10%~30%和<10%。
高度致吐风险静脉药物(呕吐发生率>90%):卡铂AUC≥4卡莫司汀>250mg/m2顺铂环磷酰胺≥ 1.5g/m2达卡巴嗪多柔比星≥60mg/m2表柔比星>90mg/m2异环磷酰胺≥2g/m2(每剂)氮芥链脲菌素中度致吐风险静脉药物(呕吐发生率30%~90%):白介素-2>12~15MIU/m2氨磷汀>300mg/m2三氧化二砷阿扎胞苷苯达莫司汀白消安卡铂AUC<4卡莫司汀≤250mg/m2氯法拉滨(Clofarbine)环磷酰胺≤1.5g/m2阿糖胞苷>200mg/m2放线菌素D 柔红霉素恩杂鲁胺(Enzalutamide)多柔比星<60mg/m2表柔比星≤90mg/m2伊达比星异环磷酰胺<2g/m2(每剂)干扰素α≥10MIU/m2伊立替康洛铂美法仑甲氨蝶呤≥250mg/m2奈达铂奥沙利铂替莫唑胺曲贝替定(Trabectedin)低度致吐风险静脉药物(呕吐发生率10%~30%):Ado-曲妥珠单抗白介素-2≤12MIU/m2氨磷汀≤300mg/m2阿糖胞苷100~200mg/m2干扰素α5~10MIU/m2甲氨蝶呤50~250mg/m2伊立替康(脂质体)多柔比星脂质体阿特珠单抗贝利司他博纳吐单抗本妥昔单抗卡巴他赛卡非佐米多西他赛艾立布林依托泊苷5-氟尿嘧啶氟脲苷吉西他滨伊沙匹隆丝裂霉素米托蒽醌耐昔妥珠单抗高三尖杉酯碱紫杉醇紫杉醇培美曲塞喷司他丁普拉曲沙雷替曲塞罗米地辛溶瘤病毒T-Vec塞替派托泊替康阿柏西普轻微致吐风险静脉药物(呕吐发生率<10%)阿糖胞苷<100mg/m2干扰素α≤5MIU/m2甲氨蝶呤≤50mg/m2奥滨尤妥珠单抗聚乙二醇干扰素阿伦单抗门冬酰胺酶贝伐珠单抗博来霉素硼替佐米西妥昔单抗克拉屈滨达雷妥尤单抗地西他滨地尼白介素右丙亚胺埃罗妥珠单抗氟达拉滨伊匹木单抗奈拉滨奥法木单抗纳武利尤单抗帕尼单抗培门冬酶帕博利珠单抗帕妥珠单抗雷莫芦单抗利妥昔单抗司妥昔单抗信迪利单抗特瑞普利单抗替西罗莫司曲妥珠单抗戊柔比星卡瑞利珠单抗长春花类药物中-高度致吐风险口服药物(致吐风险≥30%)六甲蜜胺白消安≥4mg/d 塞瑞替尼克唑替尼环磷酰胺≥100mg/(m2•d)雌莫司汀依托泊苷仑伐替尼洛莫司汀(单日)米托坦奥拉帕利帕比司他丙卡巴肼瑞卡帕布替莫唑胺>75mg/m2曲氟尿苷替匹嘧啶低度-轻微致吐风险口服药物(致吐风险<30%)阿法替尼阿来替尼安罗替尼阿帕替尼阿昔替尼贝沙罗汀博舒替尼白消安<4mg/d 卡博替尼卡培他滨西达本胺苯丁酸氮芥考比替尼环磷酰胺<100mg/(m2•d)达沙替尼达拉非尼厄洛替尼依维莫司氟达拉滨呋喹替尼吉非替尼羟基脲伊布替尼埃克替尼艾代拉里斯伊马替尼伊沙佐米拉帕替尼来那度胺美法仑巯嘌呤甲氨蝶呤尼洛替尼奥希替尼哌柏西利培唑帕尼泊马度胺帕纳替尼吡咯替尼瑞戈非尼芦可替尼索尼德吉索拉非尼舒尼替尼替吉奥替莫唑胺≤75mg/(m2•d)硫鸟嘌呤托泊替康曲美替尼维A酸凡德他尼维莫非尼维奈托克维莫德吉伏立诺他静脉药物致恶心呕吐的预防高致吐性方案所致恶心呕吐的预防:(1)化疗前采用三药联合方案,首选5-HT3受体拮抗剂、地塞米松和NK-1受体拮抗剂的联用方案。

注射用伊尼妥单抗说明书警告:心脏毒性:抗HER2单抗药物会导致亚临床和临床心力衰竭,其发生率和严重程度在合并蒽环类抗生素治疗的患者中最高。
在给予本品治疗前以及治疗过程中需对左心室功能进行评估。
在临床显著的左心室功能下降的转移性乳腺癌患者中,应停用本品。
输注相关反应及肺部反应:抗HER2单抗药物会导致严重的并可能致命的输注相关反应和肺部反应。
症状多发生于其输注过程中或24小时内。
对于发生呼吸困难或临床显著的低血压患者,应当立即停止输注本品,并对患者进行监控直至症状完全消失。
发生过敏、血管性水肿、间质性肺炎或者急性呼吸窘迫综合征的患者应停止输注。
胚胎毒性:孕期使用抗HER2单抗药物会导致羊水过少并继发造成胎儿肺发育不全、骨骼异常和新生儿死亡。
药品名称:通用名称:注射用伊尼妥单抗英文名称:Inetetamab for Injection商品名称:赛普汀成份:活性成份为伊尼妥单抗,是重组抗人表皮生长因子受体-2人源化单克隆抗体,由悬浮培养于无菌培养基中的哺乳动物细胞(中国仓鼠卵巢细胞CHO)生产,为IgG1/k型免疫球蛋白分子。
辅料:盐酸组氨酸、组氨酸、蔗糖、聚山梨酯20。
适应症:本品适用于HER2阳性的转移性乳腺癌:与长春瑞滨联合治疗已接受过1个或多个化疗方案的转移性乳腺癌患者。
用法用量:HER2检测在使用本品治疗前,应进行HER2状态的检测。
免疫组化(IHC)检测显示阳性(+++)或免疫组化检测显示可疑阳性(++)同时荧光原位杂交(FISH)检测结果阳性的患者可以使用本品。
推荐剂量和给药方法伊尼妥单抗的推荐初始负荷剂量为4mg/kg,静脉滴注90分钟以上;维持剂量为2mg/kg,每周1次,如果在首次滴注时患者耐受性良好,后续滴注可改为30分钟。
严禁静脉推注或快速静脉注射。
长春瑞滨的推荐剂量为25 mg/m2,第1,8,15天静脉滴注,在伊尼妥单抗输注后当天应用,每28天为1个周期。
有关长春瑞滨用药的详细信息,请参见长春瑞滨的药品说明书。


美珀株单抗说明书
美珀株单抗(Mepolizumab)是一种用于治疗特发性嗜酸性粒细胞性
鼻炎、嗜酸性粒细胞性支气管炎和嗜酸性粒细胞增多症(EGPA)的生物制剂。
它属于IgG1k(kappa)类单克隆抗体,是靶向IL-5受体α亚单位
的抗体。
美珀株单抗在人体内通过结合IL-5受体α亚单位来阻断IL-5的信
号通路。
IL-5是一种调节嗜酸性粒细胞增殖和活化的细胞因子,而嗜酸
性粒细胞是引起特发性嗜酸性粒细胞性鼻炎、嗜酸性粒细胞性支气管炎和
嗜酸性粒细胞增多症症状的主要细胞类型。
治疗前需要对患者进行过敏史评估和嗜酸性粒细胞水平的检测,以确
定是否符合使用该药物的适应症。
此外,患者还需要定期进行嗜酸性粒细
胞计数的监测和相关疗效的评估。
美珀株单抗的主要不良反应包括头痛、注射部位反应(如红肿、疼痛、瘙痒等)、口咽部炎症、气道感染等,一般都是轻度或中度的不良事件。
少数患者可能出现过敏反应,如荨麻疹、血管神经性水肿、喉头水肿等严
重不良事件,需要立即停药并采取适当处理措施。
美珀株单抗是一种新型的靶向嗜酸性粒细胞的生物制剂,对特发性嗜
酸性粒细胞性鼻炎、嗜酸性粒细胞性支气管炎和嗜酸性粒细胞增多症的治
疗具有重要意义。
然而,由于该药物的局限性和患者个体差异,使用前还
需权衡利弊,确保在适当的病例中合理使用,以取得最佳的疗效。
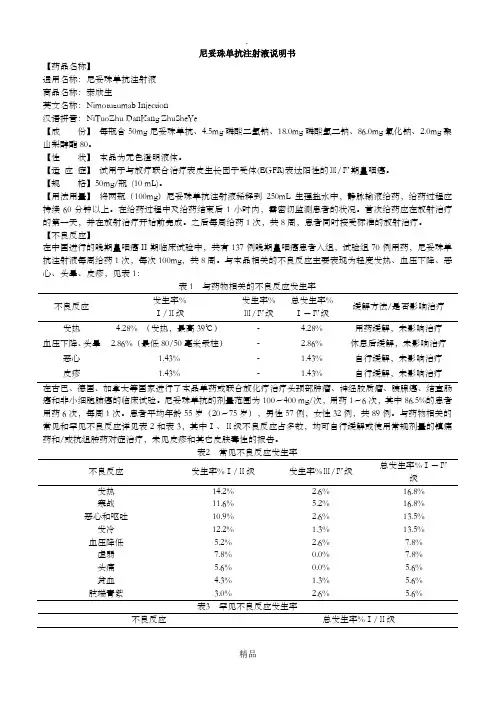
尼妥珠单抗注射液说明书【药品名称】通用名称:尼妥珠单抗注射液商品名称:泰欣生英文名称:Nimotuzumab Injection汉语拼音:NiTuoZhu DanKang ZhuSheYe【成份】每瓶含50mg尼妥珠单抗、4.5mg磷酸二氢钠、18.0mg磷酸氢二钠、86.0mg氯化钠、2.0mg聚山梨醇酯80。
【性状】本品为无色澄明液体。
【适应症】试用于与放疗联合治疗表皮生长因子受体(EGFR)表达阳性的Ⅲ/Ⅳ期鼻咽癌。
【规格】50mg/瓶(10 mL)。
【用法用量】将两瓶(100mg)尼妥珠单抗注射液稀释到250mL生理盐水中,静脉输液给药,给药过程应持续60分钟以上。
在给药过程中及给药结束后1小时内,需密切监测患者的状况。
首次给药应在放射治疗的第一天,并在放射治疗开始前完成。
之后每周给药1次,共8周,患者同时接受标准的放射治疗。
【不良反应】在中国进行的晚期鼻咽癌II期临床试验中,共有137例晚期鼻咽癌患者入组,试验组70例用药,尼妥珠单抗注射液每周给药1次,每次100mg,共8周。
与本品相关的不良反应主要表现为轻度发热、血压下降、恶心、头晕、皮疹,见表1:表1 与药物相关的不良反应发生率不良反应发生率%Ⅰ/Ⅱ级发生率%Ⅲ/Ⅳ级总发生率%Ⅰ-Ⅳ级缓解方法/是否影响治疗发热 4.28% (发热,最高39℃)- 4.28%用药缓解,未影响治疗血压下降、头晕 2.86%(最低80/50毫米汞柱)- 2.86%休息后缓解,未影响治疗恶心 1.43%- 1.43%自行缓解,未影响治疗皮疹 1.43%- 1.43%自行缓解,未影响治疗在古巴、德国、加拿大等国家进行了本品单药或联合放化疗治疗头颈部肿瘤、神经胶质瘤、胰腺癌、结直肠癌和非小细胞肺癌的临床试验。
尼妥珠单抗的剂量范围为100~400 mg/次,用药1~6次,其中86.5%的患者用药6次,每周1次。
患者平均年龄55岁(20~75岁),男性57例,女性32例,共89例。

贝伐珠单抗注射液说明书贝伐单抗注射说明请仔细阅读说明书,并在医生的指导下使用。
警告:胃肠穿孔使用贝伐单抗时可能会发生胃肠道穿孔,其发生率为0 .3 ~2 .4%,有时甚至会导致死亡。
在应用贝伐单抗期间,如果患者有腹痛,鉴别诊断时应考虑胃肠道穿孔的可能性。
对于胃肠道穿孔患者,贝伐单抗应永久停用。
(参见注意事项:胃肠穿孔和不良反应:胃肠穿孑L)手术并发症和伤口愈合使用贝伐单抗可能会增加伤口愈合和手术并发症(包括严重和致命的)的机会。
出现伤口愈合并发症的患者应暂停使用贝伐单抗,直到伤口完全愈合。
贝伐单抗治疗预计在择期手术期间暂停。
为了避免影响伤口愈合/伤口裂开的风险,贝伐单抗治疗停止和择期手术之间最合适的间隔时间尚未确定。
手术前至少停药28天。
贝伐单抗在手术后至少28 天内不能使用,直到伤口完全痊愈。
(参见注意事项:伤口愈合并发症)出血接受联合贝伐单抗化疗的患者发生严重岀血或致命性出血的可能性最多为5倍,包/S咯血' 胃肠出血' 中枢神经系统(CNS)出血' 鼻出血和阴道出血。
严重出血或近期咯血(曰/2茶匙血液)的患者不应接受贝伐单抗治疗。
对于NCI-CTC 3级或4级出血的患者,治疗期间应永久停用贝伐单抗。
(参见注意事项:出血和不良反应:岀血)[药品名称]常用名称:贝伐单抗注射液商品名称:阿瓦斯丁,阿瓦斯丁中文名称:贝伐单抗注射液汉语拼音:北发珠丹康珠蛇液[构图]活性成分:贝伐单抗(人源化抗血管内皮生长因子单克隆抗体)贝伐单抗有100毫克和400毫克规格,相应的体积分别为4毫升和16毫升(25毫克/毫升)。
贝伐单抗不含防腐剂,包装在一次性小瓶中。
本产品辅料组成如下:(x, (X-二竣甲糖,一水磷酸二氢钠,无水磷酸氢二钠,吐温20,注射用无菌水。
[性格]本品为静脉注射用无菌溶液,pH 5.9 ~ 6. 3,无色至微棕色乳白色光至透明液体。
[指示]转移性结直肠癌贝伐单抗联合基于5-氟尿喘唳的化疗适用于转移性结直肠癌患者的治疗。

帕博利珠单抗注射液通用名称:帕博利珠单抗注射液商品名称:可瑞达Keytruda英文名称:PembrolizumabInjection汉语拼音:PabolizhuAnkangZhusheye成份活性成份:帕博利珠单抗辅料:L-组氨酸,蔗糖,聚山梨酯80,注射用水性状应为液体,基本不含可见颗粒。
适应症博利珠单抗适用于经一线治疗失败的不可切除或转移性黑色素瘤的治疗。
该适应症在中国是基于一项单臂临床试验的客观缓解率结果给予的有条件批准。
本适应症的完全批准将取决于正在计划开展中的确证性临床试验能否证实中国患者的长期临床获益。
规格100mg/4ml用法用量本品须在有肿瘤治疗经验医生的指导下用药。
推荐剂量:帕博利珠单抗的推荐给药方案为2mg/kg剂量静脉输注30分钟以上,每3周给药一次,直至出现疾病进展或不可接受的毒性。
已观察到接受帕博利珠单抗治疗肿瘤的非典型反应(例如,治疗最初几个月内肿瘤出现暂时增大或出现新的小病灶,随后肿瘤缩小)。
如果患者临床症状稳定,即使有疾病进展的初步证据,但基于总体临床获益的判断,可考虑继续应用本品治疗,直至证实疾病进展。
根据个体患者的安全性和耐受性,可能需要暂停给药或停药。
不建议増加或减少剂量。
有关永久停药或暂停给药的指南,请见表1所述。
有关免疫相关性不良反应管理的详细指南,请参见[注意事项]。
既往出现过免相关性心肌炎的患者重新开始帕博利珠单抗的安全性尚不明确。
除非表1中另有规定,否则对于4级或3级复发性不良反应,帕博利珠单抗应永久停药。
特殊人群帕博利珠单抗在儿童人群(<18岁)中的安全性和有效性尚不明确。
无相关数据。
老年人群老年(≥65岁)与年轻患者(<65岁)在安全性或有效性上未出现总体的差异。
无需在这一人群中进行剂量调整。
肾功能不全轻度或中度督功能不全患者无需判量调整。
帕博利珠单抗尚未在重度肾功能不全患者中进行研究(参见[注意事项]和[药代动力学])。
肝功能不全轻度肝功能受损患者无需剂量调整。

利妥昔单抗说明书【商品名称】美罗华【拼音名】Lituoxidankang Zhusheye【英文名】Rituximab Injection【成份】主要组成成份:本品主要活性成分为重组利妥昔单抗,组成成分还包括枸橼酸钠,聚山梨醇酯80,氯化钠和注射用水。
【性状】为无色或淡黄色澄明液体,无异物、絮状物及沉淀。
【适应症】本品适用于:复发或耐药的滤泡性中央型淋巴瘤(国际工作分类B、C和D亚型的B细胞非霍奇金淋巴瘤)的治疗。
CD20阳性弥漫大B细胞性非霍奇金淋巴瘤(DLBCL)应与标准CHOP化疗(环磷酰胺、阿霉素、长春新碱、强的松)8个周期联合治疗。
【用法用量】在无菌条件下抽取所需剂量的利妥昔单抗,置于无菌无致热源的含0.9%生理盐水或5%葡萄糖溶液的输液袋中,稀释到利妥昔单抗的浓度为1mg/ml。
轻柔的颠倒注射袋使溶液混合并避免产生泡沫。
由于本品不含抗微生物的防腐剂或抑菌制剂,必须检查无菌技术。
静脉使用前应观察注射液有无微粒或变色。
利妥昔单抗稀释后通过一种专用输液管静脉滴注,适用于不卧床患者的治疗。
利妥昔单抗的治疗应在具有完备复苏设备的病区内进行,并在有经验的肿瘤医师或血液科医师的直接监督下进行。
对出现呼吸系统症状或低血压的患者至少监护24小时。
每次滴注利妥昔单抗前应预先使用止痛剂(例如扑热息痛)和抗组胺药(例如苯海拉明)(开始滴注前30到60分钟)。
如果所使用的治疗方案不包括皮质激素,那么还应该预先使用皮质激素。
每名患者均应被严密监护,监测是否发生细胞因子释放综合征。
对出现严重反应的患者,特别是有严重呼吸困难,支气管痉挛和低氧血症的患者应立即停止滴注。
还应该评估患者是否出现肿瘤溶解综合征,例如可以进行适当的实验室检查。
预先存在肺功能不全或肿瘤肺浸润的患者必须进行胸部X线检查。
所有的症状消失和实验室检查恢复正常后才能继续滴注,此时滴注速度不能超过原滴注速度的一半。
如再次发生相同的严重不良反应,应考虑停药。
【药物名】Blinatumomab 【商品名】Blincyto 【中文名】博纳吐单抗 【美国上市时间】12月3日,2014 【类别】蛋白质 【靶点】CD19、CD3 【分子结构】 分子量为:54KDA 【生产公司】Amgen Inc. 安进公司 【剂型和规格】 注射用:一次性用的小瓶盛装35微克的干冻粉。 【本质】 BLINCYTO由504个氨基酸组成。每个BLINCYTO药包包括一瓶BLINCYTO和一瓶IV溶液稳定剂。用于制备静脉注射试剂的BLINCYTO存放在一次性小瓶中,无菌、不含防腐剂的白色至米白色冻干粉。每一小瓶BLINCYTO包含35微克Blinatumomab、毫克一水柠檬酸、毫克盐酸赖氨酸、毫克聚山梨酯80、毫克海藻糖及氢氧化钠,调整PH值到7。加入3毫升的无防腐剂的蒸馏水,最终浓度为微克/毫升Blinatumomab。IV溶液稳定剂存放在一次性小瓶中,无菌、无防腐剂、无色至淡黄色的清液。成分为一水柠檬酸(毫克)、盐酸赖氨酸(毫克)、聚山梨酯80(10毫克),用氢氧化钠调整PH值到7,加入水。 【作用机理】 Blinatumomab是一种双特异性CD19指向CD3T细胞的衔接器,既可以共价结合B细胞表面表达的CD19,也可以共价结合T细胞表面表达的CD3。它通过连接T细胞受体(TCR)表面的CD3与恶性或良性B细胞表面的CD19激活内源性T细胞。Blinatumomab介导了T细胞和肿瘤细胞之间突触的形成、细胞黏附分子的上调、细胞溶解蛋白的形成、细胞炎性因子的释放、T细胞的增殖,可以导致CD19+细胞的重定向裂解。 【适应症和用途】 BLINCYTO适用为费城染色体-阴性复发的或难治性B-细胞前体急性淋巴母细胞白血病的治疗(ALL)。这个适应证是在加速批准下被批准。 【用法用量】 第一个疗程的前9天和第二个疗程前2天,建议住院。对所有随后的疗程 (治疗被中断超过4小时),建议由卫生保健专业人员护理或住院。 不要冲洗BLINCYTO输注线尤其是当改变输注袋时。改变袋或完成输注时冲洗可能导致药量过高及其并发症。曾发生制备和给药失误导致过量。 1 剂量BLINCYTO治疗的单个疗程由自由间隔连续静脉输注接着2周治疗4周组成。患者体重至少45 kg:在疗程1中,在第1–7天给药BLINCYTO 9毫克/天和在第8–28天给药28毫克/天。对随后疗程,在第1–28天给药BLINCYTO 28 毫克/天。BLINCYTO疗程间允许至少2周无治疗。一个治疗疗程由BLINCYTO至2疗程为诱导组成接着为巩固治疗由3个另加疗程(总计5疗程)。 2 给药每个BLINCYTO疗程首次剂量前1小时,一步剂量前(例如疗程 1第8天),或当中断4或更多小时后再开始一次输注预先给药静脉地塞米松20 mg。恒速用输注泵连续静脉输注给予BLINCYTO。泵应被可编程,可锁定,非弹性,和有警报。BLINCYTO输注袋应历时24小时或48小时输注。输注总计240 mL BLINCYTO溶液按照在袋上药标记指袋以乙型恒速速率之一输注:为时间24小时输注率10 毫升/小时,或为24小时时间输注率5 毫升/小时。为输注BLINCYTO溶液必须用含无菌,无热原,低蛋白-结合, 毫米在线滤膜IV管。.重要注释:不要冲洗输注线,尤其是当改变输注袋时。当改变袋或在完成输注时冲洗可能导致过量。BLINCYTO应通过专门管腔输注。输注结束时,在IV袋和IV线内任何未使用BLINCYTO溶液应按照当地要求遗弃。 3 剂量调整如不良事件后中断不长于7天,继续相同疗程至总共28天输注包括在该疗程中断前和后几天。如由于一个不良事件中断长于7天,开始一个新疗程。 4 为重建和输注溶液的制备?在本节中提供对制备指导非常重要(包括混合)和给药是严格地遵循药物错误最小化(包括剂量不足和过量)。 收集供应品?注释:1个包装 BLINCYTO包括1个BLINCYTO小瓶和1个IV溶液稳定剂小瓶。制备前,确保准备好以下供应品:?1包装BLINCYTO为制备9 毫克/天剂量历时24小时输注在速率10 毫升/小时,9 毫克/天剂量历时48小时在速率5 毫升/小时输注,和28 毫克/天剂量历时24小时在速率10 毫升/小时输注。?2 包装BLINCYTO为制备28 毫克/天剂量历时48小时在速率5 毫升/小时输注还需要以下供应品,但不包括在包装内:?无菌,一次用可遗弃注射器?21-至23-号针头(建议)?无防腐剂注射液无菌水,USP?250 mL %氯化钠IV袋?为最小化无菌转移数目,建议使用250 mL-预装IV袋。250 mL-预装IV袋典型地含总装填总容积265至275 mL。在节提供BLINCYTO剂量计算是根据开始容积的mL至275 mL %氯化钠。只使用聚烯烃,PVC非二异壬酯(非-DEHP),或乙基乙烯醋酸(EVA)输注袋/泵匣子。?聚烯烃,PVC非-DEHP,或EVA IV管与一个无菌,无-热原,低蛋白-结合 毫米在线滤膜确保IV管与输注泵兼容。? 无菌制备?当制备溶液为输注必须严格地观察无菌术因为BLINCYTO小瓶不含抗微生物防腐剂。防止意外污染,按照无菌标准制备BLINCYTO,包括但不限于:必须在一个USP <797>兼容设备进行制备。?必须在一个ISO 5级或更好层流罩进行制备。?混合区域应具备适当环境规范,通过定期监测确证。?操作人员应经无菌操作和肿瘤药物混合的适当训练。?操作人员应穿戴适当防护衣和手套。?手套和表面应进行消毒。 对支持准确制备特殊考虑⑴与BLINCYTO包装提供IV溶液稳定剂和在加入重建BLINCYTO前被用于涂层预装IV袋以防止BLINCYTO黏附至IV袋和IV线。因此,加入IV溶液稳定剂至含%氯化钠IV袋。为重建BLINCYTO不要使用IV溶液稳定剂。⑵混合的BLINCYTO的整个容积将超过给予患者(240 mL)容积计算为启动静脉线和确保患者将接受完全剂量BLINCYTO。⑶当制备一个IV袋时,从IV袋去除空气。与一个走动输注泵使用时这尤为重要。?⑷在混合指导中描述特异性容积,使计算中错误最小化。 为输注BLINCYTO溶液的制备利用一个预装250 mL %氯化钠IV袋提供对每个剂量和输注时间特异性混合指导。确证BLINCYTO处方剂量和输注时间和确定下面列出适当给药制备节。遵照重建BLINCYTO和制备IV袋的步骤.?见节为9 毫克/天历时24小时速率10 毫升/小时输注。见节为9 毫克/天历时48小时在速率5 毫升/小时输注。.?见节为28 毫克/天历时24小时速率10 毫升/小时输注。见节为28 毫克/天 历时48小时在速率5 毫升/小时输注。? BLINCYTO 9 毫克/天的制备历时24小时在速率10 毫升/小时输注?⑴使用一个预装250 mL %氯化钠IV袋。250 mL-预装袋典型地含过满总容积265至275 mL。如需要调整IV袋容积通过加入或去除%氯化钠实现开始容积在265和275 mL间。⑵用一个10 mL注射器,无菌地转移 mL的IV溶液稳定剂至有%氯化钠IV袋。轻轻混合袋内容物避免起泡。遗弃剩余IV溶液稳定剂小瓶。?⑶用一个5 mL注射器,用3 mL无防腐剂注射液无菌水,USP重建一个BLINCYTO小瓶。重建期间注射用无防腐剂无菌水,USP,指向小瓶壁。轻轻旋转内容物避免起泡。不要摇动。不要用IV溶液稳定剂重建BLINCYTO。注射用无防腐剂无菌水,USP加入至冰冻干燥粉导致最终BLINCYTO浓度 毫克/mL。⑷重建期间和输注前肉眼观察重建溶液有无颗粒物质和变色。得到溶液应是清澈至微乳白色,无色至微黄色。如溶液呈云雾状或有沉淀不要使用。⑸用一个1 mL注射器,无菌转移 mL重建BLINCYTO至IV袋。轻轻混合袋内容物避免起泡。?⑹ 在无菌条件下,有 毫米在线滤膜IV管附着至IV袋。⑺ 从IV袋去除空气和只用制备的溶液装填为输注IV线。不要用%氯化钠装填。⑻ 如不立即使用贮存在 2°C至8°C。? BLINCYTO 9 毫克/天历时48小时在速率5 毫升/小时输注的制备?⑴ 使用一个预装250 mL %氯化钠IV袋。250 mL-预装袋典型地含过满至总容积265至275 mL。如需要时通过加入或去除%氯化钠实现开始容积265和275 mL间。?⑵用一个10 mL注射器,无菌地转移 mL的IV溶液稳定剂至有%氯化钠IV袋。轻轻混合袋内容物避免起泡。遗弃剩余IV溶液稳定剂小瓶。⑶ 用一个5 mL注射器,用3 mL注射用无防腐剂无菌水,USP重建1个BLINCYTO小瓶。重建期间注射用无防腐剂无菌水,USP,指向小瓶壁。轻轻旋转内容物避免过量起泡。不要摇动。不要用IV溶液稳定剂重建BLINCYTO。?加入注射用无防腐剂无菌水,USP,至冰冻干燥粉导致最终BLINCYTO浓度 毫克/毫升。?⑷重建期间和输注前肉眼观察重建溶液有无颗粒物质和变色。得到溶液应是清澈至微乳白色,无色至微黄色⑷。如溶液呈云雾状或有沉淀不要使用。⑸用一个3 mL注射器,无菌转移 mL重建BLINCYTO至IV袋。轻轻混合袋内容物避免起泡。?⑹在无菌条件下,有 毫米在线滤膜IV管附着至IV袋。⑺ 从IV袋去除空气和只用制备的溶液装填为输注IV线。不要用%氯化钠装填。⑻ 如不立即使用贮存在 2°C至8°C。? BLINCYTO 28 毫克/天历时24小时输注在速率10 毫升/小时的制备?⑴使用一个预装250 mL %氯化钠IV袋。250 mL-预装袋典型地含过满至总容积265至275 mL。如需要时通过加入或去除%氯化钠实现开始容积265和275 mL间。?⑵用一个10 mL注射器,无菌转移 mL IV溶液稳定剂至有%氯化钠IV袋。轻轻混合袋内容物避免起泡。遗弃剩余IV溶液稳定剂小瓶。⑶ 用一个5 mL注射器,用3 mL注射用无防腐剂无菌水,USP重建一个BLINCYTO小瓶。重建期间注射用无防腐剂无菌水USP,指向小瓶壁。轻轻旋转内容物避免过度起泡。不要摇动。不要用IV溶液稳定剂重建BLINCYTO。加入注射用无防腐剂无菌水USP至冰冻干燥粉导致最终BLINCYTO浓度 毫克/毫升。⑷重建期间和输注前肉眼观察重建溶液有无颗粒物质和变色。得到的溶液应是清澈至微乳白色,无色至微黄色。如溶液呈云雾状或有沉淀不要使用。⑸ 用一个3 mL注射器,无菌转移 mL重建BLINCYTO至IV袋。轻轻混合袋内容物避免起泡。?⑹ 在无菌条件下,有 毫米在线滤膜IV管附着至IV袋。⑺ 从IV袋去除空气和只用制备的溶液装填为输注IV线。不要用%氯化钠装填。⑻ 如不立即使用贮存在 2°C至8°C。? BLINCYTO 28 毫克/天 历时48小时输注速率5 毫升/小时的制备?⑴ 使用一个预装250 mL %氯化钠IV袋。250 mL-预装袋典型地含过满至总容积265至275 mL。如需要时通过加入或去除%氯化钠实现开始容积265和275 mL间。?⑵用一个10 mL注射器,无菌转移 mL IV溶液稳定剂至有% 氯化钠IV袋。轻轻混合袋内容物避免起泡。遗弃剩余IV溶液稳定剂小瓶。⑶ 使用两个BLINCYTO小瓶。用一个