无机分析化学期末练习题1(附答案)
- 格式:pdf
- 大小:309.71 KB
- 文档页数:4

⽆机分析化学期末试卷(A)(1)⼀、选择题1.AgCl、AgBr、AgI的颜⾊依次加深,能解释这⼀现象的是( )。
(A) 晶格能(B) 杂化轨道理论(C) 离⼦极化(C) 分⼦轨道理论2.下列物质不是离⼦型化合物的是( )。
(A) BeCl2;(B) RbCl;(C) CsBr;(D) SrO。
3.下列性质哪⼀个不是过渡元素的通性( )。
(A) (n-1)d电⼦参加成键( B) 元素具有多种氧化态(C) 良好的配合物形成体(D) 单质熔点很低4.[Co(en)2(NH3)2]3+ 中⼼离⼦的配位数是( )。
(A) 3 (B) 4 (C) 5 (D) 65.采⽤EDTA滴定溶液中的Ca2+,Mg2+的⼲扰是⽤下列哪个⽅法去除( )。
(A) 掩蔽剂(B) 预先分离(C) 调整溶液pH (D) ⽆法去除6.BaCrO4溶于浓HCl后溶液的颜⾊及Cr的存在形式最合理是哪⼀种:( )。
(A) 绿⾊,CrO2-(B)黄⾊,CrO42-(C) 绿⾊,Cr3+ (D) 橙⾊,Cr2O72-7.在使⽤⾦属指⽰剂时,若MIn⾮常稳定,使得溶液颜⾊难以发⽣变化,这种现象称为( )。
(A) 指⽰剂的封闭现象(B) 指⽰剂的僵化现象(C) 指⽰剂的酸效应(D) 指⽰剂的副反应8.已知lgK BiY-=27.94,lgK FeY-=25.90,lgK FeY2-=14.33;⽤EDTA滴定Bi3+时,要消除Fe3+的⼲扰,最合适的掩蔽⽅法是( )。
(A) 沉淀掩蔽法;(B) 氧化还原掩蔽法;(C) 配位掩蔽法;(D) 没有合适的掩蔽法。
9.某元素的原⼦最外层只有两个l = 0的电⼦,该元素在周期表中必不属于()。
(A) s区元素(B) ds区元素(C) d区元素(D) p区元素10.在分⼦晶体中,分⼦内原⼦之间的结合⼒是()。
(A) 共价键(B) 离⼦键(C) ⾦属键(D) 范德华⼒11.[NiCl4]-的磁矩为2.828 (BM),该配离⼦的杂化类型和空间构型为()。

一、判断题。
(每题1分,共10分)(√)1.电负性综合地表征了原子得失电子的能力。
(×)2.酸碱指示剂在酸性溶液中呈酸色,在碱性溶液中呈碱色。
(√)3.速率常数大小总是与系统中所有物质的浓度无关。
(×)4.当可逆反应达到平衡时,反应即停止,且反应物和生成物的浓度相等。
(√)5.强碱滴定强酸的滴定突跃范围决定于溶液的浓度。
(×)6.色散作用只存在于非极性分子之间。
(√)7.非极性分子中有极性键。
(√)8.某一元酸越强,则其共轭碱越弱。
(×)9.液体的蒸气压与温度无关。
(√)10.偏差的大小可表示分析结果的精密度。
二、选择题。
(每题2分,共20分)1.下列数据中有效数字为3位的是:( C )A .0.030%B .pH =2.03 C.0.0234 D.8.9×10-42.根据有效数字运算规则,算式01120.010.3514.21031.0⨯⨯计算结果正确的是:(B)A .2×103 B.2.1×103 C.2.05×103 D.2.054×1033.理想气体是指:( A )A .气体分子本身体积和相互之间的作用力均可忽略B .气体分子本身体积不可忽略,相互之间的作用力可以忽略C .气体分子本身体积可忽略,相互之间存在着作用力D .气体分子本身体积和相互之间的作用力均不可以忽略4.增大压强,能使化学平衡向正反应方向移动的反应是:(D )A .N2O 4(g)2NO 2(g) B .Fe 3O 4(s) + 4CO(g) 3Fe(s) + 4CO 2(g) C .CaCO3(s) CaO(s) + CO 2(g) D .2NO(g) + O 2(g) 2NO 2 (g) 5.下列可逆反应2HI(g) H2(g) + I 2 (g) -Q 在密闭容器中进行,当达到平衡时,欲使混合气体的颜色加深,应采取的措施是:(D )A .减少容器体积B .降低温度C .加入催化剂D .充入HI 气体6. [Co(SCN)4]2-离子中钴的价态和配位数分别是………………( B )(A) -2,4 (B) +2,4 (C) +3,2 (D) +2,127.下列各组元素中,有一组元素原子的第一电离能分别为1086 kJ/mol、1402kJ/mol和1314 kJ/mol,该组元素为:(A)A.C N O B.F Ne Na C.Be B C D.S Cl Ar 8.比较O,S,As三种元素的电负性和原子半径大小的顺序,正确的是:(A)A.电负性O>S>As 原子半径O<S<AsB.电负性O<S<As原子半径O<S<AsC.电负性O<S<As 原子半径O>S>AsD.电负性O>S>As原子半径O>S>As9.电子构型相同的阳离子,其极化力最强的是:(C )A.高电荷和半径大的离子B.低电荷和半径大的离子C.高电荷和半径小的离子D.低电荷和半径小的离子10.共价键最可能存在于:(B)A.金属原子之间B.非金属原子之间C.金属原子和非金属原子之间D.电负性相差很大的元素的原子之间三、填空题。

无机及分析化学期末复习指导习题答案参考答案第1章化学反响速率和化学平衡一、选择题:1、B2、A3、A4、D5、A6、B7、B8、D9、A10、A 二、填空题 1、0.7250.725 2、0.550% 3、不变4、加快、向左移动5、式平衡右移三、简答题: 1、答:(1)CH3COOH+CH3OH始:1100 平:1-X1-XXX =KC=4X=0.67 ?1=×100%=67%(2)y2/(1-y)(3-y)=Kc=4,y=0.9?2=90%?2>?1,是由乙酸的浓度增大,使平衡右移导致甲醇的转化率升高2、答:升高温度,可以加快正逆反响的反响速度,平衡将逆向移动.因升高温度使速度常数增大,反响速度那么加快.(或从活化分子百分数增大,有效碰撞增多,微观角度说明).依据勒夏特列原理,升高温度,平衡向吸热方向移动.给出反响,逆向吸热,正向放热,所以平衡将逆向移动.3、答:影响化学反响速率的主要因素有:温度、压力、浓度、催化剂等。
影响化学平衡的因素有:温度、压力、浓度。
四、计算题 1.解 CH3COOCH3+H2O kc???80Kp?kc?(RT)???80?(8.314?1000)?1?9.62?10?3K=Kp(p)-△ν=9.62?10?3×(101.325)1=0.9752.(0.25)2?0.625 Kc==0.1Kp=Kc(RT)2-1×523)1=26.8 (2)PCl5的分解百分率为:65% 3.Kp=2.25K=228.27第2章定量化学根底习题一、选择题1、B2、A3、C4、B5、A6、C7、C8、C9、B10、C 二、填空题1、实际能测得的数字,准确数字,估计。
2、酸碱滴定法、配位滴定法、氧化复原滴定法、沉淀滴定法。
3、0.02000mol/L,0.1200mol/L,6.702*10g·mL。
4、直接法和标定法。
5、直接滴定法、返滴定法、置换滴定法、间接滴定法。

无机与分析化学期末考试一、单项选择题1. 取同浓度的Zn2+-EDTA配合物的溶液A、B两份。
A份:用NaOH溶液控制pH=10.0,其表观稳定常数记作K'ZnY,A;B份:用氨-氯化铵缓冲溶液控制pH= 10.0,其表观稳定常数记作K'ZnY,B。
则:(A) K'ZnY,A = K'ZnY,B(B) K'ZnY,A > K'ZnY,B(C) K'ZnY,A < K'ZnY,B(D) 无法确定2. 佛尔哈德法测定Cl-时,使用的指示剂是:(A) Ag2CrO4(B) 二氯荧光黄(C) 甲基橙(D) FeNH4(SO4)23. 在下列物质中,不能将KI氧化成I2的是:(A) KIO3 (B) FeNH4(SO4)2(C) Fe(NH4)2(SO4)2(D) CuSO44. 下列说法正确的是:(A) 非构晶离子的盐浓度越大,沉淀溶解度越大(B) 非构晶离子的盐浓度越大,沉淀溶解度越小(C) 两种沉淀的溶度积相比,溶度积小的溶解度也一定小(D) 同种类沉淀的溶解度越大,溶度积越小5. 从磷元素的电位图φo (V) H2PO2-____-2.25V____P4_______________PH3|_____________-1.23V____________|可知标准电极电位φo P4/PH3为:(A) -1.02 V (B) -1.74 V (C) -0.89 V (D) -1.16 V6. 在配离子[Co(C2O4)2(en)]-中(en为H2N-CH2-CH2-NH2),中心离子Co3+的配位数是:(A) 3 (B) 4 (C) 5 (D) 67. 用Na2C2O4标定KMnO4,加入第一滴KMnO4时,KMnO4的紫红色不会立即退去,这是因为反应速度不够快,若使第一滴KMnO4很快退色,最有效的措施是:(A) 加大Na2C2O4浓度(B) 加大酸度(C) 事先加入Mn2+(D) 加快滴KMnO4的速度8. 下列混合离子能用氨水分离的是:(A) Cr3+和Cu2+(B) Cu2+和Zn2+(C) SO42-和Cl-(D) Fe3+和Al3+9. 在酸性溶液中,以0.1000 mo l•L-1的Ce4+溶液滴定0.1000 mo l•L-1的Fe2+溶液,化学计量点的电位为1.06V,对此滴定最适宜的指示剂是:(A) 次甲基蓝(φo=0.53V)(B) 二苯胺磺酸钠(φo=0.84V)(C) 邻二氮菲亚铁(φo=1.06V)(D) 硝基邻二氮菲亚铁(φo=1.25V)-1pH0.0 1.0 2.0 3.0 4.0 5.0 6.0 7.0 8.0 9.0 10.0 11.0 12.0 lgαY(H)23.64 18.01 13.51 10.60 8.44 6.45 4.65 3.32 2.27 1.28 0.45 0.07 0.01(A) 3.0 (B) 4.0 (C) 5.0 (D) 6.011. Fe2+有6个3d电子,配合物[Fe(CN)6]4-的晶体场分裂能△o = 395 kJ·mol-1;电子成对能E p = 213 kJ·mol-1。

无机及分析化学期末考试卷及答案标题:无机及分析化学期末考试卷及答案一、选择题1、在以下四种物质中,哪种物质的水合离子颜色最深? A. 氯化铜 B. 氯化亚铁 C. 氯化锰 D. 氯化钴答案:A. 氯化铜2、以下哪种化学反应属于氧化还原反应? A. 酸碱中和 B. 碳酸钙与盐酸反应 C. 氧化铜与氢气反应 D. 硫酸铜与氢氧化钠反应答案:C. 氧化铜与氢气反应3、以下哪种试剂可以用来鉴别氯化铁和硫酸铁? A. 氢氧化钠 B.硫氰酸钾 C. 盐酸 D. 碳酸钠答案:B. 硫氰酸钾二、填空题1、请写出以下化学方程式:(1)三氯化铁与氢氧化钠反应:。
(2)碳酸钙与稀盐酸反应:。
答案:(1)FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl (2)CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O2、请简述如何利用碘化钾试纸鉴别氯化钠和氯化钾。
答案:将碘化钾试纸浸入待测溶液中,如果试纸变为蓝色,则说明溶液中含有氯离子。
因为氯化钠和氯化钾中的氯离子都会与碘离子反应生成碘单质,而碘单质可以使试纸变为蓝色。
因此,蓝色越深,说明氯离子含量越高。
三、计算题已知铜的原子量是63.55,铜的化合价为+2,请计算铜的摩尔质量。
答案:铜的摩尔质量为133.85g/mol。
根据原子量和化合价,可以得出铜的相对分子质量为63.55×2=127.1,因此铜的摩尔质量为127.1g/mol。
四、实验题请设计一个实验,测定未知浓度的氯化钡溶液的浓度。
答案:首先,需要准备已知浓度的硫酸钠溶液、待测氯化钡溶液、天平和容量瓶等实验器材。
实验步骤如下:1、将一定量的硫酸钠溶液加入到容量瓶中。
2、加入适量的氯化钡溶液,充分摇匀。
3、加入几滴酚酞指示剂,用氢氧化钠溶液滴定至颜色变化。
4、根据氢氧化钠溶液的用量和已知浓度的硫酸钠溶液,可以计算出氯化钡溶液的浓度。
通过以上实验步骤,我们可以得出未知浓度的氯化钡溶液的浓度。

无机及分析化学期末考试题及答案一、单选题1.无机化合物中的离子反应属于()A.不化反应B.单纯化学反应C.催化反应D.电解反应答案:B2.以下哪一种化学反应并不属于“催化反应”( )A.歧化反应B.过氧化呋喃反应C.银离子捕获氧反应D.还原缩合反应答案:A3.碱金属的无机盐的共价键的分类属于()A.金属–离子键B.金属–氧键C.共价键D.金属–气体键答案:A4.稀硫酸中的sulfur氧化物分子具有以下哪个稳定式()A.SO3B.SO4C.SO2D.S2O答案:B5.根据量子理论,氮原子键定电子主要发生在()A.1s orbitB.2s orbitC.2p orbitD.3d orbit答案:C二、多选题1.汞元素的共价键()A.金属–阴离子键B.金属–酸根键C.金属–气体键D.金属–离子键答案:A、B、D2.Friedel-Crafts的acylation反应的活性变为极性的物质有()A.稀硫酸B.硝酸C.硫酸D.氯化物答案:A、B、C3.化学分析中所用的主要的检测方法有()A.光谱定性分析B.滴定测定C.物质量分析D.比色测定答案:A、B、D4.下列分子结构中,属于共价键的是()A.HClB.H2OC.CH4D.NH3答案:B、D三、填空题1.细胞折射定理是 __ 物质会有折射率的理论。
答案:变性剂2.氯气可以缓慢氧化形成氯___ 。
答案:水。

《无机及分析化学》期末考试试卷附答案一、单项选择题(每空2分.共40分)1、已知 A+B = M+N, Δr H m=35kJ∙mol-1; 2M + 2N = 2D, Δr H m=-80kJ∙mol-1.则A+B = D的Δr H m= kJ∙mol-1。
2、已知分析天平能称准至±0.1mg, 要使试样的称量误差不大于1‰,则至少要称 g。
3、按有效数字规则计算 2.187×0.852 +9.82/3.425= 。
4、溶液中某物质X的浓度为2×10-5mol∙L-1, 用1 cm比色皿在465nm处测得吸光度为0.400, 则此配合物在465nm 处的摩尔吸光系数为 L·mol-1·cm-1。
5、计算0.10 mol∙L-1Na2HPO4溶液的pH值,选择最简计算公式为[H+]= (H3PO4的逐级解离常数为K a1、K a2、K a3)。
6、Ac–的分布系数与HAc的总浓度无关,取决于HAc的和溶液的。
7、加入沉淀剂后,被沉淀的离子在溶液中残留量不超过 mol∙L-1叫沉淀完全。
= 0.09961 g·mL-1, 则8、已知: Cr2O72- + 6I- + 14H+ = 2Cr3+ + 3I2 + 7H2O , M KI=166.01, T KI/K2Cr2O7C K= moL·L-1。
2Cr2O79、将反应2Ag+ 2I- + 2H+ = 2AgI↓ + H2组成原电池,则原电池符号为。
10、已知Pb2+的浓度为10-2mol·L-1,在pH=4.0时,lg Y(H)=8.44,10、lg K PbY=18.04,则Pb2+ (填“能”或“不能”) 被EDTA标准溶液准确滴定。
11、配合物:[Cu(NH3)4][PtCl4]的名称是(用系统命名法命名)。
12、用EDTA滴定Zn2+时,Al3+有干扰,可在合适的pH值下,加入NH4F使Al3+ [AlF6]3-配离子,属于掩蔽法。


无机及分析化学期末考试卷及答案一、选择题(每题2分,共20分)1、在下列元素中,哪个不是稀土元素?A.镧B.钕C.钷D.铀2、下列哪个反应不是氧化还原反应?A.铁生锈B.燃烧C.电解水D.呼吸作用3、下列哪个是极性分子?A. H2OB. CO2C. N2D. C2H64、在下列酸中,哪个是强酸?A.盐酸HClO4B. H2SO3C. H3PO4D. H2CO35、下列哪个物质有最外层电子排布式4s2?A. FeB. CoC. NiD. Ru答案:1. D,2. C,3. A,4. A,5. A二、填空题(每空2分,共30分)1、请写出元素周期表中的前五个周期的元素数。
第一周期:个元素;第二周期:个元素;第三周期:个元素;第四周期:个元素;第五周期:个元素。
2、请写出氧化还原反应中的氧化剂和还原剂。
氧化剂:,还原剂:。
3、请写出酸雨的主要成分。
酸雨的主要成分是和。
4、请写出金属铁和水蒸气反应的化学方程式。
5、请写出稀土元素的名称和英文缩写。
答案:1.第一周期:2个元素;第二周期:8个元素;第三周期:8个元素;第四周期:18个元素;第五周期:18个元素。
2.请写出氧化还原反应中的氧化剂和还原剂。
氧化剂:得到电子的物质,还原剂:失去电子的物质。
3.请写出酸雨的主要成分。
酸雨的主要成分是硫酸和硝酸。
4.请写出金属铁和水蒸气反应的化学方程式。
3Fe + 4(g) ==== Fe3O4 + 4H2。
5.请写出稀土元素的名称和英文缩写。
稀土元素的名称有镧、钕、钷、钐、铕、钆、铽、镝、钬、铒、铥、镱、镥,英文缩写分别是La、Nd、Pm、Sm、Eu、Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu。
A.氧化还原反应B.中和反应C.分解反应D.取代反应A.水B.甲烷C.二氧化碳D.氯化钠请填写下列元素的化学符号:氢__,碳__,氧__,钠__。
请填写下列化学式的电子数:H2O__,CO2__,NaCl__。
答案:H2O的电子数为10,CO2的电子数为22,NaCl的电子数为28。

《无机及分析化学》复习题一、填空题1、在相同体积相同浓度的HAc(aq)和HCl(aq)中,所含的氢离子浓度 ;若用相同浓度的NaOH 溶液去完全中和这两种溶液时,所消耗的NaOH 溶液的体积 ,恰好中和时两溶液的pH 值 。
(填“相同”或“不同”)2、任何电对的电极电势的绝对值都不能直接测定,在理论上,某电对的标准电极电势E 是将其与 电极组成原电池测定该电池的电动势而得到的。
国际上规定上述电极的标准电极电势为 。
3、配合物[Co(NH 3)4Cl 2]Cl 的名称是 ,中心离子的配位数是 。
4、某元素最高氧化数为+6,基态原子最外层电子数为1,其原子半径为同族元素中最小的,该元素的价电子层结构式为 ,元素名称为 ,该元素属于 族。
5、用莫尔法测Cl -时的适宜pH 范围是 ,滴定是 ,指示剂是 。
6.滴定分析中有不同的滴定方式,除了 这种基本方式外,还有 、 、 等。
7、分析测试数据中,随机误差的特点是大小相同的正负误差出现的概率 ,大误差出现的概率 ,小误差出现的概率 。
8、四氯化碳与单质碘之间存在的作用力类型为 。
9、准确称取20.0mg 某水溶性多肽溶于20.0mL 水中,298.15K 时,测得该溶液渗透压为2.48×103Pa ,则该多肽的相对分子量为 ,其凝固点下降值为 。
(已知水的k f =1.86K ⋅kg ⋅mol -1)10、NH 3极易溶于水,其原因是 。
11、标准摩尔生成焓 m f H ∆为零的物质称 。
标准摩尔燃烧焓 m c H ∆为零的物质为 。
12、已知K(HAc) = 1.75 ×10-5,用 0.025 mol.L-1 HAc溶液和等体积0.050 mol.L-1 NaAc 溶液配制的缓冲溶液,其pH = ,在该溶液中加入很少量HCl溶液,其pH值将。
13、取一支小试管,向其中加入10滴1 mol⋅L-1KI溶液,加10滴CCl4,再向其中加入5滴1 mol⋅L-1FeCl3溶液,振荡,CCl4层变为色,该反应的离子方程式,该实验说明Fe3+的氧化能力比I2的氧化能力_____。
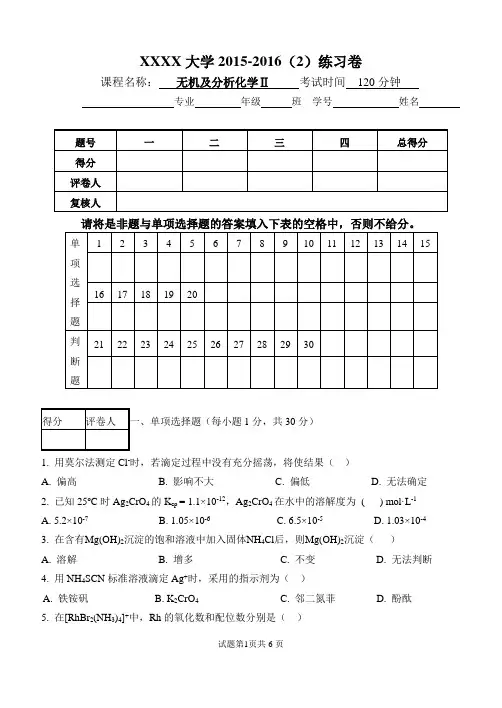
XXXX大学2015-2016(2)练习卷课程名称:无机及分析化学Ⅱ考试时间120分钟专业年级班学号姓名1分,共30分)1. 用莫尔法测定Cl-时,若滴定过程中没有充分摇荡,将使结果()A. 偏高B. 影响不大C. 偏低D. 无法确定2. 已知25o C时Ag2CrO4的K sp = 1.1×10-12,Ag2CrO4在水中的溶解度为( ) mol·L-1A. 5.2×10-7B. 1.05×10-6C. 6.5×10-5D. 1.03×10-43. 在含有Mg(OH)2沉淀的饱和溶液中加入固体NH4Cl后,则Mg(OH)2沉淀()A. 溶解B. 增多C. 不变D. 无法判断4. 用NH4SCN标准溶液滴定Ag+时,采用的指示剂为()A. 铁铵矾B. K2CrO4C. 邻二氮菲D. 酚酞5. 在[RhBr2(NH3)4]+中,Rh的氧化数和配位数分别是()A. +2和4B. +3和6C. +2和6D. +3和4 6. 已知pH=1.30时,lgαY(H)=16.80, lgK f θFeY =25.00,用0.02mol·L -1EDTA 标准溶液滴定等浓度的FeCl 3 , 若只考虑酸效应的影响,达化学计量点时其pFe 值为( ) A. 13.50 B. 12.50 C. 5.10 D. 4.10 7. 用EDTA 标准溶液滴定Al 3+采用的滴定方式是( )A. 直接滴定B. 间接滴定C. 返滴定D. 置换滴定 8.下列叙述中,不正确的为 ( ) A. EDTA 是六齿配体B. 除ⅠA 族元素外,EDTA 与金属离子一般均可形成稳定配合物C. EDTA 与金属离子配合物一般带电荷,故在水中易溶D. 若不考虑水解效应,EDTA −金属配合物稳定性不受介质酸度影响9. 在用EDTA 滴定金属离子M 的过程中,影响滴定曲线突跃范围大小的主要因素 ( ) A. c M B. (MY )lg (MY )lg ,f θf K K 和 C. (MY )lg θf M K c 和 D. (MY )lg ,f M K c 和10. 配位反应 [Cu(NH 3)4]2+ + Zn 2+ =[Zn(NH 3)4]2+ + Cu 2+,已知298K 时K θf [Cu(NH 3)4]2+ = 1013.32, K f θ[Zn(NH 3)4]2+ = 109.46,则反应在298K ,标准状态下自发进行的方向应为( ) A. 正向 B. 逆向 C. 平衡 D. 三种情况都可能 11. 下列有关KMnO 4滴定法的叙述中,错误的是( ) A. KMnO 4标准溶液必须用间接法配制B. KMnO 4滴定法可以不用氧化还原指示剂指示终点C. KMnO 4标准溶液滴入的速度应该先慢后快,但也不能太快D. KMnO 4的氧化能力较强,该法有较好的选择性12. 在硫酸-磷酸介质中,用c (K 2Cr 2O 7)=0.1 mol·L -1的K 2Cr 2O 7溶液滴定c (Fe 2+)=0.1 mol·L -1的FeSO 4溶液,其化学计量点电势为0.86 V 。
一、单项选择题(每题2分,共40分。
请将答案填入下表中,未填入表中则不计分):1. 电子的波动性是(A) 一种机械波 (B) 一种电磁波(C) 一种概率波 (D) 电子运动时呈波浪式的前进 2. 下列论述中正确的是(A) 溶解度表明了溶液中溶质和溶剂的相对含量 (B) 溶解度是指饱和溶液中溶质和溶剂的相对含量 (C) 任何物质在水中的溶解度都随着温度的升高而升高 (D) 压力的改变对任何物质的溶解度都影响不大 3. 指出下列表述中的错误(A) 吸收峰随浓度增加而增大,但最大吸收波长不变 (B) 透射光与吸收光互为补色光,黄色和蓝色互为补色光 (C) 比色法又称分光光度法(D) 在公式c b II A ⋅⋅==ε0lg 中, ε 称为摩尔吸光系数,其数值愈大,反应愈灵敏4. 对于一个给定条件下的反应,随着反应的进行(A) 速率常数k 变小 (B) 平衡常数K 变大 (C) 正反应速率降低 (D) 逆反应速率降低 5. 以下有关系统误差的论述错误的是(A) 系统误差有单向性 (B) 系统误差有随机性(C) 系统误差是可测误差 (D) 系统误差是由一定原因造成 6. 以下试剂能作为基准物的是(A) 分析纯CaO (B) 分析纯SnCl 2·2H 2O (C) 分析纯NaOH (D) 99.99%金属铜 7. 下列表述中错误的是(A) 比色分析所用的参比溶液又称空白溶液 (B) 滤光片应选用使溶液吸光度最大者较适宜 (C) 一般说,摩尔吸光系数ε 在105~106 L/(mol·cm)范围内,可认为该反应灵敏度是高的(D) 吸光度具有加和性8. 用NaOH 溶液滴定某弱酸HA ,若两者浓度相同,当滴定至50%时溶液pH =5.00; 当滴定至100%时溶液pH = 8.00;当滴定至200%时溶液pH = 12.00,则该酸p K a值是(A) 5.00 (B) 8.00 (C) 12.00 (D) 7.009. 以下表述中错误的是(A) H2O作为酸的共轭碱是OH-(B) H2O作为碱的共轭酸是H3O+(C) 因为HAc的酸性强,故HAc的碱性必弱(D) HAc的碱性弱,则H2Ac+的酸性强10. c(NaCl) = 0.1mol/L的NaCl水溶液的电荷平衡式是(A) [H+] = [OH-] (B) [Na+] = [Cl-] = 0.1 mol/L(C) [Na+]+[Cl-] = 0.1 mol/L (D) [H+]+[Na+] = [OH-]+[Cl-]11. 要使溶液的凝固点降低1.0℃, 需向100 g 水中加入KCl 的物质的量是(水的K f= 1.86K·kg·mol-1)(A) 0.027 mol (B) 0.054 mol (C) 0.27 mol (D) 0.54 mol12. 下列溶液中不能组成缓冲溶液的是(A) NH3和NH4Cl (B) H2PO4-和HPO42-(C) HCl和过量的氨水(D) 氨水和过量的HCl13. 影响气体在液体中溶解度的因素有(A) 溶质的性质(B) 温度(C) 压力(D) 以上三种都是14. 对于反应I2 + 2ClO-3= 2IO-3+ Cl2,下面说法中不正确的是(A) 此反应为氧化还原反应(B) I2 得到电子,ClO-失去电子3(C) I2是还原剂,ClO-是氧化剂3(D) 碘的氧化数由0增至+5,氯的氧化数由+5 降为015. 以下说法错误的是(A) 朗伯-比尔定律只适于单色光(B) Fe2+-邻二氮菲溶液是红色,应选择红色滤光片(C) 紫外区应选择的光源是氢灯(D) 摩尔吸光系数ε值愈大,说明反应愈灵敏16. 下列溶液中不能组成缓冲溶液的是(A) NH3和NH4Cl (B) H2PO4-和HPO42-(C) HCl和过量的氨水(D) 氨水和过量的HCl17. 用Fe3+滴定Sn2+在化学计量点的电位是[ϕ' (Sn4+/Sn2+)=0.14V]ϕ' (Fe3+/Fe2+)=0.68V,(A) 0.75V (B) 0.68V (C) 0.41V (D) 0.32V18. 在原电池中,发生氧化反应的是:(A) 正极,阳极;(B) 正极,阴极;(C) 负极,阳极;(D)负极,阴极19. 试样用量为0.1 ~ 10 mg的分析称为(A) 常量分析(B) 半微量分析(C) 微量分析(D) 痕量分析20. 能消除测定方法中的系统误差的措施是(A) 增加平行测定次数(B) 称样量在0.2g以上(C) 用标准试样进行对照试验(D) 认真细心地做实验二、填空题(每空1分,共20分):1. 配合物[Zn(OH)(H2O)3]NO3的系统命名为_________________________,中心离子的电荷是____ ,配位体是________ ,配位原子是________ 。
22 244 3 2023-2023 学年第 1 学期无机及分析化学 A一、单项选择题〔每题 2 分,共 40 分。
请将答案填入下表中,未填入表中则不计分〕:题号 答案 1 2 3 4 5 6 7 8 9 10 题号 答案111213141516171819201. 某反响在标准态和等温等压条件下,在任何温度都能自发进展的条件是(A) Δ r H m > 0 Δ r S m > 0 (B) Δ r H m < 0 Δ r S m < 0 (C) Δ r H m > 0Δ r S m < 0(D) Δ r H m < 0Δ r S m > 02. 电池反响:H (g ,100kPa) + 2AgCl(s) −−→2HCl(aq) + 2Ag(s) E = 0.220 V ,当电池的电动势为 0.358 V 时,电池溶液的pH 为(A)(C)E - EpH 20.358 - 0.220 2 ⨯ 0.0590.358 - 0.220(B)0.059(D) 03. 体系对环境作 20 kJ 的功,并失去 10kJ 的热给环境,则体系内能的变化是(A) +30 kJ(B) +10 kJ (C) −10 kJ (D) −30kJ4. 对于反响I 2 + 2ClO —= 2IO —+ Cl ,下面说法中不正确的选项是 (A) 此反响为氧化复原反响 (B) I 得到电子,ClO - 失去电子3(C) I 是复原剂,ClO - 是氧化剂3(D) 碘的氧化数由 0 增至 +5,氯的氧化数由 +5 降为 0 5. 以下说法错误的选项是(A) 朗伯-比尔定律只适于单色光(B) Fe 2+-邻二氮菲溶液是红色,应选择红色滤光片 (C) 紫外区应选择的光源是氢灯(D) 摩尔吸光系数ε值愈大,说明反响愈灵敏 6. 以下溶液中不能组成缓冲溶液的是(A) NH 3 和 NH 4Cl(B) H 2PO - 和 HPO 2-3 2444 2 (C) HCl 和过量的氨水 (D) 氨水和过量的 HCl7. 能消退测定方法中的系统误差的措施是(A) 增加平行测定次数 (B) 称样量在 0.2g 以上 (C) 用标准试样进展比照试验(D) 认真细心地做试验8. 海水平均含 1.08×103μg/g Na +和 270 μg/g SO 2-,海水平均密度为 1.02g/mL, 则海水中Na + 和 SO 2-浓度(mol/L)为 A r (Na)=23.0, M r (SO 2-)=96.1 (A) 4.79×10-5, 2.87×10-6 (B) 1.10×10-3, 2.75×10-4 (C) 4.60×10-2, 2.76×10-3(D) 4.79×10-2, 2.87×10-39. 下面不是参比电极的是:A.标准氢电极;B.银-氯化银电极;C.玻璃电极;D.甘汞电极。
一、选择题1.AgCl、AgBr、AgI的颜色依次加深,能解释这一现象的是( )。
(A) 晶格能(B) 杂化轨道理论(C) 离子极化(C) 分子轨道理论2.下列物质不是离子型化合物的是( )。
(A) BeCl2;(B) RbCl;(C) CsBr;(D) SrO。
3.下列性质哪一个不是过渡元素的通性( )。
(A) (n-1)d电子参加成键( B) 元素具有多种氧化态(C) 良好的配合物形成体(D) 单质熔点很低4.[Co(en)2(NH3)2]3+ 中心离子的配位数是( )。
(A) 3 (B) 4 (C) 5 (D) 65.采用EDTA滴定溶液中的Ca2+,Mg2+的干扰是用下列哪个方法去除( )。
(A) 掩蔽剂(B) 预先分离(C) 调整溶液pH (D) 无法去除6.BaCrO4溶于浓HCl后溶液的颜色及Cr的存在形式最合理是哪一种:( )。
(A) 绿色,CrO2-(B)黄色,CrO42-(C) 绿色,Cr3+ (D) 橙色,Cr2O72-7.在使用金属指示剂时,若MIn非常稳定,使得溶液颜色难以发生变化,这种现象称为( )。
(A) 指示剂的封闭现象(B) 指示剂的僵化现象(C) 指示剂的酸效应(D) 指示剂的副反应8.已知lgK BiY-=27.94,lgK FeY-=25.90,lgK FeY2-=14.33;用EDTA滴定Bi3+时,要消除Fe3+的干扰,最合适的掩蔽方法是( )。
(A) 沉淀掩蔽法;(B) 氧化还原掩蔽法;(C) 配位掩蔽法;(D) 没有合适的掩蔽法。
9.某元素的原子最外层只有两个l = 0的电子,该元素在周期表中必不属于()。
(A) s区元素(B) ds区元素(C) d区元素(D) p区元素10.在分子晶体中,分子内原子之间的结合力是()。
(A) 共价键(B) 离子键(C) 金属键(D) 范德华力11.[NiCl4]-的磁矩为2.828 (BM),该配离子的杂化类型和空间构型为()。
无机及分析化学期末考试试题答案附后石河子大学《无机及分析化学》考题试卷一一、选择题(1分×20=20分)1.土壤中NaCl 含量高时,植物难以生存,这与下列稀溶液性质有关的是( )。
A. 蒸气压下降B. 沸点升高C. 凝固点降低D. 渗透压2.0.10mol·L -1的下列溶液凝固点降低程度最大的是( )。
A. C 6H 12O 6(葡萄糖)B. KNO 3C. C 3H 5(OH)3(甘油)D. CuSO 43.下列反应的标准摩尔焓等于其产物的标准摩尔生成焓的反应是( )。
A. SO 2(g)+21O 2(g) SO 3(g) B. N 2(g)+O 2(g) 2NO(g) C. H 2(g)+21O 2(g) H 2O(g) D. CO(g)+21O 2(g) CO 2(g) 4.某反应的速率常数k 的单位为L·mol -1·s -1,则该化学反应的反应级数为( )。
A. 0B. 1C. 2D. 35.反应 A(g)+2B(g) E(S)+D(g) 达平衡时,下列表述正确的是( )。
A. K (正反应)+ K (逆反应)=1B. Δr G m (正反应)×Δr G m (逆反应)=1C. K (正反应)×K (逆反应)=1D. Δr G m (正反应)+Δr G m (逆反应)=16.下述四个量子数不合理的一组是( )。
A. 2,0,1,B. 3,1,0,-C. 4,2,1,D. 2,1,0,-7.下列分子都没有极性的一组是( )。
A. SO 2 NO 2 CO 2B. SO 3 BF 3 NH 3C. CH 4 BF 3 CO 2D. PCl 3 CCl 4 H 2O8.下列混合溶液中两种离子能够共存的是( )。
A. CO -23和Al 3+B. MnO -4和SO -23C. Fe 3+和Cu 2+D. Cr 2O -27和I -9.向pH=2的缓冲溶液中通入H 2S(g)达饱和时(H 2S 浓度约为0.1mol·L -1),溶液中的c (S 2-)(mol·L -1)为:{K a1 (H 2S)=1.3×10-7,K a2 (H 2S)=7.1×10-15}( )。
课程名称:无机及分析化学A课号:X01G10A试卷编号:C考试方式:闭卷班级:姓名:学号:成绩:大题号一二三四五总分得分一、单项选择题(每题 2 分,共 30 分)1.33同时混将压力为 0.67 kPa 的氮气 3.0 dm和压力为 0.54 kPa 的氢气 1.0 dm合在 2.0dm3密闭容器中 , 假定混合前后温度不变 ,则混合气体的总压力为()(A) 0.61 kPa(B) 0.64 kPa(C) 1.2 kPa(D) 1.3 kPa2.下列溶质质量相同,体积相同的溶液,凝固点降低最多的是()A、C6H12O6B、C12H22O11C、CO(NH2)2D、C2H5OH3.下列各组量子数中,合理的一组是()A n=3l=1m= +1m s=+1/2B n=4l=5m=-1m s=+1/2C n=3l=3m=+1sm =-1/2D n=4l=2m=+3s m =-1/24.下列液体只需要克服色散力就能使之沸腾的物质是()A O2B SO2C HFD H2O5.冰熔化时,在下列各性质中增大的是()A 、(A)蒸气压(B) 熔化热(C) 熵(D) 吉布斯自由能6.反应 H2(g)+I2(g)=2HI(g) 的质量作用定律的表达式为 v kc H2 c I2,则该反应一定为()A 、一级B、二级C、三级D、不能确定7.合成氨反应 3H2(g) + N 2(g)2NH3 (g) 在恒压下进行时,当体系中引入氩气后,氨的产率是()(A) 减小(B) 增加(C) 不变(D) 无法判断8.等温、等压只作体积功的条件下,化学反应自发进行的判据是()θ< 0B 、 r G m < 0 A 、 r G mC 、 r H m < 0D 、 r S m > 09.下列等式正确的是()θθ B 、ΔG=nF ε A 、 r G =- RTlnKC 、 f H m 0(CO 2,g)= c H m 0(C 金刚石 )D 、 S m,2980(H 2 ,g)=010. 下述叙述中正确的是()(A) 在恒压下,凡是自发的过程一定是放热的(B) 因为焓是状态函数,而恒压反应的焓变等于恒压反应热,所以热也是状态函数(C) 单质的f H m 和 f G m 都为零(D) 在恒温恒压条件下,体系自由能减少的过程都是自发进行的11.pH = 10 的 NH 3- NH 4+缓冲溶液 c(NH 4+)/c(NH 3)的比值为 [pK b (NH 3)=4.75]()0.250.75-0.25- 0.75A 、10B 、 10C 、10D 、1034 在水中的溶解度为 Smol ·L -1,则其 K sp 等于()12. Ag POA 、S 4 K spB 、 S2713. Na 3PO 4 的 K b1 等于(A 、 K W /K a1(H 3PO 4)C 、 K W /K a3(H 3PO 4)14.下列物理量不为零的是(3 K sp K sp KspC 、 S4 D 、 S33 274)B 、K W /K a2(H 3PO 4) D 、K a3(H 3PO 4) / K W)A 、 H / H 2B 、 H θC 、 Hθ D 、 Hθ + ,aq)mmmc2ff15. 透射比与吸光度的关系是 ( )1 A (B) 1 A (C) lg T = A (D) Tlg 1 (A) lg A T T二、判断题(每题 1 分,共 10 分)1 -= CuSCN(s) + I -的竞争平衡常数 K j = K SP SP、CuI(s)+SCN(CuI)/ K (CuSCN ) 2、已知水的电离是吸热反应, 由此可知 100℃纯水的 pH 值小于 20℃纯水的 pH 值3、当 pH>12 时, EDTA 的 Y 4- 的分布系数等于 1,酸效应系数等于零4、K 4[Fe(CN)6] 的命名为六氰合铁 (Ⅱ)酸钾5、只考虑酸效应影响时, lgK MY ˊ= lgK MY -lg αY(H)6、用吸收了二氧化碳的氢氧化钠标准溶液滴定盐酸,若用酚酞作指示剂,则将产生负误差7、用 EDTA 测水中钙时,维持 pH =12 的目的只是为了使水中的镁生成Mg(OH) 2沉淀而不被滴定8、准确称取分析纯KMnO 4(分子量 158.03 g)3.1606 g 溶解定容于 1.000L 的容量瓶中,所得KMnO 4标准溶液的浓度为0.02000 mol/L9、硫酸钠对由三氯化铁水解制备的氢氧化铁溶胶的聚沉值大于硝酸钾10、用双指示剂测定混合碱时,若V 1 >V 2>0,则该混合碱可能是NaHCO3和Na2CO3三填空题(每空 1 分,共 15 分)1. 反应 N2O4(g)2NO 2(g) 中,因为NO 2是红褐色而N2O4是无色, NO 2分压可利用光吸收来测定。
无机与分析化学期末考试一、单项选择题1. 取同浓度的Zn2+-EDTA配合物的溶液A、B两份。
A份:用NaOH溶液控制pH=10.0,其表观稳定常数记作K'ZnY,A;B份:用氨-氯化铵缓冲溶液控制pH= 10.0,其表观稳定常数记作K'ZnY,B。
则:(A) K'ZnY,A = K'ZnY,B(B) K'ZnY,A > K'ZnY,B(C) K'ZnY,A < K'ZnY,B(D) 无法确定2. 佛尔哈德法测定Cl-时,使用的指示剂是:(A) Ag2CrO4(B) 二氯荧光黄(C) 甲基橙(D) FeNH4(SO4)23. 在下列物质中,不能将KI氧化成I2的是:(A) KIO3 (B) FeNH4(SO4)2(C) Fe(NH4)2(SO4)2(D) CuSO44. 下列说法正确的是:(A) 非构晶离子的盐浓度越大,沉淀溶解度越大(B) 非构晶离子的盐浓度越大,沉淀溶解度越小(C) 两种沉淀的溶度积相比,溶度积小的溶解度也一定小(D) 同种类沉淀的溶解度越大,溶度积越小5. 从磷元素的电位图φo (V) H2PO2-____-2.25V____P4_______________PH3|_____________-1.23V____________|可知标准电极电位φo P4/PH3为:(A) -1.02 V (B) -1.74 V (C) -0.89 V (D) -1.16 V6. 在配离子[Co(C2O4)2(en)]-中(en为H2N-CH2-CH2-NH2),中心离子Co3+的配位数是:(A) 3 (B) 4 (C) 5 (D) 67. 用Na2C2O4标定KMnO4,加入第一滴KMnO4时,KMnO4的紫红色不会立即退去,这是因为反应速度不够快,若使第一滴KMnO4很快退色,最有效的措施是:(A) 加大Na2C2O4浓度(B) 加大酸度(C) 事先加入Mn2+(D) 加快滴KMnO4的速度8. 下列混合离子能用氨水分离的是:(A) Cr3+和Cu2+(B) Cu2+和Zn2+(C) SO42-和Cl-(D) Fe3+和Al3+9. 在酸性溶液中,以0.1000 mo l•L-1的Ce4+溶液滴定0.1000 mo l•L-1的Fe2+溶液,化学计量点的电位为1.06V,对此滴定最适宜的指示剂是:(A) 次甲基蓝(φo=0.53V)(B) 二苯胺磺酸钠(φo=0.84V)(C) 邻二氮菲亚铁(φo=1.06V)(D) 硝基邻二氮菲亚铁(φo=1.25V)-1pH0.0 1.0 2.0 3.0 4.0 5.0 6.0 7.0 8.0 9.0 10.0 11.0 12.0 lgαY(H)23.64 18.01 13.51 10.60 8.44 6.45 4.65 3.32 2.27 1.28 0.45 0.07 0.01(A) 3.0 (B) 4.0 (C) 5.0 (D) 6.011. Fe2+有6个3d电子,配合物[Fe(CN)6]4-的晶体场分裂能△o = 395 kJ·mol-1;电子成对能E p = 213 kJ·mol-1。