化学反应工程之反应精馏
- 格式:ppt
- 大小:997.50 KB
- 文档页数:29

反应精馏案例反应精馏是一种常见的化工分离技术,通过控制物质的沸点差异,将混合物中的组分分离出来。
在化工生产中,反应精馏被广泛应用于石油化工、化学工业和制药工业等领域。
下面我们通过一个案例来了解反应精馏的具体应用。
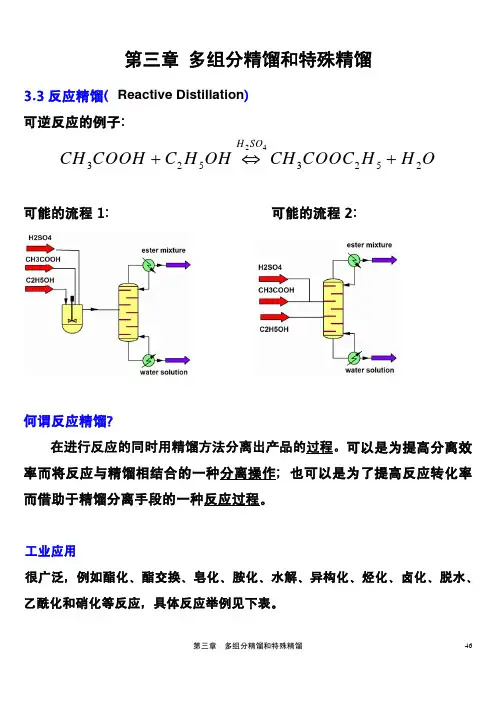
某化工厂生产苯和甲苯的混合物,需要通过反应精馏将其分离出来。
首先,在反应精馏塔中,混合物被加热至苯的沸点,苯蒸汽向上升腾,然后在塔顶冷凝成液体。
而甲苯由于沸点较高,留在塔底。
这样,苯和甲苯得以分离。
在实际操作中,反应精馏的效果受到许多因素的影响。
首先是塔内的填料选择,填料的选择会影响气液两相的接触程度,从而影响分离效果。
其次是进料的温度和压力控制,这些参数的合理选择能够提高反应精馏的效率。
此外,还需要考虑塔顶和塔底的温度和压力控制,以保证产品的纯度和收率。
在实际操作中,工艺工程师需要根据混合物的成分和性质,选择合适的操作条件和设备参数,以达到最佳的分离效果。
同时,还需要考虑能源消耗和设备维护等经济因素,以保证生产的经济效益。
反应精馏作为一种重要的分离技术,不仅在化工生产中有着广泛的应用,同时也在环保和能源领域具有重要意义。
通过对反应精馏过程的深入了解和优化,能够提高产品的质量,降低能源消耗,减少对环境的影响,从而实现可持续发展的目标。
总的来说,反应精馏作为一种重要的化工分离技术,对于提高产品质量、降低能源消耗具有重要意义。
通过合理的操作和设备选择,可以实现混合物的高效分离,从而为化工生产带来经济效益和环保效益。
希望通过本案例的介绍,能够对反应精馏技术有一个更深入的了解,为实际生产提供参考和借鉴。

反应精馏名词解释
反应精馏是一种结合了化学反应和分离过程的工艺技术。
它是在进行化学反应的同时,利用精馏的方法将反应产物从反应混合物中分离出来。
反应精馏的主要目的是利用反应热来提供精馏所需的热量,以节约能源,同时提高反应的效率和产物的纯度。
在反应精馏中,化学反应和精馏操作相互促进。
一方面,通过精馏不断移走反应的生成物,可以促使化学反应向预期的方向进行,从而提高反应的转化率和收率。
另一方面,通过加入能与被分离组分发生可逆化学反应的第三组分,可以提高其相对挥发度,使精馏过程更容易进行。
以上内容仅供参考,如需更多专业信息,建议咨询化学工程或化工工艺专家或查阅相关文献资料。

反应精馏实验报告实验目的,通过反应精馏实验,掌握精馏技术,了解反应精馏原理,提高化学实验操作能力。
实验原理,反应精馏是在精馏过程中,将反应物加入精馏瓶中,通过加热使其发生反应,然后进行精馏,从而得到产物。
这种方法适用于需要在高温下进行反应的情况。
实验仪器,反应精馏设备、精密恒温加热器、精密恒温控制仪、精密磁力搅拌器、精密温度计、精密压力计等。
实验步骤:1. 将反应精馏设备装好,连接好冷凝管和接收瓶。
2. 在精馏瓶中加入反应物,并加入适量的溶剂。
3. 装上精密恒温控制仪,设置好反应温度。
4. 打开精密恒温加热器,开始加热反应精馏瓶。
5. 在反应过程中,通过精密磁力搅拌器进行搅拌,保持反应均匀。
6. 根据产物的沸点,控制好冷凝管的温度,收集产物。
实验结果分析:通过反应精馏实验,我们成功地得到了产物,并通过测定其物理性质和化学性质,确认了产物的结构和纯度。
实验结果表明,反应精馏是一种有效的方法,可以在高温下进行反应,并得到纯净的产物。
实验结论:反应精馏是一种重要的精馏方法,它可以在反应过程中进行精馏,从而得到纯净的产物。
通过本次实验,我们掌握了反应精馏的操作技巧,加深了对反应精馏原理的理解,提高了化学实验操作能力。
实验总结:反应精馏实验是化学实验中的重要内容,通过实验可以加深对精馏技术和反应原理的理解,提高实验操作能力。
在今后的学习和工作中,我们将继续努力,不断提升自己的实验技能,为将来的科研工作打下坚实的基础。
通过本次反应精馏实验,我们不仅学会了操作反应精馏设备,还加深了对精馏原理和反应过程的理解,为今后的学习和科研工作奠定了基础。
希望在今后的实验中,我们能够继续努力,不断提高自己的实验技能,为科学研究做出更大的贡献。

反应精馏法制醋酸乙酯实验目的1.掌握反应精馏的原理及特点。
2.掌握反应精馏的操作。
3.学会塔操作过程分析。
一. 4.了解反应精馏与常规精馏的区别。
二. 5.掌握用气相色谱分析有机混合物料组成。
三. 实验原理精馏是化工生产过程中重要的单元操作, 是化工生产中不可缺少的手段, 反应精馏是精馏技术中的一个特殊领域。
在操作过程中, 化学反应与分离同时进行, 故能显著提高总体转化率。
此法在酯化、醚化、酯交换、水解等化工生产中得到应用, 而且越来越显示其优越性。
反应精馏过程不同于一般精馏, 它既有精馏的物理相变之传递现象, 又有物质变性的化学反应现象。
两者同时存在, 相互影响, 使过程更加复杂。
因此, 反应精馏对下列两种情况特别适用: (1)可逆反应。
一般情况下, 反应受平衡影响, 转化率只能维持在平衡转化的水平;但是, 若生成物中有低沸点或高沸点物存在, 则精馏过程可使其连续地从系统中排出, 结果超过平衡转化率, 大大提了效率。
(2)异构体混合物分离。
通常它们的沸点接近, 靠精馏方法不易分离提纯, 若异构体混合中某组分能发生化学反应并能生成沸点不同的物质, 这时可在反应过程中得以分离。
对醇-酸酯化反应来说, 适于第一种情况。
但该反应若无催化剂存在, 单独采用反应精馏操作也达不到高效分离的目的。
这是因为反应速度非常缓慢, 故一般都用催化反应方式, 酸是有效的催化剂, 常用硫酸。
反应随浓度增高而加快, 浓度在0.2~1.0%(wt )。
此外, 还可用离子交换树脂、重金属盐类和丝光沸石分子筛等固体催化剂。
反应精馏的催化剂用硫酸, 是由于其催化作用不受塔温度限制, 在全塔内都能进行催化反应, 而应用固体催化剂则由于存在一个最适宜的温度, 精馏塔本身难以达到此条件, 故很难实现最佳化操作。
本实验是以乙酸和乙醇为原料、在酸催化剂作用下生成乙酸乙酯的可逆反应。
反应的化学方程式为:O H H COOC CH OH H C COOH CH 2523SOH 52342+−−→←+ 实验的进料有两种方式: 一是直接从塔釜进料;另一种是在塔的某处进料。

实验一反应精馏合成乙酸乙酯一实验目的1 了解反应精馏过程原理及适用场合.2 掌握反应精馏装置的操作方法和反应精馏研究方法。
3 了解反应精馏与常规精馏的区别。
4 学会用色谱-热导检测器分析塔内物料浓度组成。
二实验原理反应精馏法是将化学反应过程与精馏分离过程同时进行生产产品的操作。
由于物理过程与化学过程同时存在,使过程更加复杂。
(1)对可逆平行反应,通过精馏将反应产物中的高沸物或低沸物连续的从系统中排出,可使总转化率超过平衡转化率,大大提高生产效率。
(2)对于异构体混合物分离比较困难时,若其中的某组分能发生化学反应并生成沸点不同的物质,就可以加以分离。
本实验用乙酸、乙醇为原料,加入少量浓硫酸为催化剂通过反应精馏合成乙酸乙酯。
边反应边将乙酸乙酯分离出来,提高乙酸的转化率。
操作方式:间歇过程;塔釜连续进料过程;塔身某处连续进料过程。
产物分析方法:采用色谱-热导检测分析,色谱工作站处理。
GDX分离柱(φ3mm,L 2m) , 柱温110度,汽化温度130度,检测温度120度;载气压力0.04Mpa;桥流100mA.出峰的先后顺序为:H2O , CH3CH2OH , CH3COOH ,CH3COOC2H5.它们的摩尔校正因子分别为:3.03, 2.09, 1.39, 0.91。
三实验装置与试剂反应精馏装置一套,直径20mm, 内装填料,可自动加热、保温、回流控制。
操作过程见说明书。
无水乙醇200mL ;含浓硫酸0.3%(wt)的冰乙酸200mL.四实验步骤1 配置1:1.3(mol)酸醇混合液250mL,加入到塔釜中。
并用色谱准确测其组成。
2 开启色谱-热导检测分析仪及色谱工作站,按分析方法操作。
3 通冷却水,接通电源。
按操作说明书对反应精馏装置加热升温,并开启保温电流。
待塔顶有液体出现时,全回流30分钟。
以微量注射器在塔身不同高度取样口取样分析,作出塔内各组分的浓度分布曲线。
4 开启回流比3:1 ,塔顶开始出产品。



化学反应工程与工艺专业实验讲义实验一反应精馏合成乙酸乙酯一实验目的1了解反应精馏过程原理及适用场合.2掌握反应精馏装置的操作方法和反应精馏研究方法。
3了解反应精馏与常规精馏的区别。
4学会用色谱-热导检测器分析塔内物料浓度组成。
二实验原理反应精馏法是将化学反应过程与精馏分离过程同时进行生产产品的操作。
由于物理过程与化学过程同时存在,使过程更加复杂。
(1)对可逆平行反应,通过精馏将反应产物中的高沸物或低沸物连续的从系统中排出,可使总转化率超过平衡转化率,大大提高生产效率。
(2)对于异构体混合物分离比较困难时,若其中的某组分能发生化学反应并生成沸点不同的物质,就可以加以分离。
本实验用乙酸、乙醇为原料,加入少量浓硫酸为催化剂通过反应精馏合成乙酸乙酯。
边反应边将乙酸乙酯分离出来,提高乙酸的转化率。
操作方式:间歇过程;塔釜连续进料过程;塔身某处连续进料过程。
产物分析方法:采用色谱-热导检测分析,色谱工作站处理。
GD某分离柱(φ3mm,L2m),柱温110度,汽化温度130度,检测温度120度;载气压力0.04Mpa;桥流100mA.出峰的先后顺序为:H2O,CH3CH2OH,CH3COOH,CH3COOC2H5.它们的摩尔校正因子分别为:3.03,2.09,1.39,0.91。
三实验装置与试剂反应精馏装置一套,直径20mm,内装填料,可自动加热、保温、回流控制。
操作过程见说明书。
无水乙醇200mL;含浓硫酸0.3%(wt)的冰乙酸200mL.四实验步骤1配置1:1.3(mol)酸醇混合液250mL,加入到塔釜中。
并用色谱准确测其组成。
2开启色谱-热导检测分析仪及色谱工作站,按分析方法操作。
3通冷却水,接通电源。
按操作说明书对反应精馏装置加热升温,并开启保温电流。
待塔顶有液体出现时,全回流30分钟。
以微量注射器在塔身不同高度取样口取样分析,作出塔内各组分的浓度分布曲线。
4开启回流比3:1,塔顶开始出产品。
当塔顶温度有明显变化时,停止出料,降温冷却,直到塔内液体全部流入塔釜。


化学工程实验之反应精馏一、反应精馏对于化工过程常见的可逆反应体系,可以通过将反应与蒸馏耦合在一个多功能的过程中而使其性能得到大大改进,这种藕合被称之为“反应蒸馏”。
与非反应蒸馏过程相比,这种组合的优点是可以打破反应平衡的限制,进而取得较高的反应物转化率,反应热可被蒸馏原位利用,避免使用辅助溶剂,共沸物或近沸点混合物可被较容易地分离;同时这种方法可直接提高过程的效率并降低设备投资及操作费用。
二、实验目的1.掌握在指定条件下,计算可逆反应平衡转化率的方法,巩固对反应热力学分析方法的学习结果;2.利用反应蒸馏塔合成高纯的乙酸甲酯产品,掌握相关的实验技能;3.掌握利用气相色谱仪分析样品组成的方法;4.通过利用分离手段强化反应过程的这一成功范例,启发利用反应与分离过程耦合开发新型反应过程,并深化对新型反应器的认识。
三、实验内容1.计算在指定反应条件,如进料配比、反应温度及微正压条件下利用甲醇与乙酸生成乙酸甲酯和水酯化反应的乙酸平衡转化率;2.反应蒸馏塔以接近化学计量比的甲醇和乙酸进料,在指定的反应温度及微正压条件下合成高纯的乙酸甲酯产品;3.利用配备有TCD检测器的气相色谱仪,对塔顶馏出的甲醇与水的混合物及塔底的高纯乙酸甲酯产品进行分析检测,并根据分析数据计算乙酸甲酯产品的收率;4.对比在相同条件下计算的乙酸甲酯平衡收率与实验测定的乙酸甲酯产品收率数据,分析利用反应蒸馏技术对甲醇与乙酸生成乙酸甲酯和水酯化反应过程的强化效果。
本次实验我们考察的是:进料位置对产品中各组分浓度的影响四、实验装置图1. 反应精馏装置示意图五、实验步骤5.1实验开始前准备1.检验装置所处的房间是否有良好的通风以及消防设施,确保在设备运行期间,房间内不存在易燃、易爆的气体,不得有其它明火、热源。
2.检验设备电源是否已正确连接上,检查各仪表显示是否正常。
3.进行气密性试验。
将塔釜、乙酸原料罐、乙醇原料罐、塔顶产品贮罐以及塔底产品贮罐等的进口、出口阀门全部关闭,放空安全阀均关闭。
反应精馏生产甲缩醛一、实验原理主反应: CH2O+2CH3OH(CH3-O-CH2-O-CH3+H2O 副反应: 2CH3OH→CH3-O-CH3+H2O主反应是可逆反应, 其平衡常数比较小, 为了增大反应物的转化率, 需要把产物及时地移出体系。
而反应精馏技术就是把反应和精馏两个过程耦合在一个体系中的工艺过程, 以精馏分离促进反应的进行, 有效解决了反应平衡常数小, 转化率低的问题。
由于反应器和分离设备的耦合, 既减少了设备投资, 又降低了反应、分离过程的能耗。
在这个反应体系中, 主反应在常压, 50到80℃, 强酸性离子交换树脂催化下即可进行。
而副反应活化能较高, 需要150℃下发生反应。
本体系可基本不考虑副反应对主反应的影响。
二、实验装置实验装置如图所示, 甲醛溶液从反应精馏塔反应段上部进料, 甲醇从反应段下部进料, 反应段为强酸性离子交换树脂, 经精馏后塔顶得到产品是甲缩醛, 塔底得到水。
三、实验步骤1.标定甲醛进料泵和甲醇进料泵的流量2.甲醇和甲醛摩尔配比为2.5: 1, 换算成体积比, 按得到数值进料3.为使甲醛转化更为彻底, 先往塔内加入适量甲醇, 使塔内甲醇和甲醛摩尔比远大于2。
4.再沸器中注入容积量的4/5的去离子水, 开启加热, 塔底温度设置为100℃。
5.当反应段上部温度大于90℃时, 打开冷凝, 同时开始进料。
6.控制回流比为2, 塔顶采出甲缩醛, 塔底出水。
7、待塔顶温度稳定在42℃时, 从反应区各段取样, 分析其组成, 并记录下各段温度。
8、实验结束后, 先关加热, 待塔温降下来之后关掉冷凝水。
四、实验数据处理五、注意事项1.甲醛易挥发, 且刺激性很强, 在甲醛进料时注意通风。
2、塔底温度不能过高, 否则气量太大, 容易引起液泛。
3.甲醇、甲醛的进料量和塔本身生产能力相匹配。
第4章特殊精馏技术了盐增强萃取精馏的作用,又克服了固体盐的回收和输送问题,目前已在工业上得到了应用。
工业应用实例有二:(1)醇一水物系的分离在乙醇、丙醇、丁醇等与水的混合液中,大多数存在着共沸物,采用加盐萃取精馏可实现预期的分离效果。
以乙醇一水共沸物体系作为研究对象,选用乙二醇作溶剂,在溶剂中加入氯化钙或乙酸钾等盐类,形成混合萃取剂制取无水乙醇,并进行了工业试验。
日产量达6~7t无水乙醇装置,以乙二醇加乙酸钾为混合萃取剂,与国外乙二醇萃取精馏方法比较,加盐后溶剂比减少为原来的1/4~1/5,节省了操作费用,减少了设备投资。
这种形式的加盐精馏流程示意图见图4—34。
目前工业上应用加盐萃取精馏分离乙醇一水抽取无水乙醇的规模为5000t/a,叔丁醇一水体系的分离已有3500t/a的中试装置。
(2)酯一水物系的分离图4—34加盐精馏流程示意图酯一水物系也是形成共沸物的系统。
传统的分离方法是共沸精馏。
近年来利用加盐萃取精馏提纯乙酸乙酯的研究已取得进展。
4.4反应精馏化工生产中,经常要遇到先进行化学反应而后将反应产物进行精馏分离的操作过程。
在反应器中为了使床层温度趋于等温并使反应向产物方向转移,就必须借助换热方式将反应热从床层中移动。
而精馏过程则又必须供给塔底物料一定的热量。
为了更好地利用反应热,传统的做法是将其用于精馏的再沸器中,使反应系统和精馏系统的能量得以部分平衡,以节约加热工程热负荷并同时减小冷却工程的冷负荷。
然而对于可逆反应,如果能利用精馏技术及时移去反应区的产物,就能使反应向产物方向移动,使反应放热与精馏的需热局部平衡,从而可达到产品分离及节能诸方面的效益。
反应精馏是进行反应的同时用精馏方法分离出产品的过程,当有催化剂存在时的反应精馏叫作催化精馏。
反应精馏进行的基本条件是化学反应的可逆性和物系有较大的相对挥发度,而且反应的温度压力条件应与精馏过程相近。
在反应精馏中,按照反应与精馏的关系可分为两种类型,一种是利用精馏促反应,另一种是利用反应促进精馏分离。