高效液相色谱法测定复方甘草酸单铵S氯化钠注射液中的甘草酸单铵S的含量
- 格式:pdf
- 大小:113.55 KB
- 文档页数:2

高效液相色谱法测定清肺颗粒中甘草酸的含量摘要:目的:建立高效液相色谱测定清肺颗粒中甘草酸含量的方法。
方法:采用C18色谱柱(4.6×250mm,5μm),流动相为乙腈-0.1%磷酸溶液(27:73),检测波长为254nm,流速为1.0mL/min,柱温为30℃。
结果:甘草酸质量浓度与峰面积在0.05~1.60μg之间呈良好的线性关系(r=0.9998),平均回收率为98.3%,相对标准偏差(RSD)为2.1%(n=6)。
结论:本方法简便、准确、重现性好,可用于清肺颗粒中甘草酸的含量测定。
引言:清肺颗粒是一种用于治疗肺热咳嗽的中药制剂,甘草酸是其主要活性成分之一。
准确测定清肺颗粒中甘草酸的含量对于保证其疗效和质量控制具有重要意义。
目前,已有一些方法应用于甘草酸的含量测定,如紫外-可见分光光度法、气相色谱法等。
这些方法存在着某些不足之处,如分析时间长、精密度不高等。
本研究旨在建立一种高效液相色谱法测定清肺颗粒中甘草酸含量的方法,以满足其质量控制的需求。
实验部分:1. 仪器和试剂- 仪器: 高效液相色谱仪、紫外-可见分光光度计、电子天平等。
- 试剂: 甘草酸(药典标准品)、清肺颗粒样品、乙腈、磷酸等。
2. 样品制备将清肺颗粒样品取10g,加入50mL乙腈中,超声提取30分钟,离心3分钟,取上清液,用乙腈定容至50mL,摇匀,毛细管动态消除内标法测定甘草酸含量。
3. 色谱条件- 色谱柱: C18色谱柱(4.6×250mm,5μm)。
- 流动相: 乙腈-0.1%磷酸溶液(27:73)。
- 检测波长: 254nm。
- 流速: 1.0mL/min。
- 柱温: 30℃。
讨论:本方法简便、准确、重现性好,可用于清肺颗粒中甘草酸的含量测定。
该方法具有快速、灵敏度高、稳定性好等优点,适用于清肺颗粒的质量控制和生产中甘草酸成分的含量测定。

HPLC法单波长同时测定六味甘草丸中甘草苷和甘草酸铵摘要: 目的建立HPLC法单波长同时测定六味甘草丸中甘草苷和甘草酸铵的含量。
方法采用色谱柱EClipse XDB-C18柱(4.6×250mm,5μm),柱温30℃,流动相为以乙腈为流动相A,以0. 05%磷酸溶液为流动相B,进行梯度洗脱;检测波长为237nm。
理论板数按甘草苷峰计算应不低于5000。
结果该方法甘草苷线性范围为0.025~0.250 μg (r=0.9999),平均加样回收率为99.78% ,RSD=1.19% (n=6);甘草酸铵线性范围为0.208~2.08μg(r=0.9998),平均加样回收率为99.33% ,RSD=1.41% (n=6);结论所建方法准确、简便、灵敏、可靠,可用于该制剂的质量控制。
关键词:高效液相色谱法;单波长;六味甘草丸;甘草苷;甘草酸铵Simultaneous determination of six kinds of licorice pill ofliquiritin and glycyrrhizic acid ammonium single wavelength HPLC methodAbstract: Objective To establish the determination of six kinds of licorice pill of liquiritin and glycyrrhizic acid ammonium single wavelength HPLC method.Methods the chromatographic column was EClipse XDB-C18 column (4.6 × 250 mm, 5μm), temperature 30℃, mobile phase with acetonitrile as mobile phase A, with 0.05% phosphoric acid solution as mobile phase B, gradient elution; the detection wavelength was237nm.The number of theoretical plates should not be less than 5000 according to the calculation of liquiritin peak.Results the method of liquiritin linear range was 0.025~0.250 μg (r=0.9999), the average recovery was 99.78%, RSD=1.19% (n=6); ammonium glycyrrhizinate linear range was 0.208~2.08μg (r=0.9998), the averagerecovery was 99.33%, RSD=1.41% (n=6); conclusion the method is accurate, simple, sensitive, reliable, can be used for the quality control of the preparation.Keywords: high performance liquid chromatography; single wavelength; six kinds of licorice pill; glycyrrhizin; glycyrrhizinic acid ammonium藏药六味甘草丸由甘草、木瓜、酸藤果、藏茴香、芫荽果、炒大米等六味中藏药材组成。
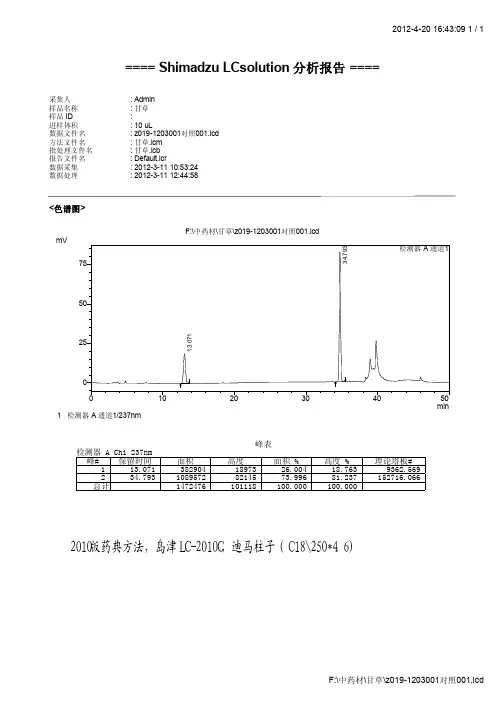
==== Shimadzu LCsolution 分析报告 ====<色谱图>采集人: Admin 样品名称: 甘草 样品 ID :进样体积: 10 uL数据文件名: z019-1203001对照001.lcd 方法文件名: 甘草.lcm 批处理文件名: 甘草.lcb 报告文件名: Default.lcr数据采集: 2012-3-11 10:53:24数据处理: 2012-3-11 12:44:58峰表检测器 A Ch1 237nm 峰# 1 2 总计保留时间 13.071 34.793 面积 382904 1089572 1472476高度 18973 82145 101118面积 % 26.004 73.996 100.000高度 % 18.763 81.237 100.000理论塔板# 9362.569 152716.0662010版药典方法,岛津LC-2010C,迪马柱子(C18\250*4.6)<色谱图>采集人: Admin 样品名称: 甘草 样品 ID :进样体积: 10 uL数据文件名: z019-1203001样品001.lcd 方法文件名: 甘草.lcm 批处理文件名: 甘草.lcb 报告文件名: Default.lcr数据采集: 2012-3-11 9:02:15数据处理: 2012-4-6 10:27:20峰表检测器 A Ch1 237nm 峰# 1 2 总计保留时间 12.888 34.610 面积 389234 224463 613697高度 19026 15225 34251面积 % 63.424 36.576 100.000高度 % 55.548 44.452 100.000理论塔板# 8817.325 142790.8822010版药典方法,岛津LC-2010C,迪马柱子(C18\250*4.6)==== Shimadzu LCsolution 分析报告 ====<色谱图>峰表检测器 A Ch1 237nm 峰# 1 总计保留时间 13.177 面积 1272159 1272159高度 63328 63328面积 % 100.000 100.000高度 % 100.000 100.000理论塔板# 9621.9662010版药典方法,岛津LC-2010C,迪马柱子(C18\250*4.6)<色谱图>采集人: Admin 样品名称: 甘草 样品 ID :进样体积: 10 uL数据文件名: z019-1203001样品001.lcd 方法文件名: 甘草.lcm 批处理文件名: 甘草.lcb 报告文件名: Default.lcr数据采集: 2012-3-11 9:02:15数据处理: 2012-4-6 10:27:20峰表检测器 A Ch1 237nm 峰# 1 2 总计保留时间 12.888 34.610 面积 389234 224463 613697高度 19026 15225 34251面积 % 63.424 36.576 100.000高度 % 55.548 44.452 100.000理论塔板# 8817.325 142790.882。

HPLC同时测定复方甘草片中吗啡和甘草酸铵摘要:目的:采用高效液相色谱法同时测定复方甘草片中的吗啡和甘草酸铵的含量。
方法:采用Waters C18(5μm×4.6mm×250mm)色谱柱,流动相为乙腈-0.02%磷酸梯度洗脱,流速1.0mL·min,检测波长为吗啡220nm、甘草酸铵250nm。
结果:吗啡、甘草酸铵的峰面积与质量的线性关系良好(r>0. 9996);加样回收率为分别为98.73%,99.53%。
结论:该方法可用于复方甘草片中吗啡、甘草酸铵2个成分快速检验。
关键词:复方甘草片;HPLC;吗啡;甘草酸铵复方甘草片为保护性祛痰镇咳药,临床上用于一般性咳嗽及上呼吸道感染、急性气管炎初期等的咳嗽治疗,能有效缓解症状,疗效确切且经济实惠。
其主要是由甘草浸膏粉、罂粟果提取物粉等组成的复方制剂,质量标准收载于《中国药典》2015年版二部[1]。
现行标准分别对组方成分阿片粉或罂粟果提取物粉中吗啡及甘草浸膏粉中甘草酸铵采用不同的系统进行含量测定,其中吗啡含量测定需采用固相萃取小柱进行预处理,操作烦琐,易产生误差;甘草酸含量测定流动相系统含盐量高,色谱柱损耗快。
二者所用色谱柱类型也不同,吗啡用C8柱,甘草酸铵用C18柱。
本方法采用高效液相色谱法法同时测定甘草酸和吗啡的含量,实现一侧多评。
方法简便、快捷、准确、环保、重复性好,对快检初筛该药品质量提供重要的依据。
1 仪器与试药Waters e2695高效液相色谱仪、XS105 型电子天平对照品:吗啡(批号:171201-201123,含量97.1%)、甘草酸铵(批号:110731-201418,含量93.1%),均购自中国食品药品检定研究院;乙腈(色谱纯,Fisher Scientific,美国);甲醇(分析纯,天津市康科德科技有限公司);磷酸(分析纯,天津佳兴化工玻璃仪器工贸有限公司);水为娃哈哈纯净水。
2 溶液的制备2.1 对照品溶液制备分别精密称取吗啡对照品0.01034g、甘草酸铵对照品0.01109g,置同一100ml量瓶中,加入50%甲醇溶液适量溶解并稀释至刻度,摇匀,即得。


高效液相色谱法测定清肺颗粒中甘草酸的含量高效液相色谱(HPLC)是一种常用的分析技术,广泛应用于药物、化学品、食品、环境等领域中药物和其他化合物的定量分析。
本文将介绍如何使用HPLC方法测定清肺颗粒中甘草酸的含量。
一、仪器和试剂1. 仪器:HPLC仪器,包括色谱柱、色谱室、泵、检测器等。
2. 试剂:甘草酸标准品、乙腈、水、磷酸二氢钾。
二、色谱条件的优化1. 选择合适的色谱柱:通常使用C18柱,柱长为250 mm,柱内径为4.6 mm。
2. 流动相:优化流动相的组成和流速,一般使用乙腈和水为流动相,可以逐渐调整乙腈的含量,流速一般为1 mL/min。
3. 检测波长:甘草酸的最大吸收波长为254 nm,因此选择254 nm作为检测波长。
4. 注射量:通常为10 μL。
三、样品制备1. 取清肺颗粒适量,粉碎并过筛,取得粒度均匀的样品。
2. 取一定量的清肺颗粒样品,加入适量的乙腈进行提取,震荡摇匀,然后离心10 min,将上清液置于离心管中。
3. 上清液进行滤过,滤液采用0.45 μm的微孔过滤膜进行过滤。
四、建立药物标准曲线1. 取甘草酸的标准品,加入足够的乙腈稀释得到一系列不同浓度的标准溶液。
2. 依次取标准溶液进行注射,记录其峰面积。
3. 绘制标准曲线,以峰面积为纵坐标,甘草酸浓度为横坐标。
五、样品测定1. 将样品的提取液进行适当稀释,并进行过滤。
2. 取一定量的稀释好的样品注入色谱柱,记录峰面积。
3. 根据标准曲线计算得到甘草酸的含量。
六、质量控制为保证测定结果的准确性和可靠性,需要进行质量控制。
1. 重复性:选取相同样品进行多次测定,比较结果的变异系数。
2. 平行实验:选取相同样品进行平行测定,比较结果的一致性。
3. 准确度:通过加标回收率试验,向样品中添加不同浓度的标准品,测定其回收率,以验证方法的准确性。
七、结果与讨论根据测定得到的甘草酸含量,可以与药典标准或其他文献报道进行比较,评估清肺颗粒质量。

甘草酸系列产品质量标准中文通用名甘草酸A英文通用名GlycyrrhizicAcidA标准号WS-10001-(HD-0506)-2002药品名称甘草酸A药品英文名GlycyrrhizicAcidA 主要成分本品按干燥品计算,含甘草酸(C42H62O16)不得少于95.0%。
处方性状本品为白色结晶性粉末,无臭,有特殊甜味。
鉴别取本品0.2g,加水5ml,盐酸3ml蒸馏,于蒸馏液中滴加2,4-二硝基苯肼乙醇试液2~3滴,产生橙红色沉淀。
检查干燥失重取本品1.0g,在80℃真空干燥8小时,减失重量不得过6.0%(中国药典2000年版二部附录VIIIL)。
炽灼残渣取本品1.0g依法检查(中国药典2000年版二部附录VIIIN),遗留残渣不得超过0.2%。
重金属取炽灼残渣项下遗留的残渣,依法检查(中国药典2000年版二部附录VIIIH第二法),含重金属不得过百万分之二十。
砷盐取本品1.0g,依法检查(中国药典2000年版二部附录VIIIJ第一法),应符合规定(0.0002%)。
含量测定取本品40mg,精密称定,置100ml量瓶中,加稀乙醇溶解并稀释至刻度,摇匀。
精密量取稀释液10ml,置100ml量瓶中,加稀乙醇溶解并稀释至刻度,摇匀,照分光光度法(中国药典2000年版二部附录IVA),在252nm的波长处测定吸收度,按甘草酸(C42H62O16)的吸收系数(E1%1cm)为141计算。
类别抗溃疡病药。
作用与用途/功能与主治/适应证用法与用量注意规格贮藏遮光,密封保存。
有效期暂定3年曾用名起草单位新疆天山制药工业有限公司复核单位新疆区药品检验所出处化学药品地方标准上升国家标准(第六册)中文通用名甘草酸二钾英文通用名DipotaiumGlycyrrhetate标准号WS-10001-(HD-0507)-2002药品名称甘草酸二钾药品英文名DipotaiumGlycyrrhetate主要成分本品按无水物计算,含甘草酸二钾(C42H60K2O16)不得少于75.0%。

高效液相色谱法测定清肺颗粒中甘草酸的含量高效液相色谱法(HPLC)是一种常用的分析技术,广泛应用于药物分析、环境监测、食品安全等领域。
清肺颗粒是一种中药制剂,甘草酸是其主要有效成分之一。
本文将介绍利用HPLC法测定清肺颗粒中甘草酸含量的方法。
一、实验目的利用HPLC法测定清肺颗粒中甘草酸的含量,为其质量控制提供依据。
二、仪器与试剂1. 仪器:HPLC仪器(型号可根据实际情况选择)2. 试剂:甘草酸标准品、乙腈、甲醇、磷酸溶液三、实验步骤1. 仪器准备:打开HPLC仪器,进行系统的准备和平衡,检查色谱柱状态和流动相系统。
2. 样品准备:取清肺颗粒中的甘草酸部分,粉碎成粉末。
3. 样品提取:取一定量的清肺颗粒粉末,加入一定体积的乙腈,超声提取一定时间,离心后取上清液。
4. 色谱条件:色谱柱为C18柱,流动相为甲醇-磷酸溶液(pH=3.0)混合物,流速为1.0 mL/min,检测波长为254 nm。
5. 建立标准曲线:取不同浓度的甘草酸标准品,用HPLC法分别测定,并绘制标准曲线。
6. 样品测定:将清肺颗粒中甘草酸提取液用HPLC法进行测定,并根据标准曲线计算出甘草酸的含量。
7. 数据处理:记录实验数据,计算甘草酸的含量。
四、结果与讨论通过HPLC法测定清肺颗粒中甘草酸的含量,得出了相应的数据。
根据标准曲线计算出清肺颗粒中甘草酸的含量为X%,符合药典规定。
根据实验结果,可以看出HPLC法能够准确、快速地测定清肺颗粒中甘草酸的含量,具有很高的灵敏度和选择性。
HPLC法可作为清肺颗粒甘草酸含量的分析方法,为其质量控制提供了有效手段。
五、结论本文利用HPLC法成功测定了清肺颗粒中甘草酸的含量,结果准确可靠。
该方法简便、快捷,适用于清肺颗粒的质量控制及相关研究。
HPLC法的应用拓宽了中药制剂中有效成分含量的分析手段,为中药制剂的研究与开发提供了更多的选择和支持。
HPLC法的应用将有助于提高清肺颗粒等中药制剂的质量和安全性,对推动中药现代化进程具有积极意义。

食品安全国家标准食品添加剂甘草酸铵1 范围本标准适用于原料为甘草(豆科植物甘草Glycyrrhiza uralensis Fisch.、胀果甘草Glycyrrhiza inflata Bat.及光果甘草Glycyrrhiza glabra L.),经水浸提、硫酸(或盐酸)酸化沉淀、乙醇浸提、氨化、结晶等工艺制得的食品添加剂甘草酸铵。
2 化学名称、结构式、分子式、相对分子质量2.1 化学名称甘草酸铵2.2 结构式2.3 分子式C42H61O16NH42.4 相对分子质量839.96(按2007年国际相对原子质量)3 技术要求3.1 感官要求:应符合表1 的规定。
表1 感官要求项目要求检验方法色泽白色、黄白色或浅黄色取适量试样置于清洁、干燥的白瓷盘中,在自然光线下,观察其色泽和状态状态粉末状细小颗粒3.2 理化指标:应符合表2的规定。
表2 理化指标项目指标检验方法甘草酸铵含量(以18β-甘草酸铵计,以干基计), w/%≥65.0 附录A中A.4干燥减量,w /%≤7.0 附录A中A.3比旋光度︒20][Dα/[(°)·mL·dm-1·g-1]+45~+53 附录A中A.5灰分,w /% ≤0.5 附录A中A.6 铅(Pb)/(mg/kg)≤ 2 GB 5009.12总砷(以As计)/(mg/kg)≤ 2 GB/T 5009.11甘草酸铵甘草酸铵甘草酸铵甘草酸铵附 录 A检验方法A.1 一般规定本标准所用试剂和水,在没有注明其他要求时,均指分析纯试剂和GB/T 6682-2008规定的三级水。
实验中所用溶液在未注明用何种溶剂配制时,均指水溶液。
A.2 鉴别试验 A.2.1 方法提要铵盐遇强碱后产生氨,利用氨的挥发性和碱性能使试管上方湿润的pH 试纸显碱性颜色的特性,鉴别铵盐的存在。
A.2.2 试剂和材料A.2.2.1 氢氧化钠溶液:40 g/L 。
A.2.2.2 pH 试纸。

2012-2013学年第二学期药用植物资源与开发论文名称甘草化学成分的提取与分离年级2010学院中药材学院专业植物科学与技术学号07107216姓名徐玉强任课教师张永刚完成时间2013-5-11甘草中化学成分的提取与分离摘要:本文主要介绍了甘草中主要的化学成分以及这些化学成分的含量和性质,并简述了甘草酸,甘草次酸和甘草甘的提取和有效成分的含量测定,为进一步的生产实践做出贡献。
关键词:甘草化学成分提取正文:甘草属于豆科甘草属,以根和根状茎入药。
甘草在我国集中分布于三北地区(东北、华北和西北各省区),而以新疆、内蒙古、宁夏和甘肃为中心产区。
随着药学及其相关学科以及科研设备的发展,甘草中主要含有的甘草酸、甘草次酸、黄酮、生物碱和氨基酸等化学成分,具有广泛的生物活性。
一、化学成分药用甘草质量与其化学成分的组成、积累变化有直接的关系。
先后从甘草属植物中提取、分离、鉴定了200多种化学成分,涉及甘草属植物10个种。
其中最重要并已证实具有生物活性的成分主要是甘草酸等三萜皂苷类、黄酮类、香豆素类、多糖、生物碱、氨基酸等。
三萜皂苷类化合物:甘草属植物中三萜皂类成分具有量高、生理活性强的特点,甘草的许多药理作用都与这类成分有直接关系。
至今在甘草属植物中已鉴定得到61种三萜类化合物,其中苷元45个。
这些三萜类化合物其苷元均为 3 B - 经基齐墩果烷型化合物的衍生物;皂苷一般为3B -羟基上的氧苷,糖元多为D- 葡萄糖酸或D-葡萄糖。
甘草酸一直被认为是甘草中最重要三萜类化合物,《中国药典》把甘草酸的量作为评价甘草药材及其制品质量的重要指标,通常要求不低于2%。
黄酮类成分:是近年来研究最活跃的天然活性成分之一,广泛存在于植物界中。
这类化合物的存在对植物生长、发育、开花、结果以及抵御异物的侵入起着重要的作用。
目前,从甘草属植物中已发现黄酮及其衍生物153种,它们的基本母核结构类型有15种,其中包括:黄酮、黄酮醇、双氢黄酮、双氢黄酮醇、查尔酮、异黄酮、双氢异黄酮、异黄烷、异黄烯等。

RP-HPLC柱前衍生法测定复方甘草酸铵S分散片的含量周海婴
【期刊名称】《吉林医学》
【年(卷),期】2009(030)012
【摘要】目的:建立复方甘草酸铵S分散片中甘氨酸和蛋氨酸的高效液相分析方法.方法:采用柱前衍生化高效液相色谱法测定复方甘草酸铵S分散片中两种氨基酸含量.结果:复方甘草酸铵S分散片中甘氨酸浓度为10.58~39.68 mg/ml,蛋氨酸浓度为10.44~39.15mg/ml,线性关系良好,r>0.99,RSD<1.0%,加样回收率为99%.结论:用HPLC柱前衍生方法测定复方甘草酸铵S分散片中甘氨酸及蛋氨酸含量的方法可行.
【总页数】3页(P1165-1167)
【作者】周海婴
【作者单位】湖南省长沙市宁乡县人民医院药剂科,湖南,长沙,410600
【正文语种】中文
【中图分类】R9
【相关文献】
1.柱前衍生RP-HPLC法测定仙鹤草中氨基酸含量 [J], 赵岩;赵天琦;徐殿文;郜玉钢;蔡恩博;刘双利;杨鹤;张连学
2.柱前衍生-RP-HPLC法测定蜂王幼虫冻干粉中16种氨基酸含量 [J], 李智;祁龙凯;林励;李静;黎香梅;邝燕珍
3.柱前衍生化RP-HPLC法测定L-叔亮氨酸含量 [J], 陈亭亭;黄金;陈蔚青;王普
4.RP-HPLC柱前衍生化法测定壳聚糖喷雾剂盐酸氨基葡萄糖含量 [J], 朱志灵;张勋;马迟;张松柏;徐伟;陈頲;林羽
5.RP—HPLC柱前衍生法测定复方甘草酸铵S分散片的含量 [J], 周海婴
因版权原因,仅展示原文概要,查看原文内容请购买。
甘草中有效成份的含量测定作者:李可鑫来源:《中国科技博览》2013年第27期论文摘要:目的建立同时测定甘草中甘草酸、甘草苷和异甘草素含量的方法。
方法采用高效液相色谱法对甘草粉末的67%甲醇提取物进行分析。
用C18反相色谱柱,1%磷酸水-乙腈梯度洗脱,对不同色谱峰分别采用248、276、360、370 nm紫外波长检测。
结果甘草酸的回归方程为Y=1×106X+16 220,r2=1;甘草苷的回归方程为Y=2×106X+49 444,r2=0.999 5;异甘草素的回归方程为Y=1×107X+4.466 7,r2=1。
甘草酸、甘草苷和异甘草素的加样回收率分别为98.01%、102.63%、98.18%。
结论本方法准确、稳定、可靠,可用于甘草中甘草酸、甘草苷和异甘草素3种成分的同时测定。
关键词:甘草含量测定中图分类号:S567.7+1在甘草质量研究中,建立稳定可靠的甘草多种成分含量测定非常必要。
甘草酸、甘草苷、异甘草素是甘草中代表性成分,甘草酸是皂苷类代表,甘草苷是黄酮类代表,而异甘草素是一种异黄酮类成分。
1 仪器与试药Agilent 1100型高效液相色谱仪(配有G1314A紫外检测器、1315B DAD检测器、G1311A 四元梯度泵、G1322A在线脱气装置、G1316A柱温箱);Agilent 1100化学工作站;Sartorius BS110S 1/万、BP211D 1/(10万)电子分析天平;KL3120D超声清洗机。
甘草Glycyrrhiza uralensis Fisch. 3年生采自甘肃总寨,1~5年生采自内蒙古杭锦旗,由北京中医药大学王文全教授鉴定。
60 ℃干燥过夜并粉碎。
甘草酸、甘草苷、异甘草素对照品(批号分别为060520、061009、060801)由上海康九化工公司提供(供含量测定用)。
乙腈为色谱纯;水为市售娃哈哈纯净水;甲醇、甲酸、磷酸、冰醋酸为分析纯。
高效液相色谱法测定清肺颗粒中甘草酸的含量清肺颗粒是一种中药制剂,由多种草药组成,具有清热解毒、润燥化痰的作用。
甘草酸是其中的一种主要活性成分,具有抗炎、镇痛、抗过敏等多种药理作用。
对清肺颗粒中甘草酸的含量进行测定具有重要的临床意义。
目前,常用的方法是采用高效液相色谱法(HPLC)进行测定。
本实验就是应用该方法,测定清肺颗粒中甘草酸的含量。
准备样品。
将清肺颗粒取出适量,粉碎并过筛,取其中约0.2g的粉末样品,加入20mL甲醇中,超声提取30分钟,放置室温静置30分钟,用0.45μm微孔过滤膜滤过,取上清液备用。
然后,进行色谱分析。
色谱柱采用Agilent TC-C18色谱柱(4.6mm×250mm,5μm)。
流动相为甲醇-0.1%磷酸溶液(30:70,体积比),流速为1.0mL/min。
检测波长为240nm,柱温恒温恒定为25℃。
进样量为20μL。
在上述条件下,进行清肺颗粒样品的HPLC测定。
利用标准曲线法进行定量分析,选用甘草酸标准品制备4个不同浓度的标准溶液,分别为12.5μg/mL、25μg/mL、62.5μg/mL、125μg/mL。
将这些标准溶液按照前述方法进行HPLC测定,得到峰面积与浓度的线性关系。
再将清肺颗粒中甘草酸的浓度计算出来。
根据测得的样品峰面积,利用标准曲线计算甘草酸的浓度。
根据样品的回收率,计算清肺颗粒中甘草酸的含量。
经过以上步骤,测定了清肺颗粒中甘草酸的含量。
该方法简便、准确、灵敏,适用于清肺颗粒的质量控制和临床研究。
需要注意的是,高效液相色谱法测定甘草酸含量时,可能存在某些干扰物质的影响。
在实际操作中,需要对样品进行适当的前处理,如超声提取、滤过等,以减少干扰物质的干扰。
还应注意保持色谱柱的良好状态,避免杂质附着。
为了确保测定结果的准确性和可靠性,建议重复测定多个样品,并比较结果的一致性。
注射用复方甘草酸单铵S与转化糖电解质溶液配伍的微粒测定与分析陈晓;谢学建;蒋凤【期刊名称】《中国药业》【年(卷),期】2014(000)013【摘要】目的:测定注射用复方甘草酸单铵S分别配伍转化糖电解质溶液、转化糖溶液和0.9%氯化钠注射液的不溶性微粒数。
方法模拟临床用药浓度,依据2010年版《中国药典(二部)》规定的不溶性微粒检查法光阻法测定复方甘草酸单铵S与转化糖电解质溶液配合后的不溶性微粒数量。
结果转化糖溶液和0.9%氯化钠注射液与其配伍液的不溶性微粒数量未超过2010年版《中国药典(二部)》标准,转化糖电解质与复方甘草酸单铵S配伍明显超过标准,且长时间存放后出现絮状沉淀。
结论转化糖电解质与复方甘草酸单铵S配伍可导致微粒超标,两者间存在配伍禁忌,临床应避免混合配伍。
%Objective To measure the number of insoluble particles in the compatibility solutions between Compound Ammonium gly-cyrrhetate S Injection with Invert Sugar Electrolytes Solution, Invert Sugar Solution and 0. 9% Sodium Chloride respectively. Methods By simulating the clinical medication concentration, the detection was performed according to the insoluble particles detection by the light blockage method stipulated by the 2010 edition of the Chinese Pharmacopoeia. Results The insoluble particles in the compatibility solution of Invert Sugar Solution and 0. 9% Sodium Chloride Solution did not exceed the standard in the 2010 edition of the Chinese Pharmacopoeia,which in the compatibility solutions of Invert Sugar Electrolytes Solution and Compound Ammonium glycyrrhetate S Injec-tion significantly exceeded the standard in the 2010 edition of Chinese Pharmacopoeia, moreover the flocculent precipitation appeared af-ter long time storage. Conclusion The compatibility of Invert Sugar Electrolytes Solution and Compound Ammonium glycyrrhetate S In-jection can cause particles exceeding the standard, the incompatibility exists between them, so this mixing compatibility should be avoid-ed in clinic.【总页数】2页(P16-16,17)【作者】陈晓;谢学建;蒋凤【作者单位】中国人民解放军南京军区南京总医院,江苏南京 210002;中国人民解放军南京军区南京总医院,江苏南京 210002;中国人民解放军南京军区南京总医院,江苏南京 210002【正文语种】中文【中图分类】R969.2;R975+.5【相关文献】1.注射用转化糖电解质与注射用痰热清临床观察存在配伍禁忌 [J], 李卫平;刘高明;朱莉2.注射用夫西地酸钠与转化糖电解质注射液存在配伍禁忌 [J], 秦立珍;张万玲3.RP-HPLC考察注射用更昔洛韦钠在转化糖注射液及转化糖电解质注射液中配伍的稳定性 [J], 郑芳;吴红菱;刘慧敏;朱雪松4.注射用二丁酰环磷腺苷钙与转化糖电解质注射液的配伍稳定性及辅助用药管理对策研究 [J], 王静;王钦;高捷;徐新;殷晓芹;陈伯华5.转化糖电解质注射液与注射用奥美拉唑配伍出现浑浊现象的原因分析与建议 [J], 刘莉因版权原因,仅展示原文概要,查看原文内容请购买。