盐酸四环素溶液的配制方法
- 格式:doc
- 大小:27.00 KB
- 文档页数:2

盐酸四环素【药品名称】通用名称:盐酸四环素英文名称:Tetracycline Hydrochloride【适应症】本品对淋病奈瑟菌具一定抗菌活性,但耐青霉素的淋球菌对四环素也耐药。
本品对弧菌、布鲁菌属、弯曲杆菌、耶尔森菌等革兰阴性菌抗菌作用良好,对铜绿假单胞菌无抗...【禁忌】1.对本品过敏者禁用;2.儿童禁用;3.老人慎用;4.孕妇及哺乳期妇女禁用。
4.孕妇禁用。
【注意事项】1.交叉过敏反应对一种四环素类药物呈过敏者可对其他四环素类药物呈现过敏;2.对诊断的干扰:(1)测定尿邻苯二酚胺(Hingerty法)浓度时,由于四环素对荧光的干扰,可使测定结果偏高;(2)本品可使碱性磷酸酶、血尿素氮、血清淀粉酶、血清胆红素、血清氨基转移酶(AST、ALT)的测定值升高;3.长期用药期间应定期随访检查血常规以肾功能;4.下列情况存在时须慎用或避免应用:(1)由于本品可致肝损害,因此原有肝病者不宜用此类药物;(2)由于本品可加重氮质血症,已有肾功能损害不宜应用此类药物,如确有指征应用时须慎重考虑,并调整剂量;5.治疗性病时,如怀疑同时合并螺旋体感染,用药前须行暗视野显微镜检查及血清学检查,后者每月1次,至少4次;6.由于较长时间静脉给药有发生血栓性静脉炎的可能,故应在病情许可时尽早改为口服给药。
【特殊人群用药】儿童注意事项:儿童禁用。
妊娠与哺乳期注意事项:孕妇禁用。
老人注意事项:老人慎用。
【批准文号】国药准字H64020206【生产企业】企业名称:宁夏启元药业有限公司生产地址:宁夏银川市望远工业园启元大道1号。

'£朽知库环境工程学报第15卷第3期2021年3月Vol. 15, No.3 Mar. 2021Eco-Environmental Knowledge Web C hinese Journal of Environmental Engineering@(010) 62941074文章栏目:水污染防治DOI 10.12030/j.cjee.202008112 中图分类号X701.3 文献标识码A丁丽丹,周家斌,刘文博,等.Cu0/Bi203光催化耦合过一硫酸盐氧化降解盐酸四环素[J].环境工程学报,2021. 15(3): 898- 910.DING Lidan, ZHOU Jiabin, LIU Wenbo, et al. Oxidative degradation of tetracycline hydrochloride by Cu0/Bi203 photocatalysis coupling with peroxymonosulfate[J]. Chinese Journal of Environmental Engineering, 2021, 15(3): 898-910.C u0/B i203光催化耦合过一硫酸盐氧化降解盐酸 四环素丁丽丹、周家斌刘文博\陈新2,冯芹芹2,杨玉玲\张天磊11. 西南石油大学化学化工学院,成都6105002. 武汉理工大学资源与环境工程学院,武汉430070第一作者:丁丽丹(1995—),女,硕士研究生。
研究方向:水处理高级氧化技术。
E-mail: ***************** *通信作者:周家斌(1972—),男,博士,教授。
研究方向:环境功能材料与污染控制:E-mail: ****************摘要利用共沉淀-浸渍法合成了基于可见光响应的Cu0/Bi203复合催化剂,并对其光催化活化过一硫酸盐 (PM S)去抗生素盐酸四环素(TC-HC1)的性能进行了探究。

微生物发酵技术任务三四环素的提取和精制四环素的提取和精制微生物发酵技术可以利用微生物进行四环素的生产,但随着生产的增加,四环素的提取和精制也变得至关重要。
下面分别介绍四环素的提取和精制的过程。
四环素的提取:
1. 收获发酵液:在微生物发酵过程中,四环素被生产并分泌到发酵液中,因此第一步是收获发酵液。
2. 沉淀菌体:将发酵液离心,得到细菌沉淀。
3. 提取四环素:将沉淀后的菌体用有机溶剂(如丙酮或甲醇)进行提取,得到含有四环素的有机相。
4. 沉淀杂质:将有机相加入酸性溶液(如盐酸中和的水),使得四环素变成更易沉淀的固体形式,然后进行高速离心,将其它溶剂、杂质和菌体析出。
5. 精制四环素:将沉淀物用另一种有机溶剂进行溶解和分离,再次重复沉淀、溶解和分离等步骤,直至得到纯化的四环素。
四环素的精制:
1. 沉淀菌体:与四环素的提取过程相同。
2. 提取四环素:与四环素的提取过程相同。
3. 过滤:将提取后的有机相过滤(如通过具有小的孔径的滤网),去除溶剂和杂质。
4. 洗涤:将过滤后的固体用一些有机溶剂进行洗涤,使其更加纯净。
5. 干燥:将洗涤后的固体在有利的条件下(如低温、低湿度)进行干燥,以便保存和使用。

盐酸四环素废水处理方法研究1 引言 (Introduction)四环素类抗生素 (Tetracyclines) 是由放线菌产生的一种广谱抗生素,广泛应用于医药行业、畜牧业和水产养殖业.四环素类抗生素的生产和使用量目前位居全球抗生素类第二然而,在使用过程中,四环素仅有部分被动物体吸收并发生代谢,其余抗生素仍然以活性形式 (母体或代谢产物) 随粪便和尿液排出体外,对生态系统和人类的健康造成极大的危害.因此,控制和降低盐酸四环素在环境中的残留已经引起了环境科学界乃至公众的广泛关注.吸附法是抗生素废水处理较为经济、简便的方法之一.然而,在实际操作过程中,吸附剂的性质、操作条件 (如温度、pH) 等都会影响吸附效果,且传统吸附剂材料存在着吸附量低、易团聚、极易产生二次污染、分离困难和循环性差等瓶颈问题.针对上述问题,近年来有研究表明,Fenton反应技术与吸附耦合可有效解决吸附剂饱和后的再生难题.该路线可在常温、常压下进行,反应条件温和,再生吸附剂过程可通过调剂H2O2浓度实现调控,吸附位点可实现原位再生.例如,研究了TiO2@酵母炭微球吸附有机染料及其原位再生,再生实验结果显示通过光催化再生反应,富集刚果红和亚甲基蓝的TiO2@酵母炭微球得到了很好的原位再生效果研究了Fe3O4@沙棘枝炭吸附去除强力霉素及其非均相Fenton氧化再生,再生实验通过构造非均相Fenton反应体系,使得表面富集有强力霉素的Fe3O4@沙棘枝炭吸附剂可实现有效再生,重复使用.海藻酸钠 (Sodium Alginate) 因具有原材料来源广泛且易于提取、表面具有丰富的化学吸附位点、吸附速率高及不会对环境造成二次污染的特点,成为目前研究中广泛应用的一种优良的吸附剂.因此,海藻酸钠不仅能够处理含有重金属离子的废水,其衍生物还在医药行业中有所应用.例如, 通过构建类Fenton体系,使得海藻酸钠/Fe@Fe3O4壳核纳米结构高效去除诺氟沙星.近年来多项研究证实,以海藻酸钠为基体,负载金属离子,可使得海藻酸钠的吸附功能和金属离子的催化功能在微观尺度上得到耦合.例如,研究了海藻酸钙包覆纳米Ni/Fe颗粒用于同时去除水中铜离子和氯苯.研究了海藻酸锰固定化细胞的乙醇发酵,结果表明, 海藻酸锰比海藻酸钙耐磷酸盐能力高、固定化细胞稳定.然而,将海藻酸钠螯合金属锰离子作为类Fenton催化剂用于废水处理的研究还未有报道.基于上述考虑,本研究以海藻酸钠为基体,螯合金属锰离子后制备了Mn@海藻酸微球复合吸附剂,并对其进行FE-SEM、FT-IR表征,将其应用在吸附处理盐酸四环素模拟废水中.随后,以表面吸附富集盐酸四环素的Mn@海藻酸微球为类Fenton体系的催化剂,在加入H2O2后,构建形成类Fenton体系,实现废水中盐酸四环素的氧化降解,最终达到吸附剂的再生和循环.研究结果可为含有盐酸四环素废水的处理提供理论依据,且研究具有重要的参考价值.2 实验部分 (Experiment) 2.1 试剂与仪器实验仪器:TDL-60B-W台式高速离心机 (湖南星科仪器有限公司); 752N紫外可见分光光度计 (上海精密科学仪器有限公司); 多功能磁力搅拌器 (杭州仪表电机厂); TE124S电子天平 (赛多利斯科学仪器 (北京) 有限公司);pH计 (上海精密仪器厂); Hitachi S-4800冷场发射扫描电镜; 101-1AB恒温干燥箱 (天津泰斯特仪器有限公司); DZF-6050真空干燥箱 (上海一恒科学仪器有限公司).实验试剂:海藻酸钠 ((C5H7O4COONa)n,CR) 购自天津市东丽区天大化学试剂厂;硫酸锰 (MnSO4,AR) 购自天津永昊精细化工有限公司;乙醇 (C2H5OH,AR) 购自天津市富宇精细化工有限公司;盐酸四环素购自阿拉丁化学股份有限公司,结构式见图 1.实验用水为蒸馏水,所有试剂均为分析纯.图 1 盐酸四环素结构式2.2 吸附剂的制备准确称取一定量的海藻酸钠溶解在蒸馏水溶液中形成2.5% (W/V) 的海藻酸钠溶液,恒温磁力搅拌0.5 h,待用.称取一定量的硫酸锰,加入到上述的海藻酸钠溶液中,得到硫酸锰/海藻酸钠混合溶液 (混合体系中硫酸锰的浓度为0.05 mol·L-1),恒温磁力搅拌1 h,静置10 h.反应后的溶液经过离心机分离,把固体沉淀物用蒸馏水和乙醇反复冲洗.冲洗后的沉淀物烘干,制得Mn@海藻酸微球复合吸附剂.2.3 吸附实验常温常压下,pH为6时,在250 mL锥形瓶中加入一定量的Mn@海藻酸和盐酸四环素溶液,每隔一段时间吸取10 mL样品进行离心分离,取上清液于波长370 nm处测其吸光度,单位吸附量 (Qe,mg·g-1) 及去除率 (η) 可有下列公式计算得出:(1)(2)式中,Qe为达到平衡时的平衡吸附量 (mg·g-1);η为相对应的去除率;C0和Ce分别为四环素的初始浓度和吸附平衡时的平衡浓度 (mg·L-1);V为溶液体积 (L);m是加入的吸附剂质量 (g).用同样的方法探究不同条件下Mn@海藻酸对盐酸四环素的吸附性能.且待样品分析完毕,立即倒入反应体系.2.4 Mn@海藻酸微球复合吸附剂的原位再生把50 mg复合吸附剂加入到50 mL的10 mg·L-1盐酸四环素溶液中,pH为6,室温搅拌0.5 h, 待吸附平衡后测定溶液的吸光度,计算溶液中盐酸四环素的去除率.然后用离心机分离Mn@海藻酸和上清液,吸附剂用蒸馏水清洗干净,烘干后于同体积、同浓度、同pH 的盐酸四环素溶液中,加入1 mL 30%的H2O2,构建类Fenton体系,使吸附在Mn@海藻酸微球上的盐酸四环素氧化降解,反应2 h之后,再次离心.沉淀物用蒸馏水洗净之后,来处理50 mL的10 mg·L-1pH为6的盐酸四环素溶液,测定溶液的吸光度并计算吸附率.按此方法循环3次.3 结果与讨论 (Results and discussion) 3.1 Mn@海藻酸微球的形成及结构表征海藻酸钠吸附金属Mn2+的形成见图 2.海藻酸钠固体颗粒加入水中之后,在水溶液中发生水解反应,生成小分子的M单元和G单元.G单元中羧基位于碳/碳/氧的三角形的顶上,比M单元具有更大的活性.当溶液中加入Mn2+后,Mn2+与海藻酸钠G单元经过协同作用相结合,海藻酸钠分子链与链之间通过Mn2+的相互作用而形成三维的网络结构.在这个三维网络结构中,Mn2+占据了中间的亲水空间,同时Mn2+与G单元上的多个O原子之间发生螯合作用,导致链与链之间结合的更加紧密,协同作用更加强烈,最终形成稳定的三维网络结构(Fang et al., 2007).图 2 海藻酸钠微球吸附Mn2+形成图海藻酸钠微球、Mn@海藻酸微球及其表面选择区域的FE-SEM和EDS如图 3所示.图 3a 是海藻酸钠微球的形貌,该微球为实验制备的空白平行样.从图中可以看出其具有明显的球形度,分散性好,且破损较少,说明海藻酸钠微球具有较好的机械强度.海藻酸钠微球的尺寸分布均匀,直径范围为 (40±0.5)~(60±0.5) μm.图 3b是一个放大了的海藻酸钠微球,可以清楚的看到样品保持了海藻酸钠的球形形态,表面粗糙.图 3d是Mn@海藻酸微球的FE-SEM照片,可以看出Ma@海藻酸钠微球大小较均匀, 直径范围为 (23±0.5)~(35±0.5) μm, 较海藻酸钠微球直径减小了约42%,这是由于锰离子与海藻酸钠发生螯合作用,海藻酸钠大分子中间的亲水空间被多价金属离子占据,使得海藻酸链间结合得更紧密,协同作用更强.图 3e是一个典型的Mn@海藻酸微球,样品保持了海藻酸钠球形形貌,表面光滑.采用EDS对海藻酸钠微球 (图 3c) 和Mn@海藻酸微球 (图 3f) 的元素成分进行分析,结果表明在Mn@海藻酸微球的EDS能谱中出现了锰的衍射峰,说明锰离子已经成功的负载到海藻酸钠微球上.图 3 海藻酸钠微球 (a, b)、Mn@海藻酸微球 (d, e) 的SEM及EDS (c, f) 分析反应得到的海藻酸钠微球和Mn@海藻酸微球复合吸附剂的FT-IR结果见图 4.海藻酸钠表面具有丰富的羧基 (—COOH) 官能团和羟基 (—OH) 官能团.具体表现在图 4曲线a和b 的FT-IR中,1000~1200 cm-1处为C—O的伸缩吸收峰 (Ryu et al., 2010);1500~2000 cm-1和1200~1500 cm-1处分别为CO和CC振动吸收峰 (Shin et al., 2008).波数范围在3000~3700 cm-1为羟基或者羧基内的羟基 (O—H) 的伸缩振动吸收峰,而波数范围在2500~3000 cm-1为C—H伸缩振动吸收峰 (Rakshit et al., 2013).从海藻酸钠微球和Mn@海藻酸微球复合吸附剂的红外谱图对比可以看出,曲线a中O—H的吸收峰较曲线b中的吸收峰向低波数区移动,这是因为羟基上的氧原子与Mn2+之间发生了螯合作用,使得O—H的弯曲振动吸收减弱;C—H面内弯曲振动吸收峰向低波数区移动,这是因为海藻酸钠大分子链之间的螯合作用形成了网状结构,使得C—H吸收峰较弱.因此,当溶液中加入Mn2+后,海藻酸钠大分子链上的氧原子与Mn2+发生螯合作用,形成了稳定的网状结构,即“蛋盒”结构.图 4 Mn@海藻酸钠微球 (a)、海藻酸微球 (b) 的FT-IR分析3.2 吸附时间及初始浓度的影响图 5为0.1 g Mn@海藻酸微球处理50 mL初始浓度分别为5、8、11、14、17 mg·L-1盐酸四环素废水的吸附曲线.图 5 初始浓度和时间对Mn@海藻酸微球吸附盐酸四环素效果的影响从图中可以看出,系统在2.5 h之后达到平衡状态,吸附剂对盐酸四环素的吸附量随着盐酸四环素浓度的增加 (从5 mg·L-1增加到17 mg·L-1) 而增大 (从3.575 mg·g-1增加到10.404 mg·g-1).这是因为当盐酸四环素浓度增加时,溶液与吸附剂之间的作用力逐渐增强,盐酸四环素小分子与吸附剂表面的有效碰撞次数增多 (Chen et al. , 2013).吸附过程分为2个吸附阶段,即前期的快速吸附阶段和后期的缓慢吸附阶段.在吸附开始的50 min内,Mn@海藻酸微球对盐酸四环素分子的吸附速率较快,吸附量增大显著.50 min后,随着时间的延长,吸附剂和盐酸四环素分子之间的相互排斥且位阻效应逐渐增强,吸附剂表面剩余的空位点很难被占据,使得吸附趋势变缓,最终2.5 h后逐渐达到吸附平衡状态 (Ma et al., 2012).3.3 pH的影响向一系列锥形瓶中加入50 mg的Mn@海藻酸微球复合吸附剂,来处理50 mL浓度为8 mg·L-1的盐酸四环素溶液,分别调节pH值分别为2、3、4、5和6(因为盐酸四环素溶液在碱性溶液中颜色加深,因此本文不讨论其在碱性条件下的吸附性能),每隔一段时间吸取10 mL溶液进行离心分离,测其吸光度.溶液pH与平衡吸附量Qe及去除率η的关系如图 6所示.图 6 pH对Mn@海藻酸微球吸附盐酸四环素效果的影响从图中可以看出,Mn@海藻酸微球复合吸附剂对盐酸四环素的吸附受pH影响较大,平衡吸附量和去除率均随着pH值的增大而增大,当酸性较强时不利于吸附反应的进行.随着pH 值的增大,吸附剂对盐酸四环素的平衡吸附量从0.938 mg·g-1(pH=2) 增加到6.178 mg·g-1(pH=6),去除率从9.38% (pH=2) 增大至61.78% (pH=6).这是因为吸附剂表面电性、盐酸四环素电离程度和离子存在形式受pH影响较大 (Chang et al., 2012).酸性较强时,盐酸四环素以阳离子TCH3+的形式存在,Mn@海藻酸微球吸附剂上的氧基官能团也带正电荷,因此,吸附剂和盐酸四环素之间主要以静电斥力为主,使得吸附反应较弱 (邹星等, 2011).然而,随着酸性的减弱,盐酸四环素以两性离子形式存在溶液中,吸附剂与盐酸四环素分子之间的静电斥力逐渐减弱,吸附作用逐渐增强 (Wang et al., 2010).由图 6可知,强酸不利于Mn@海藻酸微球吸附盐酸四环素.3.4 吸附动力学在同温同压下,通过改变盐酸四环素溶液的初始浓度,按照相同的实验操作步骤,测定溶液平衡浓度和平衡吸附量,并用Origin软件拟合吸附等温曲线.再利用准一级 (式 (3))、准二级 (式 (4)) 动力学方程及颗粒内扩散模型对Mn@海藻酸微球复合吸附剂吸附盐酸四环素的机理进行分析.(3)(4)式中,k1和k2分别为准一级动力学 (min-1) 和准二级动力学 (g·mg-1·min-1) 的速率常数,Qt为任意t时刻的吸附量 (mg·g-1).速率常数k1可由ln (Qe-Qt) 对t作图的斜率求得,k2可由t/Qt对t作图的截距求得 (图 7).从图 7可以看出,在不同浓度的盐酸四环素溶液中,准二级动力学明显优于准一级动力学拟合出的线性关系.图 7 盐酸四环素在Mn@海藻酸微球上的吸附动力学 (a.准一级动力学; b.准二级动力学)通过实验所得的吸附动力学平衡吸附量及相关参数如表 1所示.Qcal和Qexp分别代表平衡吸附量的理论值与实际值.表 1 不同初始浓度下盐酸四环素的吸附动力学参数由表 1可知,准二级动力学模型的可决系数明显高于准一级动力学模拟的可决系数.准二级动力学模型的可决系数均在0.98以上,最大值为0.996, 准一级动力学模型的系数范围在0.945~0.981之间.且准二级动力学模型计算出的吸附量与理论值更为接近.因此,Mn@海藻酸微球复合吸附剂对盐酸四环素的吸附过程更加复合准二级动力学模型,拟合效果较好.本文在准二级动力学模型拟合的基础上,进一步探讨了利用颗粒内扩散模型来拟合Mn@海藻酸微球对盐酸四环素的吸附速率.颗粒内扩散方程表示为:(5)式中,kid为颗粒内扩散的速率常数 (mg·g-1·min-1/2),常数C表示为与边界层厚度有关的常数,通常,C值越大,表示边界层效应越大.kid和C可通过Qt对t0.5作图的斜率和截距求得.图 8为不同浓度的盐酸四环素在Mn@海藻酸微球上的颗粒内扩散拟合.从图 8可以看出,颗粒内扩散拟合出的直线均未通过坐标原点,说明吸附速率不是仅由颗粒内扩散控制的,边界层扩散作用对吸附速率也有一定的影响.从拟合曲线可以看出,整个吸附过程可分为2个线性阶段.第1阶段为吸附初始阶段,吸附过程主要为表面吸附和边界层扩散,吸附速率较快.随着吸附反应的进行,第2阶段为颗粒内的扩散.随着溶液中剩余盐酸四环素浓度的降低,吸附剂表面空位点较少,而已经吸附在吸附剂表面上的盐酸四环素分子向Mn@海藻酸微球的内部扩散,吸附速率较慢,吸附反应逐渐达到平衡状态.图 8 不同浓度的盐酸四环素在Mn@海藻酸微球上的颗粒内扩散拟合表 2为颗粒内扩散拟合结果.数据显示,第1阶段扩散速率常数kid1值均高于第2阶段速率扩散常数kid2值.说明随着吸附反应时间的延长,Mn@海藻酸微球吸附剂表面孔道被大量的盐酸四环素分子占据,吸附剂的吸附速率降低.同时,常数C随着浓度的增大而增大.说明随着盐酸四环素溶液浓度的增加,边界层吸附的厚度逐渐增大,边界层效应的影响也随之增大.表 2 不同初始浓度颗粒内扩散模型拟合结果3.5 吸附等温线在相同的温度和压力下,改变溶液中盐酸四环素的初始浓度,测定溶液的平衡浓度和平衡吸附量,并对吸附等温曲线进行拟合.Langmuir (式 (6)) 和Freundlich (式 (7)) 吸附等温方程成为近年来被广泛使用的吸附模型来探索吸附机理.本文按照Langmuir和Freundlich吸附等温方程对Mn@海藻酸微球吸附盐酸四环素的数据进行非线性拟合.(6)(7)式中,Qmax为吸附剂的单层饱和吸附量 (mg·g-1),b为Langmuir常数 (L·mg-1),表示吸附亲和力, Kf表示吸附能力平衡常数,n代表不均匀系数.Freundlich吸附等温方程是一个经验公式,其n值越大,吸附性能越好.一般认为1/n在0.1~0.5之间,容易吸附;1/n 大于2时吸附较难进行.图 9为常温下Mn@海藻酸微球吸附剂吸附盐酸四环素的吸附等温线.图 9 常温下盐酸四环素的吸附等温线由图 9和表 3可知,Langmuir吸附等温模型的可决系数为0.978,较Freundlich吸附等温模型 (可决系数为0.922) 能更好的说明Mn@海藻酸微球吸附剂吸附盐酸四环素的吸附过程,拟合更为合理.同时,Freundlich模型拟合出的常数1/n小于0.5,吸附易于发生,表明盐酸四环素易被Mn@海藻酸微球吸附.为了验证吸附过程是否满足优惠吸附,引入无量纲分离因子RL,表达式见式 (8).(8)表 3 等温吸附拟合结果式中,RL为分离系数,表示吸附过程的性质,0 < RL < 1,表示吸附过程为优惠吸附;RL > 1则表示吸附过程不是优惠吸附;RL=1,吸附过程能够可逆进行;RL=0,则为不可逆吸附.通过对实验所得数据计算,RL为0.161,说明Mn@海藻酸微球对盐酸四环素的吸附为优惠吸附.3.6 吸附热力学为了考察温度对吸附过程的影响,向锥形瓶中加入制得的Mn@海藻酸微球0.1 g,处理浓度8 mg·L-1的盐酸四环素废水50 mL.在T=293.15、298.15、303.15、308.15、313.15、318.15 K下进行进行吸附试验.吸附过程中的热力学参数如吉布斯自由能变 (ΔG)、焓变(ΔH) 和熵变 (ΔS) 可通过如下方程得到:(9)(10)(11)式中,Kd是扩散系数,ΔH0是焓变 (kJ·mol-1),ΔS0是熵变 (J·mol-1·K-1), ΔG0为吉普斯自由能 (kJ·mol-1),T是开尔文温度 (K),R是理想气体常数 (8.314 J·mol-1·K-1).lnKd对1/T作图,可分别由斜率和截距求得ΔH0和ΔS0.ΔG0由式 (11) 求得.所得结果见表 4.由表中结果可知,ΔG0为负值,在-20到0 kJ·mol-1之间,吸附主要通过物理作用进行,作用力以范德华力为主 (Guan et al., 2011),吸附的发生主要为自发反应.同时,随着温度的升高,ΔG0的绝对值也随之增大,表明吸附过程受温度的影响显著.ΔH0小于40 kJ·mol-1,物理吸附占主导.说明该吸附过程为吸热反应 (Li et al., 2010).Mn@海藻酸微球吸附盐酸四环素的ΔH0为37.5 kJ·mol-1,表明盐酸四环素与Mn@海藻酸微球的吸附机理为物理吸附 (Saha et al., 2010).ΔS0为正值说明吸附过程不可逆,且随着吸附的进行,Mn@海藻酸微球表面吸附了大量的盐酸四环素分子,盐酸四环素周围的水分子逐渐减少,自由水分子增多,固液界面混乱度增加.表 4 Mn@海藻酸微球吸附盐酸四环素的热力学参数3.7 吸附剂的原位再生Fe和Mn等3 d轨道过渡金属具有相似的化学性质,Fe2+和H2O2反应产生羟基自由基的反应于1894年被称为Fenton反应.其他过渡金属如Mn等也已被证实可以参与类Fenton 反应 (Kasprzak, 2002;Liochev, 1999).许多文献报道,在Mn和帕金森氏症相互关系的研究下,Mn可表现出促氧化损伤活性 (Yamada et al., 1986; Gerlach et al., 1994).本文采用H2O2-Mn2+协同作用构建类Fenton体系再生方法,实验结果如图 10所示.从图 10可以看出,Mn@海藻酸微球复合吸附剂吸附盐酸四环素的初始吸附率为83.2%,吸附率随着循环次数的增加而降低.第3次循环结束时,未经再生的Mn@海藻酸微球复合吸附剂对溶液中盐酸四环素的吸附率下降至23%.这是因为随着吸附循环次数越多,吸附剂表面的活性位点逐渐被盐酸四环素分子占据,使得吸附剂的吸附能力逐渐减弱 (Kyzas, 2012).加入H2O2后,体系中H2O2和Mn@海藻酸微球构成类Fenton体系,经协同作用再生的吸附剂对盐酸四环素溶液的吸附率在循环3次后能达到59%,比未再生的Mn@海藻酸微球的吸附率高36%.这是由于Mn2+与H2O2构成类Fenton体系,Mn2+为反应体系提供了催化剂,加速了H2O2的分解.图 10 Mn @海藻酸微球吸附剂再生实验Mn2+与H2O2的反应主要包括3个阶段 (方茹等, 2007; 于怀东等, 2005;Yim et al., 1990).第1阶段为二价锰离子在H2O2的作用下生成三价锰离子和羟基自由基,见反应式(12).此时,Mn2+周围富集的盐酸四环素分子与羟基自由基不断反应,生成CO2和H2O及一些矿物酸.第2阶段为海藻酸钠表面富集的盐酸四环素分子不断向Mn2+周围移动,促进反应的进行.随着反应的进行,H2O2与羟基自由基反应生成的超氧阴离子O2·-.第3阶段为三价锰离子在超氧阴离子的作用下还原成二价锰离子,促使体系继续反应,且整个体系反应时间较长,并有持续的·OH产生,见反应式 (13)、(14).(12)(13)(14)另外,H2O2本身是一种强氧化剂,一方面其可作为电子受体俘获电子而产生羟基自由基;另一方面,H2O2本身可吸收电子产生羟基自由基 (·OH),反应体系中·OH的浓度增加,促进反应的进行.羟基自由基可氧化几乎所有的有机物,并在1O2的作用下生成CO2和H2O,反应式如下:(15)(16)(17)(18)(19)(20)体系中具有强氧化性的氧基基团与有机物发生的氧化反应是整个盐酸四环素降解的重要的步骤,海藻酸钠的吸附性能有效地为H2O2-Mn2+类Fenton作用提供较高的底物浓度,提高再生反应速率,促进有机物的降解.催化剂的再生过程依据反应动力学可分为吸附、迁移和降解3个过程,该反应过程远高于海藻酸钠直接吸附并降解的过程,因此,Mn@海藻酸复合催化剂在Mn2+和H2O2的协同作用下,提高了对污染物的去除率,同时实现有机物的降解和吸附剂的再生的目的,且再生效果良好.4 结论 (Conclusions)1) 以海藻酸钠为基体,通过加入Mn2+制备了Mn@海藻酸微球复合吸附剂.复合吸附剂保持了海藻酸钠的球体形貌, 表面光滑, 颗粒分布均匀,粒径约为 (23±0.5)~(35±0.5) μm,分散度好.2) 以盐酸四环素废水为处理对象,探讨了初始浓度、pH、吸附时间对吸附去除性能的影响.结果发现,强酸不利于吸附,吸附量随着盐酸四环素初始浓度的增大而增加.吸附初始阶段为吸附速率较快的外表面吸附,吸附第2阶段为吸附速率较慢的颗粒内扩散吸附.体系在2.5 h后逐渐接近吸附平衡状态.同时,通过对准一级、准二级吸附动力学模拟,表明吸附剂的吸附过程更符合准二级动力学方程.吸附过程可用Langmuir型等温模型拟合,0 < RL < 1说明该吸附过程易于进行.通过热力学模拟,表明吸附剂吸附盐酸四环素的过程是自发进行的,主要为物理吸附.具体参见污水宝商城资料或更多相关技术文档。


抗生素溶液配制
使用时,均按照1:1000稀释:
A、硫酸卡那霉素配制(50mg/ml)
(1)在10mL蒸馏水中溶解1g 硫酸卡那霉素后,用蒸馏水定容至20mL;
(2)在超净工作台中,用0.22μm滤器过滤至新的无菌管;
(3)分装成2mL小份贮存于-20℃。
B、氨苄青霉素配制(100mg/ml)
(1)在10mL蒸馏水中溶解2g氨苄青霉素后,用蒸馏水定容至20mL;
(2)在超净工作台中,用0.22μm滤器过滤至新的无菌管;
(3)分装成2mL小份贮存于-20℃。
C、氯霉素配制(25mg/ml)
(1)在8mL无水乙醇中溶解0.25g氯霉素后,定容至10mL;
(2)在超净工作台中,用0.22μm滤器过滤至新的无菌管;
(3)分装成2mL小份贮存于-20℃。
注:氯霉素见光分解会变黄,出现橘色沉淀。
D、四环素配制(10mg/ml)
(1)在8mL无水乙醇中溶解0.1g无碱的四环素后(或溶解四环素盐酸盐于水中),定容至10mL;
(2)在超净工作台中,用0.22μm滤器过滤至新的无菌管;
(3)分装成2mL小份贮存于-20℃。
注:四环素见光易分解,应避光保存。

高岭石对盐酸四环素的吸附模型与热力学研究摘要:基于高岭石是土壤中广泛分布着的黏土矿物之一,采用批处理实验方法开展高岭石对盐酸四环素(TC)的吸附性能研究,着重考查TC初始浓度、支撑电解质和温度等因素的影响。
研究结果表明:高岭石对TC的吸附非常符合Freundlich等温吸附模型,并呈现显著的非线性特征;且在pH=3的酸性条件下,TC浓度升高到一定程度(>60 mg/L),TC在高岭石上的吸附得到进一步增强。
同时温度显著地影响高岭石对TC的吸附,表现为温度促进TC在高岭石上的吸附。
此外,电解质加入显著影响高岭石对TC的吸附。
因此,静电作用对TC在高岭石上的吸附起着重要贡献。
关键词:高岭石;盐酸四环素;吸附;热力学参数A study on adsorption model and thermodynamics for tetracycline ontokaoliniteAbstrast:Based on kaolinite (Kt) that is one of widespread clay mineral in soil, the batch experiment methods were applied to explore the adsorption nature of Kt for tetracycline, with emphasis on the influences of initial TC concentration, background electrolytes, and reaction temperature on the adsorption. The obtained results showed that adsorptions of Kt for TC can be well fitted to Freundlich model, representing highly nonlinear adsorption characteristics. However, under conditions at stronger acidic medium pH (pH=3), there existed further improved TC adsorption onto kaolinite as is selected the much more increase of initial TC concentration, up to 60 mg/L and higher. Meanwhile, temperature factor can greatly influence the TC adsorption, where the temperature promotes the TC adsorption. As to background electrolytes, they can also evidently affect the TC adsorption. Hence, the electrostatic interactions involving hydrogen bonding significantly contribute to TC adsorption onto kaolinte.Key words: Kaolinte; tetracycline; adsorption; thermodynamic parameters.当前我国多种抗生素被广泛应用,主要作为动物饲料添加剂用于来防治动物疾病。
实验四:加速实验法测定药物的有效期4 实验学时:实验类型:综合实验要求:分光度计法测定药物有效期一、实验目的应用化学动力学的原理和方法,采用加速实验法测量不同温度下药物的反1.应速率,根据阿伦尼乌斯公式,计算药物在常温下的有效期。
掌握分光光度计的测量原理及应用。
2.二、实验内容 1. 加速法测定不同温度下药物反应速率。
根据动力学方法计算药物在常温下的有效期。
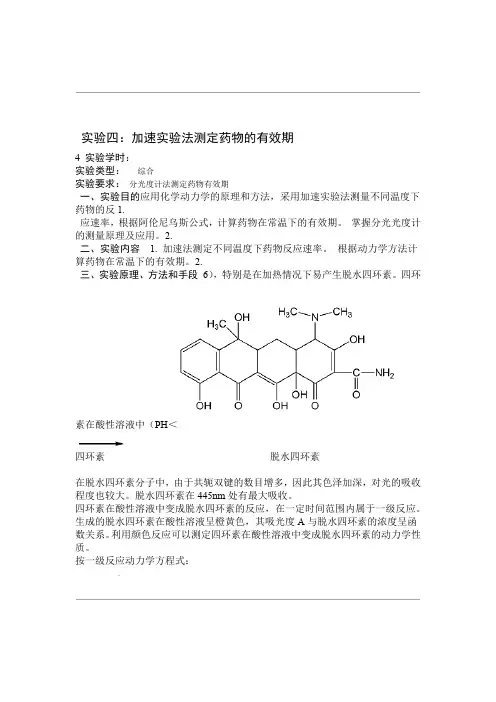
2.三、实验原理、方法和手段6),特别是在加热情况下易产生脱水四环素。
四环素在酸性溶液中(PH<四环素脱水四环素在脱水四环素分子中,由于共轭双键的数目增多,因此其色泽加深,对光的吸收程度也较大。
脱水四环素在445nm处有最大吸收。
四环素在酸性溶液中变成脱水四环素的反应,在一定时间范围内属于一级反应。
生成的脱水四环素在酸性溶液呈橙黄色,其吸光度A与脱水四环素的浓度呈函数关系。
利用颜色反应可以测定四环素在酸性溶液中变成脱水四环素的动力学性质。
按一级反应动力学方程式:.c (1) 0ln=kt cc1(2) 则0lnk=ct-1mol.L=0时反应物的浓度,式中:c为t0-1mol.L时反应物的浓度,c为反应到时间t可(2)-x,带入式为经过t时间反应物消耗掉的浓度,因此,有c=c设x0得:x-c (3) 0ktln-=c表示四环素完全脱水变成脱在酸性条件下,测定溶液吸光度的变化,用A¥时部分四环素变成脱水四环素的吸光度。
则t水四环素的旋光度,代表在时间A t)-x代替(,,即c代替公式中可用c A)(A-A00¥¥t AA-(4) ¥t kt=-ln A ¥根据以上原理,可用分光光度计测定反应生成物的浓度变化,并计算反应的值。
依据。
实验可在不同温度下进行,测得不同温度下的速率常数k速率常数k1处)25℃(即1/Tlnk对作图,得一直线,将直线外推阿伦尼乌斯公式,K15298.值。
据公式:即可得到该温度时的速率常数k1054.0(5) =t9.0 k25可计算出药物的有效期四、实验组织运行要求根据实验室可以提供的实验仪器条件,有两种方式组织实验。

实验二药物的配伍禁忌【目的】通过实验,观察两种或两种以上的药物配合在一起时,可能产生的配伍禁忌;了解药物配伍禁忌的实际意义。
【原理】两种或两种以上的药物在配合使用时,可能出现理化性质或药理性质改变,使药效减弱或丧失,或产生毒性,这些药物不宜配伍使用,称为配伍禁忌。
药物的配伍禁忌分为三种情况:(1)物理性配伍禁忌:药物配合使用时,发生物理性质改变,如吸附、潮解、液化、溶化、析出等。
例如抗生素与活性炭合用,则抗生素被吸附而降低疗效;Na2CO3与CH3COOPb 研磨会变湿润;水合氯醛(熔点57℃)与樟脑(熔点171-176℃)等量混合研磨会形成低熔点混合物(熔点-60℃)产生液化现象;浓盐水与乙醇混合会析出NaCl晶体。
(2)化学性配伍禁忌:药物配合使用时,发生化学性质改变,如沉淀、变色、产气、燃烧、爆炸等。
例如盐酸四环素以NaHCO3注射液稀释时,由于PH值升高而析出四环素结晶;Ad溶液遇光线或空气后,特别是在碱性条件下,会逐渐变成红色或棕色而降低疗效,甚至失效;KMnO4与甘油混合会发生燃烧。
(3)药理性配伍禁忌(疗效性配伍禁忌):药物配合使用时,药理作用相互抵销或毒性增强,叫药理性配伍禁忌。
例如,Ca2+与Mg2+的相互对抗;洋地黄与钙制剂合用,钙能增强洋地黄对心脏的毒性。
兽医临床上常取多种药物联合使用,此时应特别注意药物之间的理化配伍禁忌,必要时,应以不同途径给药,如青霉素与磺胺嘧啶钠,庆大霉素与羧苄或氨苄青霉素相混合则失去活性。
药理性配伍禁忌一般应予避免,但在特殊情况下,却可利用它来减少药物的副作用和在药物中毒时进行解毒,如酸中毒可用弱碱中和,毛果芸香碱等拟胆碱药中毒可用阿托品等抗胆碱药解救,以及咖啡因可用来减低水合氯醛对延脑和心脏的副作用等。
【材料】(一)动物小白鼠4只。
(二)器材电子秤,试管架,试管,1ml注射器,5号针头,药匙,乳钵,鼠笼,pH广泛试纸。
(三)药品蒸馏水,液体石蜡,水合氯醛,樟脑,樟脑醑,10%磺胺嘧啶钠注射液,维生素B1注射液,24万μ青霉素G钾溶液,1.25%盐酸四环素注射液,0.1%肾上腺素注射液,5%碳酸钠溶液,0.3%戊巴比妥钠注射液,1%安钠咖注射液,4%硫酸镁注射液, 5%氯化钙注射液。
实验四:加速实验法测定药物的有效期实验学时:4实验类型:综合实验要求:分光度计法测定药物有效期一、实验目的1. 应用化学动力学的原理和方法,采用加速实验法测量不同温度下药物的反应速率,根据阿伦尼乌斯公式,计算药物在常温下的有效期。
2. 掌握分光光度计的测量原理及应用。
二、实验内容1. 加速法测定不同温度下药物反应速率。
2. 根据动力学方法计算药物在常温下的有效期。
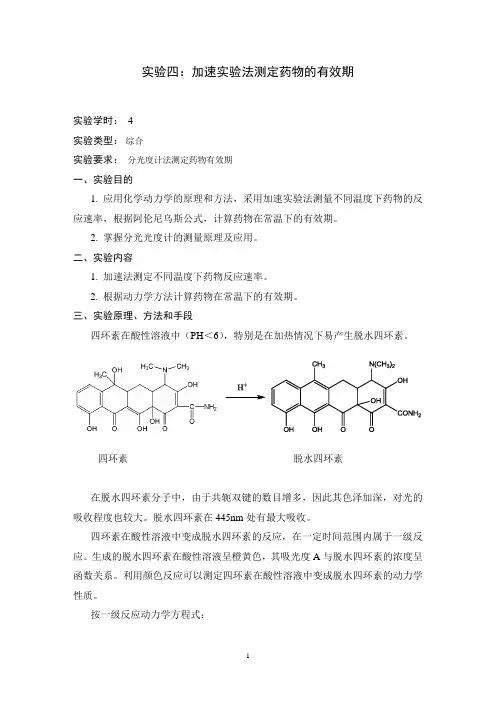
三、实验原理、方法和手段四环素在酸性溶液中(PH<6),特别是在加热情况下易产生脱水四环素。
四环素脱水四环素在脱水四环素分子中,由于共轭双键的数目增多,因此其色泽加深,对光的吸收程度也较大。
脱水四环素在445nm处有最大吸收。
四环素在酸性溶液中变成脱水四环素的反应,在一定时间范围内属于一级反应。
生成的脱水四环素在酸性溶液呈橙黄色,其吸光度A与脱水四环素的浓度呈函数关系。
利用颜色反应可以测定四环素在酸性溶液中变成脱水四环素的动力学性质。
按一级反应动力学方程式:0ln c kt c(1)则01ln c kt c(2) 式中:c 0为t =0时反应物的浓度,mol.L -1c 为反应到时间t 时反应物的浓度,mol.L -1设x 为经过t 时间反应物消耗掉的浓度,因此,有c =c 0-x ,带入式(2)可得:lnc xktc(3)在酸性条件下,测定溶液吸光度的变化,用A 表示四环素完全脱水变成脱水四环素的旋光度,tA 代表在时间t 时部分四环素变成脱水四环素的吸光度。
则公式中可用A 代替c 0,()t AA 代替(c 0-x ),即 lntA A ktA(4)根据以上原理,可用分光光度计测定反应生成物的浓度变化,并计算反应的速率常数k 。
实验可在不同温度下进行,测得不同温度下的速率常数k 值。
依据阿伦尼乌斯公式,ln k 对1/T 作图,得一直线,将直线外推25℃(即129815.K处)即可得到该温度时的速率常数k 值。
据公式:092501054..t k (5) 可计算出药物的有效期 四、实验组织运行要求根据实验室可以提供的实验仪器条件,有两种方式组织实验。

医用水胶体敷料的制备、性能及伤口应用效果作者:***来源:《粘接》2021年第09期摘要:针对传统敷料易粘附伤口,无法为创伤部位提供保护,无法抵抗外部细菌感染,进而导致组织再次损伤的问题,提出一种生物降解的抗菌医用水凝胶敷料,用于伤口愈合。
首先通过化学改性法制备海藻酸钠(OAlg),利用席夫碱交联反应制备水凝胶OAlg/CMCS;再利用乳化交联法制备载盐酸四环素明胶微球(TH/GMs)。
在水凝胶中加入不同浓度的TH/GMs,制备不同浓度的TH/GMs/Gel,性能测试结果表明,当TH/GMs为30mg/mL时,凝胶时间适宜;吸水溶胀和降解稳定性最好;最大压缩应力达到102.6MPa;压缩模量值达到8.18kPa;储能模量超过10kPa,弹性性能好,是一种结构良好,机械能力优异的医学敷料。
关键词:医用敷料;水凝胶;微球;席夫碱交联反应中图分类号:TQ437 文献标识码:A 文章编号:1001-5922(2021)09-0044-05Preparation, Properties and Wound Application Effect of Medical Hydrocolloid DressingLi Qiaolan(Wuhan NO.1 Hospital, Wuhan 430000, China)Abstract:In view of the problem that traditional dressings are easy to adhere to wounds, they can not provide protection for trauma sites, and can not resist external bacterial infection, and then cause tissue damage again. A biodegradable antibacterial medical hydrogel dressing is proposed for wound healing. Firstly, sodium alginate (OAlg) was prepared by chemical modification method, and hydrogel OAlg/CMCS was prepared by cross-linking reaction of Schiff base. Then,tetracycline gelatin microspheres (TH/GMs) were prepared by emulsion crosslinking method. Different concentrations of TH/GMs were added into the hydrogel to prepare TH/GMs/Gel with different concentrations. The performance test results show that when TH/GMs is 30mg/mL, the gel time is suitable, the water swelling and degradation stability are the best, the maximum compressive stress reaches 102.6MPa, the compression modulus reaches 8.18kPa, the storage modulus is over 10kPa, and the elastic property is good, so it is a medical dressing with good structure and excellent mechanical capability.Key words:medical dressing; hydrogel; microsphere; Schiff base crosslinking reaction現代医学技术逐年提高,药品和医用器械也走向现代化,但医用敷料却还停留在传统的纱布、绷带、棉花等物。
一、实验目的1. 了解细菌滑动抑制实验的基本原理和方法。
2. 观察并分析不同浓度抑菌剂对细菌滑动生长的影响。
3. 掌握平板划线法、菌落计数法等微生物学基本实验技术。
二、实验原理细菌滑动抑制实验是研究抑菌剂对细菌生长抑制作用的常用方法。
实验原理是:在一定条件下,细菌在固体培养基上生长时,会受到抑菌剂的抑制作用,从而影响细菌的生长和繁殖。
通过观察细菌在抑菌剂作用下的生长情况,可以评估抑菌剂的抑制效果。
三、实验材料1. 菌株:金黄色葡萄球菌(Staphylococcus aureus)标准菌株。
2. 培养基:营养琼脂平板、营养肉汤。
3. 抑菌剂:盐酸四环素、盐酸土霉素、盐酸金霉素等。
4. 工具:酒精灯、无菌镊子、无菌接种环、无菌试管、移液器、培养箱、显微镜等。
四、实验方法1. 制备培养基:将营养琼脂平板和营养肉汤按照说明书要求进行制备,并高压灭菌。
2. 制备抑菌剂溶液:将盐酸四环素、盐酸土霉素、盐酸金霉素等抑菌剂按照实验设计要求溶解于无菌蒸馏水中,配制成不同浓度的抑菌剂溶液。
3. 接种:用无菌接种环挑取金黄色葡萄球菌标准菌株,在营养琼脂平板上划线,进行平板划线法接种。
4. 滴加抑菌剂:将不同浓度的抑菌剂溶液滴加到平板上的划线处,用无菌镊子轻轻涂抹,使抑菌剂均匀分布在划线处。
5. 培养观察:将平板放入培养箱中,37℃恒温培养24小时,观察细菌的生长情况。
6. 计算抑制率:根据平板上的菌落生长情况,计算抑菌剂的抑制率。
五、实验结果与分析1. 观察到不同浓度的抑菌剂对金黄色葡萄球菌的生长具有抑制作用,且抑制作用随着抑菌剂浓度的增加而增强。
2. 通过计算抑制率,得出以下结果:- 盐酸四环素:0.1mg/mL时,抑制率为40%;0.5mg/mL时,抑制率为80%。
- 盐酸土霉素:0.1mg/mL时,抑制率为30%;0.5mg/mL时,抑制率为70%。
- 盐酸金霉素:0.1mg/mL时,抑制率为20%;0.5mg/mL时,抑制率为60%。
四环素金属络合物四环素金属络合物是指将四环素与金属离子形成的配合物,其中金属离子可以是钙、镁、铁等多种金属元素。
这种化合物在生物医药领域中具有广泛的应用,可以用于治疗感染性疾病、癌症等多种疾病。
一、四环素的结构和性质四环素是一种含氮杂环化合物,其分子式为C22H24N2O8,分子量为444.44。
其结构中包含4个苯环和一个脲环,并且在其中两个苯环上还带有羟基和甲氧基。
这些官能团赋予了四环素特殊的性质,使其能够与金属离子形成稳定的络合物。
二、金属离子与四环素的配位方式金属离子与四环素之间的配位方式主要有两种:静电作用和配位键作用。
静电作用是指当金属离子带正电荷时,可以与带负电荷的四环素分子发生吸引作用,并形成稳定的络合物。
配位键作用则是指当金属离子与四环素分子之间形成化学键时,形成的络合物更加稳定。
三、四环素金属络合物的制备方法制备四环素金属络合物的方法主要有两种:溶液法和固相法。
溶液法是指将四环素和金属离子分别溶解在适当的溶剂中,然后将两者混合并搅拌,待反应完成后进行分离、洗涤和干燥等步骤,最终得到所需的四环素金属络合物。
固相法则是指将四环素和金属离子分别混合并加热,在高温下使其反应生成所需的络合物。
这种方法具有反应时间短、产率高等优点。
四、四环素金属络合物在生物医药领域中的应用1. 治疗感染性疾病由于四环素具有广谱抗生素的作用,而且可以与多种金属元素形成稳定的络合物,在治疗感染性疾病时可以制备出不同类型的四环素金属络合物,并根据不同细菌对其敏感性选择使用不同类型的配合物进行治疗。
2. 治疗癌症近年来,研究人员发现四环素金属络合物对于某些癌细胞具有较好的抑制作用,可以用于治疗某些类型的癌症。
3. 作为药物控制释放载体四环素金属络合物具有良好的稳定性和可控性释放性,在药物控制释放领域中可以用于制备药物控制释放载体,实现对药物的精确控制和减少副作用。
五、四环素金属络合物的优缺点优点:1. 具有广谱抗生素作用,可用于治疗多种感染性疾病。
盐酸四环素干粉/盐酸四环素溶液
--------------------------------------------------------------
盐酸四环素溶液
特点:
华越洋盐酸四环素溶液是浓度为50mg/ml的四环素(硫酸盐)溶液
,
可以加到细菌液体或者固体培养基中培养含四环素抗性基因的细菌。四环素盐酸盐
的水溶性好,生物利用度比四环素碱好,故常用于临床及研究领域。
作用机制:
主要是与细菌核糖体30S亚单位的A位特异性结合,阻止tRNA在该位置上的
联结,阻止肽链延伸,从而抑制细菌蛋白质合成。四环素类还可引起细胞膜通透性
改变,使得重要成分外漏,从而抑制细菌生长繁殖。
抗性机制:
抗性基因str特异性表达一种长度为399aa的膜结合蛋白,可将四环素分子从
细胞内转移到细胞外,从而使细胞免去被四环素伤害。
运输及储存:
低温运输,-20℃保存,有效期六个月。
盐酸四环素干粉
简介:
盐酸四环素分子式为:C22H24N2O8·HCl,分子量为,。黄色结晶,无气味。味苦。
易吸湿。遇光色渐变深。易溶于水,溶于甲醇。乙醇,不溶于乙醚,羟类。它是从
放线菌金色链丛菌(Streptomycesaureofaciens)的培养液中分离出来的抗菌物质,
对革兰氏阳性菌、阴性菌、立克次体、滤过行病毒、螺旋体属乃至原虫类都有很好
的抑制作用,对结核菌、变形菌等则无效。
分子结构:
特点:
通过特异性地抑制原核及真核核糖体上的氨酰转运,使未成熟链合成种植,从
而阻碍蛋白质合成。
注意事项:
镁离子是四环素的拮抗剂,四环素抗性菌的筛选应使用不含酶盐的培养基(如
LB培养基)。
运输及储存:
低温运输,4℃干燥避光保存,有效期一年。