有机化学第七章(单)
- 格式:ppt
- 大小:2.20 MB
- 文档页数:64
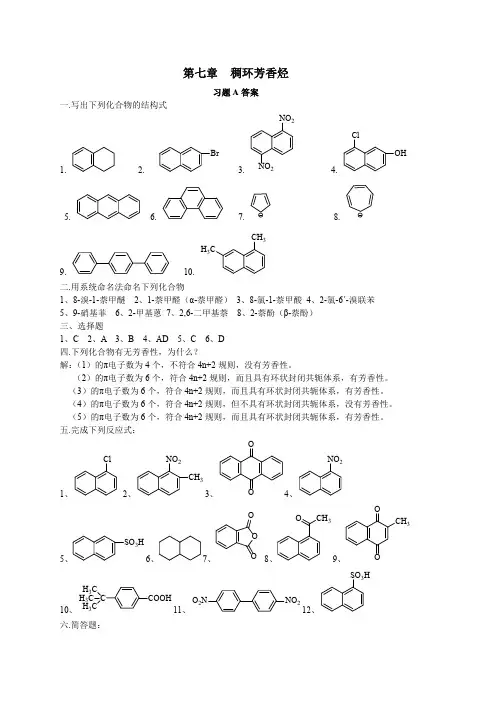



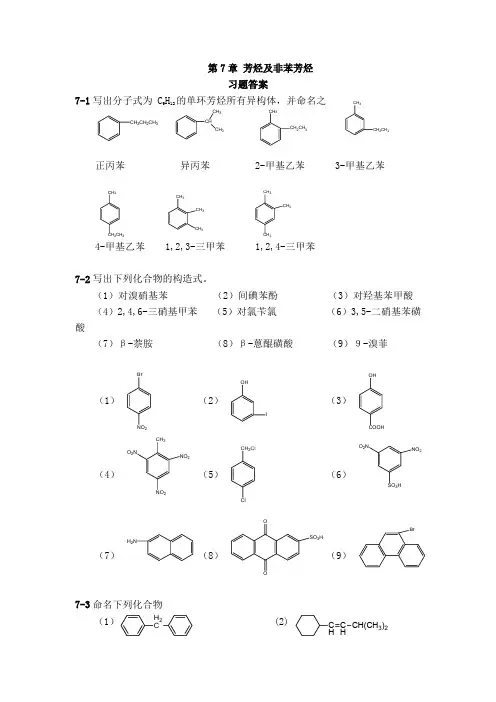


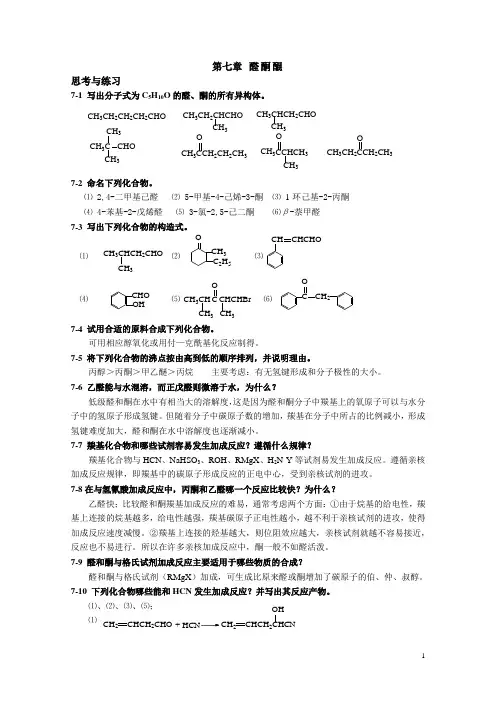
第七章 醛酮醌思考与练习7-1 写出分子式为C 5H 10O 的醛、酮的所有异构体。
7-2 命名下列化合物。
⑴ 2,4-二甲基己醛 ⑵ 5-甲基-4-己烯-3-酮 ⑶ 1-环己基-2-丙酮 ⑷ 4-苯基-2-戊烯醛 ⑸ 3-氯-2,5-己二酮 ⑹β-萘甲醛 7-3 写出下列化合物的构造式。
⑴ ⑵ ⑶⑷ ⑸ ⑹7-4 试用合适的原料合成下列化合物。
可用相应醇氧化或用付—克酰基化反应制得。
7-5 将下列化合物的沸点按由高到低的顺序排列,并说明理由。
丙醇>丙酮>甲乙醚>丙烷 主要考虑:有无氢键形成和分子极性的大小。
7-6 乙醛能与水混溶,而正戊醛则微溶于水,为什么?低级醛和酮在水中有相当大的溶解度,这是因为醛和酮分子中羰基上的氧原子可以与水分子中的氢原子形成氢键。
但随着分子中碳原子数的增加,羰基在分子中所占的比例减小,形成氢键难度加大,醛和酮在水中溶解度也逐渐减小。
7-7 羰基化合物和哪些试剂容易发生加成反应?遵循什么规律?羰基化合物与HCN 、NaHSO 3、ROH 、RMgX 、H 2N-Y 等试剂易发生加成反应。
遵循亲核加成反应规律,即羰基中的碳原子形成反应的正电中心,受到亲核试剂的进攻。
7-8在与氢氰酸加成反应中,丙酮和乙醛哪一个反应比较快?为什么?乙醛快;比较醛和酮羰基加成反应的难易,通常考虑两个方面:①由于烷基的给电性,羰基上连接的烷基越多,给电性越强,羰基碳原子正电性越小,越不利于亲核试剂的进攻,使得加成反应速度减慢。
②羰基上连接的烃基越大,则位阻效应越大,亲核试剂就越不容易接近,反应也不易进行。
所以在许多亲核加成反应中,酮一般不如醛活泼。
7-9 醛和酮与格氏试剂加成反应主要适用于哪些物质的合成?醛和酮与格氏试剂(RMgX )加成,可生成比原来醛或酮增加了碳原子的伯、仲、叔醇。
7-10 下列化合物哪些能和HCN 发生加成反应?并写出其反应产物。
⑴、⑵、⑶、⑸; ⑴CH 3CH 2CH 2CH 2CHOCH 3CH 2CHCHOCH 3CH 3CHCH 2CHOCH 3CH 3C CH 3CH 3CHOCH 3C O CH 2CH 2CH 3CH 3C O CHCH 3CH 3CH 3CHCH 2CHO 3CH CHCHOOC 2H 5CH 3CH 3CH 3CH CHCHBr C OCH 3CHO OHCH 2C O OHCH 2CHCH 2CHO CH 2CHCH 2CHCN CH 3CH 2CCH 2CH 3O⑵ ⑶⑸7-11 丙酮中混有少量丙醛,如何提纯丙酮。


了第七章 芳香烃7-1 命名下列各化合物或写出构造式。
(1)5-硝基-1-溴萘 (2)9,10-二氯菲 (3)4-苯基-2-戊烯 (4)(S )-1-苯基-1-溴丙烷 (5)4-溴联苯 (6)2-蒽磺酸(7)(8)(9)27-2 将下列各组中间体按稳定性由强至弱排列。
(1)A >B >C ; (2)B >C >A >D ; (3)C >B >A 。
7-3 将下列化合物按硝化反应的速率由快至慢排列。
(2)>(4)>(3)>(7)>(5)>(1)>(6) 7-3 将下列化合物按与HCl 反应的速率由快至慢排列。
(4)>(2)>(1)>(3) 7-5 用NMR 法鉴别下列各组化合物。
(1)、两个化合物的1H-NMR 谱都有三组信号,其中间的信号明显不同,前者是四重峰(2H)、三重峰(3H)和多重峰(5H);而后者是双峰(6H)、多重峰(1H)和多重峰(5H )。
(2)、两者芳环上H 的谱图明显不同,前者苯上的4个H 是等同的,分子共有二组峰,单峰(6H ),双峰(4H );而后者芳环的4个H 为AB 2C 型,对应的谱图(峰)较复杂[单峰(6H)、单峰(1H)和多重峰(3H)]。
7-6 完成下列各反应式。
(1)ClCH 2CH(CH 3)CH 23AlCl 3+CH 2CH 3CH 3CH3OH +++COOH (2)(3)CH 3CH 22C CCH 3CH 2C CHH CH 3+Cl 2h νPd - BaSO 4,喹啉H 2(4)CH HCHO, HCl, ZnCl 2CH 3ClH 2CCH 3CH 2Cl(5)+(6)CH CH HNO 3/H 2SO 4CH CH 2OH Cl OCH 3OCH 3OCH 3NO 2NO 2V 2O 5+NO 2O 2C O C 2OO(7)2HNO 3/H 2SO NO 2O 2N(8)AlCl 3+(9)(CH 3)2C=CH 2H 2SO 4CH 2H 3COH 3CO CH 3(10)H 3COCH CH 2COClCH 2H 3COH 3COCH CH 2C O H 3COCH 3(H 3C)3CAlCl 3+(CH 3)3Cl+24(11)O OOO OOCH 3CH 3CH 3CH 3C(CH 3)3SO 3H(12)(13)+CH 3CH 3(H 3C)3C (热力学控制产物)(主)(主)7-7 用苯、甲苯或萘为主要原料合成下列化合物。
第七章芳香亲核取代反应12芳香亲核取代反应芳香亲核取代反应机理3芳香亲核取代反应(S N 2Ar)离去基团邻对位含有强吸电子取代基芳香化合物的亲核取代反应反应机理: (S N 2Ar)1)常见S N 2Ar 反应致活基团N 2+> +NR 3>NO>NO 2>CF 3>COR>CN>CO 2H>SO 3->Cl>Br>I>CO 2->Ph 2)常见的亲核试剂H -, HS -, RO -, -CN, -SCN, -OH, -CH 2R, -CHXR, NR 3, M-CH 2R 3)芳环上可被亲核试剂取代的基团F>NO 2>Cl, Br, I>-N 2+>OSO 2R>+NR 3>OAr>OR, SR, SAr>SO 2R>NR 24芳香亲核取代反应对位含有硝基芳环上的亲核取代反应反应机理: (S N 2Ar)芳环上可被亲核试剂取代的基团的活性F > Cl, Br, I由于亲核加成是速控步, L 的吸电子能力越强, 与其相连的碳原子电正性越大,对反应越有利.从反应机理看, 芳环的邻对位有吸电子取代基可以稳定中间体环己二烯负离子,对反应有利.5芳香亲核取代反应芳环上的亲核取代反应(S N 2Ar )L + Nu :-Nu + L :-Cl10% NaOH 360o C pressure H 2O +OHCl 135-160 o C H 2O +OHO 2N O 2N NaOH, H 2O Cl 100 o CH 2O +OH O 2N O 2N Na 2CO 3, H 2O NO 2NO 2Cl H 2O +OH O 2N O 2NH 2O NO 2NO 2NO 2NO 2RT硝基的影响吸电子的诱导效应吸电子的共轭效应S N 2Ar 反应硝基为邻对位致活基团6芳香亲核取代反应芳香硝基化合物的芳香亲核取代反应Cl 是好的离去基团, 不好的活化基团.硝基是好的离去基团, 也是好的活化基团Cl 位于2个硝基的邻对位, 易离去.NO 2NO 2OHNO 2NH 2NO 25% NaOHNH 3ClNO 2OMeNO 2NHNH 2NO 2H 2NNH 2NO 2NO 2NO 2MeONa MeOH7芳香亲核取代反应芳香硝基化合物的芳香亲核取代反应实例:NMe 2HNO 2NMe 2KOHONOH + Me 2NHONFO 2N OMe 93%O 2N MeONa MeOH 25o C O 2NOEt NO 2O 2N X +NO 2PhNH 2180o CO 2N NHPh + EtOH NO 2O 2NN NO 2HN + HXX= Cl, BrX= NO 2X= OC 6H 4OMe-489芳香亲核取代反应(S N 1Ar 机理)芳香重氮盐参与的芳香亲核取代反应(无铜催化无强碱)(S N 1Ar)重氮盐热不稳定,0 o C 分解较慢, 温度升高酸性增大均可以加速分解反应.同位素标记证明第一步反应可逆.X -的亲核性不能比:Nu -的强,才有利于形成Ar-Nu ;否则会有利于生成Ar-X.X -可以为HSO 4-,BF 4-,BCl 4-,BBr 4-,Cl -,Br -,I 3-等.10芳香亲核取代反应(S N 1Ar)芳香重氮盐参与的芳香亲核取代反应(无铜催化无强碱)(S N 1Ar)芳环上取代基对反应的影响: (主要看速控步)1)吸电子取代基不利于苯正离子稳定, 对反应不利; 2)给电子取代基有利于苯正离子稳定, 对反应有利;相对速度: p -NO 2< m -Cl < H < p -Mev 1/240 1/24 1 4.53) 邻对位有易形成共轭效应的给电子取代基时, 增加了C-N 键的双键性质, 不利于氮气离去, 因此对反应不利.N N Cl -+RH 2O, 29oCR+ N 2+ Cl -+11芳香亲核取代反应(S N 1Ar)芳香重氮盐的水解(S N 1Ar 机理)HSO 4-的亲核性比H 2O 弱, 只得到酚; 若用HCl, HNO 3代替H 2SO 4还会生成副产物PhCl, PhONO 2.12芳香亲核取代反应(S N 1Ar)Schiemann 反应(制备ArF)13芳香亲核取代反应(S N 1Ar)Schiemann-Olah 反应(制备ArCl, ArBr, ArI)Olah 将该反应推广到制备ArCl 和ArBr1415芳香亲核取代反应(苯炔中间体)苯炔与芳香亲核取代反应机理一.苯炔的结构sp 2-sp 2重叠很弱二.以苯炔为中间体的芳香亲核取代反应离去基团邻对位无强吸电子取代基,但邻位有氢芳香化合物在强碱条件下的亲核取代。