九年级化学全册第三章物质构成的奥秘3.1构成物质的基本微粒教案1(新版)沪教版
- 格式:doc
- 大小:239.00 KB
- 文档页数:3

第3章物质构成的奥秘第1节构成物质的基本微粒一、知识与技能1.认识物质的微粒性,知道分子、原子、离子等都是构成物质的微粒。
2.能用微粒的观点解释某些常见的现象。
3.知道原子是由原子核和核外电子构成的。
4.知道原子可以结合成分子、同一元素的原子和离子可以互相转化,初步认识核外电子在化学反应中的作用。
二、过程与方法1.通过对实验现象的观察、分析,学会归纳整理;2.用化学知识解释日常生活中的一些变化,激发学习化学的兴趣1.能用微观粒子的观点解释某些常见的现象。
2.认识构成物质的粒子有分子、原子、离子。
知道分子、原子、离子的不同和相互关系。
3.知道原子的结构,建立物质无限可分的观点。
4.能正确求算相对分子质量。
1.能用微观粒子的观点解释某些常见的现象。
2.认识构成物质的粒子有分子、原子、离子。
知道分子、原子、离子的不同和相互关系。
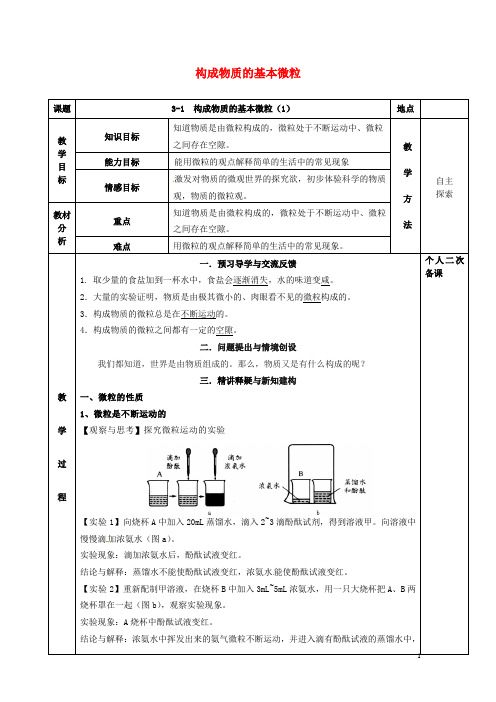
我们都知道世界是由物质组成的,那么物质是由什么构成呢?[提出问题]在10 s内,将一张纸按等比例进行分割到尽可能小,它还能再分吗?(一)微粒的性质[问题]走在校园里,你会闻到桂花香味,但你看到桂花树吗?为什么?[观察思考]:实验操作1:向烧杯A中加入20mL蒸馏水,滴入2~3滴酚酞试剂,得到溶液甲。
在烧杯B中加入3mL~5mL浓氨水,用一只大烧杯把A、B两烧杯罩在一起,观察实验现象。
现象是____________________。
现象解释是___________________。
操作2:重新配制甲溶液,向溶液中慢慢滴加浓氨水。
现象是_____________________________________________________。
现象解释是__________________________________________________。
操作3:在烧杯B中以蒸馏水代替浓氨水,重复实验1的操作。
观察现象为__________________________________________________。
构成物质的基本微粒
激发对物质的微观世界的探究欲,初步体验科学的物质
】向烧杯A中加入20mL蒸馏水,滴入2~3滴酚酞试剂,得到溶液甲。
向溶液中慢慢滴加浓氨水(图
结论与解释:蒸馏水不能使酚酞试液变红,浓氨水能使酚酞试液变红。
所以,气体往往容易被压缩,固体和液体物质不容易被压缩。
关于物质微粒的叙述中错误的是
粒在不断的运动
热
D
.某化学兴趣小组通过以下实验探究微粒的运动。
请回答实验中的有关问题:得出结论:蒸馏水不能使酚
烧杯中而使酚酞变红。
个水分子A;
10mLC
六.教学反思。


第2课时分子原子原子的构成1.知识与技能(1)认识物质是由分子、原子等微小粒子构成的。
(2)能运用分子、原子的观点解释一些简单的生活和实验现象。
(3)认识原子的内部构成。
2.过程与方法(1)学习通过观察生活、实验探究等方法获取信息。
(2)学习运用比较、分析、归纳等方法对实验所得信息进行加工。
(3)充分发挥学生的空间想象力。
3.情感、态度与价值观(1)增加学生对微观世界的好奇心和求知欲,从探究中获得成功的喜悦,激发学习化学的兴趣。
(2)逐步提高抽象思维能力、想象力和分析、推理能力。
(3)使学生在实验的探究,讨论中学会与别人交流、合作、增强协作精神。
重点:(1)理解物质是由分子、原子等微小粒子构成的。
(2)从分子和原子的观点认识物理变化与化学变化。
(3)了解原子的内部构成。
难点:(1)建立微观粒子运动的想象表象,体会它与宏观物体运动的不同点。
(2)微观角度对化学变化和物理变化的区分。
【提问】在水电解的过程中,发生变化的是什么?不变的又是什么?请把你的想法与同学相互交流、讨论。
【结论】原子是化学变化中的最小粒子【讲解】由上述讨论可知,原子可以结合成分子,不仅如此,原子还能直接构成物质。
(1)定义:分子是保持物质化学性质的最小粒子。
(2)性质:①分子的体积和质量都很小。
②分子处于不断的运动中。
③分子之间有间隙。
2.原子(1)定义:原子是化学变化中的最小粒子。
(2)性质:与分子的性质相似,体积、质量小;运动;有间隙。
用分子、原子的观点理解化学反应的本质:3.原子的构成原子的构成⎩⎪⎨⎪⎧原子核(正电)⎩⎪⎨⎪⎧质子(正电)中子(不带电)核外电子(负电)在教学过程中,教师要组织好学生完成从抽象到形象,从微观到宏观的理解过程,督促学生积极参与、相互配合,积极引导学生探究,使学生进一步掌握科学探究的过程和方法,充分体现探究学习。
1.氮气液化的过程中,发生改变的是( C ) A .氮气分子的大小 B .氮气分子的组成 C .氮气分子间的距离 D .氮气的化学性质2.下列事实能证明在化学变化中分子可分的是( C ) A .蒸发氯化钠溶液后,有固体析出 B .干冰升华形成二氧化碳气体 C .水通电可以收集到氧气和氢气 D .水蒸气冷凝为水3.下列说法中不正确的是( D ) A .水是由水分子直接构成的 B .分子和原子等都是构成物质的微粒C .分子和原子的本质区别是:分子可分,原子不可分D .氮气是由氮原子直接构成的4.能说明分子在化学变化中可再分的事实是( B ) A .湿衣服放在外面晾干 B .水通电生成氢气和氧气 C .硫加热变成硫蒸气 D .大块冰糖变成小块冰糖 5.原子核的构成是( C )A.质子和电子 B.电子和中子C.质子和中子 D.质子、中子、电子6.有两种不同的碳原子,一种原子核内有6个质子和6个中子,另一种原子核内有6个质子和7个中子,则它们不相等的是( D)A.核电荷数 B.核外电子数C.原子的带电量 D.原子的质量7.下列有关分子的叙述不正确的是( A)A.一切物质都是由分子构成的B.不同种分子的化学性质不同C.分子是由原子结合而成的D.在化学变化中分子本身发生改变8.(泰安中考)原子是构成物质的基本粒子。


构成物质的基本微粒不同物质是由不同微粒构成的,具有不同的化学性质。
结论和解释为、刚才同学们所做的都是对一个问题的不同探究,只不过控制的条件有所不同,象这时讲述:物质的微粒在不断的运动,固质由离子构成,如,氯化钠就是由钠离子和氯离子构成的。
讨论物质的三态变化:分子和原子的主要区别是(粒子会有偏转;而因为金原子中原子核存在,而且体积小,质量大,核能不能再分了呢?卢瑟福同样通过物质的相对性-新授课:由于一个原子的真实质量很小,使用不方便,提出一个相对原子质量的概念2020年中考化学模拟试卷一、选择题1.物质的性质与用途密切关系.下列说法不正确的是()A.铝的化学性质稳定,“银粉漆”(铝粉)可涂在铁栏杆防锈B.氧气能支持燃烧,可用作助燃剂C.洗洁精具有乳化功能,可用于去油污D.熟石灰呈碱性,可用于改良酸性土壤2.下列几种气体①H2②O2③CO2④SO2⑤CH4⑥NH3可用如图所示装置干燥、收集的正确组合是()A.①②⑤B.①⑤⑥C.③④⑥D.③⑤⑥3.为了探究金属与盐溶液的反应规律,将一定质量的锌粉和银粉加入Cu(NO3)2溶液中,充分反应,实验过程及实验现象如下图所示,则下列判断中正确的是()A.滤液中可能含有Ag+B.滤渣中可能含有单质锌C.滤液中一定含有Cu2+D.滤渣中一定含有单质铜4.下列化学方程式符合题意且书写正确的是A.正常雨水呈酸性的原因:CO2+H2O=H2CO3B.医疗上用碱性物质中和过多胃酸:NaOH+HCl=NaCl+H2OC.除去 NaCl 溶液中的少量 MgCl2:2KOH+MgCl2=2KCl+Mg(OH)2↓D.证明铜的金属活动性比银强:Cu+2AgCl=CuCl2+2Ag5.掌握化学用语是学好化学的关键,下列化学用语的意义叙述不正确的是 ( )A.2H表示两个氢分子B.CH4表示甲烷这种物质,还表示一个甲烷分子C.3SO42-表示三个硫酸根离子D.中的数字“2”表示镁元素的化合价为+2价6.今取12.7克氯化亚铁样品,完全溶于水制成溶液然后加入足量的硝酸银溶液,使其充分反应,得氯化银沉淀,经干燥后称量质量为30克,已知,样品内杂质为氯化物,则该杂质可能是( )A.KCl B.NaCl C.ZnCl2D.BaCl27.铬在元素周期表中信息如图所示,下列有关铬元素的说法不正确的是()A.质子数为24B.属于金属元素C.一个铬原子核外有28个电子D.相对原子质量为52.008.氯化钾(KCl)、重铬酸钾(K2Cr2O7)和氯化钠(NaCl)的溶解度随温度变化曲线如图所示,下列说法错误的是()A.KCl、K2Cr2O7和NaCl均属易溶物质B.由a点可知,70℃时KCl饱和溶液的溶质质量分数为50%C.将K2Cr2O7和NaCl的混合热饱和溶液降温,析出的晶体主要是K2Cr2O7D.将20℃时K2Cr2O7和NaC1的混合饱和溶液升温到90℃,再加入适量K2Cr2O7和NaCl的混合固体,趁热过滤得到的固体主要是NaCl9.如图所示,将胶头滴管内的液体滴入试管中与固体充分接触。
第一节构成物质的根本微粒第一课时教学目标:知识与技能:〔1〕知道微粒的性质以及分子、原子、离子都是构成物质的根本微粒。
〔2〕知道在化学反响中分子可以分成原子,原子可以结合成分子。
〔3〕是学生认识到分子、原子、离子存在的真实性。
过程与方法:〔1〕积极主动与他人进展交流和讨论,清楚的表达自己的观点。
〔2〕提出问题,进展初步的科学研究。
情感态度与价值观:〔1〕初步建立物质无限可分的观点。
〔2〕提高学生的想象能力、创新能力。
学习重难点:1、知道分子、原子、离子都是构成物质的微粒。
2、知道在化学反响中分子可以分成原子,原子可以结合成分子。
学习重难点:在实验中建立分子、原子、粒子在化学变化重的形象,完成对化学变化宏观现象中的微观解释。
课前准备教师:1、不同微粒构成的物质。
2、氢气、氧气、水的性质实验。
学生:在日常生活中,感受到分子真实存在的例子。
教学过程:一.微粒的性质【引入】有句俗语叫酒香不怕巷子深,意思是如果酒酿得好,就是在很深的巷子里,也会有人闻香知味,前来品尝。
那大家有没有思考过,为什么我们能闻到酒的闻到,为什么我们平时能闻到花香,闻到香水味?这节课我们就来解答下这些问题我们知道世界是由物质组成的,那物质又是由什么组成的呢?【学生】微粒【教师】对了,物质是由我们肉眼看不到的微粒组成的,说明微粒都很小,但是微粒有一定的质量【板书】一、微粒的性质1、微粒都非常小,但有一定质量这些微粒是我们下面几节课要学习的分子、原子和离子。
为什么我们能闻到各种味道,为什么能远远的闻到花香?【分析】因为构成酒和花的微粒,扩散到了空气中,接触到了我们的嗅觉器官,所以我们闻到了闻到,通过这个分析我们可以推测构成物质的微粒能运动,那是不是真的能运动呢,我们通过一个实验来检验下【实验】探究微粒运动实验【现象】1、甲是无色溶液,参加酚酞后,变成了红色溶液2、甲溶液变红【分析】这里我们来了解下酚酞溶液,酚酞和我们学过的紫色石蕊试剂一样,是一种酸碱指示剂,酚酞遇到酸变色,遇到碱变红色,可以用于检验溶液是否显碱性,以后酚酞以后我们还会接触到,这里的氨水是显碱性的,所以在酚酞中参加氨水以后,溶液会变红【提问】实验1中我们参加了氨水,溶液显碱性了,所以溶液变红,那实验二中的甲溶液为什么变红呢?【学生】变红证明溶液显碱性,说明B中的氨气微粒跑到了装有酚酞的A 的烧杯中,这说明了微粒能运动【教师】上述的实验说明了构成物质的微粒是不断运动的【板书】2、微粒是不断运动的【提问】晒衣服的时候,为什么太阳大衣服比拟容易干?糖水为什么温度高的时候比拟容易溶解?【分析】温度越高,微粒运动的越快【提问】水有三态,但都是水这种物质,大家知道水为什么有三态吗?我们也听说过热胀冷缩,你能解释这是为什么吗?【教师】要解释这个现象,我们先来看下下面这个实验【实验】水与酒精混合实验【现象】1、把玻璃管颠倒数次以后,玻璃管内出现了间隙【分析】这是因为微粒之间有间隙,当玻璃管颠倒数次之后,酒精微粒和红墨水微粒会相互占据微粒之间的间隙,所以最后体积缩小〔酒精微粒比拟大,水的比拟小,可以画模型表示,大球和大球之间的间隙可以塞下一个小球〕【板书】3、微粒之间有间隙【提问】那是不是所有的物质微粒的的间隙都一样大呢?【学生】不是,在固体,液体间的间隙比拟小,气体的间隙比拟大,物质存在三态的原因是因为微粒间的间隙不一样【教师】那是不是这样的呢,我们通过实验来验证下【实验2】水和空气的压缩实验【现象】吸有空气的的那支注射器比拟容易被压缩【分析】这说明气体微粒间的间隙比拟大,所以容易被压缩,那压缩前后的气体,哪种间隙比拟大?【学生】压缩前的【教师】压缩后气体间的压强比拟大,间隙比拟小,说明气体的微粒间间隙和压强有关,压强越大微粒间的间隙越小【提问】物体热胀冷缩,这是大家在物理里面学到的原理,大家能说明为什么吗?【学生】跟物体微粒间的间隙有关,间隙大了,物体的体积就大了,所以热胀说明温度升高,微粒间的间隙会变大【总结】这节课学习了微粒的特性,第一是微粒在不断的运动,第二是微粒之间有间隙,现在大家做几道题目1.为什么夏天给自行车打气不应打太满2.为什么铁路上的铁轨之间应稍留缝隙【教师】经科学家研究,构成物质的微粒有分子,原子和离子,有些物质由分子构成,如干冰、水、氮气等,有些物质由原子构成,如金刚石和一些常见的金属物质还有稀有气体。
第三章物质构成的奥秘第一节构成物质的基本微粒第二课时【学习目标】1.认识物质是由分子、原子等微小粒子构成的。
2.能运用分子、原子的观点解释一些简单的生活和实验现彖。
【学习重点】1•认识物质是由分子、原子等到微小粒子构成的。
2.从分子和原子的观点认识物质变化与化学变化。
【学习难点】1.建立微观粒子运动的想彖,体会它与宏观物体运动的不同点。
2.从分子、原子的角度对化学变化和物理变化区分。
【自学导航】阅读教材,完成以下问题:探究一、构成物质的微粒1.________________________ 构成物质的微粒有____ 、、。
2.由原子直接构成的物质有:Fe、Cu、Mgs Na、He、Ne、金刚石(C)、石墨(C)、S、Si 等。
3.由分子构成的物质有:常见气体:出、C02、02、N2> NH3> SO2、CH”、HC1 等。
液体:苯、酒精、出0等。
固体:五氧化二磷、干冰(固态二氧化碳)等。
4.由离子构成的物质有:氯化钠是市氯离子和钠离子构成的。
探究二、分子1.概念:分子是____________________ 的______ 微粒。
2.分子的基本性质:①分子的体积小,质量小。
②分子是在 ______________________ O③分子之间W ______________________ O④同种分子 _______________ ,不同种分子________________ O3.________________________________ 备注:①分子是保持物质的________________ 性质的一种微粒,不能保持物质的 ________________ 性质;②分子在_______ 变化中可以再分;在 ______________变化中不能分。
例:保持氧气化学性质的最小微粒是,能保持二氧化碳的化学式:水分子—、氧分子 ____________ 、氢分子,5. 用分子的观点解释⑴纯净物和混合物 ___________ 种分子构成纯净物。
第1节构成物质的基本微粒【教学内容】九义教科书《化学》上册第三章第一节【教学目标】1.知识目标:①认识物质的微粒性:物质由微粒构成,微粒不断运动,微粒之间有空隙;②能用微粒的观点解释某些常见的现象;③能用某些事实或设计完成某些实验说明物质的微粒性;④运用有关物质的微粒知识进行想象和推理。
2.能力和技能目标:①培养学生的观察和实验能力;②培养学生提出问题、分析问题和解决问题的能力。
3.情感、态度、价值观目标:①培养学生尊重事实、勇于探索、勇于创新的科学精神;②培养学生主动参与、合作的意识和能力。
【教学重点、难点】1.认识物质的微粒性:物质由微粒构成,微粒不断运动,微粒之间有空隙;2.能用微粒的观点解释某些常见的现象。
【教学策略】学生在第二章已学习了身边的物质,知道不同的物质的化学性质是不同的,本节课以“为什么不同的物质的化学性质不同”引入,让学生明确本章学习的内容和目的。
首先,通过实验感受物质分割过程,使学生构建微粒的观点;其次,通过学生的讨论、设计、实验探究,得到微粒的某些特征:微粒是不断运动的,微粒之间有空隙,并运用多媒体动画演示微粒的变化情况以加深认识;最后,利用物质的微观性能解释生活中常见的现象和一些实验现象。
形成微粒的观点,学生接受构成物质的三种基本微粒(分子、原子和离子)就更加顺利。
【教学准备】1.学生准备分组实验,四人一组,其中化学学习能力较强的学生为组长。
2.教具准备①多媒体教学设备②试管、烧杯、酒精灯、药匙、胶头滴管、一端封口的细玻璃管、注射器、研钵、高锰酸钾、蒸馏水、浓氨水、酚酞、酒精等。
【教学过程】附:板书设计第一节构成物质的基本微粒一、物质都是由极其微小的、肉眼看不见的微粒构成的。
不同的物质由不同的微粒构成,因此不同的物质有不同的性质。
二、微粒是不断运动的。
三、微粒之间有空隙。
气体物质中微粒之间的距离比固体、液体中的大。
构成物质的基本微粒
激发对物质的微观世界的探究欲,初步体验科学的物质
】向烧杯A中加入20mL蒸馏水,滴入2~3滴酚酞试剂,得到溶液甲。
向溶液中慢慢滴加浓氨水(图
结论与解释:蒸馏水不能使酚酞试液变红,浓氨水能使酚酞试液变红。
所以,气体往往容易被压缩,固体和液体物质不容易被压缩。
关于物质微粒的叙述中错误的是
粒在不断的运动
热
D
.某化学兴趣小组通过以下实验探究微粒的运动。
请回答实验中的有关问题:得出结论:蒸馏水不能使酚
烧杯中而使酚酞变红。
个水分子A;
10mLC
六.教学反思。