初中常见化学式及化学方程式大全(1)
- 格式:doc
- 大小:82.00 KB
- 文档页数:17
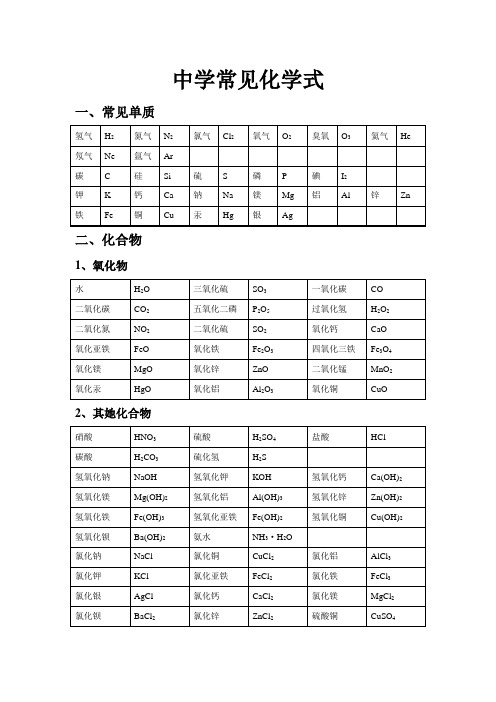
中学常见化学式一、常见单质二、化合物1、氧化物2、其她化合物3、常见有机化合物初中化学方程式汇总一、氧气的性质:(1)单质与氧气的反应:(化合反应)1、镁在空气中燃烧:2Mg+ O2点燃 2MgO2、铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43、铜在空气中受热:2Cu+ O2加热 2CuO4、铝在空气中燃烧:4Al +3O2 点燃2Al2O 35、氢气中空气中燃烧:2H2 +O2点燃 2H2O6、红磷在空气中燃烧(研究空气组成的实验):4P +5O2点燃 2P2O57、硫粉在空气中燃烧: S +O2 点燃 SO28、碳在氧气中充分燃烧2点燃 CO29、碳在氧气中不充分燃烧2点燃 2CO (2)化合物与氧气的反应:10、一氧化碳在氧气中燃烧:2CO+O2点燃 2CO211、甲烷在空气中燃烧:CH4 +2O2点燃 CO2+2H2O12、酒精在空气中燃烧:C2H52点燃 2CO2+3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg +O2↑14.加热高锰酸钾:2KMnO4加热 K2MnO4+ MnO2+O2↑(实验室制氧气原理1)15.: H2O2MnO22H2O+ O2↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电 2H2↑+O2↑17.生石灰溶于水英语六级作文:CaO +H2O == Ca(OH)218.二氧化碳可溶于水: H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+ O2点燃 2MgO20.铁与硫酸铜溶液反应44+ Cu21.氢气还原氧化铜:H2 +CuO 加热 Cu +H2O22、镁还原氧化铜:Mg+ CuO 加热 Cu +MgO四、碳与碳的氧化物:(1)碳的化学性质23、碳在氧气中充分燃烧:C + O2点燃 CO224.木炭还原氧化铜:C + 2CuO 高温 2Cu+ CO2↑25. 焦炭还原氧化铁3高温 4Fe + 3CO2↑(2)煤炉中发生的三个反应:()26.煤炉的底层:C +O2 点燃 CO227.煤炉的中层:CO2+ C 高温 2CO28.煤炉的上部蓝色火焰的产生:2CO +O2点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3+ 2HCl == CaCl2+ H2O +CO2↑30.碳酸不稳定而分解:H2CO3== H2O +CO2↑31.二氧化碳可溶于水: H2O +CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温 CaO+ CO2↑33.石灰水与中学历史教学园地二氧化碳反应):Ca(OH)2 +CO2=== CaCO3↓+H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu +CO235.一氧化碳的可燃性:2CO +O2点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO32HCl == 2NaCl+ H2O +CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 +2O2点燃 CO2+2H2O38.酒精在空气中燃烧:C2H5OH +3O2 点燃 2CO2+3H2O39. 氢气中空气中燃烧:2H2+ O2点燃 2H2六、金属(1)金属与氧气反应:40. 镁在空气中燃烧:2Mg+ O2点燃 2MgO41. 铁在氧气中燃烧:3Fe +2O2点燃 Fe3O442、铜在空气中受热:2Cu +O2加热 2CuO43、铝在空气中形成氧化膜2 = 2Al2O3(2)金属单质酸 -------- 盐氢气 (置换反应)44、锌与稀硫酸Zn+ H2SO4= ZnSO4+ H2↑45、铁与稀硫酸Fe +H2SO4= FeSO4+H2↑46、镁与稀硫酸Mg +H2SO4= MgSO4+ H2↑47、铝与稀硫酸2Al+ 3H2SO4= Al2(SO4)3+3H2↑48、锌与稀盐酸Zn+ 2HCl == ZnCl2+ H2↑49、铁与稀盐酸Fe +2HCl == FeCl2 +H2↑50、镁与稀盐酸Mg +2HCl == MgCl2+ H2↑51.铝与稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(3)金属单质盐怎样学好高中物理(溶液) ------- 新金属新盐52、铁与硫酸铜溶液反应:Fe +CuSO4 == FeSO4+Cu53、锌与硫酸铜溶液反应:Zn +CuSO4 ==ZnSO4+Cu54、铜与硝酸汞溶液反应:Cu +Hg(NO3)2== Cu(NO3)2+Hg(3)金属铁的治炼原理:55.3CO +2Fe2O3高温 4Fe +3CO2↑七、酸、碱、盐1、酸的化学性质(1)酸金属 -------- 盐氢气(见上)(2)酸金属氧化物-------- 盐水56、氧化铁与稀盐酸反应:Fe2O3+6HCl ==2FeCl3+3H2O57、氧化铁与稀硫酸反应:Fe2O3+3H2SO4 == Fe2(SO4)3+3H2O58、氧化铜与稀盐酸反应:CuO +2HCl ==CuCl2+H2O59、氧化铜与稀硫酸反应:CuO+ H2SO4 == CuSO4+ H2O(3)酸碱 -------- 盐水(中与反应)60.盐酸与烧碱起反应:HCl +NaOH == NaCl+H2O61、盐酸与氢氧化钙反应:2HCl+ Ca(OH)2 == CaCl2+2H2O62、氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 == AlCl3+3H2O63、硫酸与烧碱反应:H2SO4+ 2NaOH == Na2SO4+2H2O(4)酸盐 -------- 另一种酸另一种盐64.大理石与稀盐酸反应:CaCO3+2HCl == CaCl2+H2O+ CO2↑65.碳酸钠与稀盐酸反应: Na2CO3+2HCl == 2NaCl+ H2O+ CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+H2O+ CO2↑67、硫酸与氯化钡溶液反应:H2SO4+BaCl2== BaSO4↓+2HCl2、碱的幼儿园小班音乐教案化学性质(1) 碱非金属氧化物 -------- 盐水68.苛性钠暴露在空气中变质:2NaOH+CO2 == Na2CO3+ H2O69.苛性钠吸收二氧化硫气体:2NaOH +SO2 == Na2SO3+H2O70.苛性钠吸收三氧化硫气体:2NaOH+ SO3 == Na2SO4+H2O71.消石灰放在空气中变质:Ca(OH)2+ CO2== CaCO3↓+H2O72、消石灰吸收二氧化硫:Ca(OH)2 +SO2== CaSO3↓+ H2O(2)碱酸-------- 盐水(中与反应,方程式见上)(3)碱盐 -------- 另一种碱另一种盐73、氢氧化钙与碳酸钠:Ca(OH)2 +Na2CO3== CaCO3↓+ 2NaOH3、盐的化学性质(1)盐(溶液) 金属单质------- 另一种金属另一种盐74、铁与硫酸铜溶液反应:Fe+ CuSO4 == FeSO4+Cu(2)盐酸-------- 另一种酸另一种盐75.碳酸钠与稀盐酸反应: Na2CO3+2HCl == 2NaCl +H2O+ CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+ H2O +CO2↑(3)盐碱 -------- 另一种碱另一种盐76、氢氧化钙与碳酸钠:Ca(OH)2 +Na2CO3== CaCO3↓+ 2NaOH(4)盐盐 ----- 两种新盐77.氯化钠溶液与硝酸银溶液:NaCl +AgNO3== AgCl↓+NaNO378.硫酸钠与氯化钡:Na2SO4+BaCl2== BaSO4↓+2NaCl其她反应类型1、二氧化碳通入澄清石灰水中:CO2 + Ca(OH)2== CaCO3↓+ H2O2、氢氧化钠在空气中变质:CO2+ 2NaOH = Na2CO3+ H2O3、氢氧化钠溶液吸收二氧化硫:SO2 + 2NaOH==Na2SO3+ H2O4、一氧化碳还原氧化铜:CO + CuO Cu + CO25、酒精燃烧:C2H5OH + 3O22CO2+ 3H2O6、甲烷燃烧:CH4 + 2O2CO2+ 2H2O化学方程式反应现象应用1、 2Mg+ O2点燃或Δ2MgO 剧烈燃烧、耀眼白光、生成白色固体、放热、产生大量白烟2、 2Hg +O点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验3、 2Cu+ O点燃或Δ2CuO 红色金属变为黑色固体4、点燃或Δ2Al2O3银白金属变为白色固体5、 3Fe+ 2O点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热6、 C+ O2点燃CO2剧烈燃烧、白光、放热、使澄清石灰水变浑浊7、 S +O2点燃SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰、氧气中8、 2H2 O2点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水) 高能燃料9、 4P +5O2 点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量10、 CH4+2O点燃2H2O+ CO2蓝色火焰、放热、生成使石灰水变浑浊气体与使无水CuSO4(水) 甲烷与天然气的燃烧11、 2C2H2+ 5O点燃2H2O +4CO2蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体与使无水4(水) 氧炔焰、焊接切割金属12、 2KClO3MnO2、Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气13、 2KMnO4ΔK2MnO4MnO2+O2↑ 紫色变为黑色、生成使带火星木条复燃的气体14、 2HgOΔ2Hg+ O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实△点燃点燃验15、 2H2O通电2H2↑+ O2↑ 水通电分解为氢气与氧气电解水16、 Cu2(OH)2CO3Δ2CuO +H2O+ CO2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体17、 NH4HCO3ΔNH3↑+ H2O+ CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体18、 Zn+ H2SO4=ZnSO4+H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气19、 Fe +H2SO4=FeSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解20、 Mg +H2SO4=MgSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解21、 2Al+ 3H2SO4=Al2(SO4)3+ 3H2↑ 有大量气泡产生、金属颗粒逐渐溶解22、 Fe2O3+3H2Δ 2Fe +3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、23、 Fe3O4+4H2Δ3Fe+ 4H2O 黑色逐渐变为银白色英语翻译、试管壁有液体冶24、 WO3 +3H2Δ W +3H2O 冶炼金属钨、利用氢气的还原性25、 MoO32ΔMo +3H2O 冶炼金属钼、利用氢气的还原性26、 2Na+ Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、27、 H2+Cl2点燃或光照 2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸28、 CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验29、 2C +O2点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因30、 2CO +O点燃2CO2蓝色火焰煤气燃烧31、 C+ CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体32、 2Fe2O3+ 3C 高温4Fe+ 3CO2↑ 冶炼金属33、 Fe3O4+2C高温3Fe+ 2CO2↑ 冶炼金属34、 C+ CO2 高温2CO35、 CO2+H223碳酸使石蕊变红证明碳酸的酸性小学三语文教学论文36、 H2CO3ΔCO2↑+ H2O 石蕊红色褪去37、2 +CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验与石灰浆粉刷墙壁38、 CaCO3 +H2O+ CO2= Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化39、 Ca(HCO3)2Δ CaCO3↓+ H2O +CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体40、 2NaHCO3ΔNa2CO3+ H2O +CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头41、 CaCO3 高温 CaO +CO2↑ 工业制备二氧化碳与生石灰42、 CaCO3 2+ H2O +CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢。
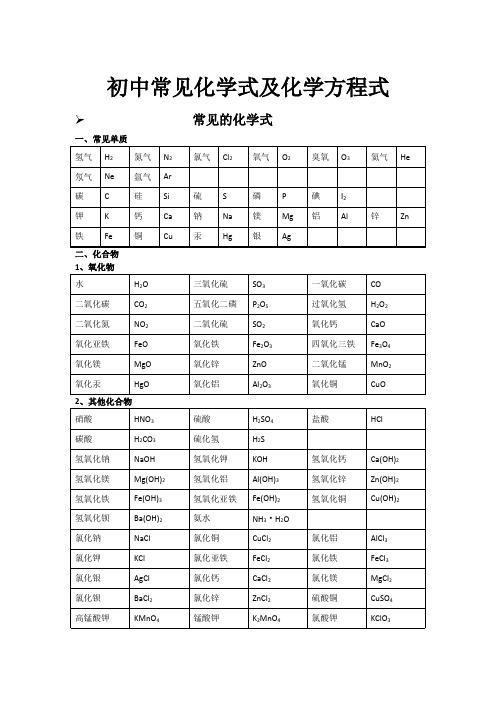

化学式(一)氧化物1.氧化钾K2O2.氧化钠Na2O3.氧化钙CaO4.氧化钡BaO5.氧化镁MgO6.氧化铝Al2O37.氧化锌ZnO8.氧化亚铁FeO9.氧化铁Fe2O3 10.氧化铜CuO 11.氧化银Ag2O(二)盐酸盐1.氯化钾KCI2.氯化钠NaCl3.氯化钙CaCl24.氯化钡BaCl25.氯化镁MgCl26.氯化铝AlCl37.氯化锌ZnCl2 8氯化亚铁FeCl29.氯化铁FeCl3 10.氯化铜CuCl2 11.氯化银AgCl 12.氯化铵NH4Cl(三)硝酸盐1.硝酸钾KNO32.硝酸钠NaNO33.硝酸钙Ca(NO3 ) 24.硝酸钡Ba(NO3 ) 25.硝酸镁Mg(NO3 ) 26.硝酸铝Al(NO3 ) 37.硝酸锌Zn(NO3 ) 28.硝酸亚铁Fe(NO3 ) 29.硝酸铁Fe(NO3 )32 10.硝酸铜Cu(NO3 ) 2 11.硝酸银AgNO3 12.硝酸铵NH4NO3(四)硫酸盐1.硫酸钾K2SO42.硫酸钠Na2SO43.硫酸钙CaSO44.硫酸钡BaSO45.硫酸镁MgSO46.硫酸铝Al2(SO4)37.硫酸锌ZnSO48.硫酸亚铁FeSO49.硫酸铁Fe2(SO4 )3 10.硫酸铜CuSO4 11.硫酸银Ag2SO4 12.硫酸铵(NH4)2SO4(五)碳酸盐1.碳酸钾K2CO32.碳酸钠Na2CO33.碳酸钙CaCO34.碳酸钡BaCO35.碳酸镁MgCO3 7.碳酸锌ZnCO3 8.碳酸亚铁FeCO3 10.碳酸铜CuCO3 11.碳酸银Ag2CO3 12.碳酸铵(NH4)2CO3(六)碱1.氢氧化钾KOH2.氢氧化钠NaOH3.氢氧化钙Ca(OH)24.氢氧化钡Ba(OH)25.氢氧化镁Mg(OH)26.氢氧化铝Al(OH)237.氢氧化锌Zn(OH)28.氢氧化亚铁Fe(OH)29.氢氧化铁Fe(OH)23 10.氢氧化铜Cu(OH)2 11.氢氧化银AgOH初中化学知识总结(化学方程式)初中化学方程式大全一、化合反应1、镁在空气中燃烧:2Mg + O2 点燃2MgO现象:(1)发出耀眼的白光(2)放出热量(3)生成白色粉末2、铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O4现象:(1)剧烈燃烧,火星四射(2)放出热量(3)生成一种黑色固体注意:瓶底要放少量水或细沙,防止生成的固体物质溅落下来,炸裂瓶底。

中学常见化学式一、常见单质二、化合物1、氧化物2、其他化合物3、常见有机化合物初中化学方程式汇总一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃2Al2O 35. 氢气中空气中燃烧:2H2 +O2点燃 2H2O6. :4P +5O2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:2点燃 CO29. 碳在氧气中不充分燃烧:2C +O2点燃 2CO (2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO2+2H2O12. 酒精在空气中燃烧:C2H52点燃 2CO2+3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg +O2↑14.加热高锰酸钾:2KMnO4加热 K242+O2↑(实验室制氧气原理1)15 H2O2MnO22H2O+ O2↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电 2H2↑+O2↑17.生石灰溶于水英语六级作文:CaO+H2O == Ca(OH)218.二氧化碳可溶于水: H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+ O2点燃 2MgO20.铁和硫酸铜溶液反应:44+ Cu21.氢气还原氧化铜:H2 +CuO 加热 Cu +H2O22. 镁还原氧化铜:Mg+ CuO 加热 Cu +MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2点燃 CO224.木炭还原氧化铜:C + 2CuO 高温 2Cu+ CO2↑25.焦炭还原氧化铁:3高温 4Fe + 3CO2↑(2)煤炉中发生的三个反应:26.煤炉的底层:C +O2 点燃 CO227.煤炉的中层:CO2+ C 高温 2CO282CO +O2点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3+ 2HCl == CaCl2+ H2O +CO2↑30.碳酸不稳定而分解:H2CO3== H2O +CO2↑31.二氧化碳可溶于水: H2O +CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温 CaO+ CO2↑33:Ca(OH)2 +CO2=== CaCO3↓+H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu +CO235.一氧化碳的可燃性:2CO +O2点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO32HCl == 2NaCl+ H2O +CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 +2O2点燃 CO2+2H2O38.酒精在空气中燃烧:C2H5OH +3O2 点燃 2CO2+3H2O39.氢气中空气中燃烧:2H2+ O2点燃 2H2六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg+ O2点燃 2MgO41.铁在氧气中燃烧:3Fe +2O2点燃 Fe3O442. 铜在空气中受热:2Cu +O2加热 2CuO43. 铝在空气中形成氧化膜:2 = 2Al2O3(2)金属单质酸 -------- 盐氢气(置换反应)44. 锌和稀硫酸Zn+ H 2SO 4 = ZnSO 4+ H 2↑45. 铁和稀硫酸Fe +H 2SO 4 = FeSO 4 +H 2↑ 46. 镁和稀硫酸Mg +H 2SO 4 = MgSO 4+ H 2↑47. 铝和稀硫酸2Al+ 3H 2SO 4 = Al 2(SO 4)3 +3H 2↑ 48. 锌和稀盐酸Zn+ 2HCl == ZnCl 2+ H 2↑ 49. 铁和稀盐酸Fe +2HCl == FeCl 2 +H 2↑ 50. 镁和稀盐酸Mg +2HCl == MgCl 2+ H 2↑ 51.铝和稀盐酸2Al+ 6HCl == 2AlCl 3 +3H 2↑(3)金属单质 盐怎样学好高中物理(溶液) ------- 新金属 新盐 52. 铁和硫酸铜溶液反应:Fe +CuSO 4 == FeSO 4 +Cu 53. 锌和硫酸铜溶液反应:Zn +CuSO 4 ==ZnSO 4 +Cu54. 铜和硝酸汞溶液反应:Cu +Hg(NO 3)2 == Cu(NO 3)2 +Hg (3)金属铁的治炼原理:55.3CO +2Fe 2O 3 高温 4Fe +3CO 2↑七、酸、碱、盐1、酸的化学性质(1)酸 金属 -------- 盐 氢气(见上) (2)酸 金属氧化物-------- 盐 水56. 氧化铁和稀盐酸反应:Fe 2O 3 +6HCl ==2FeCl 3 +3H 2O57. 氧化铁和稀硫酸反应:Fe 2O 3 +3H2SO4 == Fe 2(SO4)3 +3H 2O 58. 氧化铜和稀盐酸反应:CuO +2HCl ==CuCl 2 +H2O 59. 氧化铜和稀硫酸反应:CuO+ H 2SO4 == CuSO 4+ H 2O (3)酸 碱 -------- 盐 水(中和反应)60.盐酸和烧碱起反应:HCl +NaOH == NaCl+H 2O61. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 == CaCl 2+2H 2O62. 氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 == AlCl 3 +3H 2O 63. 硫酸和烧碱反应:H 2SO 4+ 2NaOH == Na 2SO 4 +2H 2O (4)酸 盐 -------- 另一种酸 另一种盐64.大理石与稀盐酸反应:CaCO 3+ 2HCl == CaCl 2 +H 2O+ CO 2↑ 65.碳酸钠与稀盐酸反应: Na 2CO 3 +2HCl == 2NaCl+ H 2O+ CO 2↑ 66.碳酸氢钠与稀盐酸反应:NaHCO 3 +HCl== NaCl+H 2O+ CO 2↑ 67. 硫酸和氯化钡溶液反应:H 2SO 4 +BaCl 2 == BaSO 4↓+2HCl 2、碱的幼儿园小班音乐教案化学性质 (1) 碱 非金属氧化物 -------- 盐 水68.苛性钠暴露在空气中变质:2NaOH+CO 2 == Na 2CO 3+ H 2O 69.苛性钠吸收二氧化硫气体:2NaOH +SO 2 == Na 2SO 3 +H 2O 70.苛性钠吸收三氧化硫气体:2NaOH+ SO 3 == Na 2SO 4 +H 2O 71.消石灰放在空气中变质:Ca(OH)2+ CO 2 == CaCO 3↓+H 2O 72. 消石灰吸收二氧化硫:Ca(OH)2 +SO 2 == CaSO 3↓+ H 2O (2)碱 酸-------- 盐 水(中和反应,方程式见上) (3)碱 盐 -------- 另一种碱 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 +Na2CO3== CaCO3↓+ 2NaOH3、盐的化学性质(1)盐(溶液)金属单质------- 另一种金属另一种盐74. 铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4+Cu(2)盐酸-------- 另一种酸另一种盐75.碳酸钠与稀盐酸反应: Na2CO3+2HCl == 2NaCl +H2O+ CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+ H2O +CO2↑(3)盐碱 -------- 另一种碱另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 +Na2CO3== CaCO3↓+ 2NaOH(4)盐盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl +AgNO3== AgCl↓+NaNO378.硫酸钠和氯化钡:Na2SO4+BaCl2== BaSO4↓+2NaCl其他反应类型1、二氧化碳通入澄清石灰水中:CO2 + Ca(OH)2== CaCO3↓+ H2O2、氢氧化钠在空气中变质:CO2+ 2NaOH = Na2CO3+ H2O3、氢氧化钠溶液吸收二氧化硫:SO2 + 2NaOH==Na2SO3+ H2O4、一氧化碳还原氧化铜:CO + CuO Cu + CO25、酒精燃烧:C2H5OH + 3O22CO2+ 3H2O6、甲烷燃烧:CH4 + 2O2CO2+ 2H2O化学方程式反应现象应用1. 2Mg+ O2点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2. 2Hg +O点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验3. 2Cu+ O点燃或Δ2CuO 红色金属变为黑色固体点燃或Δ2Al2O3银白金属变为白色固体5. 3Fe+ 2O点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热6. C+ O2点燃CO2剧烈燃烧、白光、放热、使澄清石灰水变浑浊7. S +O2点燃SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰8. 2H2 O2点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料9. 4P +5O2 点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量10. CH4+2O点燃2H2O+ CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4甲烷和天然气的燃烧11. 2C2H2+ 5O点燃2H2O +4CO2蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4氧炔焰、焊接切割金属12. 2KClO3MnO2、Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气13. 2KMnO4Δ K2MnO42+O2↑ 紫色变为黑色、生成使带火星木条复燃的气体实验室14. 2HgOΔ2Hg+ O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验△点燃点燃15. 2H2O通电2H2↑+ O2↑ 水通电分解为氢气和氧气电解水16. Cu223Δ2CuO +H2O+ CO2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热17. NH4HCO3ΔNH3↑+ H2O+ CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体碳18. Zn+ H2SO4=ZnSO4+H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气19. Fe +H2SO4=FeSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解20. Mg +H2SO4=MgSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解21. 2Al+ 3H2SO4=Al2(SO4)3+ 3H2↑ 有大量气泡产生、金属颗粒逐渐溶解22. Fe2O3+3H2Δ 2Fe +3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性23. Fe3O4+4H2Δ3Fe+ 4H2O 黑色逐渐变为银白色英语翻译、试管壁有液体冶炼金属、24. WO3 +3H2Δ W +3H2O 冶炼金属钨、利用氢气的还原性25. MoO32ΔMo +3H2O 冶炼金属钼、利用氢气的还原性26. 2Na+ Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、27. H2+Cl2点燃或光照 2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸28. CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验29. 2C +O点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因点燃2CO2蓝色火焰煤气燃烧31. C+ CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属32. 2Fe2O3+ 3C 高温4Fe+ 3CO2↑ 冶炼金属33. Fe3O4+2C高温3Fe+ 2CO2↑ 冶炼金属34. C+ CO2 高温2CO35. CO2+H223碳酸使石蕊变红证明碳酸的酸性小学三语文教学论文36. H2CO3ΔCO2↑+ H2O 石蕊红色褪去2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁38. CaCO3 +H2O+ CO2= Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化39. Ca(HCO3)2Δ CaCO3↓+ H2O +CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.40. 2NaHCO3ΔNa2CO3+ H2O +CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头41. CaCO3 高温 CaO +CO2↑ 工业制备二氧化碳和生石灰42. CaCO3 2+ H2O +CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢温馨提示:最好仔细阅读后才下载使用,万分感谢!。

中学常见化学式一、常见单质二、化合物1、氧化物2、其他化合物3、常见有机化合物初中化学方程式汇总一、氧气的性质:〔1〕单质与氧气的反响:〔化合反响〕1. 镁在空气中燃烧:2Mg+ O点燃2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃Fe3O43. 铜在空气中受热:2Cu+ O加热2CuO4. 铝在空气中燃烧:4Al +3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2+O点燃2H2O6. 红磷在空气中燃烧〔研究空气组成的实验〕:4P +5O点燃2P2O57. 硫粉在空气中燃烧:S +O点燃SO28. 碳在氧气中充分燃烧:C +O点燃CO29. 碳在氧气中不充分燃烧:2C +O点燃2CO〔2〕化合物与氧气的反响:10. 一氧化碳在氧气中燃烧:2CO+O点燃2CO211. 甲烷在空气中燃烧:CH4+2O点燃CO2+2H2O12. 酒精在空气中燃烧:C2H5OH +3O点燃2CO2+3H2O〔3〕氧气的来源:13.玻义耳研究空气的成分实验2HgO 加热Hg +O2↑14.加热高锰酸钾:2KMnO加热K2MnO4+ MnO2+O2↑〔实验室制氧气原理1〕15.过氧化氢在二氧化锰作催化剂条件下分解反响:H2O2MnO22H2O+ O2↑〔实验室制氧气原理2〕二、自然界中的水:16.水在直流电的作用下分解〔研究水的组成实验〕:2H2O 通电2H2↑+O2↑17.生石灰溶于水英语六级作文:CaO +H2O == Ca(OH)218.二氧化碳可溶于水:H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+ O2点燃2MgO20.铁和硫酸铜溶液反响:Fe+ CuSO4 === FeSO4+ Cu21.氢气复原氧化铜:H2 +CuO 加热Cu +H2O22. 镁复原氧化铜:Mg+ CuO 加热Cu +MgO四、碳和碳的氧化物:〔1〕碳的化学性质23. 碳在氧气中充分燃烧:C + O点燃CO224.木炭复原氧化铜:C + 2CuO 高温2Cu+ CO2↑25.焦炭复原氧化铁:3C + 2Fe2O3高温4Fe + 3CO2↑〔2〕煤炉中发生的三个反响:〔几个化合反响〕26.煤炉的底层:C +O点燃CO227.煤炉的中层:CO2+ C 高温2CO28.煤炉的上部蓝色火焰的产生:2CO +O点燃2CO2〔3〕二氧化碳的制法与性质:29.XX石与稀盐酸反响〔实验室制二氧化碳〕:CaCO3+ 2HCl == CaCl2+ H2O +CO2↑30.碳酸不稳定而分解:H2CO3== H2O +CO2↑31.二氧化碳可溶于水:H2O +CO2== H2CO332.高温煅烧石灰石〔工业制二氧化碳〕:CaCO高温CaO+ CO2↑33.石灰水与中学历史教学园地二氧化碳反响〔鉴别二氧化碳〕:Ca(OH)2+CO2=== CaCO3↓+H2O〔4〕一氧化碳的性质:34.一氧化碳复原氧化铜:CO+ CuO 加热Cu +CO235.一氧化碳的可燃性:2CO +O2点燃2CO2其它反响:36.碳酸钠与稀盐酸反响〔灭火器的原理〕:Na2CO32HCl == 2NaCl+ H2O +CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4+2O点燃CO2+2H2O38.酒精在空气中燃烧:C2H5OH +3O2 点燃2CO2+3H2O39.氢气中空气中燃烧:2H2+ O点燃2H2O六、金属〔1〕金属与氧气反响:40.镁在空气中燃烧:2Mg+ O点燃2MgO41. 铁在氧气中燃烧:3Fe +2O 点燃Fe 3O 4 42. 铜在空气中受热:2Cu +O 加热 2CuO 43. 铝在空气中形成氧化膜:4Al+ 3O 2 = 2Al 2O 3 〔2〕金属单质 酸 -------- 盐 氢气 〔置换反响〕 44. 锌和稀硫酸Zn+ H 2SO 4 = ZnSO 4+ H 2↑ 45. 铁和稀硫酸Fe +H 2SO 4 = FeSO 4+H 2↑ 46. 镁和稀硫酸Mg +H 2SO 4 = MgSO 4+ H 2↑ 47. 铝和稀硫酸2Al+ 3H 2SO 4 = Al 2(SO 4)3+3H 2↑ 48. 锌和稀盐酸Zn+ 2HCl == ZnCl 2+ H 2↑ 49. 铁和稀盐酸Fe +2HCl == FeCl 2+H 2↑ 50. 镁和稀盐酸Mg +2HCl == MgCl 2+ H 2↑ 51.铝和稀盐酸2Al+ 6HCl == 2AlCl 3+3H 2↑〔3〕金属单质 盐怎样学好高中物理〔溶液〕 ------- 新金属 新盐 52. 铁和硫酸铜溶液反响:Fe +CuSO 4 == FeSO 4+Cu 53. 锌和硫酸铜溶液反响:Zn +CuSO 4 ==ZnSO 4+Cu 54. 铜和硝酸汞溶液反响:Cu +Hg(NO 3)2 == Cu(NO 3)2+Hg 〔3〕金属铁的治炼原理: 55.3CO +2Fe 2O 3 高温 4Fe +3CO 2↑七、酸、碱、盐 1、酸的化学性质〔1〕酸 金属 -------- 盐 氢气〔见上〕 〔2〕酸 金属氧化物-------- 盐 水56. 氧化铁和稀盐酸反响:Fe 2O 3 +6HCl ==2FeCl 3+3H 2O57. 氧化铁和稀硫酸反响:Fe2O3+3H2SO4 == Fe2(SO4)3+3H2O58. 氧化铜和稀盐酸反响:CuO +2HCl ==CuCl2+H2O59. 氧化铜和稀硫酸反响:CuO+ H2SO4 == CuSO4+ H2O〔3〕酸碱-------- 盐水〔中和反响〕60.盐酸和烧碱起反响:HCl +NaOH == NaCl+H2O61. 盐酸和氢氧化钙反响:2HCl+ Ca(OH)2 == CaCl2+2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 == AlCl3+3H2O63. 硫酸和烧碱反响:H2SO4+ 2NaOH == Na2SO4+2H2O〔4〕酸盐-------- 另一种酸另一种盐64.XX石与稀盐酸反响:CaCO3+2HCl == CaCl2+H2O+ CO2↑65.碳酸钠与稀盐酸反响: Na2CO3+2HCl == 2NaCl+ H2O+ CO2↑66.碳酸氢钠与稀盐酸反响:NaHCO3+HCl== NaCl+H2O+ CO2↑67. 硫酸和氯化钡溶液反响:H2SO4+BaCl2== BaSO4↓+2HCl2、碱的幼儿园小班音乐教案化学性质〔1〕碱非金属氧化物-------- 盐水68.苛性钠暴露在空气中变质:2NaOH+CO2 == Na2CO3+ H2O69.苛性钠吸收二氧化硫气体:2NaOH +SO2 == Na2SO3+H2O70.苛性钠吸收三氧化硫气体:2NaOH+ SO3 == Na2SO4+H2O71.消石灰放在空气中变质:Ca(OH)2+ CO2== CaCO3↓+H2O72. 消石灰吸收二氧化硫:Ca(OH)2+SO2== CaSO3↓+ H2O〔2〕碱酸-------- 盐水〔中和反响,方程式见上〕〔3〕碱盐-------- 另一种碱另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2+Na 2CO 3 == CaCO 3↓+ 2NaOH 3、盐的化学性质〔1〕盐〔溶液〕 金属单质------- 另一种金属 另一种盐 74. 铁和硫酸铜溶液反响:Fe+ CuSO 4 == FeSO 4+Cu 〔2〕盐 酸-------- 另一种酸 另一种盐75.碳酸钠与稀盐酸反响: Na 2CO 3 +2HCl == 2NaCl +H 2O+ CO 2↑ 碳酸氢钠与稀盐酸反响:NaHCO 3+HCl== NaCl+ H 2O +CO 2↑ 〔3〕盐 碱 -------- 另一种碱 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 +Na 2CO 3 == CaCO 3↓+ 2NaOH 〔4〕盐 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl +AgNO 3 == AgCl ↓+NaNO 3 78.硫酸钠和氯化钡:Na 2SO 4+BaCl 2 == BaSO4↓+2NaCl其他反响类型1、二氧化碳通入澄清石灰水中:CO 2 + Ca(OH)2 == CaCO 3↓+ H 2O2、氢氧化钠在空气中变质:CO 2+ 2NaOH = Na 2CO 3 + H 2O3、氢氧化钠溶液吸收二氧化硫:SO 2 + 2NaOH==Na 2SO 3+ H 2O4、一氧化碳复原氧化铜:CO + CuO Cu + CO 25、酒精燃烧:C 2H 5OH + 3O 2 2CO 2 + 3H 2O6、甲烷燃烧:CH 4 + 2O 2 CO 2 + 2H 2O化学方程式 反响现象 应用 1. 2Mg+ O点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟 白色信号弹△ 点燃点燃2. 2Hg +O点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验3. 2Cu+ O2点燃或Δ2CuO 红色金属变为黑色固体4. 4Al+ 3O点燃或Δ2Al2O3银白金属变为白色固体5. 3Fe+ 2O点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热6. C+ O点燃CO2剧烈燃烧、白光、放热、使澄清石灰水变浑浊7. S +O点燃SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰8. 2H2 O点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体〔水〕高能燃料9. 4P +5O2 点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量10.CH4+2O点燃2H2O+ CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体〔水〕甲烷和天然气的燃烧11. 2C2H2+ 5O2点燃2H2O +4CO2蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体〔水〕氧炔焰、焊接切割金属12. 2KClO3MnO2、Δ2KCl +3O2↑生成使带火星的木条复燃的气体实验室制备氧气13. 2KMnO4ΔK2MnO4MnO2+O2↑紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧论文气14. 2HgOΔ2Hg+ O2↑红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验15. 2H2O通电2H2↑+ O2↑水通电分解为氢气和氧气电解水16. Cu2(OH)2CO3Δ2CuO +H2O+ CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热17. NH4HCO3ΔNH3↑+ H2O+ CO2↑白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失18. Zn+ H2SO4=ZnSO4+H2↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气19. Fe +H2SO4=FeSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解20. Mg +H2SO4=MgSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解21. 2Al+ 3H2SO4=Al2(SO4)3+ 3H2↑有大量气泡产生、金属颗粒逐渐溶解22. Fe2O3+3H2Δ 2Fe +3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的复原性23. Fe3O4+4H2Δ3Fe+ 4H2O 黑色逐渐变为银白色英语翻译、试管壁有液体冶炼金属、利用氢气的复原性24. WO3+3H2Δ W +3H2O 冶炼金属钨、利用氢气的复原性25. MoO3+3H2ΔMo +3H2O 冶炼金属钼、利用氢气的复原性26. 2Na+ Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、27. H2+Cl点燃或光照2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸28. CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验29. 2C +O点燃2CO 煤炉中常见反响、空气污染物之一、煤气中毒原因30. 2CO +O点燃2CO2蓝色火焰煤气燃烧31. C+ CuO 高温2Cu+ CO2↑黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属32. 2Fe2O3+ 3C 高温4Fe+ 3CO2↑冶炼金属33. Fe3O4+2C高温3Fe+ 2CO2↑冶炼金属34. C+ CO2 高温2CO35. CO2+H2O = H2CO3碳酸使石蕊变红证明碳酸的酸性小学三语文教学论文36. H2CO3ΔCO2↑+ H2O 石蕊红色褪去37. Ca(OH)2 +CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁38. CaCO3 +H2O+ CO2= Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化39. Ca(HCO3)2Δ CaCO3↓+ H2O +CO2↑白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成40. 2NaHCO32CO3+ H2O +CO2↑产生使澄清石灰水变浑浊的气体小苏打蒸馒头41. CaCO高温CaO +CO2↑工业制备二氧化碳和生石灰42. CaCO3 +2HCl=CaCl2+ H2O +CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢。

初中常见化学式及化学方程式常见的化学式一、常见单质氢气H2氮气N2氯气Cl2氧气O2臭氧O3氦气He氖气Ne氩气Ar碳C硅Si硫S磷P碘I2钾K钙Ca钠Na镁Mg铝Al锌Zn铁Fe铜Cu汞Hg银Ag二、化合物水H2O三氧化硫SO3一氧化碳CO二氧化碳CO2五氧化二磷P2O5过氧化氢H2O2二氧化氮NO2二氧化硫SO2氧化钙CaO氧化亚铁FeO氧化铁Fe2O3四氧化三铁Fe3O4氧化镁MgO氧化锌ZnO二氧化锰MnO2氧化汞HgO氧化铝Al2O3氧化铜CuO2、其他化合物硝酸HNO3硫酸H2SO4盐酸HCl碳酸H2CO3硫化氢H2S氢氧化钠NaOH氢氧化钾KOH氢氧化钙CaOH2氢氧化镁MgOH2氢氧化铝AlOH3氢氧化锌ZnOH2氢氧化铁FeOH3氢氧化亚铁FeOH2氢氧化铜CuOH2氢氧化钡BaOH2氨水NH3·H2O氯化钠NaCl氯化铜CuCl2氯化铝AlCl3氯化钾KCl氯化亚铁FeCl2氯化铁FeCl3氯化银AgCl氯化钙CaCl2氯化镁MgCl2氯化钡BaCl2氯化锌ZnCl2硫酸铜CuSO4高锰酸钾KMnO4锰酸钾K2MnO4氯酸钾KClO3碳酸钙CaCO3硝酸钾KNO3 硝酸钠NaNO3初中化学方程式全已配平.一、化合反应1、镁在空气中燃烧:2Mg+ O2点燃 2MgO2、铁在氧气中燃烧:3Fe +2O2点燃 Fe3O43、铝在空气中燃烧:4Al+ 3O2点燃 2Al2O34、氢气在空气中燃烧:2H2 +O2点燃 2H2O5、红磷在空气中燃烧:4P +5O2点燃 2P2O56、硫粉在空气中燃烧: S+ O2点燃 SO27、碳在氧气中充分燃烧:C +O2 点燃 CO28、碳在氧气中不充分燃烧:2C +O2点燃 2CO9、二氧化碳通过灼热碳层: C +CO2高温 2CO10、一氧化碳在氧气中燃烧:2CO +O2 点燃 2CO211、二氧化碳和水反应二氧化碳通入紫色石蕊试液:CO2 +H2O === H2CO312、生石灰溶于水:CaO+ H2O === CaOH213、无水硫酸铜作干燥剂:CuSO4 +5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃 2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O +O2↑16、加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 +O2↑17、水在直流电的作用下分解:2H2O 通电 2H2↑+O2↑18、碳酸化学物理学报不稳定而分解:H2CO3 === H2O +CO2↑19、高温煅烧石灰石二氧化碳工业制法:CaCO3高温 CaO+ CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu21、锌和稀硫酸反应实验室制氢气:Zn+ H2SO4 == ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl === MgCl2 +H2↑23、氢气还原氧化铜:H2 +CuO 加热 Cu +H2O24、木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑25、甲烷在空气中燃烧:CH4 +2O2 点燃 CO2+2H2O26、水蒸气通过灼热碳层:H2O +C 高温 H2 +CO27、焦炭还原氧化铁:3C +2Fe2O3高温 4Fe +3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+ CuSO4== CuOH2↓+ Na2SO429、甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O30、酒精在空气中燃烧:C2H5OH+ 3O2点燃 2CO2 +3H2O31、一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO232、一氧化碳还原氧化铁:3CO+ Fe2O3高温 2Fe+ 3CO233、二氧化碳通过澄清石灰水检验二氧化碳:CaOH2+ CO2==== CaCO3 ↓+ H2O34、氢氧化钠和二氧化碳反应除去二氧化碳:2NaOH+ CO2 ==== Na2CO3 +H2O35、石灰石或小学音乐教案大理石与稀盐酸反应二氧化碳的实验室制法:CaCO3 +2HCl === CaCl2 +H2O +CO2↑36、碳酸钠与浓盐酸反应泡沫灭火器的原理: Na2CO3+ 2HCl === 2NaCl +H2O +CO2↑一.物质与氧气的反应:1单质与氧气的反应:1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 +O2点燃 2H2O6. 红磷在空气中燃烧:4P+ 5O2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:C+ O2点燃 CO29. 碳在氧气中不充分燃烧:2C+ O2点燃 2CO2化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+ O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO2 2H2O12. 酒精在空气中燃烧:C2H5OH +3O2点燃 2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电 2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2OH2CO3加热 2CuO +H2O +CO2↑15. 加热氯酸钾有少量的二氧化锰:2KClO3 ==== 2KCl+ 3O2↑16. 加热高锰酸钾:2KMnO4加热 K2MnO4 +MnO2 +O2↑17. 碳酸不稳定而分解:H2CO3 === H2O +CO2↑18. 高温煅烧石灰石:CaCO3 高温 CaO +CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+ CuO 加热 Cu+ H2O20. 木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑2 初三化学方程式大合集21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe+ 3CO2↑22. 焦炭还原四氧化三铁:2C +Fe3O4高温 3Fe+ 2CO2↑23. 一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3高温 2Fe +3CO225. 一氧化碳还原四氧化三铁:4CO +Fe3O4高温 3Fe+ 4CO2四.单质、氧化物、酸、碱、盐的相互关系1金属单质+酸 -------- 盐+氢气置换反应26. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑27. 铁和稀硫酸Fe +H2SO4 = FeSO4+ H2↑28. 镁和稀硫酸Mg +H2SO4 = MgSO4 +H2↑29. 铝和稀硫酸2Al+ 3H2SO4 = Al2SO43 +3H2↑30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑32. 镁和稀盐酸Mg +2HCl === MgCl2+ H2↑33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑2金属单质+盐溶液 ------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu35. 锌和硫酸铜溶液反应:Zn+ CuSO4 === ZnSO4+ Cu36. 铜和硝酸汞溶液反应:Cu +HgNO32 === CuNO32 +Hg3碱性氧化物+酸 -------- 盐+水37. 氧化铁和稀盐酸反应:Fe2O3+ 6HCl === 2FeCl3+ 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 === Fe2SO43+ 3H2O39. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl2 +H2O40. 氧化铜和稀硫酸反应:CuO +H2SO4 ==== CuSO4+ H2O41. 氧化镁和稀硫酸反应:MgO+ H2SO4 ==== MgSO4+ H2O42. 氧化钙和稀盐酸反应:CaO +2HCl ==== CaCl2 +H2O4酸性氧化物+碱 -------- 盐+水43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O44.苛性钠吸收二氧化硫气体:2NaOH +SO2 ==== Na2SO3 +H2O45.苛性钠吸收三氧化硫气体:2NaOH+ SO3 ==== Na2SO4+ H2O46.消石灰放在空气中变质:CaOH2+ CO2 ==== CaCO3 ↓+ H2O47. 消石灰吸收二氧化硫:CaOH2 +SO2 ==== CaSO3↓+H2O5酸+碱 -------- 盐+水48.盐酸和烧碱起反应:HCl+ NaOH ==== NaCl+ H2O49. 盐酸和氢氧化钾反应:HCl+ KOH ==== KCl+H2O50.盐酸和氢氧化初中家长会课件铜反应:2HCl+ CuOH2==== CuCl2+2H2O51. 盐酸和氢氧化钙反应:2HCl+ CaOH2 ==== CaCl2 +2H2O52. 盐酸和氢氧化铁反应:3HCl+ FeOH3 ==== FeCl3 +3H2O53.氢氧化铝药物治疗胃酸过多:3HCl +AlOH3 ==== AlCl3 +3H2O54.硫酸和烧碱反应:H2SO4 +2NaOH ==== Na2SO4 +2H2O55.硫酸和氢氧化钾反应:H2SO4 +2KOH ==== K2SO4 +2H2O56.硫酸和氢氧化铜反应:H2SO4 +CuOH2 ==== CuSO4 +2H2O57. 硫酸和氢氧化铁反应:3H2SO4 +2FeOH3==== Fe2SO43+ 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O6酸+盐 -------- 另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO3 +2HCl === CaCl2 H2O +CO2↑60.碳酸钠与稀盐酸反应: Na2CO3 +2HCl === 2NaCl +H2O+ CO2↑61.碳酸镁与稀盐酸反应: MgCO3 +2HCl === MgCl2 +H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+ AgNO3=== AgCl↓+ HNO363.硫酸和碳酸钠反应:Na2CO3 +H2SO4 === Na2SO4 +H2O +CO2↑64.硫酸和氯化钡溶液反应:H2SO4 +BaCl2 ==== BaSO4↓+ 2HCl7碱+盐 -------- 另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO4 ==== CuOH2↓ Na2SO466.氢氧化钠与氯化铁:3NaOH FeCl3 ==== FeOH3↓ 3NaCl67.氢氧化钠与氯化镁:2NaOH MgCl2 ==== MgOH2↓ 2NaCl68. 氢氧化钠与氯化铜:2NaOH CuCl2 ==== CuOH2↓ 2NaCl69. 氢氧化钙与碳酸钠:CaOH2 Na2CO3 === CaCO3↓ 2NaOH8盐+盐 ----- 两种新盐70.氯化钠溶液新概念英语第二册和硝酸银溶液:NaCl +AgNO3 ==== AgCl↓+ NaNO371.硫酸钠和氯化钡:Na2SO4+ BaCl2 ==== BaSO4↓+ 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+ H2O === H2CO373.生石灰溶于水:CaO+ H2O === CaOH274.氧化钠溶于水:Na2O +H2O ==== 2NaOH75.三氧化硫溶于水:SO3 +H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热 CuSO4 5H2O77.无水硫酸铜作干燥剂:CuSO4+ 5H2O ==== CuSO4·5H2化学方程式反应现象应用2Mg+ O点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg +O点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验2Cu+ O点燃或Δ2CuO 红色金属变为黑色固体4Al+ 3O点燃或Δ2Al2O3银白金属变为白色固体3Fe+ 2O点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热 4Fe +3O2高温2Fe2O3C+ O2点燃CO2剧烈燃烧、白光、放热、使石灰水变浑浊S +O2点燃SO2剧大学英语四级烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2 O2点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体水高能燃料4P +5O2 点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O点燃2H2O+ CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体水甲烷和天然气的燃烧2C2H2+ 5O点燃2H2O +4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体水氧炔焰、焊接切割金属2KClO3MnO2、Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气2KMnO4Δ K2MnO4 MnO2 +O2↑ 紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧论文气2HgOΔ2Hg+ O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H2↑+ O2↑ 水通电分解为氢气和氧气电解水Cu2OH2CO3Δ2CuO +H2O+ CO2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3ΔNH3↑+ H2O+ CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+ H2SO4=ZnSO4 +H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe +H2SO4=FeSO4 +H2↑ 有大量气泡产生、金属颗粒逐渐溶解Mg +H2SO4 =MgSO4 +H2↑ 有大量气泡产生、金属颗粒逐渐溶解2Al+ 3H2SO4=Al2SO43+ 3H2↑ 有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2Δ2Fe +3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2 Δ3Fe+ 4H2O 黑色逐渐变为银白色英语翻译、试管壁有液体冶炼金属、利用氢气的还原性WO3 +3H2Δ W +3H2O 冶炼金属钨、利用氢气的还原性MoO3 +3H2ΔMo +3H2O 冶炼金属钼、利用氢气的还原性2Na+ Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2 +Cl2点燃或光照 2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4 +2NaOH=CuOH2↓+ Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C +O点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因2CO +O点燃2CO2蓝色火焰煤气燃烧C+ CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+ 3C 高温4Fe+ 3CO2↑ 冶炼金属Fe3O4 +2C高温3Fe+ 2CO2↑ 冶炼金属C+ CO2 高温2COCO2+H2O = H2CO3碳酸使石蕊变红证明碳酸的酸性小学三语文教学论文H2CO3 ΔCO2↑+ H2O 石蕊红色褪去CaOH2 +CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3 +H2O+ CO2 = CaHCO32 白色沉淀逐渐溶解溶洞的形成,石头的风化CaHCO32Δ CaCO3↓+ H2O +CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3+ H2O +CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 高温 CaO +CO2↑ 工业制备二氧化碳和生石灰CaCO3 +2HCl=CaCl2+ H2O +CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢初中化学方程式汇总一、氧气的性质:1单质与氧气的反应:化合反应1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2 +O2 点燃 2H2O6. 红磷在空气中燃烧研究空气组成的实验:4P +5O2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:C +O2点燃 CO29. 碳在氧气中不充分燃烧:2C +O2点燃 2CO2化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O12. 酒精在空气中燃烧:C2H5OH +3O2点燃 2CO2 +3H2O3氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg +O2 ↑14.加热高锰酸钾:2KMnO4加热 K2MnO4+ MnO2 +O2↑实验室制氧气原理1 15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2 MnO22H2O+ O2↑实验室制氧气原理2二、自然界中的水:16.水在直流电的作用下分解研究水的组成实验:2H2O 通电 2H2↑+O2 ↑ 17.生石灰溶于水英语六级作文:CaO +H2O == CaOH218.二氧化碳可溶于水: H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+ O2点燃 2MgO20.铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu21.氢气还原氧化铜:H2 +CuO 加热 Cu +H2O22. 镁还原氧化铜:Mg+ CuO 加热 Cu +MgO四、碳和碳的氧化物:1碳的化学性质23. 碳在氧气中充分燃烧:C + O2点燃 CO224.木炭还原氧化铜:C + 2CuO 高温 2Cu+ CO2↑25.焦炭还原氧化铁:3C + 2Fe2O3高温 4Fe + 3CO2↑2煤炉中发生的三个反应:几个化合反应26.煤炉的底层:C +O2 点燃 CO227.煤炉的中层:CO2+ C 高温 2CO28.煤炉的上部蓝色火焰的产生:2CO +O2点燃 2CO23二氧化碳的制法与性质:29.大理石与稀盐酸反应实验室制二氧化碳:CaCO3+ 2HCl == CaCl2+ H2O +CO2↑30.碳酸不稳定而分解:H2CO3 == H2O +CO2↑31.二氧化碳可溶于水: H2O +CO2== H2CO332.高温煅烧石灰石工业制二氧化碳:CaCO3高温 CaO+ CO2↑ 33.石灰水与中学历史教学园地二氧化碳反应鉴别二氧化碳:CaOH2 +CO2 === CaCO3↓+H2O4一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu +CO235.一氧化碳的可燃性:2CO +O2点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应灭火器的原理:Na2CO3 2HCl == 2NaCl+ H2O +CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O38.酒精在空气中燃烧:C2H5OH +3O2 点燃 2CO2 +3H2O 39.氢气中空气中燃烧:2H2+ O2点燃 2H2O六、金属1金属与氧气反应:40.镁在空气中燃烧:2Mg+ O2点燃 2MgO41.铁在氧气中燃烧:3Fe +2O2点燃 Fe3O442. 铜在空气中受热:2Cu +O2加热 2CuO43. 铝在空气中形成氧化膜:4Al+ 3O2 = 2Al2O32金属单质酸 -------- 盐氢气置换反应44. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑45. 铁和稀硫酸Fe +H2SO4 = FeSO4 +H2↑46. 镁和稀硫酸Mg +H2SO4 = MgSO4+ H2↑47. 铝和稀硫酸2Al+ 3H2SO4 = Al2SO43 +3H2↑48. 锌和稀盐酸Zn+ 2HCl == ZnCl2+ H2↑49. 铁和稀盐酸Fe +2HCl == FeCl2 +H2↑50. 镁和稀盐酸Mg +2HCl == MgCl2+ H2↑51.铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑3金属单质盐怎样学好高中物理溶液 ------- 新金属新盐52. 铁和硫酸铜溶液反应:Fe +CuSO4 == FeSO4 +Cu53. 锌和硫酸铜溶液反应:Zn +CuSO4 ==ZnSO4 +Cu54. 铜和硝酸汞溶液反应:Cu +HgNO32 == CuNO32 +Hg3金属铁的治炼原理:55.3CO +2Fe2O3 高温 4Fe +3CO2↑七、酸、碱、盐1、酸的化学性质1酸金属 -------- 盐氢气见上2酸金属氧化物-------- 盐水56. 氧化铁和稀盐酸反应:Fe2O3 +6HCl ==2FeCl3 +3H2O57. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 == Fe2SO43 +3H2O58. 氧化铜和稀盐酸反应:CuO +2HCl ==CuCl2 +H2O59. 氧化铜和稀硫酸反应:CuO+ H2SO4 == CuSO4+ H2O3酸碱 -------- 盐水中和反应60.盐酸和烧碱起反应:HCl +NaOH == NaCl+H2O61. 盐酸和氢氧化钙反应:2HCl+ CaOH2 == CaCl2+2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl +AlOH3 == AlCl3 +3H2O63. 硫酸和烧碱反应:H2SO4+ 2NaOH == Na2SO4 +2H2O4酸盐 -------- 另一种酸另一种盐64.大理石与稀盐酸反应:CaCO3+2HCl == CaCl2 +H2O+ CO2↑ 65.碳酸钠与稀盐酸反应: Na2CO3 +2HCl == 2NaCl+ H2O+ CO2↑ 66.碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+H2O+ CO2↑ 67. 硫酸和氯化钡溶液反应:H2SO4 +BaCl2 == BaSO4↓+2HCl 2、碱的幼儿园小班音乐教案化学性质1 碱非金属氧化物 -------- 盐水68.苛性钠暴露在空气中变质:2NaOH+CO2 == Na2CO3+ H2O 69.苛性钠吸收二氧化硫气体:2NaOH +SO2 == Na2SO3 +H2O 70.苛性钠吸收三氧化硫气体:2NaOH+ SO3 == Na2SO4 +H2O 71.消石灰放在空气中变质:CaOH2+ CO2 == CaCO3↓+H2O72. 消石灰吸收二氧化硫:CaOH2 +SO2 == CaSO3↓+ H2O2碱酸-------- 盐水中和反应,方程式见上3碱盐 -------- 另一种碱另一种盐73. 氢氧化钙与碳酸钠:CaOH2 +Na2CO3 == CaCO3↓+ 2NaOH3、盐的化学性质1盐溶液金属单质------- 另一种金属另一种盐74. 铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu2盐酸-------- 另一种酸另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 +2HCl == 2NaCl +H2O+ CO2↑ 碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+ H2O +CO2↑3盐 碱 -------- 另一种碱 另一种盐76. 氢氧化钙与碳酸钠:CaOH 2 +Na 2CO 3 == CaCO 3↓+ 2NaOH 4盐 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl +AgNO 3 == AgCl↓+NaNO 3 78.硫酸钠和氯化钡:Na 2SO 4 +BaCl 2 == BaSO4↓+2NaCl一、其他反应类型1、二氧化碳通入澄清石灰水中:CO 2 + CaOH 2 == CaCO 3↓+ H 2O2、氢氧化钠在空气中变质:CO 2+ 2NaOH = Na 2CO 3 + H 2O3、氢氧化钠溶液吸收二氧化硫:SO 2 + 2NaOH ==Na 2SO 3+ H 2O4、一氧化碳还原氧化铜:CO + CuO Cu + CO 25、酒精燃烧:C 2H 5OH + 3O 2 2CO 2 + 3H 2O6、甲烷燃烧:CH 4 + 2O 2 CO 2 + 2H 2O△点燃 点燃。
初中化学常见物质的化学式一、常见的单质:(一)金属单质:钾:K 钙:Ca 钠:Na 镁:Mg 铝:Al 锌:Zn 铁:Fe 锡:Sn 铅:Pb 铜:Cu 汞:Hg 银:Ag 铂:Pt 金:Au 钡:Ba 钨:W (二)非金属单质:碳:C 硫:S 磷:P硅:Si 碘:I2溴:Br2 氧气:O2氮气:N2氢气:H2氯气:Cl2(三)稀有气体单质:氦气:He 氖气:Ne 氩气:Ar 氪气:Kr 氙气:Xe二、常见的化合物:(一)氧化物:氧化钾:K2O 氧化钠:Na2O 氧化银:Ag2O 水:H2O氧化钙:CaO 氧化钡:BaO 氧化镁:MgO 氧化锌:ZnO 氧化铜;CuO 氧化铝:Al2O3二氧化锰:MnO2二氧化硅:SiO2五氧化二磷:P2O5一氧化碳:CO 二氧化碳:CO2一氧化氮:NO 二氧化氮:NO2二氧化硫:SO2三氧化硫:SO3氧化亚铁:FeO 氧化铁:Fe2O3四氧化三铁:Fe3O4(二)氯化物:氯化钾:KCl 氯化钠:NaCl 氯化银:AgCl 氯化氢;HCl氯化钙:CaCl2氯化钡:BaCl2氯化镁:MgCl2氯化锌:ZnCl2氯化铜:CuCl2 氯化铝:AlCl3氯化亚铁:FeCl2氯化铁:FeCl3(三)含原子团的化合物:硝酸:HNO3硫酸:H2SO4碳酸:H2CO3磷酸:H3PO4氢氧化钾:KOH 氢氧化钠:NaOH 氢氧化钙:Ca(OH)2氢氧化钡:Ba(OH)2氢氧化镁:Mg(OH)2氢氧化铜:Cu(OH)2氢氧化铝:Al(OH)3氢氧化亚铁:Fe(OH)2氢氧化铁:Fe(OH)3硝酸钾:KNO3硝酸钠:NaNO3硝酸钙:Ca(NO3)2硝酸钡:Ba(NO3)2硝酸镁:Mg(NO3)2硝酸铜:Cu(NO3)2硝酸铝:Al(NO3)3硝酸亚铁:Fe(NO3)2硝酸铁:Fe(NO3)3硫酸钾:K2SO4硫酸钠:Na2 SO4硫酸钙:Ca SO4硫酸钡:BaSO4硫酸镁:MgSO4硫酸铜:CuSO4硫酸铝:Al2 (SO4)3硫酸亚铁:FeSO4硫酸铁:Fe2 (SO4)3碳酸钾:K2CO3碳酸钠:Na2CO3碳酸钙:CaCO3碳酸钡:BaCO3碳酸镁:MgCO3碳酸铜:CuCO3氯化铵:NH4Cl 硝酸铵:NH4NO3硫酸铵:(NH4)2SO4碳酸铵:(NH4)2CO3碳酸氢铵:NH4HCO3(四)其他化合物:氯酸钾:KClO3高锰酸钾:KMnO4锰酸钾:K2MnO4过氧化氢:H2O2氨气:NH3初中常用的化学方程式 一、物质与氧气的反应:1、硫燃烧:S+O 2====SO 22、碳燃烧:C+O 2====CO 23、磷燃烧:4P+5O 2====2P 2O 54、镁燃烧:2Mg+O 2====2MgO5、铁丝燃烧:3Fe+2O 2====Fe 3O 46、铝箔燃烧:4Al+3O 2====2Al 2O 37、氢气燃烧:2H 2+O 2====2H 2O8、汞加热:2Hg+O 2====2HgO 二、生成氧气的反应:1、过氧化氢制氧气:2H 2O 2 ===== 2H 2O+O 2↑2、高锰酸钾制氧气 : 2KMnO 4====K 2MnO 4+MnO 2+O 2↑3、氯酸钾制氧气: 2KClO 3===== 2KCl+3O 2↑4、电解水:2H 2O===== 2H 2↑+O 2↑5、氧化汞受热分解:2HgO====2Hg+O 2↑三、氢气的性质与制法:1、锌粒与稀硫酸反应:Zn+H 2SO 4====ZnSO 4+H 2↑2、氢气还原氧化铜:H 2+CuO====Cu+H 2O点燃点燃 点燃点燃 点燃点燃点燃 点燃MnO 2 △ MnO 2△通电 △△。
初中常见化学式及化学方程式常见的化学式一、常见单质氢气H2氮气N2氯气Cl2氧气O2臭氧O3氦气He 氖气Ne氩气Ar碳C硅Si硫S磷P碘I2钾K钙Ca钠Na镁Mg铝Al锌Zn 铁Fe铜Cu汞Hg银Ag二、化合物1、氧化物水H2O三氧化硫SO3一氧化碳CO二氧化碳CO2五氧化二磷P2O5过氧化氢H2O2二氧化氮NO2二氧化硫SO2氧化钙CaO氧化亚铁FeO氧化铁Fe2O3四氧化三铁Fe3O4氧化镁MgO氧化锌ZnO二氧化锰MnO2氧化汞HgO氧化铝Al2O3氧化铜CuO2、其他化合物硝酸HNO3硫酸H2SO4盐酸HCl碳酸H2CO3硫化氢H2S氢氧化钠NaOH氢氧化钾KOH氢氧化钙Ca(OH)2氢氧化镁Mg(OH)2氢氧化铝Al(OH)3氢氧化锌Zn(OH)2氢氧化铁Fe(OH)3氢氧化亚铁Fe(OH)2氢氧化铜Cu(OH)2氢氧化钡Ba(OH)2氨水NH3·H2O氯化钠NaCl氯化铜CuCl2氯化铝AlCl3氯化钾KCl氯化亚铁FeCl2氯化铁FeCl3氯化银AgCl氯化钙CaCl2氯化镁MgCl2氯化钡BaCl2氯化锌ZnCl2硫酸铜CuSO4高锰酸钾KMnO4锰酸钾K2MnO4氯酸钾KClO33、常见有机化合物初中化学方程式全(已配平).一、化合反应1、镁在空气中燃烧:2Mg+ O2点燃 2MgO2、铁在氧气中燃烧:3Fe +2O2点燃 Fe3O43、铝在空气中燃烧:4Al+ 3O2点燃 2Al2O34、氢气在空气中燃烧:2H2 +O2点燃 2H2O5、红磷在空气中燃烧:4P +5O2点燃 2P2O56、硫粉在空气中燃烧: S+ O2点燃 SO27、碳在氧气中充分燃烧:C +O2 点燃 CO28、碳在氧气中不充分燃烧:2C +O2点燃 2CO9、二氧化碳通过灼热碳层: C +CO2高温 2CO10、一氧化碳在氧气中燃烧:2CO +O2 点燃 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O === H2CO312、生石灰溶于水:CaO+ H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 +5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃 2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O +O2↑16、加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 +O2↑17、水在直流电的作用下分解:2H2O 通电 2H2↑+O2↑18、碳酸化学物理学报不稳定而分解:H2CO3 === H2O +CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温 CaO+ CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu21、锌和稀硫酸反应(实验室制氢气):Zn+ H2SO4 == ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl === MgCl2 +H2↑23、氢气还原氧化铜:H2 +CuO 加热 Cu +H2O24、木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑25、甲烷在空气中燃烧:CH4 +2O2 点燃 CO2+2H2O26、水蒸气通过灼热碳层:H2O +C 高温 H2 +CO27、焦炭还原氧化铁:3C +2Fe2O3高温 4Fe +3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+ CuSO4== Cu(OH)2↓+ Na2SO429、甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O30、酒精在空气中燃烧:C2H5OH+ 3O2点燃 2CO2 +3H2O31、一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO232、一氧化碳还原氧化铁:3CO+ Fe2O3高温 2Fe+ 3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+ CO2==== CaCO3 ↓+ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+ CO2 ==== Na2CO3 +H2O35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 +2HCl === CaCl2 +H2O +CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+ 2HCl === 2NaCl +H2O +CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 +O2点燃 2H2O6. 红磷在空气中燃烧:4P+ 5O2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:C+ O2点燃 CO29. 碳在氧气中不充分燃烧:2C+ O2点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+ O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO2 2H2O12. 酒精在空气中燃烧:C2H5OH +3O2点燃 2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电 2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3加热 2CuO +H2O +CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl+ 3O2↑16. 加热高锰酸钾:2KMnO4 加热 K2MnO4 +MnO2 +O2↑17. 碳酸不稳定而分解:H2CO3 === H2O +CO2↑18. 高温煅烧石灰石:CaCO3 高温 CaO +CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+ CuO 加热 Cu+ H2O20. 木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑2 初三化学方程式大合集21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe+ 3CO2↑22. 焦炭还原四氧化三铁:2C +Fe3O4高温 3Fe+ 2CO2↑23. 一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3高温 2Fe +3CO225. 一氧化碳还原四氧化三铁:4CO +Fe3O4高温 3Fe+ 4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+酸 -------- 盐+氢气(置换反应)26. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑27. 铁和稀硫酸Fe +H2SO4 = FeSO4+ H2↑28. 镁和稀硫酸Mg +H2SO4 = MgSO4 +H2↑29. 铝和稀硫酸2Al+ 3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑32. 镁和语文教案格式稀盐酸Mg 2HCl === MgCl2+ H2↑33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(2)金属单质+盐(溶液) ------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu35. 锌和硫酸铜溶液反应:Zn+ CuSO4 === ZnSO4+ Cu36. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2 === Cu(NO3)2 +Hg (3)碱性氧化物+酸 -------- 盐+水37. 氧化铁和稀盐酸反应:Fe2O3+ 6HCl === 2FeCl3+ 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 === Fe2(SO4)3+ 3H2O39. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl2 +H2O40. 氧化铜和稀硫酸反应:CuO +H2SO4 ==== CuSO4+ H2O41. 氧化镁和稀硫酸反应:MgO+ H2SO4 ==== MgSO4+ H2O42. 氧化钙和稀盐酸反应:CaO +2HCl ==== CaCl2 +H2O(4)酸性氧化物+碱 -------- 盐+水43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O 44.苛性钠吸收二氧化硫气体:2NaOH +SO2 ==== Na2SO3 +H2O 45.苛性钠吸收三氧化硫气体:2NaOH+ SO3 ==== Na2SO4+ H2O 46.消石灰放在空气中变质:Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O 47. 消石灰吸收二氧化硫:Ca(OH)2 +SO2 ==== CaSO3↓+H2O (5)酸+碱 -------- 盐+水48.盐酸和烧碱起反应:HCl+ NaOH ==== NaCl+ H2O49. 盐酸和氢氧化钾反应:HCl+ KOH ==== KCl+H2O50.盐酸和氢氧化初中家长会课件铜反应:2HCl+ Cu(OH)2 ==== CuCl2 +2H2O51. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 ==== CaCl2 +2H2O52. 盐酸和氢氧化铁反应:3HCl+ Fe(OH)3 ==== FeCl3 +3H2O53.氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 ==== AlCl3 +3H2O54.硫酸和烧碱反应:H2SO4 +2NaOH ==== Na2SO4 +2H2O55.硫酸和氢氧化钾反应:H2SO4 +2KOH ==== K2SO4 +2H2O56.硫酸和氢氧化铜反应:H2SO4 +Cu(OH)2 ==== CuSO4 +2H2O57. 硫酸和氢氧化铁反应:3H2SO4 +2Fe(OH)3==== Fe2(SO4)3+ 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸+盐 -------- 另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO3 +2HCl === CaCl2 H2O +CO2↑60.碳酸钠与稀盐酸反应: Na2CO3 +2HCl === 2NaCl +H2O+ CO2↑ 61.碳酸镁与稀盐酸反应: MgCO3 +2HCl === MgCl2 +H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+ AgNO3=== AgCl↓+ HNO363.硫酸和碳酸钠反应:Na2CO3 +H2SO4 === Na2SO4 +H2O +CO2↑64.硫酸和氯化钡溶液反应:H2S O4 +BaCl2 ==== BaSO4↓+ 2HCl(7)碱+盐 -------- 另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO4 ==== Cu(OH)2↓ Na2SO466.氢氧化钠与氯化铁:3NaOH FeCl3 ==== Fe(OH)3↓ 3NaCl67.氢氧化钠与氯化镁:2NaOH MgCl2 ==== Mg(OH)2↓ 2NaCl68. 氢氧化钠与氯化铜:2NaOH CuCl2 ==== Cu(OH)2↓ 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 Na2CO3 === CaCO3↓ 2NaOH(8)盐+盐 ----- 两种新盐70.氯化钠溶液新概念英语第二册和硝酸银溶液:NaCl +AgNO3 ==== AgCl↓+ NaNO371.硫酸钠和氯化钡:Na2SO4+ BaCl2 ==== BaSO4↓+ 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+ H2O === H2CO373.生石灰溶于水:CaO+ H2O === Ca(OH)274.氧化钠溶于水:Na2O +H2O ==== 2NaOH75.三氧化硫溶于水:SO3 +H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热 CuSO4 5H2O77.无水硫酸铜作干燥剂:CuSO4+ 5H2O ==== CuSO4·5H2化学方程式反应现象应用2Mg+ O点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg +O点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验2Cu+ O点燃或Δ2CuO 红色金属变为黑色固体4Al+ 3O点燃或Δ2Al2O3银白金属变为白色固体3Fe+ 2O点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热 4Fe +3O2高温2Fe2O3C+ O2点燃CO2剧烈燃烧、白光、放热、使石灰水变浑浊S +O2点燃SO2剧大学英语四级烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2 O2点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P +5O2 点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O点燃2H2O+ CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+ 5O点燃2H2O +4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3MnO2、Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气2KMnO4Δ K2MnO4 MnO2 +O2↑ 紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧论文气2HgOΔ2Hg+ O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H2↑+ O2↑ 水通电分解为氢气和氧气电解水Cu2(OH)2CO3Δ2CuO +H2O+ CO2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3ΔNH3↑+ H2O+ CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+ H2SO4=ZnSO4 +H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe +H2SO4=FeSO4 +H2↑ 有大量气泡产生、金属颗粒逐渐溶解Mg +H2SO4 =MgSO4 +H2↑ 有大量气泡产生、金属颗粒逐渐溶解2Al+ 3H2SO4=Al2(SO4)3+ 3H2↑ 有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2Δ2Fe +3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2 Δ3Fe+ 4H2O 黑色逐渐变为银白色英语翻译、试管壁有液体冶炼金属、利用氢气的还原性WO3 +3H2Δ W +3H2O 冶炼金属钨、利用氢气的还原性MoO3 +3H2ΔMo +3H2O 冶炼金属钼、利用氢气的还原性2Na+ Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2 +Cl2点燃或光照 2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C +O点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因2CO +O点燃2CO2蓝色火焰煤气燃烧C+ CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+ 3C 高温4Fe+ 3CO2↑ 冶炼金属Fe3O4 +2C高温3Fe+ 2CO2↑ 冶炼金属C+ CO2 高温2COCO2+H2O = H2CO3碳酸使石蕊变红证明碳酸的酸性小学三语文教学论文H2CO3 ΔCO2↑+ H2O 石蕊红色褪去Ca(OH)2 +CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3 +H2O+ CO2 = Ca(HCO3)2 白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2Δ CaCO3↓+ H2O +CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3+ H2O +CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 高温 CaO +CO2↑ 工业制备二氧化碳和生石灰CaCO3 +2HCl=CaCl2+ H2O +CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢初中化学方程式汇总一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2 +O2 点燃 2H2O6. 红磷在空气中燃烧(研究空气组成的实验):4P +5O2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:C +O2点燃 CO29. 碳在氧气中不充分燃烧:2C +O2点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O12. 酒精在空气中燃烧:C2H5OH +3O2点燃 2CO2 +3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg +O2 ↑14.加热高锰酸钾:2KMnO4加热 K2MnO4+ MnO2 +O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2 MnO22H2O+ O2↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电 2H2↑+O2 ↑17.生石灰溶于水英语六级作文:CaO +H2O == Ca(OH)218.二氧化碳可溶于水: H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+ O2点燃 2MgO20.铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu21.氢气还原氧化铜:H2 +CuO 加热 Cu +H2O22. 镁还原氧化铜:Mg+ CuO 加热 Cu +MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2点燃 CO224.木炭还原氧化铜:C + 2CuO 高温 2Cu+ CO2↑25.焦炭还原氧化铁:3C + 2Fe2O3高温 4Fe + 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C +O2 点燃 CO227.煤炉的中层:CO2+ C 高温 2CO28.煤炉的上部蓝色火焰的产生:2CO +O2点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3+ 2HCl == CaCl2+ H2O +CO2↑30.碳酸不稳定而分解:H2CO3 == H2O +CO2↑31.二氧化碳可溶于水: H2O +CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温 CaO+ CO2↑ 33.石灰水与中学历史教学园地二氧化碳反应(鉴别二氧化碳):Ca(OH)2 +CO2 === CaCO3↓+H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu +CO235.一氧化碳的可燃性:2CO +O2点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 2HCl == 2NaCl+ H2O +CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O38.酒精在空气中燃烧:C2H5OH +3O2 点燃 2CO2 +3H2O39.氢气中空气中燃烧:2H2+ O2点燃 2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg+ O2点燃 2MgO41.铁在氧气中燃烧:3Fe +2O2点燃 Fe3O442. 铜在空气中受热:2Cu +O2加热 2CuO43. 铝在空气中形成氧化膜:4Al+ 3O2 = 2Al2O3(2)金属单质酸 -------- 盐氢气(置换反应)44. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑45. 铁和稀硫酸Fe +H2SO4 = FeSO4 +H2↑46. 镁和稀硫酸Mg +H2SO4 = MgSO4+ H2↑47. 铝和稀硫酸2Al+ 3H2SO4 = Al2(SO4)3 +3H2↑48. 锌和稀盐酸Zn+ 2HCl == ZnCl2+ H2↑49. 铁和稀盐酸Fe +2HCl == FeCl2 +H2↑50. 镁和稀盐酸Mg +2HCl == MgCl2+ H2↑51.铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(3)金属单质盐怎样学好高中物理(溶液) ------- 新金属新盐52. 铁和硫酸铜溶液反应:Fe +CuSO4 == FeSO4 +Cu53. 锌和硫酸铜溶液反应:Zn +CuSO4 ==ZnSO4 +Cu54. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2 == Cu(NO3)2 +Hg(3)金属铁的治炼原理:55.3CO +2Fe2O3 高温 4Fe +3CO2↑七、酸、碱、盐1、酸的化学性质(1)酸金属 -------- 盐氢气(见上)(2)酸金属氧化物-------- 盐水56. 氧化铁和稀盐酸反应:Fe2O3 +6HCl ==2FeCl3 +3H2O57. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 == Fe2(SO4)3 +3H2O58. 氧化铜和稀盐酸反应:CuO +2HCl ==CuCl2 +H2O59. 氧化铜和稀硫酸反应:CuO+ H2SO4 == CuSO4+ H2O(3)酸碱 -------- 盐水(中和反应)60.盐酸和烧碱起反应:HCl +NaOH == NaCl+H2O61. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 == CaCl2+2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 == AlCl3 +3H2O63. 硫酸和烧碱反应:H2SO4+ 2NaOH == Na2SO4 +2H2O(4)酸盐 -------- 另一种酸另一种盐64.大理石与稀盐酸反应:CaCO3+2HCl == CaCl2 +H2O+ CO2↑ 65.碳酸钠与稀盐酸反应: Na2CO3 +2HCl == 2NaCl+ H2O+ CO2↑ 66.碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+H2O+ CO2↑ 67. 硫酸和氯化钡溶液反应:H2SO4 +BaCl2 == BaSO4↓+2HCl2、碱的幼儿园小班音乐教案化学性质(1)碱非金属氧化物 -------- 盐水68.苛性钠暴露在空气中变质:2NaOH+CO2 == Na2CO3+ H2O 69.苛性钠吸收二氧化硫气体:2NaOH +SO2 == Na2SO3 +H2O 70.苛性钠吸收三氧化硫气体:2NaOH+ SO3 == Na2SO4 +H2O 71.消石灰放在空气中变质:Ca(OH)2+ CO2 == CaCO3↓+H2O72. 消石灰吸收二氧化硫:Ca(OH)2 +SO2 == CaSO3↓+ H2O(2)碱酸-------- 盐水(中和反应,方程式见上)(3)碱盐 -------- 另一种碱另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 +Na2CO3 == CaCO3↓+ 2NaOH 3、盐的化学性质(1)盐(溶液)金属单质------- 另一种金属另一种盐74. 铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu(2)盐酸-------- 另一种酸另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 +2HCl == 2NaCl +H2O+ CO2↑ 碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+ H2O +CO2↑ (3)盐碱 -------- 另一种碱另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 +Na2CO3 == CaCO3↓+ 2NaOH (4)盐盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl +AgNO3== AgCl↓+NaNO3 78.硫酸钠和氯化钡:Na2SO4 +BaCl2== BaSO4↓+2NaCl。
初中常见化学式及化学方程式常见的化学式一、常见单质二、化合物1、氧化物2、其他化合物3、常见有机化合物初中化学方程式全(已配平).一、化合反应1、镁在空气中燃烧:2Mg+ O2点燃 2MgO2、铁在氧气中燃烧:3Fe +2O2点燃 Fe3O43、铝在空气中燃烧:4Al+ 3O2点燃 2Al2O34、氢气在空气中燃烧:2H2 +O2点燃 2H2O5、红磷在空气中燃烧:4P +5O2点燃 2P2O56、硫粉在空气中燃烧: S+ O2点燃 SO27、碳在氧气中充分燃烧:C +O2 点燃 CO28、碳在氧气中不充分燃烧:2C +O2点燃 2CO9、二氧化碳通过灼热碳层: C +CO2高温 2CO10、一氧化碳在氧气中燃烧:2CO +O2 点燃 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 +H2O === H2CO312、生石灰溶于水:CaO+ H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 +5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃 2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O +O2↑16、加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 +O2↑17、水在直流电的作用下分解:2H2O 通电 2H2↑+O2↑18、碳酸化学物理学报不稳定而分解:H2CO3 === H2O +CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温 CaO+ CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu21、锌和稀硫酸反应(实验室制氢气):Zn+ H2SO4 == ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl === MgCl2 +H2↑23、氢气还原氧化铜:H2 +CuO 加热 Cu +H2O24、木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑25、甲烷在空气中燃烧:CH4 +2O2 点燃 CO2+2H2O26、水蒸气通过灼热碳层:H2O +C 高温 H2 +CO27、焦炭还原氧化铁:3C +2Fe2O3高温 4Fe +3CO2↑四。
初中常见化学式及化学方程式常见的化学式二、化合物初中化学方程式大全一、化合反应1、镁在空气中燃烧:2Mg+ O2点燃 2MgO2、铁在氧气中燃烧:3Fe +2O2点燃 Fe3O43、铝在空气中燃烧:4Al+ 3O2点燃 2Al2O34、氢气在空气中燃烧:2H2 +O2点燃 2H2O5、红磷在空气中燃烧:4P +5O2点燃 2P2O56、硫粉在空气中燃烧: S+ O2点燃 SO27、碳在氧气中充分燃烧:C +O2 点燃 CO28、碳在氧气中不充分燃烧:2C +O2点燃 2CO9、二氧化碳通过灼热碳层: C +CO2高温 2CO10、一氧化碳在氧气中燃烧:2CO +O2 点燃 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 +H2O === H2CO312、生石灰溶于水:CaO+ H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 +5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃 2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O +O2↑16、加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 +O2↑17、水在直流电的作用下分解:2H2O 通电 2H2↑+O2↑18、碳酸化学物理学报不稳定而分解:H2CO3 === H2O +CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温 CaO+ CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu21、锌和稀硫酸反应(实验室制氢气):Zn+ H2SO4 == ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl === MgCl2 +H2↑23、氢气还原氧化铜:H2 +CuO 加热 Cu +H2O24、木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑25、甲烷在空气中燃烧:CH4 +2O2 点燃 CO2+2H2O26、水蒸气通过灼热碳层:H2O +C 高温 H2 +CO27、焦炭还原氧化铁:3C +2Fe2O3高温 4Fe +3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+ CuSO4 == Cu(OH)2↓+ Na2SO429、甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O30、酒精在空气中燃烧:C2H5OH+ 3O2点燃 2CO2 +3H2O31、一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO232、一氧化碳还原氧化铁:3CO+ Fe2O3高温 2Fe+ 3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+ CO2 ==== Na2CO3 +H2O35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 +2HCl === CaCl2 +H2O +CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+ 2HCl === 2NaCl +H2O +CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 +O2点燃 2H2O6. 红磷在空气中燃烧:4P+ 5O2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:C+ O2点燃 CO29. 碳在氧气中不充分燃烧:2C+ O2点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+ O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO2 2H2O12. 酒精在空气中燃烧:C2H5OH +3O2点燃 2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电 2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3加热 2CuO +H2O +CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl+ 3O2↑16. 加热高锰酸钾:2KMnO4 加热 K2MnO4 +MnO2 +O2↑17. 碳酸不稳定而分解:H2CO3 === H2O +CO2↑18. 高温煅烧石灰石:CaCO3 高温 CaO +CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+ CuO 加热 Cu+ H2O20. 木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe+ 3CO2↑22. 焦炭还原四氧化三铁:2C +Fe3O4高温 3Fe+ 2CO2↑23. 一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3高温 2Fe +3CO225. 一氧化碳还原四氧化三铁:4CO +Fe3O4高温 3Fe+ 4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+酸 -------- 盐+氢气(置换反应)26. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑27. 铁和稀硫酸Fe +H2SO4 = FeSO4+ H2↑28. 镁和稀硫酸Mg +H2SO4 = MgSO4 +H2↑29. 铝和稀硫酸2Al+ 3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑32. 镁和语文教案格式稀盐酸Mg 2HCl === MgCl2+ H2↑33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(2)金属单质+盐(溶液) ------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu35. 锌和硫酸铜溶液反应:Zn+ CuSO4 === ZnSO4+ Cu36. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2 === Cu(NO3)2 +Hg(3)碱性氧化物+酸 -------- 盐+水37. 氧化铁和稀盐酸反应:Fe2O3+ 6HCl === 2FeCl3+ 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 === Fe2(SO4)3+ 3H2O39. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl2 +H2O40. 氧化铜和稀硫酸反应:CuO +H2SO4 ==== CuSO4+ H2O41. 氧化镁和稀硫酸反应:MgO+ H2SO4 ==== MgSO4+ H2O42. 氧化钙和稀盐酸反应:CaO +2HCl ==== CaCl2 +H2O(4)酸性氧化物+碱 -------- 盐+水43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O44.苛性钠吸收二氧化硫气体:2NaOH +SO2 ==== Na2SO3 +H2O45.苛性钠吸收三氧化硫气体:2NaOH+ SO3 ==== Na2SO4+ H2O46.消石灰放在空气中变质:Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O47. 消石灰吸收二氧化硫:Ca(OH)2 +SO2 ==== CaSO3↓+H2O(5)酸+碱 -------- 盐+水48.盐酸和烧碱起反应:HCl+ NaOH ==== NaCl+ H2O49. 盐酸和氢氧化钾反应:HCl+ KOH ==== KCl+H2O50.盐酸和氢氧化初中家长会课件铜反应:2HCl+ Cu(OH)2 ==== CuCl2 +2H2O51. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 ==== CaCl2 +2H2O52. 盐酸和氢氧化铁反应:3HCl+ Fe(OH)3 ==== FeCl3 +3H2O53.氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 ==== AlCl3 +3H2O54.硫酸和烧碱反应:H2SO4 +2NaOH ==== Na2SO4 +2H2O55.硫酸和氢氧化钾反应:H2SO4 +2KOH ==== K2SO4 +2H2O56.硫酸和氢氧化铜反应:H2SO4 +Cu(OH)2 ==== CuSO4 +2H2O57. 硫酸和氢氧化铁反应:3H2SO4 +2Fe(OH)3==== Fe2(SO4)3+ 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸+盐 -------- 另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO3 +2HCl === CaCl2 H2O +CO2↑ 60.碳酸钠与稀盐酸反应: Na2CO3 +2HCl === 2NaCl +H2O+ CO2↑ 61.碳酸镁与稀盐酸反应: MgCO3 +2HCl === MgCl2 +H2O+CO2↑ 62.盐酸和硝酸银溶液反应:HCl+ AgNO3=== AgCl↓+ HNO363.硫酸和碳酸钠反应:Na2CO3 +H2SO4 === Na2SO4 +H2O +CO2↑64.硫酸和氯化钡溶液反应:H2S O4 +BaCl2 ==== BaSO4↓+ 2HCl (7)碱+盐 -------- 另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO4 ==== Cu(OH)2↓ Na2SO4 66.氢氧化钠与氯化铁:3NaOH FeCl3 ==== Fe(OH)3↓ 3NaCl 67.氢氧化钠与氯化镁:2NaOH MgCl2 ==== Mg(OH)2↓ 2NaCl68. 氢氧化钠与氯化铜:2NaOH CuCl2 ==== Cu(OH)2↓ 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 Na2CO3 === CaCO3↓ 2NaOH(8)盐+盐 ----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl +AgNO3==== AgCl↓+ NaNO3 71.硫酸钠和氯化钡:Na2SO4+ BaCl2 ==== BaSO4↓+ 2NaCl 五.其它反应:72.二氧化碳溶解于水:CO2+ H2O === H2CO373.生石灰溶于水:CaO+ H2O === Ca(OH)274.氧化钠溶于水:Na2O +H2O ==== 2NaOH75.三氧化硫溶于水:SO3 +H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热 CuSO4 5H2O77.无水硫酸铜作干燥剂:CuSO4+ 5H2O ==== CuSO4·5H2化学方程式反应现象应用2Mg+ O点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg +O点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验2Cu+ O点燃或Δ2CuO 红色金属变为黑色固体4Al+ 3O点燃或Δ2Al2O3银白金属变为白色固体3Fe+ 2O点燃Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热4Fe +3O高温2Fe2O3C+ O2点燃CO2剧烈燃烧、白光、放热、使石灰水变浑浊S +O2点燃SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2 O2点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P +5O2点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O2点燃2H2O+ CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+ 5O2点燃2H2O +4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3MnO2、Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气2KMnO4Δ K2MnO4 MnO2 +O2↑ 紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧论文气2HgOΔ2Hg+ O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H2↑+ O2↑ 水通电分解为氢气和氧气电解水Cu2(OH)2CO3Δ2CuO +H2O+ CO2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3ΔNH3↑+ H2O+ CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+ H2SO4=ZnSO4 +H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe +H2SO4=FeSO4 +H2↑ 有大量气泡产生、金属颗粒逐渐溶解Mg +H2SO4 =MgSO4 +H2↑ 有大量气泡产生、金属颗粒逐渐溶解2Al+ 3H2SO4=Al2(SO4)3+ 3H2↑ 有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2Δ 2Fe +3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4 +4H2 Δ3Fe+ 4H2O 黑色逐渐变为银白色英语翻译、试管壁有液体冶炼金属、利用氢气的还原性2Na+ Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl2点燃或光照 2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C+O点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因2CO+O点燃2CO2蓝色火焰煤气燃烧C+CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+ 3C 高温4Fe+ 3CO2↑ 冶炼金属Fe3O4 +2C高温3Fe+ 2CO2↑ 冶炼金属C+ CO2高温2COCO2+H2O = H2CO3碳酸使石蕊变红证明碳酸的酸性H2CO3 ΔCO2↑+ H2O 石蕊红色褪去Ca(OH)2 +CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3 +H2O+ CO2 = Ca(HCO3)2 白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2Δ CaCO3↓+ H2O +CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3+ H2O +CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 高温 CaO +CO2↑ 工业制备二氧化碳和生石灰CaCO3 +2HCl=CaCl2+ H2O +CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢。
初中常见化学式及化学方程式大全(1) 1 / 17 初中常见化学式及化学方程式 ➢ 常见的化学式 一、常见单质 氢气 H2 氮气 N2 氯气 Cl2 氧气 O2 臭氧 O3 氦气 He 氖气 Ne 氩气 Ar 碳 C 硅 Si 硫 S 磷 P 碘 I2
钾 K 钙 Ca 钠 Na 镁 Mg 铝 Al 锌 Zn
铁 Fe 铜 Cu 汞 Hg 银 Ag 二、化合物 1、氧化物
水 H2O 三氧化硫 SO3 一氧化碳 CO 二氧化碳 CO2 五氧化二磷 P2O5 过氧化氢 H2O2
二氧化氮 NO2 二氧化硫 SO2 氧化钙 CaO
氧化亚铁 FeO 氧化铁 Fe2O3 四氧化三铁 Fe3O4
氧化镁 MgO 氧化锌 ZnO 二氧化锰 MnO2
氧化汞 HgO 氧化铝 Al2O3 氧化铜 CuO 2、其他化合物 硝酸 HNO3 硫酸 H2SO4 盐酸 HCl 碳酸 H2CO3 硫化氢 H2S 氢氧化钠 NaOH 氢氧化钾 KOH 氢氧化钙 Ca(OH)2
氢氧化镁 Mg(OH)2 氢氧化铝 Al(OH)3 氢氧化锌 Zn(OH)2
氢氧化铁 Fe(OH)3 氢氧化亚铁 Fe(OH)2 氢氧化铜 Cu(OH)2
氢氧化钡 Ba(OH)2 氨水 NH3·H2O
氯化钠 NaCl 氯化铜 CuCl2 氯化铝 AlCl3
氯化钾 KCl 氯化亚铁 FeCl2 氯化铁 FeCl3
氯化银 AgCl 氯化钙 CaCl2 氯化镁 MgCl2
氯化钡 BaCl2 氯化锌 ZnCl2 硫酸铜 CuSO4
高锰酸钾 KMnO4 锰酸钾 K2MnO4 氯酸钾 KClO3
碳酸钙 CaCO3 硝酸钾 KNO3 硝酸钠 NaNO3 初中常见化学式及化学方程式大全(1) 2 / 17 硝酸铁 Fe(NO3)3 硝酸亚铁 Fe(NO3)2 硝酸铝 Al(NO3)3
碳酸钠 Na2CO3 碳酸钙 CaCO3 碳酸铵 (NH4)2CO3
碳酸氢钠 NaHCO3 硫酸铁 Fe2(SO4)3 硫酸亚铁 FeSO4
硝酸银 AgNO3 硝酸钡 Ba(NO3)2 硝酸铵 NH4NO3
硫酸钡 BaSO4
3、常见有机化合物
甲烷 CH4 乙醇 C2H5OH 葡萄糖 C6H12O6
初中化学方程式全(已配平).
一、化合反应 1、镁在空气中燃烧:2Mg+ O2 点燃 2MgO 2、铁在氧气中燃烧:3Fe +2O2 点燃 Fe3O4 3、铝在空气中燃烧:4Al+ 3O2 点燃 2Al2O3 4、氢气在空气中燃烧:2H2 +O2 点燃 2H2O 5、红磷在空气中燃烧:4P +5O2 点燃 2P2O5 6、硫粉在空气中燃烧: S+ O2 点燃 SO2 7、碳在氧气中充分燃烧:C +O2 点燃 CO2 8、碳在氧气中不充分燃烧:2C +O2 点燃 2CO 9、二氧化碳通过灼热碳层: C +CO2 高温 2CO 10、一氧化碳在氧气中燃烧:2CO +O2 点燃 2CO2 11、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 +H2O === H2CO3 初中常见化学式及化学方程式大全(1) 3 / 17 12、生石灰溶于水:CaO+ H2O === Ca(OH)2 13、无水硫酸铜作干燥剂:CuSO4 +5H2O ==== CuSO4·5H2O 14、钠在氯气中燃烧:2Na+ Cl2点燃 2NaCl 二、分解反应 15、实验室用双氧水制氧气: 16、加热高锰酸钾: 17、水在直流电的作用下分解: 18、碳酸化学物理学报不稳定而分解: 19、高温煅烧石灰石(二氧化碳工业制法): 三、置换反应
铁和硫酸铜溶液反应: 锌和稀硫酸反应(实验室制氢气): 镁和稀盐酸反应:
21、氢气还原氧化铜: 22、木炭还原氧化铜: 23、甲烷在空气中燃烧: 24、水蒸气通过灼热碳层: 25、焦炭还原氧化铁: 26、氢氧化钠溶液与硫酸铜溶液反应: 27、甲烷在空气中燃烧: 初中常见化学式及化学方程式大全(1) 4 / 17 30、酒精在空气中燃烧:C2H5OH+ 3O2 点燃 2CO2 +3H2O 31、一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO2 32、一氧化碳还原氧化铁:3CO+ Fe2O3 高温 2Fe+ 3CO2 33、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O 34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+ CO2 ==== Na2CO3
+H2O
35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 +2HCl === CaCl2 +H2O +CO2↑ 36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+ 2HCl === 2NaCl +H2O +CO2↑ 一. 物质与氧气的反应: (1)单质与氧气的反应: 1. 镁在空气中燃烧:2Mg+ O2 点燃 2MgO 2. 铁在氧气中燃烧:3Fe+ 2O2 点燃 Fe3O4 3. 铜在空气中受热:2Cu+ O2 加热 2CuO 4. 铝在空气中燃烧:4Al +3O2 点燃 2Al2O3 5. 氢气中空气中燃烧:2H2 +O2 点燃 2H2O 6. 红磷在空气中燃烧:4P+ 5O2 点燃 2P2O5 7. 硫粉在空气中燃烧: S +O2 点燃 SO2 8. 碳在氧气中充分燃烧:C+ O2 点燃 CO2 9. 碳在氧气中不充分燃烧:2C+ O2 点燃 2CO 初中常见化学式及化学方程式大全(1) 5 / 17 (2)化合物与氧气的反应: 10. 一氧化碳在氧气中燃烧:2CO+ O2 点燃 2CO2 11. 甲烷在空气中燃烧:CH4 +2O2 点燃 CO2 2H2O 12. 酒精在空气中燃烧:C2H5OH +3O2 点燃 2CO2+ 3H2O 二.几个分解反应: 13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电 2H2↑+ O2 ↑ 14. 加热碱式碳酸铜:Cu2(OH)2CO3 加热 2CuO +H2O +CO2↑ 15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl+ 3O2 ↑ 16. 加热高锰酸钾:2KMnO4 加热 K2MnO4 +MnO2 +O2↑ 17. 碳酸不稳定而分解:H2CO3 === H2O +CO2↑ 18. 高温煅烧石灰石:CaCO3 高温 CaO +CO2↑ 三.几个氧化还原反应: 19. 氢气还原氧化铜:H2+ CuO 加热 Cu+ H2O 20. 木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑ 2 初三化学方程式大合集 21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe+ 3CO2↑ 22. 焦炭还原四氧化三铁:2C +Fe3O4 高温 3Fe+ 2CO2↑ 23. 一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO2 24. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温 2Fe +3CO2 25. 一氧化碳还原四氧化三铁:4CO +Fe3O4 高温 3Fe+ 4CO2 四.单质、氧化物、酸、碱、盐的相互关系 初中常见化学式及化学方程式大全(1) 6 / 17 (1)金属单质+酸 -------- 盐+氢气 (置换反应) 26. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑ 27. 铁和稀硫酸Fe +H2SO4 = FeSO4+ H2↑ 28. 镁和稀硫酸Mg +H2SO4 = MgSO4 +H2↑ 29. 铝和稀硫酸2Al+ 3H2SO4 = Al2(SO4)3 +3H2↑ 30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑ 31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑ 32. 镁和语文教案格式稀盐酸Mg 2HCl === MgCl2+ H2↑ 33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑ (2)金属单质+ 盐(溶液) ------- 另一种金属+另一种盐 34. 铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu 35. 锌和硫酸铜溶液反应:Zn+ CuSO4 === ZnSO4+ Cu 36. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2 === Cu(NO3)2 +Hg (3)碱性氧化物+酸 -------- 盐+ 水 37. 氧化铁和稀盐酸反应:Fe2O3+ 6HCl === 2FeCl3+ 3H2O 38. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 === Fe2(SO4)3+ 3H2O 39. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl2 +H2O 40. 氧化铜和稀硫酸反应:CuO +H2SO4 ==== CuSO4+ H2O 41. 氧化镁和稀硫酸反应:MgO+ H2SO4 ==== MgSO4+ H2O 42. 氧化钙和稀盐酸反应:CaO +2HCl ==== CaCl2 +H2O (4)酸性氧化物+碱 -------- 盐+水 43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O