酶促反应影响因素
- 格式:ppt
- 大小:1012.00 KB
- 文档页数:29

酶促反应影响因素实验中存在的问题与改进探讨
酶促反应影响因素实验中可能存在的问题有以下几点:
1. 实验条件的控制不准确:实验室环境的温度、湿度、光照等因素可能会对酶的活性产生影响,如果这些因素没有得到准确的控制,就会对实验结果造成影响。
2. 酶的纯度问题:酶的纯度影响其活性,如果实验中使用的酶样品纯度不高,可能会导致实验结果误差较大。
3. 酶底物浓度的选择:酶底物浓度的选择也会影响实验结果。
如果酶底物浓度过低,可能会导致反应速率过慢,难以测量;而如果酶底物浓度过高,可能会产生底物竞争,导致实验结果不准确。
4. 反应时间的选择:反应时间的选择也要注意。
如果反应时间过短,可能会无法测量到足够的反应产物,影响实验结果;而反应时间过长,则可能会导致反应过度,产生误差。
针对这些问题,可以采取以下改进措施:
1. 准确控制实验条件:确保实验室环境的温度、湿度、光照等因素在实验过程中保持稳定,并对这些因素进行准确的记录。
2. 使用高纯度酶样品:选择高纯度的酶样品进行实验,以确保实验结果准确可靠。
3. 合理选择酶底物浓度:根据实验目的和酶的特性,选择合适的酶底物浓度,确保反应速率适中,方便结果的测量。
4. 合理选择反应时间:根据酶的反应速率和实验目的,选择合适的反应时间,确保能够得到足够的反应产物,而不产生过度反应。
5. 进行对照实验和重复实验:进行对照实验和重复实验,以验证实验结果的可靠性,并能够对实验误差进行评估和控制。
通过以上改进措施的采取,可以提高酶促反应影响因素实验的准确性和可重复性,并得到更可靠的实验结果。

影响酶促反应的因素——温度,ph,激活剂及抑制剂,生化实验报告(共8篇) 影响酶促反应速度的因素生化实验实验二影响酶促反应速度的因素【目的】观察温度、PH、激活剂、抑制剂对酶促反应速度的影响。
【原理】唾液淀粉酶催化淀粉水解,生成一系列水解产物,即糊精、麦芽糖和葡萄糖等。
淀粉及其水解产物遇碘会呈现不同的颜色。
在不同温度,不同PH值下,唾液淀粉酶活性不同,催化淀粉水解程度不一,生成的产物也就不同。
此外,激活剂、抑制剂也能影响淀粉酶活性,影响淀粉的水解。
因此可根据在不同反应条件下,溶液加碘呈现的不同颜色来判断淀粉的水解程度,从而验证了温度、pH、激活剂、抑制剂对酶促反应速度的影响。
淀粉I2 【操作】1. 温度对酶促反应速度的影响取3支试管,编号,按下表操作:2. PH对酶促反应速度的影响取3支试管,编号,按下表操作:3.激活剂与抑制剂对酶促反应速度的影响取4支试管,编号,按下表操作:【结果及分析】观察各管颜色变化,说明温度、pH、激活剂、抑制剂对酶促反应的影响。
【实验注意事项】篇二:生化实验思考题参考答案生化实验讲义思考题参考答案实验一淀粉的提取和水解1、实验材料的选择依据是什么?答:生化实验的材料选择原则是含量高、来源丰富、制备工艺简单、成本低。
从科研工作的角度选材,还应当注意具体的情况,如植物的季节性、地理位置和生长环境等,动物材料要注意其年龄、性别、营养状况、遗传素质和生理状态等,微生物材料要注意菌种的代数和培养基成分的差异等。
2、材料的破碎方法有哪些?答:(1) 机械的方法:包括研磨法、组织捣碎法;(2) 物理法:包括冻融法、超声波处理法、压榨法、冷然交替法等;(3) 化学与生物化学方法:包括溶胀法、酶解法、有机溶剂处理法等。
实验二总糖与还原糖的测定1、碱性铜试剂法测定还原糖是直接滴定还是间接滴定?两种滴定方法各有何优缺点?答: 我们采用的是碱性铜试剂法中的间接法测定还原糖的含量。
间接法的优点是操作简便、反应条件温和,缺点是在生成单质碘和转移反应产物的过程中容易引入误差;直接法的优点是反应原理直观易懂,缺点是操作较复杂,条件剧烈,不易控制。

影响酶促反应的因素
酶促反应指的是由酶作为催化剂进行催化的化学反应。
影响酶促反应的因素有温度,酸碱度,酶浓度,底物浓度,抑制剂和激活剂等。
1.温度:酶促反应在一定温度范围内反应速度随温度的升高而加快;但当温度升高到一定限度时,酶促反应速度不仅不再加快反而随着温度的升高而下降。
在一定条件下,每一种酶在某一定温度时活力最大,这个温度称为这种酶的最适温度。
2.酸碱度:每一种酶只能在一定限度的pH范围内才表现活性,超过这个范围酶就会失去活性。
3.酶浓度:在底物足够,其它条件固定的条件下,反应系统中不含有抑制酶活性的物质及其它不利于酶发挥作用的因素时,酶促反应的速度与酶浓度成正比。
4.底物浓度:在底物浓度较低时,反应速度随底物浓度增加而加快,反应速度与底物浓度近乎:成正比,在底物浓度较高时,底物浓度增加,反应速度也随之加快,但不显著;当底物浓度很大且达到一定限度时,反应速度就达到一个最大值,此时即使再增加底物浓度,反应也几乎不再改变。
5.抑制剂:能特异性的抑制酶活性,从而抑制酶促反应的物质称为抑制剂。
6.激活剂:能使酶从无活性到有活性或使酶活性提高的物质称为酶的激活剂。


2018--2018学年生物(苏教版)必修一同步导学案4.1.3酶促反应的影响因素一、目标导航1.酶促反应的影响因素二、知识网络1.影响酶活性的因素:温度和pH。
①温度:在较低的温度范围内,酶促反应的效率随着温度的升高而加快。
反应速率最高时的温度称为酶促反应的最适温度。
适当升高温度能加速酶促反应,但过高的温度又加速了酶蛋白的变性。
②pH:在一定的pH下,酶表现出最大活性,此时的pH称为最适pH,高于或低于此pH,酶的活性均降低。
过酸、过碱会使蛋白质变性而失去活性。
不同的酶最适pH是不同的。
(6)影响酶促反应速率的因素:pH、温度、酶的浓度、底物浓度等。
三、导学过程知识点一影响酶催化作用的因素甲乙丙1.酶相关实验的设计思路(1)根据两类催化剂催化H 2O 2产生O 2的多少判断酶的高效性 2H 2O 2――→H 2O 2酶2H 2O +O 2↑(气泡多而大);2H 2O 2――→Fe 3+2H 2O +O 2↑(气泡少而小)。
(2)根据斐林试剂与还原糖发生氧化还原反应判断酶的专一性蔗糖――→淀粉酶蔗糖(非还原糖)+斐林试剂→蔗糖+斐林试剂(无砖红色)。
(3)根据碘试剂与淀粉的颜色变化判断淀粉的水解淀粉+蒸馏水→淀粉+碘液→蓝紫色复合物(淀粉未被水解); 淀粉+淀粉酶→麦芽糖+碘液→无蓝紫色复合物(淀粉已被水解)。
(4)根据温度变化来判断酶的活性和结构的变化温度:低温(0 ℃)→升温→最适温度(37 ℃)→再升温→高温(大于70 ℃)| | | | | 活性:活性低―→活性增高→活性最高―→活性降低→无活性 | | | | | 结构:未变性―→未变性―→未变性―→渐变性―→已变性 (5)根据酸碱度变化来判断酶的活性和结构的变化 酸碱度:过酸←酸性增强←最适酸碱度→碱性增强→过碱 | | | | | 活性:无活性←活性降低←活性最高→活性降低→无活性 | | | | | 结构:变性← 渐变性 ← 未变性 ―→ 渐变性―→变性 【例1】 甲、乙、丙三图依次表示酶浓度一定时,反应速率和反应物浓度、温度、pH的关系。

影响酶促反应速度的因素酶作为生物催化剂,其活性受到多种因素调节,这是酶自身的特点,也是生物体能够调控代谢速度,从而适应环境的物质基础。
酶促反应的影响因素,主要是pH、温度、激活剂和抑制剂四大类。
了解这些影响因素,不论对于生产、生活,还是科学研究,都有重要作用。
限于篇幅,本文介绍前三类。
大部分酶的活力受pH值的影响,在一定的pH值活力最高,称最适pH。
一般酶的最适pH在6-8,少数酶需偏酸或碱性条件。
如人体胃蛋白酶最适pH为2.0,而肝脏精氨酸酶为9.7。
胃蛋白酶最适pH大部分酶的pH-酶活曲线是钟形曲线,但也有少数酶只有钟形的一半,甚至是直线。
如木瓜蛋白酶底物的电荷变化对催化没有影响,在pH4-10之间是一条直线。
一些酶的pH-酶活曲线,引自百度图片pH影响酶的构象,也影响与催化有关基团的解离状况及底物分子的解离状态。
最适pH有时因底物种类、浓度及缓冲溶液成分不同而变化,不是完全不变的。
温度也是常见的影响因素。
酶活随温度变化的曲线也是钟形曲线,有一个最高点,即最适温度。
温血动物的酶最适温度一般是35-40度,植物酶通常在40-50度。
这是温度升高时化学反应加速(每升温10℃反应速度加快1-2倍)与酶失活综合平衡的结果。
一般酶在60度以上变性,少数酶可耐高温,如牛胰核糖核酸酶加热到100度仍不失活。
因为酶的变形过程需要水参与,所以干燥的酶可耐受高温,而液态酶失活较快。
最适温度也不是固定值,它受反应时间影响,酶可在短时间内耐受较高温度,反应时间延长则最适温度降低。
热失活的活化能一般为50-100 Kcal/mol,比一般反应的活化能高10倍,所以一般酶在30℃以下是稳定的。
最适温度受反应时间影响,引自百度图片凡是能提高酶活性的物质都称为激活剂。
大部分激活剂是离子或简单有机化合物。
根据无激活剂时酶是否具有活性,可分为必需激活剂和非必需激活剂;根据激活剂分子性质,可分为以下三类:1.无机离子可分为金属离子、氢离子和阴离子三种。

酶促反应影响因素酶促反应影响因素1. 温度:温度高于酶的最适活性温度,会加速酶分子的活性,而酶活性过高则可导致酶烧伤或破坏,从而降低反应的速率,所以保持合适的温度是影响酶促反应的重要因素之一。
2. 酶浓度:酶浓度是影响酶促反应速率的主要因素,它直接影响反应中酶与底物之间的接触次数,当酶浓度增加时,酶与底物越多,接触次数越多,反应速率自然越快,反之,当酶浓度过低时,反应速率就变慢。
3. pH值:pH值也会影响酶促反应,每种酶都有自己最适宜的pH值,若pH值过高或过低,酶活性可能会下降,甚至在一定的极端条件下可能造成酶的解离,因此需要控制反应的pH值。
4. 辅助因子:对于一些特定的酶,还需要加入某些激活剂或辅助因子,才能促进反应,引起酶活性。
例如,维生素是不可缺少的辅助因子,它们可能和一些酶结合形成介质型酶,影响酶促反应的反应速率。
5. 抑制剂:在生理反应过程中,也需要抑制酶的活性,而一些有机分子可以抑制酶的活性,从而降低反应的速率。
抑制剂的效果受其类型、浓度和pH值等影响,如果抑制剂的浓度过高,将会完全抑制酶活性,从而降低反应的速率。
6. 氧化剂和还原剂:氧化剂和还原剂都会影响酶促反应,氧化剂可以促进酶的反应速率,而还原剂则可以降低酶的反应速率。
例如,苯酚可以作为氧化剂加速酶促反应,而过氧化氢则可以作为还原剂,降低酶促反应的速率。
7. 金属离子:一些金属离子也可以影响酶的反应速率,其中锰、铜、铁等离子可能介导酶的正向活性,而硫酸钙、硫酸镁、硫酸铝等离子可能起抑制作用,降低酶的反应速率。
因此,温度、酶浓度、pH值、辅助因子、抑制剂、氧化剂和还原剂以及金属离子等都是影响酶促反应速率的重要因素。
基于此,实验室工作者可以在有效控制这些条件条件的基础上,改善反应的质量和效率,从而获得更佳的实验结果。
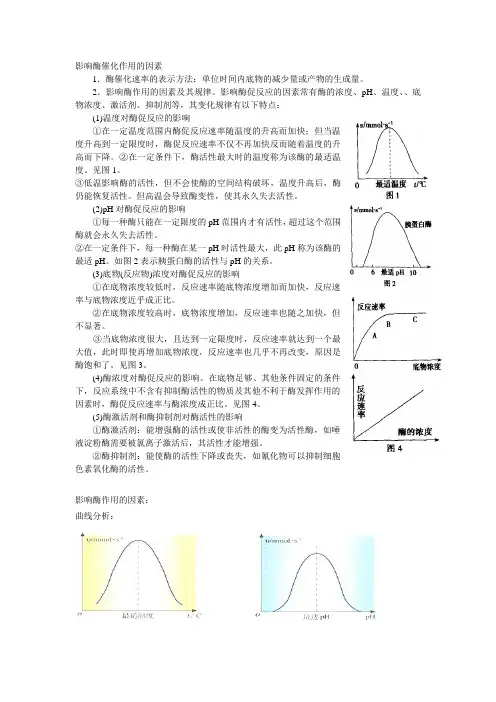
影响酶催化作用的因素1.酶催化速率的表示方法:单位时间内底物的减少量或产物的生成量。
2.影响酶作用的因素及其规律。
影响酶促反应的因素常有酶的浓度、pH、温度、、底物浓度、激活剂、抑制剂等,其变化规律有以下特点:(1)温度对酶促反应的影响①在一定温度范围内酶促反应速率随温度的升高而加快;但当温度升高到一定限度时,酶促反应速率不仅不再加快反而随着温度的升高而下降。
②在一定条件下,酶活性最大时的温度称为该酶的最适温度。
见图1。
③低温影响酶的活性,但不会使酶的空间结构破坏,温度升高后,酶仍能恢复活性。
但高温会导致酶变性,使其永久失去活性。
(2)pH对酶促反应的影响①每一种酶只能在一定限度的pH范围内才有活性,超过这个范围酶就会永久失去活性。
②在一定条件下,每一种酶在某一pH时活性最大,此pH称为该酶的最适pH。
如图2表示胰蛋白酶的活性与pH的关系。
(3)底物(反应物)浓度对酶促反应的影响①在底物浓度较低时,反应速率随底物浓度增加而加快,反应速率与底物浓度近乎成正比。
②在底物浓度较高时,底物浓度增加,反应速率也随之加快,但不显著。
③当底物浓度很大,且达到一定限度时,反应速率就达到一个最大值,此时即使再增加底物浓度,反应速率也几乎不再改变,原因是酶饱和了。
见图3。
(4)酶浓度对酶促反应的影响。
在底物足够、其他条件固定的条件下,反应系统中不含有抑制酶活性的物质及其他不利于酶发挥作用的因素时,酶促反应速率与酶浓度成正比。
见图4。
(5)酶激活剂和酶抑制剂对酶活性的影响①酶激活剂:能增强酶的活性或使非活性的酶变为活性酶,如唾液淀粉酶需要被氯离子激活后,其活性才能增强。
②酶抑制剂:能使酶的活性下降或丧失,如氰化物可以抑制细胞色素氧化酶的活性。
影响酶作用的因素:曲线分析:曲线含义的准确表述:B 点:该酶发挥催化作用的最适温度或最适pH 值AB 段:达到最适温度(pH 值)前,随着温度(pH 值)升高,酶的催化效率提高酶的最适pH 值往往随底物种类、浓度等的变化而不同,因此,并不是一个常数,只是在一定条件下才有意义。

酶活性浓度测定的主要影响因素及控制影响酶促反应的因素主要有酶浓度、底物浓度、温度、pH及离子强度、电解质、辅酶、激活剂及抑制剂等。
(一)酶浓度在底物浓度远大于酶浓度时,酶促反应速率随酶浓度的增加而增加,即反应速率与酶的浓度成正比。
酶浓度特别高的标本,底物将过快且过多地消耗,影响酶活性测定,故需进行适当稀释,但要注意稀释产生的基质效应影响。
(二)反应系统温度的影响温度对酶促反应影响有两重性。
一方面,按照一般催化反应规律,温度升高可促进分子热运动,增加碰撞机会,提高酶促反应速率;另一方面,温度过高可因酶蛋白变性反而使酶反应速率下降。
多数酶在60℃时开始变性,80℃时已不可逆变性。
酶反应速率最大时的反应系统温度称为酶反应的最适温度(optimumtemperature)。
低于最适温度时,温度每升高10℃反应速率可增加1.7~2.5倍。
当高于最适温度时,反应速率则可能因酶变性失活反降低。
测定酶活性的温度长期未统一,学术团体推荐主要有3种:①德国临床生化学会(GSCC)推荐25℃;②国际临床化学联合会(IFCC)推荐30℃;③斯堪地那维亚临床生化学会(SSCC)推荐37℃。
我国推荐温度为37℃,现IFCC也改为推荐37℃。
测定酶活性时,温度的误差不能大于±0.1℃,以保证测定结果的准确性。
不同温度测定酶活性结果之间,不推荐使用酶的温度校正系数转换。
因此,不同反应温度测定酶活性应有相应参考区间,不能混用。
(三)底物的种类和浓度底物专一性不强的酶,可作用于多种底物,测定酶活性时,应优先考虑有较高诊断价值的底物。
底物专一性强的酶,如其所催化的为可逆反应,则需要从测定技术和实用方面考虑选择测定正向或负向反应。
在米氏方程中,当底物浓度[S]≫Km时,Km可忽略不计,则v=Vmax=K2[E],即反应速率与底物浓度无关,仅和酶浓度[E]成正比,此为零级反应(图28-1中的c段)。
因此,临床测定酶活性时,一般均给予充分的底物浓度,最好为Km的10~20倍,保证反应速率与酶浓度[E]成正比,以准确测定酶活性。

种因素。
在探讨各种因素对酶促反应速度的影响时,通常测定其初始速度来代表酶促反应速度,即底物转化量<5%时的反应速度。
影响酶促反应速度的因素包括:1. 酶浓度:在其他因素不变的情况下,底物浓度的变化对反应速率影响的作图时呈矩形双曲线。
底物足够时,酶浓度对反应速率的影响呈直线关系。
2. 底物浓度:在其他因素不变的情况下,随着底物浓度的增加,反应速率也会相应增加。
3. pH值:pH值通过改变酶和底物分子解离状态影响反应速率。
4. 温度:温度对反应速率的影响具有双重性。
在适宜的温度范围内,随着温度的升高,反应速率加快。
但当温度过高时,酶的活性会受到抑制,反应速率反而下降。
5. 抑制剂和激活剂:抑制剂可逆或不可逆的降低酶促反应速率,而激活剂可加快酶促反应速率。
在实际生产中要充分发挥酶的催化作用,以较低的成本生产出较高质量的产品,就必须准确把握酶促反应的条件。
酶促反应的动力学研究与探讨的是酶促反应的速率及影响酶促反应速率的各种因素。
其中,主要的因素包括酶浓度、底物浓度、pH值、温度、激活剂和抑制剂等。
1. 酶浓度:在其他因素不变的情况下,底物浓度的变化对反应速率的影响呈矩形双曲线。
当底物浓度足够时,酶浓度对反应速率的影响则呈直线关系。
2. 底物浓度:在酶浓度不变的情况下,底物浓度的增加会促进反应速度的增加,但当底物浓度达到一定值后,再增加底物浓度对反应速度的影响不大。
3. pH值:pH值通过改变酶和底物分子解离状态影响反应速率。
4. 温度:温度对酶促反应速率的影响具有双重性。
在低温条件下,由于分子运动速度较慢,反应速度比较慢;随着温度的升高,分子运动速度加快,反应速度也会加快;但当温度升高到一定值后,过高的温度会使酶变性,反应速度反而下降。
5. 激活剂和抑制剂:激活剂可以加快酶促反应速度,而抑制剂可以降低酶促反应速度。
在实际生产中要充分发挥酶的催化作用,以较低的成本生产出较高质量的产品,就必须准确把握酶促反应的条件。

实验酶促反应的影响因素此实验可以根据酶的特性,设计影响酶促反应的各种因素,并进行实验检验。
(一)酶的激活剂和抑制剂一、实验目的1.了解酶促反应的激活与抑制。
2.学习鉴定激活剂和抑制剂影响酶反应的方法和原理。
二、实验原理酶的活性常受某些物质的影响,有些物质能使酶的活性增加,称为酶的激活剂;有些物质能使酶的活性降低,称为酶的抑制剂。
例如,氯化钠为唾液淀粉酶的激活剂,硫酸铜为其抑制剂。
通常少量的激活剂或抑制剂就会影响酶的活性,而且常具有特异性。
但是,值得注意的是激活剂和抑制剂不是绝对的,有些物质在低浓度时为某种酶的激活剂,而在高浓度时则为该酶的抑制剂。
例如氯化钠达到1/3饱和度时就可抑制唾液淀粉酶的活性。
三、器材1.试管及试管架 2.烧杯、椎形瓶和量筒(100mL)3.玻璃漏斗 4.吸管 5.滤纸 6.恒温水浴锅四、试剂1. 1% 淀粉溶液2.稀释100~200倍的新鲜唾液3. 1%氯化钠溶液4.0.1 %硫酸铜溶液5.碘化钾-碘溶液:将碘化钾20g 和碘10g 溶于100 mL水中,使用前稀释10倍。
五、操作方法取3支试管,向第一支试管中加入1%氯化钠溶液1 mL,向第二支试管中加入 0.1%硫酸铜溶液1 mL,向第3支试管中加入蒸馏水1mL作对照。
再向每支试管各加入 0.1%淀粉溶液3 mL和稀释的唾液1 mL。
摇匀各管,充分混合,一起放入37℃恒温水浴中保温10~15分钟后取出。
冷却后,各滴入2-3滴碘化钾-碘溶液。
混匀。
观察比较3支试管颜色的深浅,并解释之。
如果激活剂或抑制剂的作用不明显,主要可能原因是唾液淀粉酶的活性不够高,可以适当延长反映时间或者降低唾液稀释的倍数。
思考题1.激活剂可以分为哪几类?本实验中氯化钠属于其中的哪一类?2.抑制剂和变性剂有什么不同?试举例说明。
3.酶反应的抑制作用有哪些类型?根据什么划分的?它们都有什么特点?(二)温度对酶活性的影响一、实验目的通过检验不同温度下唾液淀粉酶的活性,了解温度对酶活性的影响。