全国高中学生化学竞赛(决赛)理论试题
- 格式:doc
- 大小:40.50 KB
- 文档页数:2

年全国高中学生化学竞赛(决赛)理论试题 ...杭州(背面朝上)放在桌面上,立即起立撤离考场。
试卷装订成册,不得拆散。
所有解答必须写在答卷纸的指定地方(方框内),不得用铅笔填写,写在其他地方的应答一律无效。
使用指定的草稿纸。
不得持有任何其他纸张。
把营号写在所有试卷(包括草稿纸)右上角处,不写姓名和所属学校,否则按废卷论。
允许使用非编程计算器、直尺、橡皮等文具,但不得带文具盒进入考场。
1.008Zr NbMo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Hf Ta W Re OsIr Pt Au Hg Tl Pb Bi Po At Ac-LrHLi Be B C N O FNa Mg Al Si P Cl S K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn G a G e As Se BrRb Cs Fr Sr BaRaY La Lu -6.9419.01222.9924.3139.1040.0885.4787.62132.9137.3[223][226]44.9647.8850.9452.0054.9455.8558.9363.5558.6965.3910.8126.9869.7212.0128.0972.61114.8204.4118.7207.2112.4200.6107.9197.0106.4195.1102.9192.2101.1190.298.91186.295.94183.992.91180.991.22178.588.9114.0116.0019.0030.9774.92121.8209.032.0778.96127.6[210][210]126.979.9035.454.00320.1839.9583.80131.3[222]He Ne Ar Kr Xe Rn Ïà ¶Ô Ô- ×Ó ÖÊ Á¿第题的单质和的单质在常温下激烈反应,得到化合物。

中国化学会第 20 届全国高中学生化学竞赛(决赛)理论试题参考答案及评分细则第 1 题(14 分)1-1 当g G m< 0时,反应可正向进行,由此解得T1>1186K, T2>1500 K,T3>1761K,故只有反应①在 1500K 以下可自动正向进行。
(计算2分,结果1分,共3分)Ti O2+ 2Cl2= Ti Cl4+2CO(1 分)1-2(方程式未配平不得分 )1-3 VOCl 3与 TiCl 4沸点相近(1分)Cu+ VOCl 3= VOCl 2+CuCl(1 分)1-4 TiCl 4 +2Mg=Ti+2MgCl 2(1分)1-5(1)Mg C O=Mg O + C O(1分)32Mg O + Cl+ C=Mg Cl+ C O(1分)22(2)阴极反应:Mg 2+-= Mg( 0.5 分)+2e阳极反应:--( 0.5 分)2Cl = Cl 2+2e电解反应: MgCl 2= Mg +Cl 2(1 分)1( 0.5分)(3)r H m = ∑v B f H m = 596.32 kJ molr S m =∑v B S m = 77.30+268.20-231.02=114.48(J·K-1·mol-1)( 0.5分)r G m = r H m —T r S m =596.32—1023×114.48×10-3=479.21(kJ·mol-1)(1 分)E = –r G m/ZF=–479210/(2×96500)= -2.48(V)E理 =2.48V(1分)第2 题2-12-2 ( 1) ZnS + 2H 2SO4=ZnSO 4+SO2+S+2H 2OCuS + 2H 2 SO4=CuSO4+SO2+S+2H 2O 加水的目的是浸取反应生成的可溶性硫酸盐。
(2) As2S3 +3Na 2S=2Na3AsS3SnS2 +Na 2S=NaSnS3加入氢氧化钠的目的是防止硫化钠水解2-3(1)S2O42-+Fe2O3+2H+=2SO32-+2Fe2++H2O (2) Na4[FeA 2]第 3 题(10 分)3-1[(3++ H O[(] )2++F e H) ]2= F e O H H O 2O6 2O5+ H 33-2(3 分)(1 分)(1 分)(0.5 分)(1 分)(1 分)(2 分)(1 分)H4 + O2[F e O H(H]) 2 +=(H2O)4 F e F e( H 2 O )4+ 2 H O(12分)2O5OHH 2 O H H 2 O H 2OH H 2 OH 2 O O.....OF e F e F e F eH 2 O O.....OH 2 O H 2OH 2 OH 2 O H H3-3Al 2O3+6HCl+9H 2O=2[Al(H 2O)6]Cl 3 [Al(H2O)6]Cl 3= [Al(OH) 2(H2O)4]Cl+2HCl[Al(OH) 2(H2 O)4]Cl+NH 3 H·2O=Al(OH) 3+NH 4Cl+4H 2O (nm-4m)Al(OH) 3+(6m-nm)[Al(OH) 2(H 2O)4]Cl=[Al 2(OH) n Cl 6-n] m+(24m-4nm)H2O 3-4第 4 题(22 分)4-1n NaBH 4 +4n CH 3CH2OH =[NaB(OC 2H5 )4] n +4n H 2↑(分子式错误,方程式未配平不得分;未写n 不扣分)4-2 A 属于混合晶体4-3[NaB(OC 2H 5)4]n 的一维结构示意图及一维点阵如下:m +O H 2O H 2(2分)(1 分)(1 分)(1 分)(1 分)(2分)4-4 Na 的配位数为4, B 原子采取SP3杂化(2分)H O2[F e O H(H]) 2 +=(H2O)4 F e F e( H 2 O )4+ 2 H O(12分)2O5OHH 2 O H H 2 O H 2OH H 2 OH 2 O O.....OF e F e F e F eH 2 O O.....OH 2 O H 2OH 2 OH 2 O H H3-3Al 2O3+6HCl+9H 2O=2[Al(H 2O)6]Cl 3 [Al(H2O)6]Cl 3= [Al(OH) 2(H2O)4]Cl+2HCl[Al(OH) 2(H2 O)4]Cl+NH 3 H·2O=Al(OH) 3+NH 4Cl+4H 2O (nm-4m)Al(OH) 3+(6m-nm)[Al(OH) 2(H 2O)4]Cl=[Al 2(OH) n Cl 6-n] m+(24m-4nm)H2O 3-4第 4 题(22 分)4-1n NaBH 4 +4n CH 3CH2OH =[NaB(OC 2H5 )4] n +4n H 2↑(分子式错误,方程式未配平不得分;未写n 不扣分)4-2 A 属于混合晶体4-3[NaB(OC 2H 5)4]n 的一维结构示意图及一维点阵如下:m +O H 2O H 2(2分)(1 分)(1 分)(1 分)(1 分)(2分)4-4 Na 的配位数为4, B 原子采取SP3杂化(2分)H O2[F e O H(H]) 2 +=(H2O)4 F e F e( H 2 O )4+ 2 H O(12分)2O5OHH 2 O H H 2 O H 2OH H 2 OH 2 O O.....OF e F e F e F eH 2 O O.....OH 2 O H 2OH 2 OH 2 O H H3-3Al 2O3+6HCl+9H 2O=2[Al(H 2O)6]Cl 3 [Al(H2O)6]Cl 3= [Al(OH) 2(H2O)4]Cl+2HCl[Al(OH) 2(H2 O)4]Cl+NH 3 H·2O=Al(OH) 3+NH 4Cl+4H 2O (nm-4m)Al(OH) 3+(6m-nm)[Al(OH) 2(H 2O)4]Cl=[Al 2(OH) n Cl 6-n] m+(24m-4nm)H2O 3-4第 4 题(22 分)4-1n NaBH 4 +4n CH 3CH2OH =[NaB(OC 2H5 )4] n +4n H 2↑(分子式错误,方程式未配平不得分;未写n 不扣分)4-2 A 属于混合晶体4-3[NaB(OC 2H 5)4]n 的一维结构示意图及一维点阵如下:m +O H 2O H 2(2分)(1 分)(1 分)(1 分)(1 分)(2分)4-4 Na 的配位数为4, B 原子采取SP3杂化(2分)H O2[F e O H(H]) 2 +=(H2O)4 F e F e( H 2 O )4+ 2 H O(12分)2O5OHH 2 O H H 2 O H 2OH H 2 OH 2 O O.....OF e F e F e F eH 2 O O.....OH 2 O H 2OH 2 OH 2 O H H3-3Al 2O3+6HCl+9H 2O=2[Al(H 2O)6]Cl 3 [Al(H2O)6]Cl 3= [Al(OH) 2(H2O)4]Cl+2HCl[Al(OH) 2(H2 O)4]Cl+NH 3 H·2O=Al(OH) 3+NH 4Cl+4H 2O (nm-4m)Al(OH) 3+(6m-nm)[Al(OH) 2(H 2O)4]Cl=[Al 2(OH) n Cl 6-n] m+(24m-4nm)H2O 3-4第 4 题(22 分)4-1n NaBH 4 +4n CH 3CH2OH =[NaB(OC 2H5 )4] n +4n H 2↑(分子式错误,方程式未配平不得分;未写n 不扣分)4-2 A 属于混合晶体4-3[NaB(OC 2H 5)4]n 的一维结构示意图及一维点阵如下:m +O H 2O H 2(2分)(1 分)(1 分)(1 分)(1 分)(2分)4-4 Na 的配位数为4, B 原子采取SP3杂化(2分)H O2[F e O H(H]) 2 +=(H2O)4 F e F e( H 2 O )4+ 2 H O(12分)2O5OHH 2 O H H 2 O H 2OH H 2 OH 2 O O.....OF e F e F e F eH 2 O O.....OH 2 O H 2OH 2 OH 2 O H H3-3Al 2O3+6HCl+9H 2O=2[Al(H 2O)6]Cl 3 [Al(H2O)6]Cl 3= [Al(OH) 2(H2O)4]Cl+2HCl[Al(OH) 2(H2 O)4]Cl+NH 3 H·2O=Al(OH) 3+NH 4Cl+4H 2O (nm-4m)Al(OH) 3+(6m-nm)[Al(OH) 2(H 2O)4]Cl=[Al 2(OH) n Cl 6-n] m+(24m-4nm)H2O 3-4第 4 题(22 分)4-1n NaBH 4 +4n CH 3CH2OH =[NaB(OC 2H5 )4] n +4n H 2↑(分子式错误,方程式未配平不得分;未写n 不扣分)4-2 A 属于混合晶体4-3[NaB(OC 2H 5)4]n 的一维结构示意图及一维点阵如下:m +O H 2O H 2(2分)(1 分)(1 分)(1 分)(1 分)(2分)4-4 Na 的配位数为4, B 原子采取SP3杂化(2分)H O2[F e O H(H]) 2 +=(H2O)4 F e F e( H 2 O )4+ 2 H O(12分)2O5OHH 2 O H H 2 O H 2OH H 2 OH 2 O O.....OF e F e F e F eH 2 O O.....OH 2 O H 2OH 2 OH 2 O H H3-3Al 2O3+6HCl+9H 2O=2[Al(H 2O)6]Cl 3 [Al(H2O)6]Cl 3= [Al(OH) 2(H2O)4]Cl+2HCl[Al(OH) 2(H2 O)4]Cl+NH 3 H·2O=Al(OH) 3+NH 4Cl+4H 2O (nm-4m)Al(OH) 3+(6m-nm)[Al(OH) 2(H 2O)4]Cl=[Al 2(OH) n Cl 6-n] m+(24m-4nm)H2O 3-4第 4 题(22 分)4-1n NaBH 4 +4n CH 3CH2OH =[NaB(OC 2H5 )4] n +4n H 2↑(分子式错误,方程式未配平不得分;未写n 不扣分)4-2 A 属于混合晶体4-3[NaB(OC 2H 5)4]n 的一维结构示意图及一维点阵如下:m +O H 2O H 2(2分)(1 分)(1 分)(1 分)(1 分)(2分)4-4 Na 的配位数为4, B 原子采取SP3杂化(2分)。
全国高中学生化学竞赛决赛理论试题及答案第一题(6分)选取表1中的合适物质的字母代号(A~H)填人相应标题(①一⑧)后的括号中(单选),并按要求填空。
A B C D E F G HNO2+ NO N2O3N2H4NH3 N2O4H2N2O2NH2OH)不是平面分子,其衍生物用作高能燃料。
②()存在两种异构体,其中一种异构体的结构为。
③()具有线型结构,Lewis结构式中每个键的键级为2.0。
④()是无色的,平面分子,它的一种等电子体是。
⑤()既有酸性,又有碱性,可作制冷剂。
⑥()既有酸性,又有碱性;既是氧化剂,又是还原剂,主要做剂。
⑦()是顺磁性分子。
⑧()水溶液会分解生成N20,反应式为。
第二题(6分)图1是元素的△f G m/F一Z图,它是以元素的不同氧化态Z与对应物种的△f G m/F 在热力学标准态pH =0或pH == 14的对画图。
图中任何两种物种联线的斜率在数值上等于相应电对的标准电极电势ψA或ψB,A、B分别表示pH=0(实线)和pH=14(虚线)。
上图中各物种的△f G m/F的数值如表2所示。
表2 各物质的△f G m/FA X- X2HXO HXO2 XO3- XO4-F -3.06 0 / / / /Cl -1.36 0 1.61 4.91 7.32 9.79Br -1.06 0 1.60 / 7.60 11.12I -0.54 0 1.45 / 5.97 9.27B X-X2XO- XO2- XO3-XO4-F -3.06 0 / / / /Cl -1.36 0 0.40 1.72 2.38 3.18Br -1.06 0 0.45 / 2.61 4.47I -0.54 0 0.45 / 1.01 2.41⒈用上表提供的数据计算:ψA(IO3-/I-) ψB(IO3-/I-) ψA(ClO4-/HClO2)⒉由上述信息回答:对同一氧化态的卤素,其含氧酸的氧化能力是大于、等于还是小于其含氧酸盐的氧化性。


●竞赛时间4小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
●试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
●姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
●允许使用非编程计算器以及直尺等文具。
第1题大自然中的金属A只存在于化合物中,主要是通式为M x(SiO4)y硅酸盐和它的氧化物。
氧化物存在多种形态,并且易形成配位数CN metal = 7的单斜结构。
温度高于1100°C,它的晶格转变为四方结构。
温度超过2000°C它转变成立方结构。
后者的晶格结构是氟化钙型,晶格常数为a0 = 507 pm.。
这个结构在室温下可以被CaO稳定。
纯的氧化物(立方结构)密度为6.27 g·cm-3。
1.画出立方结构的晶胞。
2. 这个氧化物的实验式是什么?3. 这个氧化物中金属的配位数为多少?4. 金属在氧化物中的氧化数和在硅酸盐中的一样。
给出硅酸盐的实验式。
5.这个金属是什么?给出过程。
6.写出这个金属的电子构型。
7. 该氧化物中阳离子和阴离子的配位数为多少?8.运用如下热力学数据,计算氧的电子亲和能∆EA H°(O(g) + 2 e-→ O2-(g)):∆sub H°(M) = 609 kJ·mol-1; ∆IE H°(M/M n+) = 7482 kJ·mol-1; ∆diss H°(O2) = 498 kJ·mol-1;∆lattice H°(M-oxide) = -10945 kJ·mol-1; ∆f H°(M-oxide) = -1100 kJ·mol-1;得到这个金属的过程是一个两步合成。
第一步是硅酸盐的碳氯化,即在高温下与碳和气体氯反应。


第29届中国化学奥林匹克(决赛)试题2015年11月28日 合肥注意事项1. 考试时间4小时。
迟到超过30分钟者不能进考场。
开始考试后30分钟内不得离场。
2. 考试“开始铃声”响起后方可拆开资料袋答题。
考试“结束铃声”响起后,立即停止答题,把试卷和答题纸放于桌面,由监考人员检查并将答题纸装订后一并放入资料袋。
听到可以离开指令后方可离开考场。
3. 发出停止答题指令后仍继续答题者,正在解答的试题(大题)以零分计。
4. 本试卷含9道大题,共5页。
试卷已装订成册,不得拆散。
所有解答必须写在答卷上指定的框格内,写于其他地方无效。
若有改动,需将新内容写于答卷的附页,并标明题号。
5. 凡要求计算的问题,只有计算结果而无计算过程,即使结果正确也不得分。
6. 用黑色墨水笔或黑色圆珠笔答题,不得携带任何其他纸张进入考场。
若需要草稿纸,可举手向监考人员索取。
7. 将营员号写在试卷首页和每页答卷指定位置,否则无效。
8. 允许使用非编程计算器以及直尺等文具,。
不得携带铅笔盒、书籍、通讯工具入场。
不得将草稿纸带出考场。
9. 欲上卫生间,举手示意,经监考人员允许方可离开座位出考场,考场外由志愿者全程引领。
第1题 (7分)1-1 CH 3SiCl 3和金属钠在液氨中反应,得到组成为Si 6C 6N 9H 27的分子,此分子有一条三重旋转轴,所有Si 原子不可区分,画出该分子结构图(必须标明原子各类,H 原子可不标),并写出化学反应方程式。
1-2 金属钠和(C 6H 5)3CNH 2在液氨中反应,生成物中有一种红色钠盐,写出化学反应方程式,解释红色产生的原因。
1-3 最新研究发现,高压下金属Cs 可以形成单中心的CsF 5分子,试根据价层电子对互斥理论画出CsF 5的中心原子价电子对分布,并说明分子形状。
第2题(11分)将银电极插入298 K 的1.000×10-1 mol/L NH 4NO 3和1.000×10-3 mol/L AgNO 3混合溶液中,测得其电极电势Ag Ag /+ϕ随溶液pH 的变化如下图所示,已知氨水的解离常数(K b )为1.780×10-5,理想气体常数R = 8.314 J •mol -1•K -1,法拉第常数F = 96500 C •mol -1。
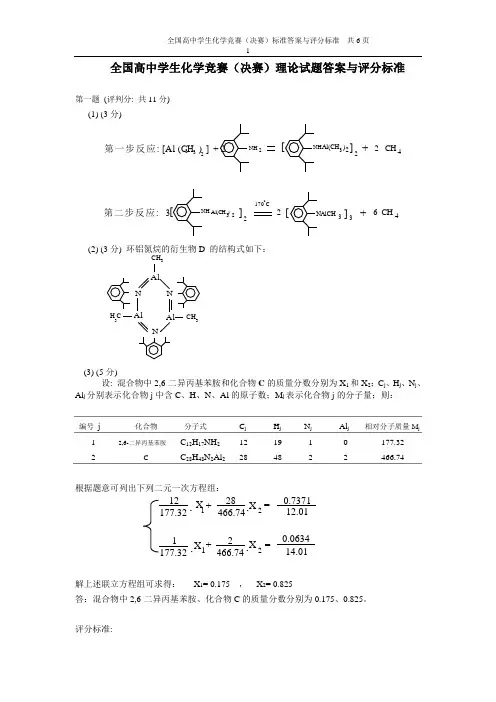
全国高中学生化学竞赛(决赛)理论试题答案与评分标准第一题 (评判分: 共11分)(1) (3分)3NAlCH 第一步反应: [Al (CH ) ] + 2 NH 2332[NH Al(CH )322]+2CH 4]223 Al(CH )NH [第二步反应: 3170C3]+6 CH 42[(2) (3分) 环铝氮烷的衍生物D 的结构式如下:CH 3Al NN AlAl N3CH 3H C(3) (5分)设: 混合物中2,6-二异丙基苯胺和化合物C 的质量分数分别为X 1和X 2;C j 、H j 、N j 、Al j 分别表示化合物j 中含C 、H 、N 、Al 的原子数;M j 表示化合物j 的分子量;则:编号 j 化合物分子式 C j H j N j Al j 相对分子质量M j1 2,6-二异丙基苯胺C 12H 17NH 21219 1 0 177.32 2 CC 28H 48N 2Al 2 284822466.74根据题意可列出下列二元一次方程组:12+28=0.7371177.32466.7412.011+2=0.0634177.32466.7414.01 X X X X 1212....解上述联立方程组可求得: X 1= 0.175 , X 2= 0.825答:混合物中2,6-二异丙基苯胺、化合物C 的质量分数分别为0.175、0.825。
评分标准:全题评判分: 共11分.(1) 评判分: 共3分,其中第一步反应为1分, 第二步反应为2分, 没用结构简式表示的不给分, 未配平、但方程中各化合物结构简式写对的, 第一步扣0.5分, 第二步扣1分;(2) 评判分: 3分(3) 评判分: 共5分, 写对求解联立方程组得3分, 方程结果X1、X2各占1分,全对得2分, 错一个扣1分;用百分数表示者, 只要正确不扣分, 结果数字有效位数不正确者, 每个结果扣0.25分。
第二题(评判分: 共18分)1. (评判分: 6分)第一步反应为CaC2O4·H2O脱水反应, N2和O2对反应无影响, 所以热重曲线相同(2分);第二步反应为CaC2O4的分解,由于CO在O2中氧化放热,使温度升高,加快了反应速率,所以在较低的炉温下CaC2O4即开始分解(2分);第三步反应为CaCO3 的分解,N2和O2对反应无影响,但由于第二步反应分解速率不同,使所生成的CaCO3有所不同,所以曲线有差异(2分)。


竞赛:碘酸钙的制备及含量测定注意事项:●实验时间为5.0小时,请仔细阅读试题内容,合理安排时间,完成全部内容。
每超过5分钟要扣1分,最长不超过20分钟。
●若制备失败可向监考教师索取原料重做,但要扣5分;若产品不够纯度测定所需量,可向监考教师索取分析样品,但要扣16.5分。
●需监考教师签字的,考生务必主动配合,未当场签字者无效。
伪造数据者,以零分计。
●完成全部实验内容后,将产品、实验报告(包括试题)交给监考教师,并清洗所用仪器和整理桌面,经监考教师签字后方可离开考场。
●废弃物应放入指定容器内。
●实验过程请注意安全。
一、实验内容1.产品的合成:碘在酸性条件下被氯酸钾氧化成碘酸氢钾(KIO3·HIO3),溶液经氢氧化钾中和后,与氯化钙发生复分解反应生成碘酸钙。
2.产品的分析:用间接碘量法测定。
3.完成实验报告。
二、主要仪器、试剂及材料1.主要仪器圆底烧瓶100mL 1只球形冷凝管(带磨口塞)1支磁力搅拌器1台电接点温度计(导电表)1支电子继电器1台电加热器(300W)1只结晶皿(水浴缸)1只温度计(100℃) 1支漏斗、吸滤瓶、表面皿各1只布氏漏斗和抽滤瓶(带橡皮塞)1只滴定管夹1只烧杯600ml、500ml 1只量筒100ml 1只150ml 2只10ml 2只100ml 1只玻管(直管、弯管)各1支碘量瓶250ml 3只移液管(胖肚)50ml 1支橡皮管25ml 1支碱式滴定管50ml 1支塑料洗瓶、木夹各1只容量瓶250ml 2只滴管2支洗耳球、角匙、镊子各1只玻棒2支铁架台、铁圈、铁夹3付●公用仪器电子天平(最大称量100克,±0.0001克)电炉(800W)电子天平(最大称量100克,±0.01克)循环水式真空泵2.试剂及材料碘化学纯(CP) 1 mol·L-1 氯化钙溶液氯酸钾化学纯(CP)1∶1 高氯酸溶液碘化钾分析纯(AR)碘酸钾标准溶液30%氢氧化钾溶液0.1 mol·L-1硫代硫酸钠标准溶液0.5mol·L-1 氢氧化钠溶液0.5% 淀粉溶液6 mol·L-1盐酸无水乙醇化学纯(CP)1 mol·L-1硫酸pH试纸(1-14)滤纸、称量纸、碎冰3.主要原料和产品的某些性质3.1几种盐的溶解度(克/100克水)碘酸钙无水盐389.88 一水合物407.90 六水合物497.90硫代硫酸钠158.10 碘酸钾170.80 碘253.80 氯酸钾122.55三、操作步骤1.制备碘酸钙在100mL圆底烧瓶中依次加入2.20克碘、2.00克氯酸钾(均由教师定量供给)和45mL 水,放入搅拌磁子,然后把烧瓶置入水浴缸内,用铁夹固定,开动搅拌器,使氯酸钾溶解,滴加6mol·L-1盐酸8滴(pH~1),装上冷凝管,通冷却水,冷凝管顶部塞上带玻璃管塞子,用橡皮管把反应产生的气体导向盛有约100mL氢氧化钠溶液的大烧杯内吸收。
中国会第20届全国高中生竞赛(决赛)论试题2007年1月17日● 本竞赛试题共8题,总分120分,竞赛时间4小时。
迟到超过30分钟者不得进入考场,考试开始后1小时内不得离开考场。
解答完毕,将试卷和答卷及草稿纸折好,背面朝上放于桌面,撤离考场。
● 试卷和答卷已分别装订成册,不得拆散,所有解答必须写在答卷的指定位置,写于其他位置无效.● 选手营号写在答卷每页左边指定位置,不得写所属地区,校名称和姓名,否则按废卷论。
● 使用黑色墨水钢笔或圆珠笔答题,不得使用铅笔(包括作图)。
使用提供的草稿纸.不得携带任何其他纸张进入考场。
● 允许使用非编程计算器及直尺,橡皮、涂改液等文具,不得将文具盒以及手机、小灵通、BP机等通讯工具带入考场,一经发现将严肃处。
原予量: H 1008 B 1081 201 N 1401 O 1600第1题 (14分)钛及其合金具有密度小、强度高、耐腐蚀等优良性能,被广泛用于航天、航空、航海、石油、工、医药等部门。
我国四川省有大型钒钛磁铁矿。
从由钒钛磁铁矿经“选矿”得到的钛铁矿提取金属钛(海绵钛)的主要工艺过程如下:钛铁矿还原熔炼生铁高钛渣氯化、精制焦炭氯气还原镁海面钛TiCl4碳-1 钛铁矿的主要成分为FTO3。
控制电炉熔炼温度(<1500),用碳还原出铁,而钛则进入炉渣浮于熔融铁之上,使钛与铁分离,钛被富集。
已知:FeTiO3C TiO2TiCFe COFeTiO3 FeTiO3+=++++++CC43==Fe CO3Ti++Fe3CO①②③G mrJ.mol-1===G mrJ.mol-1G mrJ.mol-1190900-161T750000--500T913800519T通过计算判断在电炉熔炼中主要发生以上哪个反应? (3分)1-2 写出在1073—1273下氯反应的方程式。
(1分)1-3 氯得到的T4中含有的VO3必须用高效精馏的方法除去,为什么? 实际生产中常在409 下用还原VO3,反应物的摩尔比为1:,生成氯亚铜和难溶于T4的还原物,写出还原反应方程式。
第23届全国高中学生化学竞赛理论试题第1题用传统的工艺方法从矿物中提取锰和锌存在能耗高、三废排放量大和工艺流程长等缺点。
2009年报道,采用1:1硫酸溶液同槽浸出锰结核矿[质量分数20.0)(2=MnO ϖ]和锌精矿[质量分数70.0)(=ZnS ϖ]的工艺方法提取锰和锌获得成功,对资源综合利用、节能减排和清洁生产生有重要的实际意义。
已知44.0)/(,77.0)/(223-==+++Fe Fe E V Fe Fe E θθ V ZnS S E V Mn MnO E V 265.0)/(,23.1)/(.22==+θθ。
1-1 锰结核矿和锌精矿单独酸浸结果很不理想。
请通过热力学计算,说明锰结核矿和锌精矿同槽酸浸时发生化学反应的可行性。
1-2 模拟实验发现,二氧化锰和硫化锌同槽酸浸时反应速率很慢,若在酸溶液中加入少量的铁屑则能明显使反应速率加快。
写出铁进入溶液后分别与二氧化锰和硫化锌发生化学反应的离子方程式,并简述反应速率加快的原因。
1-3 研究发现,2种矿物同槽酸浸4小时后,锰和锌的浸出率只有~80%,为了提高浸出率,在实际工艺中,须将过滤后的滤渣用四氯乙烷处理后再做二次酸浸,请简要说明四氯乙烷的作用。
1-4 锌精矿中常有部分铅共生,同槽酸浸工艺回收铅的方法之一是在浸渣中加入足量的食盐水使铅溶出,写出溶出铅的化学方程式。
第2题我国的稀土资源约占世界总量的80%,居世界第一位。
稀土元素的化学性质极其相似,分离十分困难,仅从1794年发现钇到1945年从铀裂变产物中得到钷就花了150年。
稀土萃取化学的研究为大规模分离和提纯稀土元素带来了新飞跃。
2008年国家最高科学技术奖授予化学家徐光宪,以表彰他在创立稀土 串级萃取理论及其工艺方面的杰出贡献,该项成就使我国高纯稀土产品成本下降3/4,单一高纯稀土产品占世界产量的90%以上。
2-1 目前在稀土分离工业中广泛应用国产萃取剂P 507,它的化学名称为(2 乙基己基)膦酸(2 乙基己基)酯,画出其化学结构简式,写出萃取三价稀土离子的化学反应方程式(萃取剂用HA 表示,稀土离子用RE3+表示)。
全国高中学生化学竞赛暨冬令营实验试题
−−−3-α-呋喃基丙烯酸的制备及含量测定
注意事项:
1.实验竞赛时间为5.0小时,请合理安排好时间。
2.详细阅读实验内容和步骤, 并规范操作,若制备失败, 可向监考教师索取原料重做, 但要扣分。
3.需由监考教师签字的,考生务必主动配合,未签字者无效。
伪造数据者以零分计。
4.实验结束将产品、实验报告(包括试题)交给监考教师, 并清洗所用仪器和整理台面, 经监考教师签字后, 方可离开考场。
5.废弃物应投放于指定容器内。
6.实验过程中请注意安全。
一、实验内容:
1.产品的合成:以呋喃甲醛(O CHO)和乙酸酐为原料,在碱性条件下经Perkin 反应制得粗产品,再经纯化得到3-α-呋喃基丙烯酸纯品干燥并计算产率。
2.产品的分析:用中和滴定法测定产品纯度。
3.完成实验报告。
二、主要仪器和试剂:
1、主要仪器
标准磨口仪器1套
布氏漏斗和吸滤瓶1套
电热套1个
铁架台2个
烧瓶夹1支
白瓷板1块
防护眼镜1副
冷凝管(供选择)
冷凝管夹1只滴定管夹1只手套(棉、塑料) 各1只漏斗2个升降台1个烧杯400mL,150mL,250mL 各1个锥形瓶50mL、100mL 各1个
250mL 2个量筒25mL 1个不锈钢刮刀1把研钵1副
表面皿(贴标签者用于烘干产品)
2块玻璃棒2支
称量瓶1个
药匙1把
塑料洗瓶1个
试剂瓶1个
碱式滴定管50mL 1支
广泛pH试纸
滤纸
沸石
称样纸
碎滤纸
循环水泵(公用)
烘箱(公用)
电子天秤(公用)
最大称量100g,±0.0001g
扭力天秤(公用) ±0.005g
2、试剂
呋喃甲醛化学纯cp 乙酸酐化学纯cp 无水碳酸钾化学纯cp 碳酸钠化学纯cp 浓盐酸化学纯cp
活性炭已活化
1:3乙醇水溶液
1:1中性乙醇水溶液(经处理)
0.1mol/L的NaOH标准液
(已装于试剂瓶中)300mL
邻苯二甲酸氢钾(基准物在天平室) 酚酞指示剂:0.2%乙醇水溶液
5%硝酸银水溶液
3、原料和产品主要性质
3.1 呋喃甲醛相对分子质量96.08 浅黄色液体,密度1.16×103kg/m3,熔点-38.7℃、沸点161.7℃,难溶于水,易溶于乙醇。
3.2 乙酸酐相对分子质量102.09 无色有刺激气味液体,沸点139℃,遇水水解。
3.3 3-α-呋喃基丙烯酸相对分子量138.12无色针状晶体,熔点137~138℃,难溶于水,易溶于碱液中。
3.4 3-α-呋喃基丙烯酸钠易溶于水。
3.5邻苯二甲酸氢钾相对分子质量20
4.21
三、操作步骤:
1·3-α-呋喃基丙烯酸的制备:
在100mL圆底烧瓶中,依次加入5mL呋喃甲醛(由教师定量供给)、14mL乙酸酐和6g无水碳酸钾,用电热套加热回流1.5小时。
反应开始时应控制加热速度(由于逸出二氧化碳,最初有泡沫出现)。
在搅拌下趁热将反应物倒入盛有100mL蒸馏水的烧杯中,用固体碳酸钠中和3-α-呋喃基丙烯酸至弱碱性,加入活性炭后煮沸5~10分钟,趁热过滤, 滤液在冰水浴中边搅拌边滴加浓盐酸,使3-α-呋喃基丙烯酸析出完全,抽滤。
用少量蒸馏水洗涤晶体2次。
粗产品用适量1:3乙醇水溶液重结晶,抽滤,洗涤,尽量抽干,经监考教师认可后,将产品移到贴有标签的表面皿上,烘干30分钟后,经监考教师确认已干燥,当考生在场时,称重,并将产品的重量及外观记录在考生的实验报告上。
考生当场将产品用研钵研细,装入称量瓶中供纯度测定用。
2·产品的分析
2·(1)产品纯度测定
1.1 0.1 mol·L-1NaOH溶液的标定
用减量法准确称取0.4~0.6g邻苯二甲酸氢钾基准物质两份分别于两个250mL锥形瓶中,加入40~50mL水使之溶解(必要时可加热),加入2~3滴酚酞指示剂,用NaOH溶液滴定至呈微红色,保持半分钟内不褪色,即为终点。
计算每次标定的NaOH溶液的浓度,并计算相对极差。
1.2 产品纯度的测定
用增量法准确称取产品0.27~0.35g,用20~30mL 1:1乙醇水溶液溶解,加入2~ 3滴酚酞指示剂,用NaOH溶液滴定至呈微红色,保持半分钟内不褪色,即为终点。
平行进行两次,计算每次测得样品中3-α-呋喃基丙烯酸的百分含量,并计算相对极差。