第三节化学平衡(第四课时 等效平衡)(2012)
- 格式:ppt
- 大小:226.50 KB
- 文档页数:20

第三节 第四课时 等效平衡 教案高二化学【教学目标】1、掌握什么是等效平衡2、在不同条件下,等效平衡的判断【教学重点】等温等容条件下等效平衡的条件等温等压条件下等效平衡的条件【教学难点】等温等容条件下等效平衡的条件等温等压条件下等效平衡的条件【复习提问】1. 什么是化学平衡状态?2、判断是否达到平衡状态的标志?【讲解】一、 等效平衡1、定义:一定条件(温度体积一定或温度压强一定)下的同一可逆反应,只是起始加入物质的情况不同,达到平衡后,任何相同组分的分数(体积分数、物质的量分数、质量分数等)均相同,这样的化学平衡互称为等效平衡。
2、同一平衡还有一类特殊的等效平衡,不仅任何相同组分的分数相同,而且相同组分的物质的量也相同,这类平衡又称为同一平衡。
(同一平衡是等效平衡的特例)例:浓度/mol ·L -1间/s浓度/mol ·L -1 21间从正反应开始3、探究等效平衡的条件探究1:等温等容条件下等效平衡的条件相同物质的起始物质的量相等或按化学计量数折合后对应量相等。
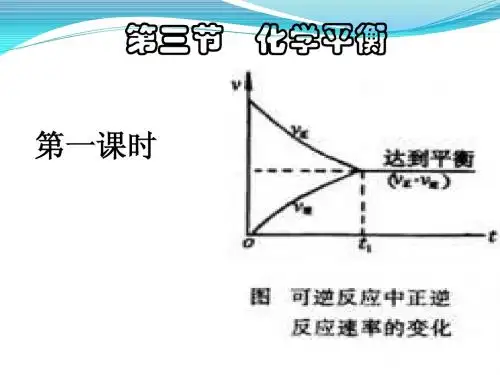
(一边倒、投料量相同)例题:在一定温度下,把2 mol SO2和1 mol O2通入一个一定容积的密闭容器里,发生如下反应: 2SO2+O2 ≒ 2SO3 当此反应进行到一定程度时,反应混合物就处于化学平衡状态。
现在该容器中,维持温度不变,令a、b、c分别代表初始加入的SO2、O2和SO3的物质的量(mol)。
如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时反应混合物中三种气体的百分含量仍跟上述平衡时的完全相同。
请填写下列空白:(1)若a=0,b=0,则c=___________。
(2)若a=0.5,则b=_________,c= _________。
(3)a、b、c取值必须满足的一般条件是(用两个方程式表示,其中一个只含a和c,另一个只含b和c):______ ,_____。
探究2:等温等压条件下等效平衡的条件把不同的起始状态,通过化学方程式中的计量数,换算成同一边物质(反应物一边或生成物一边),如果各反应物或生成物的物质的量之比相同,则是等效平衡。




第三节化学平衡(3)—等效平衡学习目标知识与技能:理解等效平衡的含义。
过程与方法:1.自主学习,培养学生自学的能力。
2.通过比较、分析、归纳、总结,提高学生的理解能力。
情感态度与价值观:通过等效平衡的学习,加深理解“透过现象看本质”的道理。
自主学习(先学后教)1.等效平衡的含义在同一条件下的同一可逆反应,由于起始浓度不同可形成多个不同的平衡体系。
对同一可逆反应体系,起始时加入物质的物质的量不同,而达到化学平衡时,同种物质的百分含量相同,这样的平衡称为等效平衡。
理解等效平衡的含义,回答下列问题:【问题1】形成“等效平衡”有什么条件?【问题2】形成“等效平衡”的反应类型?【问题3】形成“等效平衡”的对象是什么?【问题4】形成“等效平衡”的标志是什么?练习:在相同温度和压强下,1 L密闭容器中发生如下反应:CO(g)+H2高温2(g)+H2(g)CO H2O CO2H2投料1(mol) 1 1 0 0平衡时物质的量(mol)0.5 0.5 0.5 0.5 浓度(mol/L)0.5 0.5 0.5 0.5 物质的量的分数0.25 0.25 0.25 0.25 体积分数0.25 0.25 0.25 0.25 投料2(mol)0 0 1 1平衡时物质的量(mol)0.5 0.5 0.5 0.5 浓度(mol/L)0.5 0.5 0.5 0.5 物质的量的分数0.25 0.25 0.25 0.25 体积分数0.25 0.25 0.25 0.25观察上表,回答下列问题:【问题1】投料1和2达到化学平衡时,是否形成等效平衡?【问题2】若形成等效平衡,以上哪些数据可作为判断依据?【问题3】除上表数据外,你还可以根据什么数据判断是否形成等效平衡?2.等效平衡的分类(1)恒温恒容已知投料1、2、3能形成等效平衡,你能找出其中的规律吗?(2)恒温恒压已知投料1、2、3能形成等效平衡,你能找出其中的规律吗? 练习:对于反应2SO 2(g)+O 2(g)2SO 3(g),在500 ℃、1个标准大气压时,进行六次实验,实验时的有关物质的起始浓度数据如下:编 号 SO 2 O 2 SO 3 ⑴ 2a a 0 ⑵ 0 0 2a ⑶ a 0.5a a ⑷ 4a 2a 0 ⑸ 0 a 3a ⑹a0.5a3a其中达到平衡时属于等效平衡的体系有_ 。


仁文教育仁寿总校第____讲学生:电话:仁文教育精品堂培训学校名校冲刺仁文教育温馨提醒:人天天都学到一点东西,而往往所学到的是发现昨日学到的是错的。
【基础知识】.1、等效平衡问题的解题思路:⑴、概念:同一反应,在一定条件下所建立的两个或多个平衡中,混合物中各成分的含量相同,这样的平衡称为等效平衡。
⑵分类:①等温等容条件下的等效平衡:在温度和容器体积不变的条件下,改变起始物质的加入情况,只要可以通过可逆反应的化学计量数比换算成左右两边同一边物质的物质的量相同,则两平衡等效,这种等效平衡可以称为等同平衡。
②等温等压条件下的等效平衡:在温度和压强不变的条件下,改变起始物质的加入情况,只要可以通过可逆反应的化学计量数比换算成左右两边同一边物质的物质的量比值相同,则两平衡等效,这种等效平衡可以称为等比例平衡。
③等温且△n=0条件下的等效平衡:在温度和容器体积不变的条件下,对于反应前后气体总分子数不变的可逆反应,只要可以通过可逆反应的化学计量数比换算成左右两边任意一边物质的物质的量比值相同,则两平衡等效,这种等效平衡可以称为不移动的平衡。
解决化学平衡的技巧:化学平衡计算的基本模式——平衡“三步曲”:比如: m A + n B p C + q D起始: a b0 0转化: mx nx px qx平衡: a-mx b-nx px qx其中:①转化量与方程式中各物质的系数成比例;②这里a、b可指物质的量、浓度、体积等。
③对反应物:平衡浓度=起始浓度-转化浓度;对生成物:平衡浓度=起始浓度+转化浓度由定义式法求反应速率,需先求浓度的变化量和时间,据浓度的变化量可得出物质的量的变化量与体积的比。
例:一定温度下密闭容器中发生反应:1L容器800℃时可逆反应CO(g) + H2O(g) CO2(g) + H2(g)途径1:起始 0.01mol 0.01mol 0 0平衡 0.004mol 0.004mol 0.006mol 0.006mol途径2:起始 0 0 0.01mol 0.01mol平衡 0.004mol 0.004mol 0.006mol 0.006mol上述两种途径,同一可逆反应;外界条件相同;通过不同的途径(正向和逆向);平衡时同种物质的物质的量相等(同种物质的含量相等)-----效果相同的平衡对于同一个可逆反应,在相同的条件下(恒温恒容或恒温恒压),不管是从正反应开始,还是从逆反应开始,或从正反应和逆反应同时开始,都可以建立同一平衡状态。
](https://uimg.taocdn.com/8a0283177cd184254b35352a.webp)

第3节化学平衡----等效平衡问题分析1.等效平衡的原理在一定条件(恒温、恒容或恒温、恒压)下,只是起始加入情况不同的同一可逆反应达到平衡后,任何相同组分的物质的量分数(或体积分数)均相同,这样的化学平衡互称等效平衡.2.等效平衡的建立化学平衡状态的建立与条件(如浓度、温度、压强等)有关,而与建立平衡时的途径无关,因而同一可逆反应,从不同的状态开始,只要达到平衡时的条件(浓度、温度、压强等)完全相同,则可形成等效平衡.如常温常压下,可逆反应:2SO2 +O2 ⇌2SO3①2mol 1mol 0②0 0 2mol③1mol 0.5mol 1mol①从正反应开始,②从逆反应开始,③从正、逆反应同时开始,由于①、②、③三种情况如果按方程式的化学计量数比折算成同一方向的反应物,对应各组分的物质的量均相等如将②、③折算为①],因此三者为等效平衡。
【例1】在一个固定体积的密闭容器中,保持一定温度,进行以下反应:H2(g)+I2(g)⇌2HI(g).已知起始时加入1mol H2和2mol I2(g),当达到平衡时H2的体积分数为φ.下列四种情况分别投入上述容器,且始终保持原温度,平衡时H2的体积分数也为φ的是( )A.2 mol H2(g)和1 mol I2(g) B.3 mol HI(g)C.2 mol H2(g)和2 mol I2(g) D.1 mol I2(g)和2 mol HI(g)3.等效平衡的规律(1)恒温、恒容条件下的等效平衡Ⅰ类:在恒温、恒容条件下,对于反应前后气体化学计量数不相等的可逆反应,只改变起始时加入物质的物质的量,若通过可逆反应的化学计量数之比换算成同一边物质的物质的量,所得反应物(或生成物)的物质的量与原起始量对应相同,则两平衡等效.简记:必须对应相同.【例2】在一密闭的容器中充入2mol A和1mol B发生反应:2A(g)+B(g)⇌xC(g),达到平衡后,C的体积分数为w%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mol充入容器,达到平衡后,C的体积分数仍为w%,则x的值为( )A.只能为2 B.只能为3 C.可能为2,也可能为3 D.无法确定Ⅱ类:在恒温、恒容条件下,对于反应前后气体化学计量数相等的可逆反应,只改变起始时加入物质的物质的量,若通过可逆反应的化学计量数之比换算成同一边物质的物质的量,所得反应物(或生成物)的物质的量之比与原起始量之比对应相同,则两平衡等效.简记:对应成比例.【例3】一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)⇌3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%.其它条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数小于a%的是( )A.2mol C B.2mol A、1mol B和1mol He(不参加反应)C.1mol B和1mol C D.2mol A、2mol B和3mol C(2)恒温、恒压条件下的等效平衡在恒温、恒压条件下,对于反应前后气体化学计量数任意性的可逆反应,只改变起始时加入物质的物质的量,若通过可逆反应的化学计量数之比换算成同一边物质的物质的量,所得反应物(或生成物)的物质的量之比与原起始量之比对应相同,则两平衡等效.简记:对应成比例【例4】将3mol A和1mol B混合于一体积可变的密闭容器P中,以此时的温度、压强和体积作为起始条件,发生了如下反应:3A(g)+B(g)⇌2C(g)+D(g),达到平衡时C的浓度为wmol/L保持温度和压强不变,按下列四种配比充入容器P中,平衡后C的浓度仍为w mol/L 的是( )A.6molA+2molB B.3molA+1molB+2molCC.2molC+1molB+1molD D.1molC+2molD课堂练习:1.在恒温恒容条件下,将4molA和2molB放入一密闭容器中2A(g)+B(g)⇌2C(g)+D(s),达到平衡时,C的体积分数为a;在相同条件下,按下列配比分别投放A、B、C、D,达到平衡时,C的体积分数不等于a的是( )A.4mol、2mol、0mol、2mol B.2mol、1mol、2mol、2molC.2mol、1mol、2mol、1mol D.2mol、1mol、0mol、1mol【答案】D2.如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:N2(g)+3H2(g)⇌2NH3(g)△H=-192kJ•mol-1.向 M、N 中,都通入 xmol N2 和ymol H2的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )A.若x:y=1;2,则平衡时,M中的转化率:N2>H2B.若x:y=1:3,当M中放出热量172.8kJ时,N2的转化率为90%C.若x=1,y=3,则达到平衡时反应物的转化率N<MD.平衡时N2气体在两容器中体积分数可能相等【答案】D3.向一固定体积的密闭容器中通入 a mol N2O4气体,在密闭容器内发生反应:N2O4(g)⇌2NO2(g),达到平衡时再通入a mol N2O4气体,再次达到平衡时,与第一次达平衡时相比,N2O4的转化率( )A.不变 B.增大 C.减小 D.无法判断【答案】C4.在一固定体积的密闭容器中加入2mol A和1mol B发生反应2A(g)+B(g)⇌3C(g)+D(g),达到平衡时C的浓度为w mol•L-1,若维持容器的体积和温度不变,按下列四种配比方案作为反应物,达平衡后,使C的浓度仍为w mol•L-1的配比是( )A.4 mol A+2 mol BB.3 mol C+1 mol D+2mol A+1 mol BC.3mol C+1 mol D+1 mol BD.3 mol C+1 mol D【答案】D5.(双选)Fe2O3(s)+3CO(g)⇌2Fe(s)+3CO2(g),该反应的平衡常数K=64,在1L恒容密闭容器甲和乙中,甲中加有四种物质各1mol,乙中加有Fe2O3,Fe,CO2各1mol,CO 2mol.达平衡后,两容器中不等的是( )A.用CO表示反应速率B.平衡混合气体的平均相对分子质量C.CO的转化率D.CO2的体积分数【答案】AC。