固体比热容
- 格式:ppt
- 大小:1.95 MB
- 文档页数:26


实验五 固体比热容的测量(电热法)金属是重要的固态物质,本文对固体物质比热容的测量重点介绍了金属比热容的测量,金属比热容是金属物质的重要特性,本文重点介绍电热法测量固体比热容。
【实验目的】1、掌握基本的量热方法——用量热器测热量法。
2、学习用电热法测固体的比热容。
【实验仪器】热学综合实验平台、量热器、待测钢球、测温探头【实验原理】固体比热容指单位质量的热容量,也是特定粒子电子、原子、分子等结构及其运动特性的宏观表现。
测量固体物质比热容对于了解固体物质性质,物质内部结构等都具有重要的意义,常用于测量固体物质比热容的方法有动态法、混合法、冷却法等。
金属是重要的固态物质,本书对固体物质比热容的测量重点介绍了金属比热容的测量,金属比热容是金属物质的重要特性,本实验重点介绍电热法测量固体比热容。
在量热器中加入质量为m 的待测物,并加入质量为0m 的水,如果加在加热器两端的电压为U ,通过电阻的电流为I ,通电时间为t ,则电流作功为:UIt A = (5-1)如果这些功全部转化为热能,使量热器系统的温度从1T ℃升高至2T ℃,则下式成立()()1201100T T c c m c m mc UIt -+++=ω (5-2)c 为待测物的比热容,0c 为水的比热热容,1m 为量热器内筒的质量,1c 为量热器内筒的比热容, 2m 为铜电极和铜搅拌器总质量,2c 为铜比热容。
由(5-2)式得()[]m c c m c m T T UIt c //0110012ω----= (5-3)为了尽可能使系统与外界交换的热量达到最小,在实验的操作过程中就应注意以下几点:1、不应当直接用手去把握量热筒的任何部分,不应当在阳光直接照射下进行实验。

固体比热容的测量(混合法)实验目的:1、学会基本的量热方法——混合法。
2、测定金属的比热容。
3、学习一种修正散热的方法——用外推法修正温度。
仪器和用具:量热器 温度计 物理天平 停表 小量筒 待测物(金属块)实验原理:温度不同的物体混合之后,热量从高温物体传给低温物体,若与外界无热量交换,最后将达到一均匀稳定的平衡温度。
将质量为m 、温度为2t 、比热容为x c 的金属块,投入量热器内筒中,根据热平衡原理,可列出20011221()( 1.9)()x mc t t m c m c m c V t t -=+++-20011221()( 1.9)()m c t t m c m c m c V t t ⨯-=+++- 00112212( 1.9)()()x m c m c m c V t t c m t t +++-=- 内筒和搅拌器0.216C =⨯200铝J 卡(9.0410C )kg 克C ,V 单位:cm 3 实验内容:1、调节物理天平,称衡待测金属块、内筒及搅拌器的质量。
2、将高于室温(20—250C)的温水倒入内筒,盖好绝热盖,插好温度计不断搅拌,每隔30秒记录一次温度,当温度不再下降时,迅速将系有细线的金属块(其温度t 2为室温)放入量热器内筒水中,盖好绝热盖,继续搅拌,每隔30秒记录一次温度至温度变化缓慢为止,将测量的t ί、 τί记入自拟表格中。
3、取出内筒(连同金属块,搅拌器和水)称衡其质量,再减去m 、m 1和m 2,即为水的质量。
4、用小量筒测量温度计浸入水中部分的体积V 。
5、作温度—时间(t —τ)曲线,用外推法确定初温t 1和终温t 。
6、将以上各量代入公式计算x c ,并估算误差。
实验报告(60分)(一)实验目的、仪器、原理与实验内容:叙述有条理、逻辑性强,公式正确,内容完整。
(20分)(二)数据记录和处理1、数据记录部分(1)表格设计科学、合理、注明物理单位。
(5分)(2)正确进行读数,数据记录格式规范,数据记录完整、无遗漏,无多余记录,有效数字表述正确(原始数据附在实验报告上)。

固体比热容的测量实验原理
固体比热容的测量实验原理:
1. 准备固体样品,常用金属块。
2. 使用电热器加热样品,电热器功率可调节。
3. 使用热电偶测量样品温度的升高。
4. 供给已知的电功率Q在时间t内AddTo样品,使温度上升ΔT。
5. 根据能量守恒,电功率=样品吸收的热量。
Q=mCΔT
6. 其中m为样品质量,C为样品的比热容。
7. 重复实验测量不同ΔT下的Q和t。
8. 求比热容C=Q/mΔT。
9. 多组数据求平均可提高准确度。
10. 也可测试不同材料,对比其比热容。
通过测量已知功率加热造成的温升,根据能量守恒计算样品比热容,是一种直接且简便的测量比热容的方法。


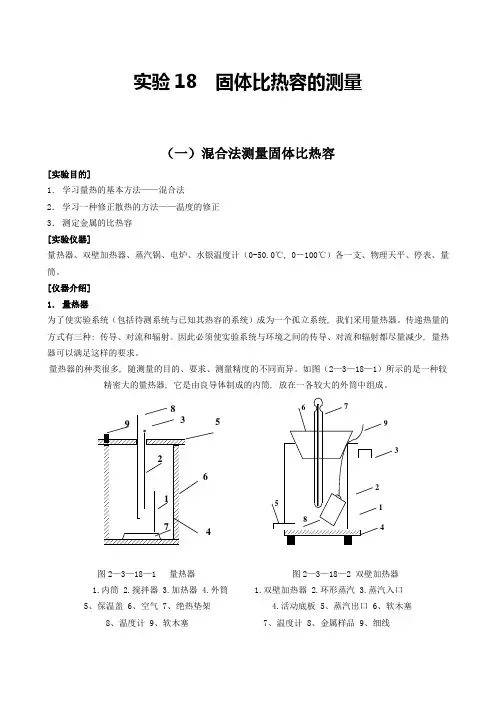
实验18 固体比热容的测量(一)混合法测量固体比热容[实验目的]1.学习量热的基本方法——混合法2.学习一种修正散热的方法——温度的修正3.测定金属的比热容[实验仪器]量热器、双壁加热器、蒸汽锅、电炉、水银温度计(0-50.0℃, 0-100℃)各一支、物理天平、停表、量筒。
[仪器介绍]1.量热器为了使实验系统(包括待测系统与已知其热容的系统)成为一个孤立系统, 我们采用量热器。
传递热量的方式有三种: 传导、对流和辐射。
因此必须使实验系统与环境之间的传导、对流和辐射都尽量减少, 量热2.外筒是双层结构, 空气封闭其中, 因为空气是热的不良导体, 故可避免空气传导而引起热量的损失;外筒上端的木盖可严密地盖着, 避免空气对对流所引起的热量损失;外筒的内壁和内筒的外壁均电镀得十分光亮, 可减少热辐射, 外筒的底部放上一个隔外筒的外表再包一层绒布, 这样就能使整个系统尽可能根据上述测量的T-t数据, 以T为纵坐标, 以t为横坐标, 即得如图(2—3—18—4)的T-t曲线。
A点对应的时刻就是测水温开始的时间 , B点对应的时刻就是, 而不是5分钟末的时间。
然后作图即得混合前后冷水的初温和末温T。
把各个物理量的测量值代入式(2-3-18-1)即可算出金属样品的比热容。
图(2—3—18—4)中的G点所对应的温度应为室温所在的位置, 这样才不影响温度的修正。
[实验内容和要求]1. 混合法测定铜块的比热容2.混合过程中散热的温度修正法3.混合前量热器(含水)系统温度低于室温(加冰块), 测量系统随时间吸热变化的温度。
4. 混合过程快速测量变化的温度5. 数据处理:Cx与标准值求百分误差[注意事项]1. 作温度值修正法曲线图, FE垂直于t轴, 满足S1=S2, 图中G点对应的温度接近室温为佳。
2. 从曲线图中定出初温T2和末温T。
[实验思考]请分析本实验主要的误差来源。
(二)冷却法测量金属的比热容[实验目的]学习冷却法测量金属比热容的方法[实验仪器]FB312型冷却法金属比热容测量仪[实验原理]根据牛顿冷却定律, 用冷却法测定金属的比热容是量热学常用方法之一。



实验简介19世纪,随着工业文明的建立与发展,特别是蒸汽机的诞生,量热学有了巨大的进展。
经过多年的实验研究,人们精确地测定了热功当量,逐步认识到不同性质的能量(如热能、机械能、电能、化学能等)之间的转化和守恒这一自然界物质运动的最根本的定律,成为19世纪人类最伟大的科学进展之一。
从今天的观点看,量热学是建立在“热量”或“热质”的基础上的,不符合分子动理论的观点,缺乏科学内含。
但这无损量热学的历史贡献。
至今,量热学在物理学、化学、航空航天、机械制造以及各种热能工程、制冷工程中都有广泛的应用。
比热容是单位质量的物质升高(或降低)单位温度所吸收(或放出)的热量。
比热容的测定对研究物质的宏观物理现象和微观结构之间的关系有重要意义。
本实验采用混合法测固体(锌粒)的比热容。
在热学实验中,系统与外界的热交换是难免的。
因此要努力创造一个热力学孤立体系,同时对实验过程中的其他吸热、散热做出校正,尽量使二者相抵消,以提高实验精度。
实验原理混合法测比热容设一个热力学孤立体系中有种物质,其质量分别为,比热容为()。
开始时体系处于平衡态,温度为,与外界发生热量交换后又达到新的平衡态,温度为,若无化学反应或相变发生,则该体系获得(或放出)的热量为假设量热器和搅拌器的质量为,比热容为,开始时量热器与其内质量为的水具有共同温度,把质量为的待测物加热到后放入量热器内,最后这一系统达到热平衡,终温为。
如果忽略实验过程中对外界的散热或吸热,则有式中为水的比热容。
代表温度计的热容量,其中是温度计浸入到水中的体积。
⏹系统误差的修正在量热学实验中,由于无法避免系统与外界的热交换,实验结果总是存在系统误差,有时甚至很大,以至无法得到正确结果。
所以,校正系统误差是量热学实验中很突出的问题。
为此可采取如下措施:●要尽量减少与外界的热量交换,使系统近似孤立体系。
此外,量热器不要放在电炉旁和太阳光下,实验也不要在空气流通太快的地方进行。
●采取补偿措施,就是在被测物体放入量热器之前,先使量热器与水的初始温度低于室温,但避免在两热器外生成凝结水滴。
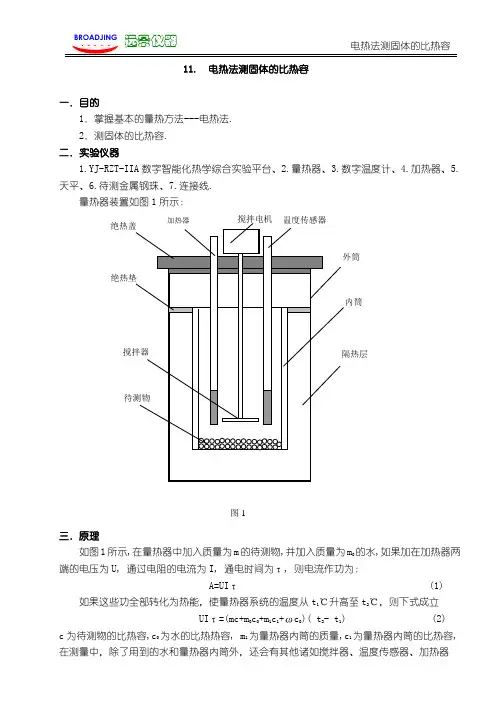
11. 电热法测固体的比热容一.目的1.掌握基本的量热方法---电热法.2.测固体的比热容.二.实验仪器1.YJ-RZT-IIA数字智能化热学综合实验平台、2.量热器、3.数字温度计、4.加热器、5.天平、6.待测金属钢珠、7.连接线.三.原理如图1所示,在量热器中加入质量为m的待测物,并加入质量为m的水,如果加在加热器两端的电压为U, 通过电阻的电流为I, 通电时间为τ, 则电流作功为:A=UIτ (1)如果这些功全部转化为热能,使量热器系统的温度从t1℃升高至t2℃,则下式成立UIτ=(mc+m0c+m1c1+ωc)( t2- t1) (2)c为待测物的比热容,c0为水的比热热容, m1为量热器内筒的质量,c1为量热器内筒的比热容,在测量中,除了用到的水和量热器内筒外,还会有其他诸如搅拌器、温度传感器、加热器等物质参加热交换, 我们把搅拌器、加热器和温度传感器等的质量用水当量ω表示. ω可以由实验室给出.由2式得:c=〔UIτ/( t2- t1)- mc- m1c1-ωc〕/m (3)为了尽可能使系统与外界交换的热量达到最小,在实验的操作过程中就应注意以下几点:不应当直接用手去把握量热筒的任何部分;不应当在阳光直接照射下进行实验;不在空气流通过快的地方或在火炉旁或暖气旁做实验.此外,由于系统与外界温差越大,在它们之间传递越快;时间越长,传递的热量越多.因此在进行量热实验时,要尽可能使系统与外界的温差小些,并尽量使实验进行得快些.四.实验步骤1. 用天平称出不锈钢量热器内筒质量m1,加入一定量的水后用天平称出其总质量M,则水的质量m0=M- m1,2.用天平称取一定量m(约100g)的金属颗粒放于量热器水中,如图1所示,安装好量热器装置.3.打开电源开关,如图2所示,调节恒压调节钮, 使其恒压输出12V左右,4.如图2所示,连接好加热器电路, 将测温电缆和搅拌电机电缆与YJ-RZT-IIA数字智能化热学综合实验平台面板上对应电缆座连接好,安装好搅拌电机、测温探头、加热器.4.打开搅拌开关,记录系统温度t15.连接好加热电阻电路。
常用液体、固体比重-比热表名称相态比重15.6至21℃比热15.6时kJ/Kg℃乙酸100% 液 1.05 2.01乙酸10% 液 1.01 4.02丙酮100% 液0.78 2.15醇含乙醇95% 液0.81 2.51醇含乙醇90% 液0.82 2.72 铝固 2.64 0.96 氨100% 液0.61 4.61氨26% 液0.9 4.19Aroclor 液 1.44 1.17石棉板固0.88 0.8沥青液 1 1.76固体沥青固 1.1-1.5 0.92-1.67 苯液0.84 1.72砖墙固 1.0-2.0 0.92盐水-氯化钙25% 液 1.23 2.89盐水-氯化钠25% 液 1.19 3.29 干粘土固 1.9-2.4 0.94煤固 1.2-1.8 1.09-1.55(4℃)煤焦油固 1.2 1.47固体焦固 1.0-1.4 1.11铜固8.82 0.42软木固0.25 2.01棉固 1.5 1.34棉籽油液0.95 1.97导热姆 A 液0.99 2.64导热姆 C 液 1.1 1.747-2.72 乙二酸液 1.11 2.43 脂肪酸-软脂液0.85 2.73 脂肪酸-硬脂液0.84 2.3 鲜鱼固 3.14-3.43鲜水果固 3.35-3.68汽油液0.73 2.22耐热玻璃固 2.25 0.84玻璃棉固0.072 0.66胶,2份水1份干胶液 1.09 3.73 甘油100%(丙三醇)液 1.26 2.43 蜂蜜液 1.42 盐酸31.55%(氯化)液 1.15 2.51 盐酸10%(氯化)液 1.05 3.14 冰固0.9 2.09冰淇淋固 2.93猪油固0.92 2.68铅固11.34 0.13皮革固0.86-1.02 1.51亚麻油液0.93 1.84 氧化镁85% 液0.208 1.13 枫树浆液/ 2.01鲜猪肉固/ 3.27牛奶液 1.03 3.77-3.89镍固8.9 0.46 硝酸95% 液 1.05 2.09 硝酸60% 液 1.37 2.68 硝酸10% 液 1.05 3.77 1#燃油(煤油)液0.81 1.97 2#燃油液0.86 1.843#燃油液0.88 1.84#燃油液0.9 1.765#燃油液0.93 1.726#燃油液0.95 1.67 API中部原油液0.85 1.84 API汽油液0.88 1.76 纸固 1.7-1.15 1.88石蜡固0.86-0.91 2.6 熔融石蜡液0.9 2.89 酚(碳酸)液 1.07 2.34 磷酸20% 液 1.11 3.56 磷酸10% 液 1.05 3.89 邻苯二酸酐液 1.53 0.97 硫化橡胶固 1.10 1.74 SAE-SW(8#机油)液0.88 /SAE-20(20#机油)液0.89 / SAE-30(30#机油)液0.89 / 矽固 1.45-1.35 0.8 海水液 1.03 3.94丝绸固 1.25-1.35 1.38 烧碱50% 液 1.53 3.27 烧碱30% 液 1.33 3.52 豆油液0.92 1.0-1.38 钢固7.9 0.46 不锈钢300系列固8.04 0.5 蔗糖60%糖浆液 1.29 3.1 蔗糖40%糖浆液 1.18 2.76 糖,甘蔗及甜菜固 1.66 1.26 硫磺液 2 0.85 硫酸110%(发烟)液/ 1.13 硫酸90% 液 1.84 1.47 硫酸60% 液 1.5 2.18 硫酸20% 液 1.14 3.52 钛(商用)固 4.5 0.54 甲苯液0.86 1.76 四氯化碳液 1.58 0.88 松木油液0.86 1.76 鲜蔬菜固/ 3.06-3.94 水液 1 4.19果酒液 1.03 3.77木材固0.35-0.9 3.77羊毛固 1.32 1.36锌固7.05 0.4相对空(空气的密度是 1.29kg/m3)的比重15.8至21℃比热15.8℃时kJ/Kg℃空气气 1 1氨气0.6 2.26苯气 1.36丁烷气 2 1.91 二氧化碳气 1.5 0.88 一氧化碳气0.97 1.07 氯气 2.5 0.5乙烷气 1.1 2.09 乙烯气0.97 1.88 氟利昂-12 气/ 0.67 氢气0.07 14.32 硫化氢气 1.2 1.05 甲烷气0.55 2.51 氮气0.97 1.06 汽气 1.1 0.94 丙烷气 1.5 1.93 二氧化硫气/ 0.68 水蒸汽气 2.3 1.9几种常见物质的比热容物质化学符号模型相态比热容量(基本)J/(kg・K)比热容量(25℃)J/(kg・K)氢H 2 气14000 14300 氦He 1 气5190 5193.2 氨NH3 4 气2055 2050 氖Ne 1 气1030 1030.1 锂Li 1 固3580 3582 乙醇CH3CH2OH 9 液2460 2440 汽油混混液2200 2220石蜡CnH2n+2 62至122固2200 2500甲烷CH4 5 气2160 2156 油混混液2000 2000 软木塞混混固2000 2000 乙烷C2H6 8 气1730 1729 尼龙混混固1700 1720乙炔C2H2 4 气1500 1511聚苯乙烯CH2 3 固1300 1300 硫化氢H2S 3 气1100 1105 氮N 2 气1040 1042 空气(室温)混混气1030 1012空气(海平面、干燥、混混气1005 1035 0℃)氧O 2 气920 918 二氧化碳CO2 3 气840 839 一氧化碳CO 2 气1040 1042 铝Al 1 固900 897 石绵混混固840 847 陶瓷混混固840 837 氟 F 2 气820 823.9 砖混混固750 750 石墨 C 1 固720 710 四氟甲烷CF4 5 气660 659.1 二氧化硫SO2 3 气600 620 玻璃混混固600 84 氯Cl2 2 气520 520 钻石 C 1 固502 509.1 钢混混固450 450 铁Fe 1 固450 444 黄铜Cu,Zn 混固380 377 铜Cu 1 固385 386 银Ag 1 固235 233汞Hg 1 液139 140固135 135 铂Pt1金Au 1 固129 126铅Pb 1 固125 128水蒸气(水)H2O 3 气1850 1850 水H2O 3 液4200 4186 冰(水)H2O 3 固2060 2050 (-10℃)。
对固体比热容的研究陈芳蕊(天水师范学院 物理系 甘肃,天水 741000 )摘要:固体比热容根据能量均分原理可得其定容比热容应为Nk C v 3= 在室温下与杜隆—珀蒂定律相符,但在低温范围内偏离杜隆—珀蒂定律,温度越低,比热容越小。
固体的定容比热容v C 包括晶格比热容和电子比热容两方面。
由于这两方面之间相互作用很弱,所以在本文中,从经典统计理论和量子统计理论出发将分别讨论晶格振动和电子热运动对固体比热容的贡献,并加以比较作出结论。
关键词:固体 温度 比热容The research on the specific heat capacity of solidChenfangrui(College of Physics and Information Science, Tianshui Normal University ,Tianshui ,741000)Abstract: The solid may result in its specific heat at constant volume compared to the heat capacity according to the equipartition of energy principle to accommodate is Nk C v 3=Under room temperature with Du prosperous - Podi law match case, but deviates Du in the low temperature scope the prosperous - Podi law, the temperature is lower, is smaller than the heat capacity. The solid specific heat at constant volume accommodates including the crystal lattice compares the heat capacity two aspects compared to the heat capacity and the electron. Because between these two aspects the interaction is very weak, therefore in this paper, will embark from the classics statistical theory and the quantum statistics theory will discuss the lattice vibration and the electronic heat movement separately compares the heat capacity to the solid the contribution, and will compare draws the conclusion.Key words: Solid Specific heat capacity Temperature1.引言固体比热容是指单位质量的物质在某一过程温度升高1K 所吸收的热量,也是特定粒子(电子、原子、分子等)结构及其运动特性的宏观表现。
比热容的定义及物理意义比热容是化学与物理学中的一个重要概念,它用来表征物质在受到加热等外部刺激时,其热量的吸收或放出的速率,也即物质在热能的转变过程中,所需要的能量。
比热容定义为物质吸收或放出每单位质量的每单位温度的能量,记为C,单位为牛顿/千克平方摄氏度(N/kgK)。
比热容是表示物质热性质的量度,其值会随着温度发生变化,且比热容值与物质组成等有关;由于比热容的水平节点不同,金属的比热容值相对于液体来说,要比较的低。
根据物质的不同性质,可以将比热容分为三类:固体比热容、液体比热容和气体比热容。
固体比热容是指固体吸收或放出每单位质量每单位温度的热量,它表示物质在加热或冷却过程中,物质分子发生的作用力,或者说是发生一定温度变化时,单位质量物质所吸收或释放的热量。
它是由元素组成而成,比热容可以与物质的组成元素、结构及温度等相关联,会受到物质温度的影响,温度的升高会使比热容也随之发生变化。
液体比热容是指液体吸收或放出每单位质量每单位温度的热量,它反映了液体分子受到外力作用时,液体会吸收或放出多少热量,一般液体比热容较低,这是由于液体分子性质决定的,液体分子的弹性较小,能量会很快转变,从而使比热容较低。
气体比热容是指气体吸收或放出每单位质量每单位温度的热量,它反映了气体分子受到外力作用时,气体会吸收或放出多少热量。
气体的比热容一般较高,由于气体分子的弹性较大,从而能量转变速率较慢,在一定温度范围内,气体的比热容和温度之间没有明显的关系。
总之,比热容是表示物质热性质的量度,比热容值可以与物质组成以及温度相关联,温度升高时,比热容会发生变化,根据物质的不同性质,可以将比热容分为固体比热容、液体比热容和气体比热容。
因此,比热容与物质的温度变化、热量的传递等有着极大的关系,在实际中有重要的意义。