高三有机化学1轮复习
- 格式:ppt
- 大小:837.01 KB
- 文档页数:46

高中化学一轮复习:有机化学知识点总结1、有机反应类型(1)取代反应:有机化合物分子里的某些原子或原子团被其它原子或原子团所代替的反应。
特征:一般有光照条件;一上一下,交换位置(2)加成反应:有机物分子中双键/叁键上的碳原子与其他原子直接结合生成新的化合物分子的反应。
特征:双键变单键(叁键变双键),原子加两边(3)加聚反应:含碳碳双键或是叁键的相对分子质量小的化合物,在一定条件下,互相结合成相对分子质量大的高分子的反应,简称加聚反应。
特征:双键,小分子变大分子(4)氧化反应:有机物燃烧;醇或醛的催化氧化。
特征:点燃;Cu /Ag 催化(5)酯化反应:醇跟羧酸生成酯和水的反应,也属于取代反应。
2、烃类:仅含碳和氢两种元素的有机物称为碳氢化合物 分为:烷烃、烯烃和炔烃(1)烷烃:碳原子之间都以碳碳单键结合成链状,碳原子剩余的价键全部跟氢原子结合而达到饱和的烃。
如:甲烷(CH 4)、乙烷(C 2H 6)、丙烷(C 3H 8)、丁烷(C 4H 10)等,烷烃通式为:C n H 2n+2(n≥1) 分子式(碳原子数)不同的烷烃互为同系物;分子式相同、结构不同的烷烃互为同分异构体。
(2)烷烃的物理性质a. 随着分子里含碳原子数的增加,熔点、沸点逐渐升高,相对密度逐渐增大;b. 碳原子数等于或小于4的烷烃,在常温常压下都是气体;其他烷烃在常温常压下都是液体或固体;c. 烷烃的相对密度小于水的密度;d. 一般不溶于水,而易溶于有机溶剂,液态烷烃本身就是良好的有机溶剂。
(3)烷烃的化学性质稳定,跟酸、碱及氧化物都不发生反应,也难与其他物质化合;但在特定的条件下能发生下列反应:a. 能燃烧:C n H 2n+2 +3n 12+O 2 −−−→点燃nCO 2 + (n+1)H 2O b. 易与卤素单质X 2取代:C n H 2n+2 + Cl 2 −−−→光照C n H 2n+1Cl + HCl有机物主要化学性质甲烷(1)燃烧(点燃时要验纯)(淡蓝色火焰,无黑烟,甲烷含碳量低)(2)取代反应(与氯气)CH4 + Cl2CH3Cl + HCl CH3Cl + Cl2CH2Cl2 + HClCH2Cl2 + Cl2 CHCl3 + HCl CHCl3 + Cl2CCl4 + HCl现象:黄绿色逐渐消失,试管内壁有油状液滴产生,试管内上升一段水柱。


高三化学一轮复习计划及进度表
目标
本文档旨在制定高三学生化学一轮复的计划及进度表,以确保复过程有条不紊,并帮助学生达到优秀的复成果。
计划
第一阶段:知识整理与梳理(2周)
- 复基础知识点,包括化学反应、离子反应等。
- 温化学实验原理和方法,注意实验操作细节。
- 复周期表和元素周期性规律,掌握各元素的重要特性。
第二阶段:理解与掌握(3周)
- 深入研究有机化学知识,包括有机反应类型和反应机理。
- 认真研究无机化合物的命名规则和性质。
- 研究溶液浓度计算和酸碱反应的平衡计算方法。
第三阶段:应用与拓展(2周)
- 考察并巩固化学知识的应用能力,解决综合性的化学问题。
- 积累一定数量的化学题目,进行模拟考试,提高解题速度和准确度。
- 阅读相关化学文献,了解前沿的科学研究与应用。
进度表
注意:以上进度表仅供参考,具体安排应根据个人情况和学校要求灵活调整。
以上进度表仅供参考,具体安排应根据个人情况和学校要求灵活调整。
总结
制定一份合理的复习计划是高三化学复习的关键所在,希望通过此文档的指导,学生能够有序地进行复习,提高化学成绩,为顺利完成高考做好准备。

高三化学一轮复习计划【导语】以下是作者帮大家整理的高三化学一轮复习计划(共16篇),仅供参考,希望能够帮助到大家。
篇1:高三化学一轮复习计划一、第一轮复习之策略:1、重视教材,狠抓双基课本是学科知识的精华,在第一轮复习中,自始至终都应以教材为本。
注重知识的全面性,重点性,精确性,联系性和应用性。
对教材中的关键性知识(我们常说的考点)进行反复阅读,深刻理解,以点带面形成知识网络,能准确、科学、全面地理解、使用和描述化学知识。
2 、掌握原理、灵活应用,注重解题思路化学原理如元素守恒原则,氧化还原反应、电子得失守恒、化学平衡,物质结构的一般规律,要重点回顾。
掌握化学基本原理和规律,在解题中灵活应用,拓宽解题思路,增强解题技巧。
如:应用守恒法,差量法,讨论法解一些计算题,可以提高解题的速度和准确性。
《化学反应原理》模块在学习能力层次上属于综合应用,此内容在高考考试中约占30%-40%。
如电解质溶液中离子浓度大小的比较是高考的“热点”之一。
这种题型考查的知识点多,综合性强,有较好的区分度,它能有效地考查学生对强、弱电解质的电离、离子反应、电离平衡、水解平衡、PH值及各种守恒关系的掌握程度及综合运用能力。
复习中着重对“两平衡、三守恒”即水解平衡、电离平衡、电荷守恒、物料守恒和质子守恒进行分析,列举典型例题进行分类练习和变式练习。
3、注重实验能力的培养化学是一门实验科学,今年高考化学以实验为主线的命题数量明显多于往年,所占分数也明显高于往年。
4、强化解题训练,提高解题能力,培养应考实战能力(1)、加强题型训练。
根据章节内容和要求,结合高考真题,透彻理解知识点,切实打好基础。
加强章节题型训练,举一反三。
(2)、第一轮复习中也要适当穿插综合模拟训练。
(3)、把规范训练落实到复习的每一个环节中,减少非智力因素丢分。
化学用语规范、语言表达规范、计算题解答规范,实验现象和操作规范等。
(4)、注重做题的质量,提高解题速度。

高中有机化学整理烃烃:仅含C、H两种元素的有机物叫做烃。
甲烷烷烃一、构造特点和通式:1、构造特点:全部以C—C,和C—H结合的饱和链烃,烷烃。
2、通式:C n H2n+2 (满足此通式的必然为烷烃)3、同系物和同分异构体:同系物:构造相似,组成上相差一个或假设干个CH2的有机物,互称为同系物;同分异体:分子式一样,构造不同的物质互称为同分异构体。
二、物理性质:随碳原子数目的增加,烷烃由g→l→s;随碳原子数目的增加,烷烃的熔点、沸点逐渐升高。
〔碳原子一样的烷烃,支链多的熔、沸点低。
〕三、化学性质:1、氧化反响:〔1〕燃烧:CH4+2O2CO2+2H2O〔2〕烷烃不能使酸性KMnO4溶液褪色。
2、取代反响:(反响不可控制)CH4 + Cl2CH3Cl+HCl CH3Cl+Cl2CH2Cl2+HClCH2Cl2+Cl2CHCl3+HCl CHCl3+Cl2CCl4+HClCH3CH3+Cl2CH3CH2Cl+HCl〔可生成6种取代物〕3、高温分解:CH4C+2H2 2CH4C2H4+2H2乙烯烯烃一、构造特点和通式:1、构造特点:只含一个C=C,其余全部以C—C,和C—H结合的链烃叫烯烃。
2、通式:C n H2n (满足此通式的还可能为环烷烃)二、物理性质:随碳原子数目的增加,烯烃由g→l→s;随碳原子数目的增加,烯烃的熔点、沸点逐渐升高。
三、化学性质:1、氧化反响:〔1〕燃烧:C2H4+3O22CO2+2H2O〔2〕烯烃能使酸性KMnO4溶液褪色。
乙烯与KMnO4溶液作用生成CO22、加成反响:CH2=CH2 +HBr CH3CH2Br CH2=CH2 +H2O CH3CH2OH CH2=CH2 +H2催化剂CH3CH3△3、加聚反响:nCH2=CH2 n四、乙烯的实验室制法:CH3CH2OH浓硫酸CH2=CH2↑+H2O170℃注意:1、浓H2SO4催化剂、脱水剂的作用;2、参加碎瓷片防止暴沸;3、温度计的水银球应置于液面以下;4、应迅速升温到170℃,防止较多的副反响发生;5、除去乙烯中的杂质,最好用NaOH溶液。

2025年高三化学一轮复习计划随着高考的临近,2025年高三化学的一轮复习工作正式展开。
本复习计划旨在帮助学生系统回顾和巩固化学知识,提升化学成绩,并为接下来的冲刺阶段打下坚实的基础。
一、复习目标本轮复习的主要目标包括:1. 全面提升化学成绩,确保在高考中取得优异成绩;2. 巩固和深化对化学基础知识的理解和应用;3. 提高解题能力和速度,熟练掌握各类题型的解题方法;4. 培养良好的化学学科素养和实验能力。
二、复习内容根据高三化学课程的知识体系,本次复习将围绕以下几个主要内容进行:1. 物质结构与性质:掌握原子、分子、晶体等的基本概念及相互关系;2. 化学反应原理:深入理解化学反应的实质、速率、平衡等原理;3. 有机化学:系统学习各类有机物的结构、性质、反应类型及合成方法;4. 化学实验:熟悉化学实验的基本操作和技能,培养实验设计和分析能力。
三、复习方法针对不同的复习内容,我们将采取以下有效的复习方法:1. 讲解典型例题:通过分析历年高考真题和模拟题中的典型例题,帮助学生掌握解题方法和技巧;2. 实战演练:安排大量的练习题和模拟题进行实战演练,提高学生的解题能力和速度;3. 总结规律技巧:引导学生总结解题规律和技巧,形成自己的解题思路和方法。
四、时间安排为确保复习计划的顺利进行,我们将制定详细的时间安排和进度表,分阶段进行复习。
具体安排如下:1. 第一阶段(约8周):重点复习物质结构与性质和化学反应原理;2. 第二阶段(约6周):重点复习有机化学和化学实验;3. 第三阶段(约5周):进行模拟试题演练和真题分析,查漏补缺。
五、学习资源与辅助材料在复习过程中,我们将充分利用以下学习资源和辅助材料:1. 高中化学教材和配套练习册;2. 历年高考真题和模拟题集;3. 化学学习网站和APP,提供在线学习和辅导服务;4. 化学实验操作手册和实验报告模板。
六、自我测试与评估为了及时了解学生的复习进度和效果,我们将定期进行自我测试和评估。

第7讲有机合成合成高分子复习目标1.能对单体和高分子进行相互推断,能分析高分子的合成路线,能写出典型的加聚反应和缩聚反应的反应方程式。
2.能举例说明塑料、合成橡胶、合成纤维的组成和结构特点,能列举重要的合成高分子,说明它们在材料中的应用。
3.能综合应用有关知识完成推断有机化合物、检验官能团,设计有机合成路线等任务。
考点一合成高分子1.有机高分子及其结构特点(1)定义相对分子质量比一般有机化合物大得多,通常在01104以上。
大部分高分子是由小分子通过02聚合反应制得的,所以常被称为高分子聚合物或高聚物。
(2)组成①单体:能够进行聚合反应形成高分子的低分子化合物。
②链节:高分子中03可重复的结构,也称04重复结构单元。
③聚合度(n):高分子链中含有的05链节数目。
2.高分子的分类及性质特点05塑料、合成纤维、合成橡胶又被称为三大合成材料。
3.合成高分子的两个基本反应(1)加聚反应①定义:由不饱和的单体加成聚合生成高分子的反应。
②产物特征:高聚物与单体具有相同的组成,生成物一般为线型结构。
③反应类型a.聚乙烯类(塑料)b.聚1,3丁二烯类(橡胶)c.混合加聚类:两种或两种以上单体加聚催化剂n CH2===CH—CH===CH2+n CH2===CH—CN――――→03。
d .聚乙炔类:04。
(2)缩聚反应①定义:含有两个(或两个以上)05官能团的单体分子间通过缩合反应生成高分子的反应。
②产物特征:生成高聚物和小分子,高聚物与单体有不同的组成。
③产物类型a .聚酯类:—OH 与—COOH 间的缩聚n HOCH 2—CH 2OH +n HOOC —COOH催化剂△06,n HOCH2—CH 2—COOH催化剂△07。
b .聚氨基酸类:—NH 2与—COOH 间的缩聚n H 2N —CH 2COOH催化剂△08,n H 2NCH 2COOH +n H 2NCHCH 3COOH催化剂△09。
c.酚醛树脂类10。

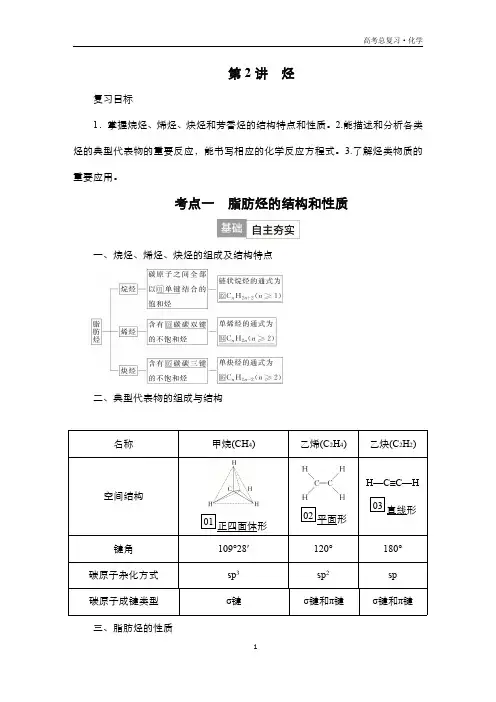
第2讲烃复习目标1.掌握烷烃、烯烃、炔烃和芳香烃的结构特点和性质。
2.能描述和分析各类烃的典型代表物的重要反应,能书写相应的化学反应方程式。
3.了解烃类物质的重要应用。
考点一脂肪烃的结构和性质一、烷烃、烯烃、炔烃的组成及结构特点二、典型代表物的组成与结构名称甲烷(CH 4)乙烯(C 2H 4)乙炔(C 2H 2)空间结构01正四面体形02平面形H—C≡C—H03直线形键角109°28′120°180°碳原子杂化方式sp 3sp 2sp 碳原子成键类型σ键σ键和π键σ键和π键三、脂肪烃的性质1.物理性质物理性质变化规律常温下01≤4个碳原子的烃都是气态,随着碳原子数的增多,逐渐状态过渡到02液态、固态随着碳原子数的增多,沸点逐渐03升高;同分异构体之间,支链越沸点多,沸点04越低相对密度随着碳原子数的增多,相对密度逐渐增大,密度均比水05小水溶性均难溶于水2.化学性质(1)氧化反应(2)烷烃的取代反应①取代反应:有机物中某些原子或原子团被其他原子或原子团所替代的反应。
②烷烃的卤代反应。
如甲烷和氯气生成一氯甲烷:06CH 4+Cl 2――→光照CH 3Cl +HCl 。
a .反应条件:07光照。
b .无机试剂:08卤素单质。
c .产物特点:09多种卤代烃混合物+HX(X 为卤素原子)。
d .量的关系:取代1mol 氢原子,消耗101mol 卤素单质。
(3)烯烃、炔烃的加成反应(写出有关反应方程式)(4)烯烃、炔烃的加聚反应①乙烯的加聚反应方程式:20n CH 2===CH 2――――→催化剂CH 2—CH 2。
②乙炔的加聚反应方程式:21n CH ≡CH――――→催化剂CH===CH 。
③1,3丁二烯的加聚反应方程式:22n CH 2===CH —CH===CH 2――――→催化剂CH 2—CH===CH —CH2。
四、脂肪烃的来源和用途脂肪烃来源用途甲烷天然气、沼气、煤矿坑道气燃料、化工原料乙烯工业:01石油裂解植物生长调节剂、催熟果实、化工原料实验室:02乙炔实验室:CaC 2+2H 2O ―→Ca(OH)2+CH≡CH ↑切割、焊接金属、化工原料请指出下列各说法的错因(1)1mol CH 4和1mol Cl 2发生取代反应生成的有机产物只有CH 3Cl 。

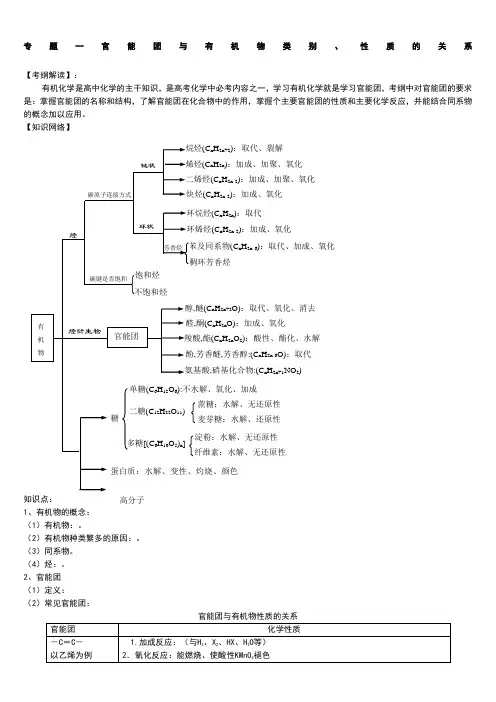
专题一官能团与有机物类别、性质的关系【考纲解读】:有机化学是高中化学的主干知识,是高考化学中必考内容之一,学习有机化学就是学习官能团,考纲中对官能团的要求是:掌握官能团的名称和结构,了解官能团在化合物中的作用,掌握个主要官能团的性质和主要化学反应,并能结合同系物的概念加以应用。
【知识网络】1(1)有机物:。
(2)有机物种类繁多的原因:。
(3)同系物。
(4)烃:。
2、官能团 (1)定义: (2)常见官能团:官能团与有机物性质的关系RCOOH3、三羟基对比4.四种有机分子的空间结构5、重要有机物的物理性质归纳(1)溶解性:有机物均能溶于有机溶剂.能溶于水的有机物为:低级的醇、醛、酸;微溶于水:①苯酚②苯甲酸③C2H5-O-C2H5注意:水溶性规律。
有机物是否溶于水与组成该有机物的原子团(包括官能团)有密切关系。
在有机物分子常见的官能团中,—OH 、—CHO 、—COC —、—COOH 、—SO 3H 等,皆为亲水基,—R 、—NO 2、—X 、—COOR —等皆为憎水基。
一般来讲,有机物分子中当亲水基占主导地位时,该有机物溶于水;当憎水基占主导地位时,则难溶于水。
由此可推知: ①烃类均难溶于水,因其分子内不含极性基团。
②含有—OH 、—CHO 、及—COOH 的各类有机物(如醇、醛、酮、羧酸),其烃基部分碳原子数小于等于3时可溶于水。
③当活泼金属原子取代有机物分子中的氢原子后所得的产物可溶于水。
如CH 3CH 2ONa 、CH 3COONa 、C 6H 5ONa 等。
(2)密度:比水轻的:①烃(含苯及其同系物、矿物油)②酯(含油脂)③一氯烷烃 比水重:①溴苯②溴乙烷③四氯化碳液态④硝基苯⑤苯酚 (3)有毒的物质:苯、硝基苯、甲醇、甲醛(4)常温下呈气态:①分子中含碳原子数小于或等于4的烃(新戊烷除外)②CH 3Cl ③HCHO(5)有特殊气味或香味:①苯②甲苯③CH 3COOC 2H 5④CH 3CH 2OH6、几类重要的有机物(1)糖类:又叫碳水化合物,一般符合C n (H 2O)m 的通式,但是符合该通式的不一定就属于糖类,不符合该通式的也可以属于糖类。
于对市爱美阳光实验学校高三一轮综合复习:有机化合物——烃和卤代烃一.教学内容:高三综合复习第一轮:有机化合物——烃和卤代烃二.、难点1.烃和卤代烃的性质的要点和综合运用是本节的。
三.具体内容:A. 脂肪烃〔一〕烷烃和烯烃的物理性质1.沸点:烷烃和烯烃的物理性质随着分子中碳原子数的递增,呈规律性的变化,沸点逐渐_ ___分子式相同的烃,支链越多,熔沸点越____。
2.相对密度:相对密度逐渐_____,常温下的存在状态,也由____逐渐过渡到____。
3.状态:当烃分子中的碳原子数≤4时,常温下呈______态。
〔二〕烷烃、烯烃的化学性质1.烷烃的化学性质:烷烃的化学性质一般比拟稳,在通常情况下跟酸、碱和高锰酸钾强氧化剂____。
但在特条件下可以发生以下反:〔写出反类型及化学方程式〕① ____:乙烷与氯气反生成一氯乙烷_________。
②燃烧:通式为___________________。
③裂解反:丁烷_______________。
2.烯烃的化学性质〔1〕氧化反:①能使酸性高锰酸钾溶液____________。
②可燃烧:通式为 CnH2n+ O2 →__________〔2〕加成反:可与______加成。
〔3〕加聚反:丙烯加聚反为_____________。
1,3—丁二烯的1,2—加成与1,4—加成1,2—加成:_______________。
1,4—加成:_______________。
〔三〕烯烃的顺反异构由于______而导致分子中_______不同所产生的异构现象,称为顺反异构。
_________排列在_________的称为顺式结构,如:顺— 2—丁烯__________。
______排列在_____的称为反式结构,如反—2—丁烯_______。
〔四〕炔烃1.乙炔室制法:在圆底烧瓶里放入几小块____,旋开分液漏斗的活塞,逐滴滴入_____,便产生乙炔气体。
反原理为:_____________。