农药微胶囊剂的研制共20页文档
- 格式:ppt
- 大小:2.77 MB
- 文档页数:20





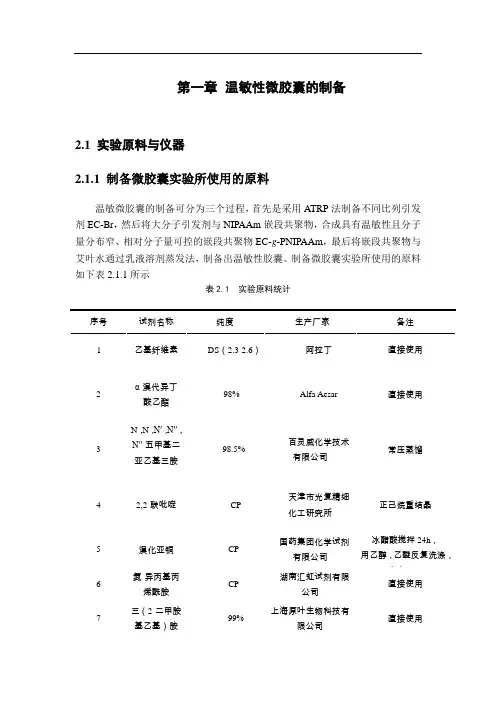
第一章温敏性微胶囊的制备2.1 实验原料与仪器2.1.1 制备微胶囊实验所使用的原料温敏微胶囊的制备可分为三个过程,首先是采用ATRP法制备不同比列引发剂EC-Br,然后将大分子引发剂与NIPAAm嵌段共聚物,合成具有温敏性且分子量分布窄、相对分子量可控的嵌段共聚物EC-g-PNIPAAm,最后将嵌段共聚物与艾叶水通过乳液溶剂蒸发法,制备出温敏性胶囊。
制备微胶囊实验所使用的原料如下表2.1.1所示表2.1 实验原料统计2.1.2 制备微胶囊实验所使用的仪器制备温敏性微胶囊所使用的原料如下表2.2所示:表2.2 实验仪器2.2 温敏聚合物的合成与表针2.2.1 大分子引发剂的合成乙基纤维素大分子引发剂EC-Br的合成过程如图 2.1,将乙基纤维素(EC 11.60g)溶于四氢呋喃(90ml)中,加入三乙胺(20.8ml),使其溶解,搅拌均匀。
将2-溴异丁酰溴(3.27ml)溶于THF(60ml)中,在冰水浴的条件下,缓慢滴加到EC/THF 溶液中。
待2-溴异丁酰溴滴加完毕后,于室温下继续反应24小时。
然后静置过夜,使盐沉于瓶底。
倒出上层清液,旋转蒸发浓缩后,滴加到二次水中沉淀,得到白色絮状的沉淀。
再用THF溶解,反复在二次水水中沉淀三次。
产物置真空烘箱中于45℃下干燥12小时得到乙基纤维素大分子引发EC-Br。
在本次实验过程中通过调节乙基纤维素上羟基与2-溴异丁酰溴的摩尔比来制得不同取代度的大分子引发剂,如图2.1所示。
图2.1 乙基纤维素大分子引发剂的合成过程2.3 测试与表征2.3.1 傅立叶变换红外光谱(FTIR)采用美国热电—尼高力仪器公司生产的Nicolet 380型傅立叶变换红外光谱仪对产物进行测试。
样品为粉末,经KBr压片制样,观察波长为400~4000 cm-1。
2.4 结果与讨论2.4.1 乙基纤维素及大分子引发剂红外谱图分析将EC和EC-Br干燥后,磨成粉状,将样品置于KBr盐片之上,在红外光谱仪上进行扫描测试。

氟乐灵微胶囊的研制巴雄军(福建新农大正生物工程有限公司)微胶囊技术是一种用成膜材料把固体或液体包覆使形成微小粒子的技术。
2O世纪7O 年代微胶囊化技术已用于农药剂型加工。
美国Pennwalt公司首先制成甲基对硫磷微胶囊,并在生产应用上获得成功。
微胶囊化能使高毒性、易挥发、易氧化分解的农药性能大为改善。
氟乐灵是芽前土壤处理除草剂,杂草萌发时抑制其细胞分裂而致死。
其除草性质是1960年由美国礼来公司的E.F.奥尔德等发现的,并由该公司开发生产,到70年代已成为世界重要除草剂品种之一。
其性质稳定,但在日光照射下易分解。
本研究使用原位聚合法对氟乐灵进行囊化,通过微胶囊化以降低其在光照条件下的分解率,达到控制释放的目的。
1 实验部分1.1 实验仪器和药品氟乐灵(≥95%)、尿素、37%甲醛、氢氧化钠、氯化铵、环己烷,以上试剂均为化学纯。
生物显微镜,日本OLYMPUS;JL9200型激光粒度仪,济南微纳仪器有限公司。
1.2 氟乐灵微胶囊的制备在装有搅拌装置的三口烧瓶中加入尿素和甲醛(摩尔比约为l:1.5~2.0),用氢氧化钠溶液调节溶液的pH值到8~9左右。
升温至70~80℃,反应得到稳定的脲醛树脂预聚体。
取一定量的氟乐灵原药溶于环己烷中,并在溶液中加入乳化分散剂,伴随剧烈搅拌,配成以含乳化分散剂的水溶液为水相的O/W型稳定乳液。
将上述的脲醛树脂预聚体加入乳液中,调节pH值,在酸催化条件下发生聚合反应,使油相物质被包裹起来,形成微胶囊颗粒。
缓慢升温,固化,温度控制在40~50℃,固化时间1h。
选择加入适量的助剂,即可得稳定的微囊悬浮剂。
1.3 氟乐灵微胶囊囊化条件的优化(l)载药量的优化:本研究分别设置三个目标载药量,通过氟乐灵的成囊率来考察一定量的囊皮条件下的最大载药量。
成囊率(%)=(微胶囊内的药量/系统中的总药量)×100微胶囊内的药量由以下方法测出:取一定量的微胶囊,用研钵研磨,用DMF溶解,经超声和高速离心机处理,提取上清液,用气相色谱仪测定其含量。

阿维菌素微胶囊剂制备的方法(2010-02-28 14:26:29)产品特点:农药阿维菌素微胶囊的方法,属农药制备技术领域。
本工艺采用现有的原位聚合法改进后制备,本发明的工序包括尿素-甲醛树脂预聚体水溶液的制备、阿维菌素混合物溶液的制备及阿维菌素微胶囊的制备。
本发明与现有技术相比,具有设备投资少,工艺易控制,反应稳定,适合于工业化生产,收率高于90%,包封率高于90%,且具有缓释性能等优点。
本方法生产的阿维菌素胶囊不但解决了阿维菌素与土壤结合影响药效的问题,同时通过缓释减少用量,延长药效有效期,巩固防治效果,不易使农药被大气,阳光和雨水破坏及流失,有效控制对地下水的污染,防治生态环境的改变。
制备工艺与方法农药阿维菌素微胶囊的方法,采用原位聚合法制备,工序包括预聚体的制备、阿维菌素混合物溶液的制备、阿维菌素微胶囊的制备,其特征在于:a.预聚体的制备:将尿素溶于甲醛,甲醛与尿素的摩尔比为2∶3~2∶5,用磁力搅拌器搅拌至澄清,用三乙醇胺调节PH值为8~9,在反应温度65℃~70℃,反应时间 1~1.5小时后生成粘稠状的液体,再用两倍于甲醛用量的蒸馏水稀释即得稳定的尿素 -甲醛树脂预聚体水溶液;b.阿维菌素混合物溶液的制备:将在常温状态呈粉状或颗粒状的阿维菌素溶于溶剂中,溶剂为二氯甲烷、三氯甲烷、甲苯或环己酮,溶剂使用量以使阿维菌素溶解或分散为止,本方法中1g阿维菌素使用20~30ml溶剂;然后加入2%~10%的乳化剂进行充分分散与乳化,溶好后的溶液再加入密度小于1的石油醚,石油醚的用量为所生成的阿维菌素微胶囊的密度与水的密度相等,在60℃~90℃的温度下,经1000r/min~1500r/ min搅拌后使其充分分散,当混合物相溶澄清后即可;c.阿维菌素微胶囊的制备:将尿素-甲醛树脂预聚体水溶液加入到在1000r/min~ 1500r/min搅拌下的阿维菌素混合物溶液中,搅拌15min后,向其中缓慢的加入1M的 HCl,搅拌速度降到500r/min~750r/min,30min后将其pH值调到2.5,反应一小时后加温到45℃,反应2.5小时后取消加温,向反应物中加入5ml吐温-20,并用NaOH将反应产物中和成pH=7,然后过滤离心收集阿维菌素微胶囊;最后将所得的微胶囊保存于 0.5%的羧甲基纤维素钠和1.9%的吐温-20的混合溶液中。
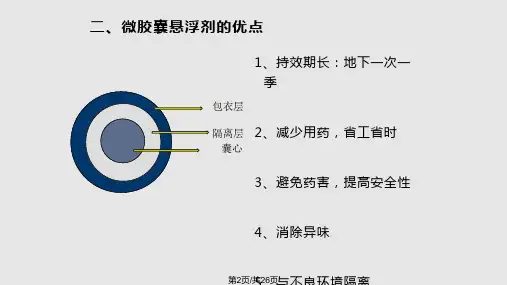

农药微胶囊剂的制备工艺1、原位聚合法把36%浓度的甲醛溶液488.5g与240g尿素混合,加入三乙醇胺调节pH =8,并加热至70℃,保温下反应1h得到粘稠的液体,然后用1000ml水稀释,形成稳定的尿素—甲醛预聚体溶液。
把油溶性原药活性成分加到上述尿素—甲醛预聚体溶液中,并充分搅拌分散成极细微粒状。
加入盐酸调节pH在1-5范围,在酸催化作用下缩聚形成坚固不易渗透的微胶囊。
控制溶液pH值很重要,当溶液pH值高于4时,形成的微胶囊不够坚固,易被渗透;而当pH在1.5以下时,由于酸性过强,囊壁形成过快,质量不易控制。
如要获得直径在2.5μm以下的微小胶囊,加酸调节pH的速度要慢,比如在1h内分3次加酸,同时要配合高速搅拌。
而在碱性条件下,同样可得到尿素—甲醛预聚体制成的微胶囊,pH控制在7.5-11范围,反应时间为15min-3h,温度控制在50-80℃。
温度高,反应时间则可缩短。
当缩聚反应进行1h后,适当升温至60-90℃,有利于微胶囊壁形成完整,但注意温度不能超过原药活性成分和预聚体溶液的沸点。
一般反应时间控制在1-3h,实践证明,反应时间延长至6h以上并没有显著改进效果。
用尿素—甲醛预聚体进行聚合形成的微胶囊有惊人的韧性和抗渗透性。
这种方法制得的微胶囊有别的制法无可比拟的良好密封性。
缺点是甲醛的气味难以全部除干净。
2、锐孔—凝固浴法把褐藻酸钠水溶液用滴管或注射器一滴滴加入到氯化钙溶液中时,液滴表面就会凝固形成一个个胶囊,这就是一种最简单的锐孔—凝固浴法操作。
滴管或注射器是一种锐孔装置,而氯化钙溶液是一种凝固浴。
锐孔—凝固浴法一般是以可溶性高聚物做原料包覆香精,而在凝固浴中固化形成微胶囊的。
用1.6%褐藻酸钠、3.5%聚乙烯醇、0.5%明胶、5%甘油等水溶液作微胶囊壁材,凝固浴使用15%浓度的氯化钙水溶液。
用锐孔装置以褐藻酸钠包覆原药活性成分滴入氯化钙凝固浴时,在液滴表面形成一层致密、有光滑表面、有弹性但不溶于水的褐藻酸钙薄膜。

摘要本文综述了农药微胶囊剂的国内外研究进展及应用现状。
在总结农药微胶囊芯材与壁材种类及农药微胶囊制备方法的基础上,对难溶性农药微胶囊化方法、吸附型缓控技术、包合型缓控技术以及化学键合缓控技术等研究进展进行了概述,指出了我国农药微胶囊研发中存在的问题,对其发展方向作出了展望。
1 农药微胶囊化方法微胶囊的制备方法很多,主要有物理、化学、物理化学和生物方法。
目前农药微胶囊剂多采用前3种方法制备。
生物学方法是利用酵母菌等真菌微生物细胞壁的半透性,使芯材进入细胞内,得到粒径为几十微米的微囊产品。
目前采用此方法制备农药微胶囊的研究还很少。
1.1 物理法利用物理和机械的方法制备微胶囊即为物理法。
其又分为喷雾干燥法、冷冻干燥法、包合法、超临界流体法、溶剂蒸发法和旋转分离法等。
物理法制备过程相对简单,但难以制得粒径较小的颗粒(粒径一般大于100 μm),易出现无芯胶囊,且有效成分的释放速率难以控制,药效不稳定,生产能力低。
因此,在农药微胶囊剂生产中应用较少。
其中应用相对广泛的是喷雾干燥法和溶剂蒸发法。
喷雾干燥法多以食用蛋白质或多糖为囊材,先将芯材分散在含囊壁材料的溶液中,制成悬浮液或乳浊液,之后物料雾化,并干燥使得雾化液滴中溶剂蒸发,壁材析出成囊。
该法在食品领域应用最广。
溶剂蒸发法先将芯材和壁材分散到有机相中,后移至与壁材不相溶的溶液中,加热使溶剂蒸发,进而壁材析出成囊。
其常用的壁材有丙烯酸甲酯、壳聚糖、聚己内酯和聚乳酸等。
1.2 物理化学法物理化学法有干燥浴法、熔化分散冷凝法、相分离法、囊芯交换法等。
其中相分离法是农药生产中最常用的方法,又分为水相相分离法(复合凝聚法和简单凝聚法)和油相相分离法。
在芯材与囊材混合溶液中,加入溶剂、凝聚剂、凝聚诱导剂等,通过改变温度或pH使聚合物的溶解度降低,并从溶液中凝聚出来,沉积在芯材表面形成微胶囊。
凝聚法一般以天然大分子物质如阿拉伯胶、明胶、海藻酸钠等为壁材。
由于其主要通过分子间作用力形成囊壁,因而囊壁的机械强度相对较低且易降解,囊芯活性成分在壁材降解后很快释放到环境中,不宜制备持效期较长的药剂。