高中化学竞赛专题考试—分子结构(含答案)
- 格式:doc
- 大小:131.00 KB
- 文档页数:5

专题9 分子结构一、选择题:1.以下物质种,含有非极性共价键的离子化合物是〔〕A、Na2O2B、NaOHC、H2O2D、MgCl22.以下物质中,含有极性共价键的是〔〕〔1〕N2(2)H2O (3)CCl4(4)Na2O2(5)NaOH (6)Na2OA、〔1〕〔2〕〔3〕 B.〔4〕〔5〕〔6〕C、〔2〕〔3〕〔5〕D(2)(4)(6)3.A原子的L电子层比B原子的L电子层少3个电子,B原子核外的电子总数比A原子电子总数多5个,那么A、B可能形成( )A、离子化合物B2A3B、离子化合物B3A2 C.共价化合物B3A2D、共价化合物BA24、根据“相似相溶〞的规律,以下溶剂可以用来从溴水中萃取溴的是〔〕(1)酒精〔2〕CCl4〔3〕液氨〔4〕苯〔5〕直馏汽油A、〔1〕〔2〕〔4〕〔5〕B、〔2〕〔4〕〔5〕C、〔1〕〔3〕〔5〕D、〔1〕〔3〕〔4〕5.以下各组物质中,化学键类型相同,分子的极性也相同的是〔〕A SO2和CH4B、CO2和CCl4C、SO2和CO2D、NH3和CCl46.含有极性键的非极性分子是〔〕(1)SO2(键角119ο)〔2〕CS2(直线型)〔3〕CCl4(4)NH3(5)CH2Cl2(6)BF3(平面正三角形)A、〔2〕〔3〕〔4〕B、〔1〕〔4〕〔6〕C、〔2〕〔3〕〔6〕D、〔2〕〔3〕〔5〕7.关于化学键的表达,正确的选项是〔〕A.离子化合物可能含共价键B.共价化合物可能含离子键C.离子化合物中只含离子键D.共价化合物中不含离子键8.以下分子中所含原子都满足最外层8电子结构的是〔〕A、光气〔COCl2〕 B.六氟化硫C、二氟化氙D、三氟化硼9.以下分子的结构中,原子的最外层电子不能满足8电子稳定结构的是〔〕A、CO2B、PCl3C、CCl4D、NO210.以下各分子中所有原子都满足最外层8电子结构的是〔〕A、BeCl2B、PCl3 C、PCl5 D、N211.以下性质中,可以证实某化合物内一定存在离子键的是〔〕A、可溶于水B、具有较高的熔点C、水溶液可以导电D、熔融状态能导电12、最近科学家研制的一种新分子,它具有空心的类似于足球的结构,分子式为C60,以下说法正确的选项是〔〕A、C60是一种新型的化合物B、C60和石墨都是碳的同素异形体C、C60中含有离子键D、C60的相对分子质量是720二、填空题:13、写出以下物质的电子式:〔1〕Cl2____________(2)N2_____________(3)HCl_______________(4)NH3_______________ 〔5〕H2O___________(6)H2O2___________(7)CO2____________(8)CH4________________ (9)PCl3____________(10)NaCl____________(11)MgCl2__________〔12〕Na2S____________ (13)NaOH___________(14)Na2O2__________(15)NH4Cl__________(16)甲基_____________ 17〕羟基__________〔18〕醛基___________〔19〕乙烯_________〔20〕乙炔______________ 〔21〕甲酸_______________14、用电子式表示以下物质的形成过程:(1)H2_____________________________________(2)HCl_______________________________ (3)H2S____________________________________(4)NH3______________________________ (5)KCl____________________________________(6)CaCl2_____________________________ (7)K2S___________________________________(8)BaCl2_____________________________________________ 15、化合物A是一种不稳定的物质,它的分子组成可用O x F y表示,10Ml氧气和10Ml氟气〔同温同压〕下,试答复:(1)A的化学式______________,理由______________________________(2)A分子中,x个氧原子呈-O-O-键状排列,每一根短线代表_________,A的电子式为____________,A分子的结构式为______________________.答案:1、A2、C3、B4、B5、B6、C7、AD8、A 9、D 10、BD 11、D 12、BD15、O3F2;1mol A分解产生了3mol O 原子,2mol F原子;在同温同压,体积比等于物质的量的比. F-O-O-O-F .。

分子结构练习20题1、下列分子中,两个相邻共价键的夹角最小的是:A、BF3B、HS2C、NH3OD、H2正确答案:B2、下列分子和离子中,中心原子成键轨道不是sp2杂化的是:-A、NO3B、HCHOC、BF3D、NH3正确答案:D3、下列化合物中,极性最大的是:A、CS2B、HS2C、SO3D、SnCl4正确答案:B4、下列分子中,偶极矩不等于零的是:A、BeCl2B、BF3C、NF3D、CO2正确答案:C5、下列液态物质中只需克服色散力就能使之沸腾的是:A、HO2B、COC、HFD、Xe正确答案:D6、下列各组离子中,离子的极化力最强的是:A、K+、Li+B、Ca2+、Mg2+C、Fe3+、Ti4+D、Sc3+、Y3+正确答案:C7、下列物质熔点变化顺序中,不正确的是:A、NaF>NaCl>NaBr>NaIB、NaCl<MgCl 2<AlCl 3<SiCl 4C、LiF>NaCl>KBr>CsID、Al 2O 3>MgO>CaO>BaO正确答案:B8、下列原子轨道的n 相同,且各有一个自旋方式相反的不成对电子,则沿X 轴方向可形成π键的是:A、P X -P XB、P X -PyC、Py-P ZD、Pz-Pz正确答案:D9、下列分子或离子中,具有反磁性的是:A、O 2B、O 2-C、O 2+D、O 22-正确答案:D10、按分子轨道理论,下列稳定性排列正确的是:A、O 2>O 2+>O 22-B、O 2+>O 2>O 22-C、O 22->O 2>O 2+D、O 2+>O 22->O 2正确答案:B11、下列分子或离子中,中心原子的价层电子对几何构型为四面体,而分子(离子)的空间构型为V 字形的是:A、NH 4+B、SO 2C、ICl 2-D、OF 2正确答案:D12、几何形状是平面三角形的分子或离子是:A、SO 3B、SO 32-C、CH 3-D、PH 3正确答案:A13、下列分子中偶极矩大于零的是:A、BF 3B、PF 3C、SiF 4D、PF 5正确答案:B14、根据VSEPR 理论,BrF 3分子的几何构型为:A、平面三角形B、三角锥形C、三角双锥形D、T 字形正确答案:D15、下列分子中,离域π键类型为П33的是:A、O 3B、SO 3C、NO 2D、HNO 3正确答案:C16、下列晶格能大小顺序中正确的是:A、CaO>KCl>MgO>NaClB、NaCl>KCl>RbCl>SrOC、MgO>RbCl>SrO>BaOD、MgO>NaCl>KCl>RbCl正确答案:D17、在下列各种含氢化合物中,有氢键的是:A、CHF 3B、C 2H 6C、C 6H 6D、HCOOHE、CH 4正确答案:D18、在石墨晶体中,层与层之间的结合力是:A、金属键B、共价键C、范德华力D、大π键正确答案:C19、下列关于O 22-和O 2-的性质的说法中,不正确的是:A、两种离子都比O 2分子稳定性小B、O 22-的键长比O 2-键长短C、O 22-是反磁性的,而O 2-是顺磁性的D、O 22-的键能比O 2-的键能小正确答案:B20、若中心原子采用sp 3d 杂化轨道成键的分子,其空间构型可能是:A、三角双锥形B、变形四面体C、直线形D、以上三种均有可能正确答案:D。

中学化学竞赛试题资源库——高分子化学A组1.下列物质一定不是天然高分子的是A 橡胶B 蛋白质C 尼龙D 纤维素2.下列物质一定不属于有机高分子的是A 树脂镜片B 维生素C 高碳钢D 不粘锅上防粘物质3.下列物质中,不属于高分子化合物的是A 生油B 棉花C 淀粉D 橡胶4.下列物质不属于高分子化合物的是A 硫化橡胶B 脂肪C 醋酸纤维D 硬脂酸钠5.相同质量的下列材料制成相同长度的绳子,能吊起的重物质量最大的是A 涤纶绳B 锦纶绳C 金属钛绳D 碳钢绳6.俗作“塑料王”的聚四氟乙烯,结构式为CF2-CF2,它不具有的性质是A 耐高温B 电绝缘性C 耐腐蚀性D 热固性7.下列高分子材料中属于线型结构的是A 有机玻璃B 硫化橡胶C 电木D 聚乙烯8.下列原料或制成的产品中,若出现破损不可以进行热修补的是A 聚氯乙烯凉鞋B 电木插座C 自行车内胎D 聚乙烯塑料膜9.下列原料或制品中,若出现破损不可以进行修补的是A 聚氯乙烯凉鞋B 电木插座C 自行车内胎D 聚乙烯塑料膜10.可用来修补和粘合有机玻璃制品的是A 乙醇B 乙酸C 丙酮D 氯仿11.天然橡胶是下列哪种物质的聚合物A B CH2=CH-CH=CH2C D12.下列关于天然橡胶的说法中,不正确的是A 能在汽油中溶胀B 天然橡胶日久后会老化,实质上发生的是氧化反应C 天然橡胶加工时要进行硫化,实质上是打开碳碳双键,形成碳硫键或双硫键D 天然橡胶是具有网状结构的高分子化合物13.下列物质中,能自身聚合成高分子化合物的是A CH3(CH2)4COOHB CH3CH(NH2)COOHC D -OH14.现有两种烯烃:CH2=CH2和CH2=CR2(R为烃基),把它们的混合物进行聚合反应后,产物中含①CH 2-CH2②CHR-CHR③CH2-CH2-CR2-CH2④CH 2-CH2-CHR-CHR⑤CH2-CR2A 只有①⑤B ②④C ①③⑤D 只有①15.有4种有机物:①②③④CH3-CH=CH-CN,其中可用于合成结构简式为的高分子材料的正确组合为A ①③④B ①②③C ①②④D ②③④16.下列高聚物不是由两种单体缩聚而成的是A BC D17.乙烯和丙烯按1︰1的物质的量比聚合,生成聚合物乙丙树脂,该聚合物的结构简式可能是A BC D18.异戊二烯和苯乙烯按1︰1比例发生加聚反应生成高聚物经结构简式可能是ABCD19.下列有机物可通过氧化、酯化、加聚三种反应制得高聚物的是A CH3CH2CH2OHB ClCH2CHClCH2OHC H2C=CHCH2OHD CH3CH(OH)CH2OH20.某有机物的结构简式为,下列叙述不正确的是A 1mol该有机物与NaOH溶液完全反应时,消耗NaOH 1molB 该有机物水解所得的产物不能发生加成反应C 该有机物可通过加聚反应生成D 该有机物分子中含有双键21.下列有关线型高分子和体型高分子的说法错误的是A 线型高分子是由许多链节相互连接成链状,通常不具有或很少具有支链,而体型高分子则是长链跟长链之间产生交联B 线型高分子通常具有热塑性,而体型高分子通常具有热固性C 线型高分子可在适当溶剂中溶解,而体型高分子通常很难在任何溶剂中溶解D 体型高分子化合物的相对分子质量一定比线型高分子化合物相对分子质量大22.写出合成下列高分子化合物的单体的结构简式:23.丁苯橡胶是由两种单体聚合而成的高分子化合物,已知它的结构简式如右图所示。

分子结构——答案1.下列分子中只含键的为()。
A、HCN;B、H2O;C、CO;D、N2;E、C2H4解答或答案:B。
2.下列化合物中分子极性最大的是()A、CCl4;B、C2H5OH;C、I2;D、H2O;E、H2S解答或答案:D3.下列化合物=0的是()A、H2O;B、NH3;C、BF3;D、CH3Cl;E、HCl解答或答案:C4.在下列分子或离子中,没有孤对电子的是()。
A、H2O;B、NH3;C、H2S;D、NH4+;E、OH-5.乙醇和水之间的作用力为()。
A、色散力;B、取向力和诱导力;C、色散力和诱导力;D、取向力、诱导力和色散力;E、除D所述之外还有氢键解答或答案:E6.惰性气体在低温下能够被液化的原因在于()。
A、单原子分子有一定的体积;B、单原子分子有一定的质量;C、单原子分子间有相互作用;D、单原子分子在低温下形成氢键;E、原子是由带正电荷的核和带负电荷的电子组成的解答或答案:C7.下列说法中正确的是()。
A、p轨道之间以“肩并肩”重叠可形成键;B、p轨道之间以“头碰头”重叠可形成键;C、s轨道和p轨道“头碰头”重叠可形成键;D、s轨道和p轨道“头碰头”重叠可形成键;E、共价键是两个原子轨道“头碰头”重叠形成解答或答案:C8.甲烷(CH4)分子中,碳原子所采用的杂化方式为()。
A、sp;B、sp2;C、sp3;D、dsp2;E、spd2解答或答案:C9.下列各分子之间仅存在着色散力的是()。
A、甲醇和水;B、溴化氢和氯化氢;C、氮气和水;D、乙醇和水;E、苯和四氯化碳解答或答案:B10.下列分子中极性最小的是()。
A、NaF;B、HF;C、HCl;D、HBr;E、HI解答或答案:E11.下列分子中存在氢键的是()。
A、HF;B、CH4;C、HI;D、CCl4;E、CO2解答或答案:A12.下列化合物中,能形成分子内氢键的是()。
A、C O O HO H;B、CH3F;C、COOHHO;D、H2O;E、PH3解答或答案:A13.NH3分子中N原子采取不等性sp3杂化,分子在空间的构型为()。

高中化学竞赛专题考试——分子结构1(路易斯结构式、共振式、VSPER 理论)1.008Zr Nb Mo T cRu Rh Pd Ag Cd In S n S b T e I Hf T a W Re OsIr Pt Au Hg T l Pb Bi Po At Ac-Lr HLi BeB C N O F Na MgAl S i P Cl S K Ca S c T i V Cr Mn Fe Co Ni Cu Zn G a G e As S e BrRb Cs Fr S r Ba RaY La Lu -6.9419.01222.9924.3139.1040.0885.4787.62132.9137.3[223][226]44.9647.8850.9452.0054.9455.8558.9363.5558.6965.3910.8126.9869.7212.0128.0972.61114.8204.4118.7207.2112.4200.6107.9197.0106.4195.1102.9192.2101.1190.298.91186.295.94183.992.91180.991.22178.588.9114.0116.0019.0030.9774.92121.8209.032.0778.96127.6[210][210][210]126.979.9035.454.00320.1839.9583.80131.3[222]He Ne Ar Kr Xe Rn 相对原子质量Rf Db Sg Bh Hs Mt一. 选择题(每题只有一个正确选项,每题2分,共50分)1. 根据鲍林近似能级图,在多电子原子中,基态时,下列电子均处于一定的能级,其中占据能级最高轨道的电子是: ( )A 2,1,1,+1/2B 3,1,1,+1/2C 3,2,1,+1/2D 4,0,0,1/2 2. 下列离子的电子构型可以用[Ar]3d 6表示的是( )A Mn 2+B Fe 3+C Co 3+D Ni 2+3.下列离子半径变小的顺序正确的是( )A F ->Na +>Mg 2+Al 3+B Na +>Mg 2+>Al 3+>F -C Al 3+>Mg 2+>Na +>F -D F ->Al 3+>Mg 2+>Na +4. 下列元素的原子中,第一电离能最大的是 ( )A BeB BC CD N5. 下列物质中,含极性键的非极性分子是()A H2OB HClC SO3D NO26. 下列分子中,没有配位键的是()A COB (BeCl2)2C CH3OBF3D N2H47. NO3—合理的共振式总数为()A 1B 2C 3D 48.下列分子中,键级等于零的是()A.O2 B. F2 C. N2 D. Ne29.原子轨道沿两核连线以“肩并肩”方式进行重叠的是()A. б键B. 氢键C. π键D. 离子键10. 下列物种中,键长最短的是( )A O2B O2+C O2—D O22—11. 下列化合物中,极性最大的是()A CS2B H2OC SO3D SnCl412. 下列物种中,既是路易斯酸,也是路易斯碱的是()ACCl4 B SOCl2 C NH2— D Hg2+13. 估计下列分子中,键角最小的是()()A NH3B PH3C AsH3D SbH314.估计下列分子或离子中,键角最小的是()A NH3B NO3—C NF3D NCl315. 几何形状是平面三角形的离子是()A SO-23 B SnCl-3C CH-3D NO-316. 下列分子或离子为平面四方构型的是()A ICl4—B ClO4—C BrF4+D SF417. 下列分子或离子中,属于三角锥构型的是()A BCl3B H3O+C BrF3D CH+318. 下列化合物中,可能含有卤桥键的是()A SnCl4B BeCl2C CCl4D NCl319. IF5是共价化合物,但液态IF5是电的良导体,原因是IF5二聚后电离,得到各带一个单位正负电荷的阴阳离子,则在该液体中存在的阳离子的几何构型是()A 三角双锥B 四方锥C 平面四方D 变形四面体20 下列哪一个分子的空间构型为折线型()A N3—B I3—C SO32—D CO32—21.下列分子中,偶极矩不为零的是()A BeCl2B BF3C NF3D CH422. 下列分子或离子中,键角最大的是()A XeF2B NCl3C CO-23 D PCl+423 通过测定AB2型分子的偶极距,能够判断:()A分子的空间构型 B 两元素的电负性之差C A—B键的极性D A—B键的键长24. 下列分子中含有两个不同键长的是()A CO2B SO3C SF4D XeF425. 下列分子中,最不容易聚合的是()A N2O5B BeCl2C AlCl3D NO2二、填空题(共50分)26.(10分)指出下列分子中有几个σ键和π键数目。

中学化学竞赛试题——化学键和分子结构班级:姓名:座号:1.有一种多聚硼酸盐为无限网状结构(如右图):其结构的基本单元可表示为(B5On)m-,则m=、n=。
2.叠氮化合物在化学工业上有其重要应用。
N3-叫做叠氮离子,请写出由三个原子构成的含有同N3-相同电子数的微粒的化学式(三种)。
3.下列分子结构图中的大黑点表示原子序数小于10的元素的“原子实”(指原子除去最外层电子的剩余部分),小黑点表示没形成共价键的最外层电子,短线表示共价键。
其中分子结构图与化学式关系错误的是A (NH 3)B(HCN)C (C3H4O)D (BF3)4.根据热化学方程式:S(s)+O2(g)=SO2(g)△H=-297.23kJ。
分析下列说法中正确的是A S(g)+O2(g)=SO2(g),△H=-Q,Q值大于297.23kJB S(s)+O2(g)=SO2(s),△H=-Q,Q值小于297.23kJC 1mol SO2的键能总和大于1mol S和1mol O2的键能之和D 1mol SO2的键能总和小于1mol S和1mol O2的健能之和5.三硫化四碳分子的结构研究表明,该分子中没有不饱和键,且各原子的最外层均已达到了八个电子的结构。
在一个三硫化四磷分子中含有的共价键个数是A 7个B 9个C 19个D 不能确定6.已知[Co(NH3)6]3+呈正八面体结构:各NH3分子间距相等,Co3+位于正八面的中心。
若其中二个NH3分子被Cl-取代,所形成的[Co(NH2)4Cl2]+的同分异构体的种数有A 2种B 3种C 4种D 5种7.SF6是一种无色气体,具有很强的稳定性,可用于灭火。
SF6的分子结构如图3-3所示,呈正八面体型。
如果F元素有两种稳定的同位素,则SF6的不同分子种数为A 6种B 7种C 10种D 12种8.某共价化合物含碳、氢、氮三种元素,分子内有四个氮原子,且四个氮原子排列成内空的四面体(如白磷结构),每两个氮原子间都有一个碳原子。


高中化学奥林匹克竞赛辅导分子结构-2009-2019年全国初赛真题2019第7题1960年代,稀有气体化合物的合成是化学的重要突破之一。
Barlett从O2+[PtF6]-的生成得到启发,推测可以形成Xe+[PtF6]-。
于是尝试通过Xe和PtF6反应合成相应的稀有气体化合物,这一工作具有深远的意义。
7-1.后续研究发现,Barlett当时得到的并非Xe+[PtF6]-,而可能是XeF+Pt2F11-。
7-1-1.写出XeF+Pt2F11-中Xe的氧化态。
7-1-2.在Pt2F11-结构中,沿轴向有四次轴,画出Pt2F11-的结构。
7-2.后来,大量含Xe-F和Xe-O键的化合物被合成出来,如XeOF2。
根据价层电子对互斥理论(VSEPR),写出XeOF2的几何构型及中心原子所用的杂化轨道类型。
7-3.1974年合成了第一例含Xe-N键的化合物:XeF2和HN(SO2F)2在0℃的二氯二氟甲烷溶剂中按1:1的计量关系反应,放出HF,得到白色固体A。
A受热到70℃分解,A中的Xe一半以Xe气放出,其他两种产物与Xe具有相同的计量系数且其中一种是常见的氙的氟化物。
写出A的化学式及其分解的反应方程式。
7-4.1989年,随着超高压下Xe单质固体由立方密堆积变为六方密堆积结构并显示出金属性,Xe 的惰性帽子被彻底摘掉。
理论预测,高压下Xe可以参与形成更复杂的化合物,如Cs℃Xe℃Au3。
若Cs℃Xe℃Au3采用钙钛矿类型的结构,分别写出Cs℃和Xe℃最近邻的金的原子数。
解:2018第2题2-1.195K,三氧化二磷在二氯甲烷中与臭氧反应生成P4O18,画出P4O18分子的结构示意图。
2-2.CH2SF4是一种极性溶剂,其分子几何构型符合价层电子对互斥理论(VSEPR)模型。
画出CH2SF4的分子结构示意图(体现合理的成键及角度关系)。
2-3.2018年足球世界比赛用球使用了生物基元三元乙丙橡胶(EPDM)产品Keltan Eco。

奥赛真题《结构化学》精析第一题(1999年初赛第三题12分)铬的化学丰富多采,实验结果常出人意料。
将过量30% H 2O 2加入(NH 4)2CrO 4的氨水溶液, 热至50o C 后冷至0o C ,析出暗棕红色晶体A 。
元素分析报告:A 含Cr 31.1%,N 25.1%,H 5.4%。
在极性溶剂中A 不导电。
红外图谱证实A 有N-H 键,且与游离氨分子键能相差不太大,还证实A 中的铬原子周围有7个配位原子提供孤对电子与铬原子形成配位键,呈五角双锥构型。
3-1 以上信息表明A 的化学式为: ;可能的结构式为: 。
3-2 A 中铬的氧化数为: 。
3-3 预期A 最特征的化学性质为: 。
3-4 生成晶体A 的反应是氧化还原反应,方程式是: 。
【解析】此题是利用已经形成的但一般教科书未涉及的知识编制成的探究式试题。
如本文开头所述,属于谜底为新知识的谜语式试题。
此题信息很多,为缕清信息相互关系,最形象的方法是制作一张破案式的线索图,下面只是一例(制作什么样的图并无模式可循,依应试者思维特征不同而异,图也不一定在纸上画出来,在脑中构建也一样可以——这要看应试者脑子清晰不清晰,右脑发达不发达而定):从这个“破案线索图”可以判断出“犯案人”A 只能是含2个过氧团的铬(IV)配合物。
因为过氧团可以从过氧化氢中转移过来,有来源(如果此题没有A 的生成反应的信息,当然也可以假设配合物里存在H 2N —NH 2,同时有—OH 的配体,但生成反应排除了这个“嫌疑犯”);同时也排除1个过氧团或者没有过氧团的可能,因为生成反应是氧化还原反应,在K 2CrO 4中铬的价态(或说氧化态)已经达到最高价,只能发生还原反应,铬的价态必低于+6,因此A 是唯一的。
【解析】3-1 A 的化学式Cr(NH 3)3 O 4 或CrN 3H 9O 4(写成其他形式也可以) (2分)A 的可能结构式如下图: (4分)333and/or1式和/或2式均得满分,但无2个过氧键O —O 者得零分。
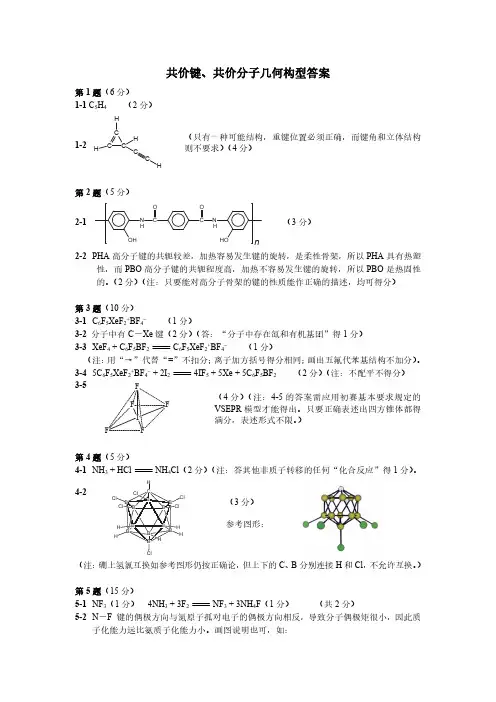
共价键、共价分子几何构型答案第1题(6分)1-1C 5H 4(2分)1-2C CCCCH H HH(只有一种可能结构,重键位置必须正确,而键角和立体结构则不要求)(4分)第2题(5分)2-1NCOHN CHOOO HH n(3分)2-2PHA 高分子键的共轭较差,加热容易发生键的旋转,是柔性骨架,所以PHA 具有热塑性,而PBO 高分子键的共轭程度高,加热不容易发生键的旋转,所以PBO 是热固性的。
(2分)(注:只要能对高分子骨架的键的性质能作正确的描述,均可得分)第3题(10分)3-1C 6F 5XeF 2+BF 4-(1分)3-2分子中有C -Xe 键(2分)(答:“分子中存在氙和有机基团”得1分)3-3XeF 4+C 6F 5BF 2C 6F 5XeF 2+BF 4-(1分)(注:用“→”代替“=”不扣分;离子加方括号得分相同;画出五氟代苯基结构不加分)。
3-45C 6F 5XeF 2+BF 4-+2I 24IF 5+5Xe +5C 6F 5BF 2(2分)(注:不配平不得分)3-5(4分)(注:4-5的答案需应用初赛基本要求规定的VSEPR 模型才能得出。
只要正确表述出四方锥体都得满分,表述形式不限。
)第4题(5分)4-1NH 3+HCl NH 4Cl (2分)(注:答其他非质子转移的任何“化合反应”得1分)。
4-2B CCl H(3分)参考图形:(注:硼上氢氯互换如参考图形仍按正确论,但上下的C 、B 分别连接H 和Cl ,不允许互换。
)第5题(15分)5-1NF 3(1分)4NH 3+3F 2NF 3+3NH 4F (1分)(共2分)5-2N -F 键的偶极方向与氮原子孤对电子的偶极方向相反,导致分子偶极矩很小,因此质子化能力远比氨质子化能力小。
画图说明也可,如:(1分)5-32NF3+2Hg N2F2+2HgF2(1分)trans cis(14+19)⨯2=66(每式1分,共3分)5-4D:[N N-F]+E:F:(每式1分)2N2F2+SnF4[N2F+]2[SnF6]2-(1分)[N2F+]2[SnF6]2-[N2F]+[SnF5]-+N2F2(1分)(共5分)5-5阳离子的化学式为NF4+(1分)NF3+F2+BF3NF4+BF4-(1分)NF4+水解反应首先得到HOF(否则写不出配平的NF4+水解反应):NF4++H2O NF3+HOF+H+定量生成NF3(1分)而反应2HOF2HF+O2和反应HOF+H2O HF+H2O2哪一反应为主与反应条件有关,但无论哪一反应为主却总是定量生成HF。

中学化学竞赛试题资源库——分子的结构A组1.下列分子中所有原子都满足最外层为8电子结构的是A BeCl2B PCl3C PCl5D N2O2.下列分子结构中各原子的最外层电子都满足8电子稳定结构的是A SF6B XeF2C CS2D CH43.下列分子中,所有原子的最外层均为8电子结的是A BeCl2B H2SC NCl3D SF64.下列分子中所有原子都满足最外层为8电子结构的是A SiCl4B H2OC BF3D PCl55.下列分子中,所有原子都满足最外层为8电子结构的是A BF3B PCl5C HClD CF2Cl26.下列各分子中所有原子都满足最外层为8电子结构的是A C2H4B BeCl2C PCl5D CCl47.下列各分子中,所有原子都满足最外层为8电子结构的是A H2OB BF3C CCl4D PCl58.下列分子中所有的原子都满足最外层8电子结构的是A 次氯酸B 二氟化硫C 三氟化硼D 氯化硫(S2Cl2)9.下列温室气体中,和CO2一样,既是非极性分子,所有的原子又都达到8电子稳定结构的是A N2OB CF2=CF2C CCl2F2D SF610.下列微粒中碳原子都满足最外层为8电子结构的是A 甲基(—CH3)B 碳正离子(CH3+)C 碳负离子(CH3-)D 碳烯(∶CH2)11.下列分子中所有原子都满足最外层8电子结构的是A 六氟化氙(XeF6)B 次氯酸(HClO)C 二硫化碳(CS2)D 三氟化硼(BF3)12.六氧化四磷的分子结构中只含有单键,且每个原子的最外层都满足8电子结构,则该分子中含有的共价键的数目是A 10B 12C 24D 2813.具有极性键的非极性分子是A CS2B H2SC Cl2D NH314.下列分子中,具有极性键而不是极性分子的是A H2OB HFC COD CO215.下列分子有极性的是A CH≡CHBC CH3ClD N216.只含极性键的非极性分子是①BF3(平面正三角型分子)②CCl4(正四面体型分子)③NH3④H2O ⑤CH3Cl ⑥CS2A ①②⑥B ①②⑤C ②⑤③D ①②③17.下列物质:①干冰,②石英,③白磷,④氯仿,⑤过氧化钠。
2022届高一化学竞赛习题:分子结构1在已有的原子中,当基态原子的第7电子层只有2个电子时,它的第6层电子数( A •肯定是8个电子C . 8〜18个电子 2 •形成HCI 分子时原子轨道重叠是(C . s —p x 重叠3. 下列分子中键有极性,分子也有极性的是(4. 下列气态卤化氢中,分子偶极矩由大到小的顺序是(5. 下列分子中偶极矩不等于零的是(6. 下列分子中几何构型为三角形的是(7. 下列哪一个化合物具有直线形分子构型&用价层电子对互斥理论判断下列分子或离子的几何形状为三角锥的是(9.用价层电子对互斥理论判断下列分子或离子的几何形状为三角双锥的是( )10 .下列分子中含有两个不同键长的是() A . CO 2B . SO 3C . SF 4D . XeF 4o II11 .在…分子中,四个原子处在同一个平面上, C 原子采用的杂化轨道是 (A . spB . sp 2C . sp 3D .其它杂化形式12. sp 3杂化可以用于描述哪一种分子中共价键的形成( A . H 2OB . NH 3C . CH 4D .三种分子都可以]2 313 .叠氮酸的结构式是.£—:.■—?■, 1> 2、3号氮原子采用的杂化轨道类型是( )II姓名班级 学号B . 18个电子 D . 18+ 2个电子 A . s — s 重叠 B . p y — p y 重叠P x —p x 重叠 A . CCI 4B . COC . BF 3D . PCI 5A . HCI 、HBr 、HI 、HF HF 、 HCI 、HBr 、 HI C . HI 、HBr 、HCI 、HFHCI 、HBr 、HF 、 HIA . BeCl 2B . BCI 3C . CO 2D . NH 3A . CIF 3B . BF 3C . NH 3D . PCI 3A . OF 2B . O 3C . ICI 2D . NO 2A . SO 3B . SO 32「C . NO 3D . CH 3+A . SeF 6B . A S F 5C . XeOF 4D . PbCl 4A . sp3、sp、sp B. sp2、sp、sp C. sp3、sp、sp2D. sp2、sp、sp214. (2010北京市赛)1998年美国科学家合成出具有极强爆炸力的“N5 ”,已知它是带电荷的呈V形构型,5个氮原子最外层都满足8电子结构,且含2个N-N,可将其视为“ N ? ”,则n值为()A . 1 B. 2 C . 3 D . 415 •如果已经发现167号元素A ,若已知的原子结构规律不变。
高三化学分子结构和性质试题答案及解析1.近年来,科学家合成了一种稳定的氢铝化合物Al2H6。
Al2H6的球棍模型如下图所示,它的熔点为150℃,可用作高能燃料或储氢材料。
下列说法正确的是 ( )A.Al2H6可以燃烧,产物为氧化铝和水B.1mol Al2H6中约含有4.8×1024个σ键C.60g Al2H6中含铝原子约为1.2×1023个D.Al2H6在固态时所形成的晶体是离子晶体【答案】A【解析】A. 氢铝化合物Al2H6燃烧,其中Al变为Al2O3,H变为H2O。
因此燃烧产物为氧化铝和水。
正确。
B、在Al2H6中Al化合价为+3价,H为-1价,每1mol Al2H6中含有6mol的Al—H键。
即含3.6×1024个σ键.错误。
C、Al2H6的式量为60,所以60g Al2H6的物质的量为1mol。
含铝原子约为1.2×1024个.错误。
D、根据Al2H6的熔点为150℃可确定在固态时所形成的晶体是分子晶体。
离子晶体熔化要克服离子键,键能大,熔点高。
错误。
【考点】考查氢铝化合物Al2H6的结构与性质的关系的知识。
2.纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。
单位质量的A和B单质燃烧时均放出大量热,可用作燃料。
已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:(1)某同学根据上述信息,推断B的核外电子排布如图所示,该同学所画的电子排布图违背了。
(2)ACl2分子中A的杂化类型为。
(3)我国部分城市雾霾天占全年一半,引起雾霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等,其中SO42-的空间构型是 (用文字描述),与NO3-互为等电子体的分子是。
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。
写出基态钾原子的价电子排布式,该物质的K原子和C60分子的个数比为。
DNA分子结构练习题一、单选题1、下列哪一项不是DNA的基本组成单位?A.核糖核酸B.脱氧核糖核酸C.磷酸和脱氧核糖交替连接的化合物D.碱基、脱氧核糖和磷酸组成的化合物正确答案:A.核糖核酸。
2、下列哪一项不是DNA分子结构的特点?A.由两条反向平行的多核苷酸链组成B.脱氧核糖和磷酸交替连接形成的基本骨架位于双链的外侧C.碱基之间以氢键连接,形成了碱基对D.两股链之间的横桥连接形成了双螺旋结构正确答案:D.两股链之间的横桥连接形成了双螺旋结构。
1、DNA分子结构中,哪些部分组成了双链?A.两条反向平行的多核苷酸链B.脱氧核糖和磷酸交替连接形成的基本骨架C.碱基之间以氢键连接,形成了碱基对D.两股链之间的横桥连接形成了双螺旋结构正确答案:A.两条反向平行的多核苷酸链和C.碱基之间以氢键连接,形成了碱基对。
2、DNA分子结构中,哪些部分构成了基本骨架?A.脱氧核糖和磷酸交替连接形成的基本骨架位于双链的内侧B.脱氧核糖和磷酸交替连接形成的基本骨架位于双链的外侧C.碱基、脱氧核糖和磷酸组成的化合物构成了基本骨架正确答案:B.脱氧核糖和磷酸交替连接形成的基本骨架位于双链的外侧和C.碱基、脱氧核糖和磷酸组成的化合物构成了基本骨架。
1、DNA分子结构中,两股链之间的横桥连接形成了双螺旋结构。
()错误。
DNA分子结构中,两股链之间通过互补配对原则形成碱基对,且双螺旋结构是由脱氧核糖和磷酸交替连接形成的基本骨架在外侧构成的。
2、DNA分子结构中,碱基排列顺序的千变万化构成了DNA分子的多样性。
()正确。
碱基排列顺序的千变万化是DNA分子多样性的原因之一。
DNA分子复制练习题一、选择题1、在DNA复制过程中,下列哪一项不是必须的?A.解旋酶B. DNA聚合酶C.引物D.螺旋酶正确答案是:D.螺旋酶。
在DNA复制过程中,螺旋酶不是必须的,因为DNA双螺旋结构在高温下会自动打开,不需要螺旋酶来破坏双螺旋结构。
2、下列哪一种酶不是参与DNA复制的?A. DNA聚合酶B.解旋酶C.引物酶D.连接酶正确答案是:D.连接酶。
中学化学竞赛试题资源库——分子的结构A组1.下列分子中所有原子都满足最外层为8电子结构的是A BeCl2B PCl3C PCl5D N2O2.下列分子结构中各原子的最外层电子都满足8电子稳定结构的是A SF6B XeF2C CS2D CH43.下列分子中,所有原子的最外层均为8电子结的是A BeCl2B H2SC NCl3D SF64.下列分子中所有原子都满足最外层为8电子结构的是A SiCl4B H2OC BF3D PCl55.下列分子中,所有原子都满足最外层为8电子结构的是A BF3B PCl5C HClD CF2Cl26.下列各分子中所有原子都满足最外层为8电子结构的是A C2H4B BeCl2C PCl5D CCl47.下列各分子中,所有原子都满足最外层为8电子结构的是A H2OB BF3C CCl4D PCl58.下列分子中所有的原子都满足最外层8电子结构的是A 次氯酸B 二氟化硫C 三氟化硼D 氯化硫(S2Cl2)9.下列温室气体中,和CO2一样,既是非极性分子,所有的原子又都达到8电子稳定结构的是A N2OB CF2=CF2C CCl2F2D SF610.下列微粒中碳原子都满足最外层为8电子结构的是A 甲基(—CH3)B 碳正离子(CH3+)C 碳负离子(CH3-)D 碳烯(∶CH2)11.下列分子中所有原子都满足最外层8电子结构的是A 六氟化氙(XeF6)B 次氯酸(HClO)C 二硫化碳(CS2)D 三氟化硼(BF3)12.六氧化四磷的分子结构中只含有单键,且每个原子的最外层都满足8电子结构,则该分子中含有的共价键的数目是A 10B 12C 24D 2813.具有极性键的非极性分子是A CS2B H2SC Cl2D NH314.下列分子中,具有极性键而不是极性分子的是A H2OB HFC COD CO215.下列分子有极性的是A CH≡CHBC CH3ClD N216.只含极性键的非极性分子是①BF3(平面正三角型分子)②CCl4(正四面体型分子)③NH3④H2O ⑤CH3Cl ⑥CS2A ①②⑥B ①②⑤C ②⑤③D ①②③17.下列物质:①干冰,②石英,③白磷,④氯仿,⑤过氧化钠。
高三化学分子结构和性质试题答案及解析1.下表为周期表的一部分,其中的编号代表对应的元素。
试填空。
(1)写出上表中元素I的基态原子的电子排布式和价层电子排布图:。
元素C、D、E、F的第一电离能由大到小的顺序是 (用元素符号表示)。
(2)元素A分别与C、D、E形成最简单的常见化合物分子甲、乙和丙。
下列有关叙述不正确的有。
A.甲、乙和丙分子的空间构型分别为正四面体形、三角锥形、V形B.甲、乙和丙分子中,中心原子均采取sp3的杂化方式C.三种分子中键角由大到小的顺序是丙>乙>甲D.甲、乙和丙分子均为由极性键构成的极性分子(3)由元素J、C、E组成一种化学式为J(CE)5的配位化合物,该物质常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂。
据此可判断:①该化合物的晶体类型为。
②该化合物的晶体中存在的作用力有。
A.离子键B.极性键C.非极性键D.范德华力E.氢键F.配位键③根据共价键理论和等电子体理论分析,CE分子中σ键与π键的数目比为。
(4)在测定A与F形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是。
(5)某些不同族元素的性质也有一定的相似性,如表中元素G与元素B,原因是。
【答案】(1)1s22s22p63s23p63d54s1(或[Ar]3d54s1) F>N>O>C(2)CD(3)①分子晶体②BDF③1∶2(4)氟化氢气体中存在因氢键而相互缔合形成的缔合分子(HF)n(5)Be与Al在元素周期表中位于对角线的位置【解析】根据这几种元素在周期表中的位置推知:A为H(氢),B为Be,C为C(碳),D为N,E 为O,F为F(氟),G为Al,H为Cl,I为Cr,J为Fe,(1)Cr元素基态原子的电子排布式为1s22s22p63s23p63d54s1或[Ar]3d54s1,其价层电子排布图为,一般来说,同周期元素从左到右第一电离能逐渐增大,但N元素原子2p轨道上电子达到半充满,故其第一电离能要大于O的第一电离能,因此这四种元素的第一电离能由大到小的顺序为F(氟)>N>O>C(碳)。
共价键、共价分子几何构型(全国初赛)第1题(6分)1999年合成了一种新化合物,本题用X 为代号。
用现代物理方法测得X 的相对分子质量为64;X 含碳93.8%,含氢6.2%;X 分子中有3种化学环境不同的氢原子和4种化学环境不同的碳原子;X 分子中同时存在C -C 、C =C 和C C 三种键,并发现其C =C 键比寻常的C =C 短。
(2000年第3题)1-1X 的分子式是____。
1-2请将X 的可能结构式画在下面的方框内。
第2题(5分)据统计,40%的飞机失事时机舱内壁和座椅的塑料会着火冒烟,导致舱内人员窒息致死。
为此,寻找装修机舱的阻燃聚合物是化学研究的热点之一。
最近,有人合成了一种叫PHA 的聚酰胺类高分子,即主链内有“酰胺键”(-CO -NH -)。
温度达180~200℃时,PHA 就会释放水变成PBO (结构式如右图所示),后者着火点高达600℃,使舱内人员逃离机舱的时间比通常增大10倍。
该发明创造的巧妙之处还在于,PHA 是热塑性的(加热后可任意成型),而PBO 却十分坚硬,是热固性的(加热不能改变形状)。
(2000年第10题)2-1写出PHA 的结构式。
2-2根据高分子结构来解释,为什么PHA 有热塑性而PBO 却是热固性的。
第3题(10分)去年报道了在-55℃条件下,由XeF 4(A)和C 6F 5BF 2(B)化合,得到一离子化合物(C),测得其中Xe 的质量分数为31%,阴离子为四氟硼酸根离子,阳离子结构中有(B)的苯环。
(C)是首例有机氙(IV)化合物,在-20℃以下稳定,是强氟化剂和强氧化剂,如与碘反应得到五氟化碘,放出氙,同时得到(B)。
(2001年第4题)3-1写出(C)的化学式,正负离子应分开写。
3-2根据什么结构特征可以把(C)归为有机氙化合物?3-3写出合成(C)的反应方程式。
3-4写出(C)和碘的反应。
3-5画出五氟化碘分子的立体结构。
第4题(5分)最近有人用称为“超酸”的化合物H (CB 11H 6Cl 6)和C 60反应,使C 60获得一个质子,得到一种新型离子化合物[HC 60]+[CB 11H 6Cl 6]-。
高中化学竞赛专题考试——分子结构1 (路易斯结构式、共振式、VSPER 理
论)
1.008
Zr Nb Mo T c
Ru Rh Pd Ag Cd In S n S b T e I Hf T a W Re Os
Ir Pt Au Hg T l Pb Bi Po At Ac-Lr H
Li Be
B C N O F Na Mg
Al S i P Cl S K Ca S c T i V Cr Mn Fe Co Ni Cu Zn G a G e As S e Br
Rb Cs Fr S r Ba Ra
Y La Lu -6.9419.01222.9924.3139.1040.0885.4787.62132.9137.3[223][226]44.9647.8850.9452.0054.9455.8558.9363.5558.6965.3910.8126.9869.7212.0128.0972.61114.8204.4118.7207.2112.4200.6107.9197.0106.4195.1102.9192.2101.1190.298.91186.295.94183.992.91180.991.22178.588.9114.0116.0019.0030.9774.92121.8209.032.07
78.96127.6[210][210]
[210]126.979.9035.454.003
20.18
39.9583.80
131.3
[222]He Ne Ar Kr Xe Rn 相对原子质量
Rf Db Sg Bh Hs Mt
一. 选择题(每题只有一个正确选项,每题2分,共50分)
1、 根据鲍林近似能级图,在多电子原子中,基态时,下列电子均处于一定得能级,其中占据能级最高轨道得电子就是: ( )A 2,1,1,+1/2 B 3,1,1,+1/2 C 3,2,1,+1/2 D 4,0,0,1/2
2、 下列离子得电子构型可以用[Ar]3d 6
表示得就是 ( )A Mn 2+ B Fe 3+ C Co 3+ D Ni 2+
3. 下列离子半径变小得顺序正确得就是 ( )A F ->Na +>Mg 2+Al 3+ B Na +>Mg 2+>Al 3+>F - C Al 3+>Mg 2+>Na +>F - D F ->Al 3+>Mg 2+>Na +
4、 下列元素得原子中,第一电离能最大得就是 ( )A Be B B C C D N
5、 下列物质中,含极性键得非极性分子就是 ( ) A H 2O B HCl C SO 3 D NO 2
6、 下列分子中,没有配位键得就是 ( ) A CO B (BeCl 2)2 C CH 3OBF 3 D N 2H 4
7、 NO 3—
合理得共振式总数为 ( )A 1 B 2 C 3 D 48.下列分子中,键级等于零得就是 ( )A.O 2 B 、 F 2 C 、 N 2 D 、 Ne 2
9.原子轨道沿两核连线以“肩并肩”方式进行重叠得就是
( )A 、 б键 B 、 氢键 C 、 π键 D 、 离子键
10、下列物种中,键长最短得就是( )
A O2
B O2+
C O2—
D O22—
11、下列化合物中,极性最大得就是( )
A CS2
B H2O
C SO3
D SnCl4
12、下列物种中,既就是路易斯酸,也就是路易斯碱得就是( )
ACCl4 B SOCl2 C NH2— D Hg2+
13、估计下列分子中,键角最小得就是 ( ) ( )
A NH3
B PH3
C AsH3
D SbH3
14.估计下列分子或离子中,键角最小得就是( )
A NH3
B NO3—
C NF3
D NCl3
15、几何形状就是平面三角形得离子就是( )
A SO-2
3 B SnCl-
3
C CH-
3
D NO-
3
16、下列分子或离子为平面四方构型得就是( )
A ICl4—
B ClO4—
C BrF4+
D SF4
17、下列分子或离子中,属于三角锥构型得就是( )
A BCl3
B H3O+
C BrF3
D CH+
3
18、下列化合物中,可能含有卤桥键得就是( )
A SnCl4
B BeCl2
C CCl4
D NCl3
19、 IF5就是共价化合物,但液态IF5就是电得良导体,原因就是IF5二聚后电离,得到各带一个单位正负电荷得阴阳离子,则在该液体中存在得阳离子得几何构型就是( )
A 三角双锥
B 四方锥
C 平面四方
D 变形四面体
20 下列哪一个分子得空间构型为折线型 ( )
A N3—
B I3—
C SO32—
D CO32—
21.下列分子中,偶极矩不为零得就是 ( )
A BeCl2
B BF3
C NF3
D CH4
22、下列分子或离子中,键角最大得就是 ( )
A XeF2
B NCl3
C CO-2
3 D PCl+
4
23 通过测定AB2型分子得偶极距,能够判断: ( )
A分子得空间构型 B 两元素得电负性之差
C A—B键得极性
D A—B键得键长
24、下列分子中含有两个不同键长得就是( )
A CO2
B SO3
C SF4
D XeF4
25、下列分子中,最不容易聚合得就是( )
A N2O5
B BeCl2
C AlCl3
D NO2
二、填空题 (共50分)
26.(10
27.(10分)写出下列物质得Lewis结构(若有多种共振式,请规范写出,注明形式电荷):
28.(20分)填写下列表格
XeO4
29.(12分) 在极性分子中,正电荷重心同负电荷重心间得距离称偶极长,通常用d表示。
极性分子得极性强弱同偶极长与正(或负)电荷重心得电量(q)有关,一般用偶极矩(μ)来衡量。
分子得偶极矩定义为偶极长与偶极上一端电荷电量得乘积,即μ=d·q。
试回答以下问题:
(1)HCl、CS2、H2S、SO2 4种分子中μ=0得就是 ;
(2)实验测得:μPF3=1、03德拜、μBCl3=0德拜。
由此可知,PF3分子就是构型,BC13分子就
是构型。
(3)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3与Cl分别处在四边形得4个角上。
已知该化合物有两种异构体,棕黄色者μ>0,淡黄色者μ=0。
试画出两种异构体得构型图,并比较在水中得溶解度。
构型图:
淡黄色 ,棕黄色 ;
在水中溶解度较大得就是。
29、(1)CS2 (2)三角锥形 (3)平面三角形
(4) ; ;棕黄色者
30.(4分)NCl5能否稳定存在? 并简述理由。
30.NCl5不能稳定存在。
因为N属于第二周期元素,其可以稳定存在得化合物得最大配位数就是4。
31.(6分)(1)画出NH3与NF3分子得空间构型,并用σ+与σ-表示出键得极性。
(2)比较这两个分子极性大小并说明原因。
31、(1) (2)NF3分子得极性比NH3分子得极性小。
在这两个分子中,都有一个sp3杂化
轨道为N原子得一对孤对电子所占据。
对NF3来说,N-F键得极性较大,而且偶极矩指向F原子,而N原子中由于孤对电子产生得偶极矩就是指向孤对电子,方向正好与N-F键产生得偶极矩相反,抵消了N-F键产生得偶极矩,所以N-F分子得极性较小;对于NH3来说,N-H键产生得偶极矩指向N原子,与N原子中由孤对电子产生得偶极矩得方向相同,使N-H键得极性加强,所以NH3分子得极性大。
32.(8分)在地球得电离层中,可能存在下列离子:ArCl+、OF+、NO+、PS+、SCl+。
分析这些微粒得键级,进而预测哪种离子最稳定,哪种离子最不稳定。
写成分析过程。
32、ArCl+、OF+、NO+、PS+、SCl+分子离子得杂化及成键形式、键级、成键轨道得周期数得关系列于下表中:
杂化态键得性质键级成键轨道得周期数
ArCl+sp3 σ 1 4~3
2 2~2
OF+sp2 1σ+1∏2
2
由键级可知,NO+、PS+稳定,AlCl+不稳定。
由于NO+成键轨道为2p与2s,形成得键比PS+用3p与3s 成键更稳定,所以NO+最稳定。
提示:本题主要考查键级对分子或离于稳定性得影响。
一般来说,键级越大,分子越稳定。
相同键级得分子则瞧成键轨道得能级大小,能级越低、成键越稳定。