第十六章 有机化学糖类
- 格式:ppt
- 大小:13.83 MB
- 文档页数:55
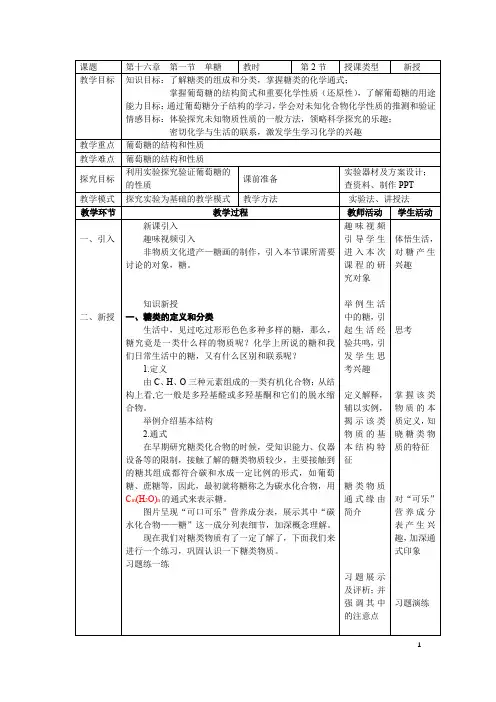
基于选项C提示注意点:注意:1、有些糖不符合通式,如:鼠李糖(C6H12O5);2、有些符合通式的却不属于糖类,例如:甲醛(CH2O)、乙酸(C2H4O2)基于选项D,那该类物质如何分类呢?3.分类下面我们进入本次课的重点,认识并学习一下最简单的糖。
二、单糖(一)重要的单糖自然界分布最广的单糖:葡萄糖和果糖,存在来源简介;●物理性质(样品呈现,认识葡萄糖)观察样品,归纳葡萄糖物理性质,呈现糖类相对甜度表,了解单糖的甜度。
●分子结构分子式:C6H12O6结构简式:(葡萄糖结构简式略)乙醛糖(果糖结构简式略)己酮糖两种单糖,葡萄糖的性质更为丰富和重要,因此本节单糖我们以葡萄糖的学习为主,那葡萄糖的结构中都有哪些基团呢?可能的性质有哪些呢?(二)葡萄糖的化学性质1.氧化反应有机物多数可以燃烧,葡萄糖也是可以的,完全燃烧可转化为CO2和H2O,化学方程式展示。
C6H12O6 + 6O2→6CO2 + 6H2O葡萄糖注意:书写化学方程式时,若以分子式表示糖类物质,需在糖分子下标注糖的名称,以免混淆。
生命体内,1mol葡萄糖约可以释放出2804kJ的能量2.与碱性弱氧化剂的反应(1)与银氨溶液反应呈现实验步骤,提问过程中银氨溶液配制时的现象变化。
观察实验现象,记录反应方程式CH2OH(CHOH)4CHO+2Ag(NH3)2OH→CH2OH(CHOH)4COONH4+2Ag↓+3NH3 +H2O(2)与新制Cu(OH)2反应呈现实验步骤,观察实验现象CH2OH(CHOH)4CHO+2Cu(OH)2+ NaOH→CH2OH(CHOH)4COONa + Cu2O↓ + 3H2O还原糖定义:可以被碱性弱氧化剂氧化的糖。
注意:果糖虽然是酮糖,但也可以被碱性弱氧化剂氧化,也是还原糖。
上述均是发生的氧化反应,那和氧化相对应的是什么反应呢?葡萄糖可以被还原吗?3.加成反应葡萄糖分子在一定条件下,可以被还原为己六醇。
那么果糖可以被还原吗?习题练一练练习2对应的是醛基的性质,练习3对应的是羟基和羧基的性质,因为葡萄糖结构中存在羟基,同样可以发生酯化反应。









有机化学糖类《有机化学糖类》嗨,同学们!今天咱们来唠唠有机化学里的糖类,这糖类啊,可和咱们的生活息息相关,像咱们吃的米饭、馒头里都有糖类呢。
不过咱化学课上得从化学的角度来认识它们,这就离不开糖类的化学式啦。
首先呢,咱得知道啥是化学式。
化学式就像是糖类的身份证,能告诉咱们它是由哪些原子组成的,以及这些原子是怎么排列组合的。
这原子之间的组合可不像把一堆小球随便堆在一起,它们是靠化学键连接起来的。
化学键呢,就好比原子之间的小钩子。
这里面有不同类型的小钩子哦。
比如说离子键,大家可以想象带正电和带负电的原子就像超强磁铁一样,正电的和负电的相互吸引就紧紧地吸在一起了,这就是离子键。
而共价键呢,就是原子们共用小钩子连接起来的。
咱们先来说说葡萄糖,葡萄糖的化学式是C₆H₁₂O₆。
这里面的碳(C)、氢(H)、氧(O)原子就是通过共价键连接起来的。
这就好比盖房子,碳原子、氢原子和氧原子就是不同的建筑材料,共价键就是把这些材料连接在一起的钉子或者胶水。
那它们为啥要这样连接呢?这就和原子的结构有关系啦,每个原子都想让自己的最外层电子达到稳定状态,就像咱们人都想让自己处于舒服的状态一样。
通过共价键共用电子,它们就能达到这个目的啦。
那在糖类里啊,还涉及到分子的极性这个概念。
这分子的极性呢,就类似小磁针。
比如说水,水是极性分子,氧原子这一端就像磁针的南极,带负电,氢原子那一端就像北极,带正电。
这就使得水有很多特殊的性质,像能溶解很多极性物质。
而糖类分子里有些部分也有极性,这就影响了它们在生物体里的功能和一些化学性质。
那像二氧化碳(CO₂)呢,它是直线对称的分子,就像一个两边一样重的跷跷板,它是非极性分子。
咱再来说说糖类里涉及到的氧化还原反应。
这个氧化还原反应就像是原子之间的一场交易。
比如说在生物体内,葡萄糖的氧化反应,就像是葡萄糖分子把自己的电子给了其他分子。
就好比你有一些小玩具(电子),然后你把这些小玩具送给了别的小伙伴。

有机化学基础知识点糖类的结构和性质糖类是有机化合物中最常见的一类物质,广泛存在于自然界和生物体内。
它们不仅是重要的营养物质,也在生物体内担任着重要的功能角色。
本文将就糖类的结构和性质进行详细的讨论。
一、糖类的结构糖类的基本结构可以归纳为单糖、双糖和多糖三种类型。
单糖是最简单的糖类,包括三种常见的单糖:葡萄糖、果糖和半乳糖。
它们的分子式均为C6H12O6,但它们的结构却有所不同。
葡萄糖和果糖都是环状的结构,而半乳糖则是线性结构。
双糖是由两个单糖分子通过缩合反应形成的,比如蔗糖和乳糖。
多糖是由多个单糖分子缩合而成,常见的有淀粉和纤维素。
二、糖类的性质1. 溶解性: 糖类常用作食品中的添加剂,如砂糖和蜂蜜。
它们具有良好的溶解性,尤其是在水中能够迅速溶解。
这也是为什么糖类常被用于制作饮料、甜点等食品的原因。
2. 甜味: 糖类具有独特的甜味,是许多食物中不可或缺的调味品。
这是由于糖类分子中含有许多羟基,能够与味蕾上的受体相结合,从而引起甜味感觉。
3. 反应性: 糖类具有一定的反应性,可以与其他物质产生化学反应。
例如,糖类能够与氨基酸缩合形成糖基化合物,这在生物体内起着重要的作用。
此外,糖类还可以与氧化剂反应发生糖的焦糖化反应,生成焦糖色素。
4. 发酵性: 糖类可以被微生物发酵产生酒精和二氧化碳。
这也是为什么糖类常被用于酿造过程中的原因。
在酵母菌的作用下,糖类可以转化为乙醇和二氧化碳,并且在此过程中释放能量。
5. 构象异构性: 糖类分子的立体结构存在构象异构性。
例如,在溶液中,葡萄糖分子可以存在α型和β型两种构象。
这种构象异构性对于糖类的生物活性和化学性质都有一定的影响。
综上所述,糖类作为有机化合物的一类,其结构和性质的研究对于我们了解生物体内的基本过程和化学反应机制具有重要意义。
通过对糖类结构和性质的深入研究,我们可以更好地理解糖类在生物体内的作用,从而为相关领域的研究和应用提供基础支持。