试验动物麻醉
- 格式:doc
- 大小:145.50 KB
- 文档页数:12

一、实训目的通过本次实训,了解和掌握动物全身麻醉的基本原理、操作方法和注意事项,提高动物实验操作技能,确保实验动物在实验过程中的安全和福利。
二、实训时间2023年11月15日三、实训地点XX大学实验动物中心四、实训内容1. 实训准备- 熟悉动物全身麻醉的原理和操作流程。
- 准备实验动物(如大鼠、小鼠等)。
- 准备麻醉药物(如戊巴比妥钠、乌拉坦等)、注射器、导管、呼吸机等设备。
2. 麻醉操作- 根据实验动物种类和体重,计算麻醉药物剂量。
- 选择合适的给药途径(如腹腔注射、静脉注射等)。
- 静脉注射麻醉药物,观察动物反应,调整麻醉深度。
- 连接呼吸机,调整呼吸参数,确保动物呼吸平稳。
- 观察动物生命体征,如呼吸、心率、血压等。
3. 麻醉深度判断- 根据动物呼吸频率、眼球、瞳孔、足和脚趾的刺激反应、肌肉紧张度等变化,将动物麻醉分为诱导期、浅外科期、深外科期和脱离深外科期。
4. 麻醉维持- 根据实验需要,调整麻醉药物剂量和给药频率,维持麻醉深度。
- 观察动物生命体征,确保麻醉效果。
5. 麻醉恢复- 实验结束后,逐渐减少麻醉药物剂量,观察动物恢复情况。
- 待动物完全清醒后,释放动物。
五、实训结果与分析1. 麻醉效果- 实验动物在麻醉过程中呼吸平稳,心率、血压等生命体征正常。
- 麻醉深度适中,动物在实验过程中无疼痛反应。
2. 麻醉操作- 麻醉药物剂量计算准确,给药途径选择合理。
- 麻醉操作规范,无操作失误。
3. 注意事项- 麻醉药物剂量不宜过大,以免导致动物死亡。
- 观察动物生命体征,确保麻醉效果。
- 麻醉过程中,避免动物挣扎,以免造成伤害。
六、实训总结通过本次实训,我掌握了动物全身麻醉的基本原理、操作方法和注意事项。
在实训过程中,我学会了如何根据实验动物种类和体重计算麻醉药物剂量,选择合适的给药途径,观察动物生命体征,调整麻醉深度,确保实验动物在实验过程中的安全和福利。
同时,我认识到麻醉操作的重要性,以及在实验过程中要严格遵守操作规范,确保实验结果的准确性。

动物实验常见操作技术动物实验是科学研究中常用的一种手段,通过对动物进行各种操作和处理,获得与人类相关的科学数据和知识。
以下是动物实验中常见的操作技术。
一、麻醉和镇痛技术动物实验中会应用麻醉药物使动物失去感觉和意识,以减少动物在实验过程中的痛苦和压力。
常用的麻醉技术包括静脉麻醉、吸入麻醉和局部麻醉。
镇痛技术用于减轻术后疼痛,常采用各种药物如阿片类和非甾体抗炎药等。
二、手术技术手术技术是动物实验中常见的一项操作技术,用于在动物体内插入仪器、移除组织样本、修复组织或器官的损伤等。
常见的手术技术包括卵巢切除术、肝脏切片术、心脏手术等。
三、体内采样技术体内采样技术是从动物体内获取生物样本的一种方法,用于分析动物的生理和生化指标。
常见的体内采样技术包括血液采样、尿液采样、肠道内容物采样等。
四、药物给药技术药物给药技术是将药物通过各种途径输入动物体内,以研究药物的药代动力学和药效学等。
常见的给药途径包括静脉注射、腹腔注射、皮下注射等。
五、环境控制技术环境控制技术用于控制实验动物的环境条件,以确保实验结果的准确性和可靠性。
常见的环境控制技术包括温度控制、湿度控制、光照控制等。
六、行为测定技术行为测定技术用于评估动物的行为特征和认知功能,常用于研究动物的学习记忆、情绪行为等。
常见的行为测定技术包括开放田间测试、旋转杆测定、挖洞测试等。
七、分子生物学技术分子生物学技术用于研究动物的基因表达、DNA/RNA的分离和测定等。
常用的分子生物学技术包括PCR技术、凝胶电泳技术、蛋白质电泳技术等。
八、影像学技术影像学技术用于研究动物的器官结构、功能和病理变化等。
常见的影像学技术包括X线摄影技术、CT扫描、MRI等。
九、细胞培养技术细胞培养技术用于研究动物的细胞生长、增殖和代谢等。
常用的细胞培养技术包括离心培养、悬浮培养、共培养等。
以上列举了动物实验中常见的操作技术,不同实验目的和研究领域需要选用不同的操作技术,以获得准确和可靠的实验结果。

实验动物麻醉方法及注意事项麻醉(anesthesia)的基本任务是消除实验过程中所至的疼痛和不适感觉,保障实验动物的安全,使动物在实验中服从操作,确保实验顺利进行。
一、常用的麻醉药(一)常用局部麻醉剂:普鲁卡因,此药毒性小,见效快,常用于局部浸润麻醉,用时配成0.5%~1%;利多卡因,此药见效快,组织穿透性好,常用1%~2%溶液作为大动物神经干阻滞麻醉,也可用0.25%~0.5%溶液作局部浸润麻醉。
(二)常用全身麻醉剂:1.乙醚乙醚吸入法是最常用的麻醉方法,各种动物都可应用。
其麻醉量和致死量相差大,所以其安全度大。
但由于乙醚局部刺激作用大,可刺激上呼吸道粘液分泌增加;通过神经反射还可扰乱呼吸、血压和心脏的活动,并且容易引起窒息,在麻醉过程中要注意。
但总起来说乙醚麻醉的优点多,如麻醉深度易于掌握,比较安全,而且麻醉后恢复比较快。
其缺点是需要专人负责管理麻醉,在麻醉初期出现强烈的兴奋现象,对呼吸道又有较强的刺激作用,因此,需在麻醉前给予一定量的吗啡和阿托品(基础麻醉),通常在麻醉前20-30分钟,皮下注射盐酸或硫酸吗啡(每公斤体重5~10mg)及阿托品(每公斤体重0.1mg)。
盐酸吗啡可降低中枢神经系统兴奋性,提高痛阈,还可节省乙醚用量及避免乙醚麻醉过程中的兴奋期。
阿托品可对抗乙醚刺激呼吸道分泌粘液的作用,可避免麻醉过程中发生呼吸道堵塞,或手术后发生吸入性肺炎。
进行手术或使用过程中,需要继续给予吸入乙醚,以维持麻醉状态。
慢性实验预备手术的过程中,仍用麻醉口罩给药,而在一般急性使用,麻醉后可以先进行气管切开术,通过气管套管连接麻醉瓶继续给药。
在继续给药过程中,要时常检查角膜反射和观察瞳孔大小(如发现角膜反射消失,瞳孔突然放大,应立即停止麻醉。
万一呼吸停止,必须立即施行人工呼吸。
待恢复自动呼吸后再进行操作。
2.苯巴比妥钠此药作用持久,应用方便,在普通麻醉用量情况下对于动物呼吸、血压和其它功能无多大影响。

实验动物的麻醉方法
实验动物的麻醉方法是根据实验的目的和动物物种的不同而有所区别。
以下是一些常用的麻醉方法:
1. 全身麻醉:使用全身麻醉药物,如氯化乙酰胺或异氟醚等,通过静脉注射或吸入的方式进行麻醉。
这种方法适用于大型动物或需要长时间麻醉的实验。
2. 局部麻醉:使用局部麻醉药物,如利多卡因或普鲁卡因等,通过局部注射或浸润的方式进行麻醉。
这种方法适用于小型动物或需要局部麻醉的实验。
3. 镇静剂:使用镇静剂,如地西泮或苯巴比妥等,通过口服或注射的方式进行麻醉。
这种方法适用于需要轻度麻醉或对镇静剂敏感的动物。
4. 吸入麻醉气体:使用麻醉气体,如笑气或七氟醚等,通过吸入的方式进行麻醉。
这种方法适用于小鼠或需要快速麻醉的实验。
需要注意的是,麻醉方法的选择应根据实验的需要和动物的安全性来确定,并且应严格按照相关伦理和法规要求进行操作。
另外,麻醉时应监测动物的生理指标,确保其在麻醉状态下保持稳定。

实验动物麻醉所有可能引起实验动物疼痛或不适的实验方案都必须使用合适的麻醉剂、止痛剂和镇静剂。
如麻醉剂、止痛剂或镇静剂可能影响实验数据,该实验方案可不使用麻醉剂、止痛剂或镇静剂,但必须在实验方案中予以详细说明,并在实验动物管理委员会批准后方可开展相关实验。
包括动物品系、使用途径、体重、性别、动物健康状况、温度、其它同时使用的药物在内的多种因素影响麻醉剂、止痛剂或镇静剂的使用剂量和有效时间。
因此,在使用麻醉剂时必须时刻监测实验动物的麻醉深度,以防止过度麻醉导致动物死亡或麻醉不足无法缓解动物的疼痛。
足底反射、角膜反射、肌肉紧张和对皮肤夹捏的反应是检测动物麻醉深度的有用指标,在条件许可时,推荐测量动物心率、血压、呼吸频率及体温作为检测动物麻醉深度更为精确的指标。
使用麻醉剂时,一定要注意方法的可靠性,根据不同的动物选择合适的方法。
1.麻醉剂的用量,除参照一般标准外,还应考虑个体对药物的耐受性不同。
一般说,衰弱和过胖的动物,其单位体重所需剂量较小。
在使用麻醉剂过程中,特别是使用巴比妥类药物时,一般应首先使用较小剂量,随时检查动物的反应情况,并逐步提高剂量。
2.动物在麻醉期体温容易下降,要采取保温措施。
相比清醒的动物,麻醉后的动物反应相对迟钝。
因此,推荐使用循环水浴保温垫,不推荐使用照明灯、电加热器等不易控制温度的设备,以免灼伤实验动物。
3.静脉注射麻醉剂发挥作用速度快,静脉注射必须缓慢,同时观察肌肉紧张、角膜反射和对皮肤夹捏的反应,当这些活动明显减弱或消失时,应立即停止注射。
配制的药液浓度要适中,不可过高,以免麻醉过急;但也不能过低,以减少注入溶液的体积。
实验操作涉及腹腔注射时,不应使用腹腔注射麻醉剂。
4.气温较低时,麻醉剂在注射前应加热至动物体温水平。
5.注射麻醉剂前12小时实验动物应禁食,以防止食物回流。
注射前3小时应限制饮水。
6.如需使用抗生素以防止术后感染,手术前1小时应肌肉注射抗生素,并于手术过程中静脉注射抗生素。

动物实验麻醉报告模板引言动物实验是科学研究的重要手段之一,而麻醉是动物实验中保证实验动物的无痛苦和安全的关键环节。
本报告旨在总结和分析动物实验中使用的麻醉方法和效果,并提供进一步改进的建议。
方法实验动物本次实验使用了40只雌性小鼠(Mus musculus),体重在20克至25克之间。
麻醉方法本次实验采用了三种常见的麻醉方法,分别是:1. 乙醚麻醉:将乙醚溶于柔性纱布片上,放于密闭的麻醉箱中,让小鼠吸入乙醚进行麻醉。
2. 吸入式异氟醚麻醉:将异氟醚注入吸入器中,在特定领域内产生吸入式麻醉。
3. 静脉注射戊巴比妥麻醉:在小鼠的尾静脉注射戊巴比妥至麻醉状态。
结果与讨论乙醚麻醉乙醚麻醉方法对小鼠的麻醉效果较好,迅速进入麻醉状态,并保持相对较长时间的麻醉效果。
然而,需要注意的是乙醚在高浓度下可能引起小鼠呼吸及心率过慢等副作用,因此在实验过程中需要控制乙醚浓度并监测小鼠的生命体征。
吸入式异氟醚麻醉吸入式异氟醚麻醉方法也能够迅速进入麻醉状态,并且对呼吸和心率的影响较小。
而且,异氟醚具有良好的调控性,可以根据实验需要调整麻醉深度。
不过,需要注意的是异氟醚价格较高,且在吸入式麻醉过程中需配备专业的吸入器。
静脉注射戊巴比妥麻醉静脉注射戊巴比妥是一种在动物实验中常用的麻醉方法。
它可以快速、有效地诱导小鼠进入麻醉状态,且对呼吸和心率的影响相对较小。
然而,注意戊巴比妥属于镇痛作用较弱的麻醉药物,若在手术操作中需进一步控制小鼠的疼痛感,需要配合其他麻醉药物使用。
结论根据本次实验结果和讨论,我们可以得出以下结论:1. 乙醚、异氟醚和戊巴比妥均为常用的麻醉方法,具有不同的特点和适用场景。
2. 在选择麻醉方法时,需要根据实验的具体要求和预期效果来综合考虑。
3. 在实验过程中,需要严密监测小鼠的生命体征,确保麻醉效果良好且安全。
4. 麻醉方法的选择和使用应符合伦理规范和实验要求,确保动物实验的科学性和可靠性。
进一步改进的建议根据本次实验的结果和讨论,可以提出以下改进的建议:1. 在长时间实验中,应考虑使用具有较长麻醉效果的麻醉药物,以减少频繁麻醉的需求。
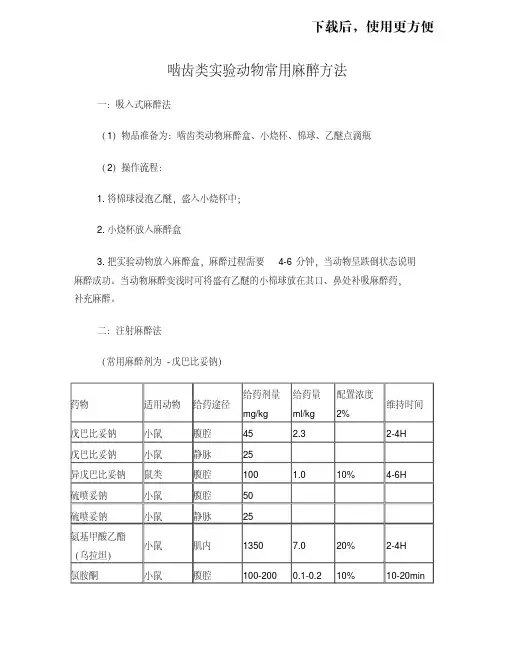
啮齿类实验动物常用麻醉方法
一:吸入式麻醉法
(1)物品准备为:啮齿类动物麻醉盒、小烧杯、棉球、乙醚点滴瓶(2)操作流程:
1.将棉球浸泡乙醚,盛入小烧杯中;
2.小烧杯放入麻醉盒
3.把实验动物放入麻醉盒,麻醉过程需要
4-6分钟,当动物呈跌倒状态说明
麻醉成功。
当动物麻醉变浅时可将盛有乙醚的小棉球放在其口、鼻处补吸麻醉药,补充麻醉。
二:注射麻醉法
(常用麻醉剂为-戊巴比妥钠)
药物适用动物给药途径给药剂量mg/kg 给药量ml/kg 配置浓度2%
维持时间戊巴比妥钠小鼠腹腔45 2.3
2-4H
戊巴比妥钠小鼠静脉25 异戊巴比妥钠鼠类腹腔100 1.0
10%
4-6H
硫喷妥钠小鼠腹腔50 硫喷妥钠小鼠静脉25 氨基甲酸乙酯(乌拉坦)小鼠肌内1350 7.0 20% 2-4H 氯胺酮
小鼠
腹腔
100-200
0.1-0.2
10%
10-20min
腹腔注射给药时一般先给药总剂量的2/3,然后进行观察,如果已经达到所需的麻醉程度,可以不再注射余下的麻醉药。

动物实验常用操作技术动物实验常用操作技术是指在动物实验过程中常用的一些操作技术,用于进行动物实验的各项实验操作。
这些操作技术的选择和使用对于实验结果的准确性和可靠性有着重要的影响。
在动物实验中,常用的操作技术主要包括动物麻醉、注射、剖检、培养和观察等。
一、动物麻醉技术动物麻醉技术是在动物实验中常用的首要操作技术之一、麻醉技术的运用可以使实验动物保持在一定的安静状态下,减轻动物实验过程中的痛苦和压力,同时还可以提高实验的可靠性和准确性。
常用的动物麻醉技术主要有局部麻醉、全身麻醉和麻醉复苏等技术。
局部麻醉常用的方法有局麻药物的表面涂擦、注射、浸渍和包扎等方式;全身麻醉常用的方法有麻醉药物的口服、皮下、肌肉注射、静脉注射等方式;麻醉复苏技术包括将动物由麻醉状态逐渐恢复到清醒状态,并监测复苏过程中的生理指标。
二、动物注射技术动物注射技术是在动物实验中常用的操作技术之一、注射技术的运用可以向实验动物的体内引入药物、疫苗或其他试剂,观察其对动物的作用和效果。
常用的动物注射技术主要有皮下注射、肌肉注射、静脉注射和腹腔注射等。
皮下注射一般是将药物或试剂注射到动物的皮下组织中;肌肉注射是将药物或试剂注射到动物的肌肉组织中;静脉注射是将药物或试剂注射到动物的血管中;腹腔注射是将药物或试剂注射到动物的腹腔腔隙中。
三、动物剖检技术动物剖检技术是在动物实验中常用的操作技术之一、剖检技术的运用可以观察动物内部器官的结构和病变,对实验结果的解释和分析起到关键的作用。
常用的动物剖检技术主要包括尸体解剖和活体解剖两种。
尸体解剖是在动物死亡后对尸体进行的解剖,以观察其内部器官的结构和异常情况;活体解剖是在动物存活的情况下进行的解剖,以观察其内部器官的运动和功能情况。
四、动物培养技术动物培养技术是在动物实验中常用的操作技术之一、培养技术的运用可以在体外条件下维持动物细胞和组织的生长和繁殖,为研究动物细胞和组织的生物学特性提供便利。
常用的动物培养技术主要有细胞培养和组织培养两种。

实验动物麻醉方法实验动物麻醉方法一、动物实验中常用的麻醉剂1、挥发性麻醉剂这类麻药包括乙醚、氯仿等。
乙醚吸入麻醉适用于各种动物,其麻醉量和致死量差距大,所发安全度亦大,动物麻醉深度容易掌握,而且麻后苏醒较快。
其缺点是对局部刺激作用大,可引起上呼吸道粘膜液体分泌增多,再通过神经反射可影响呼吸、血压和心跳活动,并且容易引起窒息,故在乙醚吸入麻醚时必需有人照看,以防麻醉过深而出现上情况。
2、非挥发性麻醉剂这类麻醉剂种类较多,包括苯巴比妥钠、戊巴比妥钠、硫喷妥钠等巴比妥类的衍生物,氨基甲酸乙脂和水合氯醛。
这些麻醉剂使用方便,一次给药可维持较长的麻醉时间,麻醉过程较平衡,动物无明显挣扎现象。
但缺点是苏醒较慢。
3、中药麻醉剂动物实验时有时也用到象洋金花和氢溴酸东莨菪碱等中药麻醉剂,但由于其作用不够稳定,而且常需加佐剂麻醉效果才能理想,故在使用过程中不能得到普及,因而,多数实验室不选用这类麻醉剂进行麻醉二、实验动物的麻醉方法1、全身麻醉(1)吸入法(2)腹腔和静脉给药麻醉法2、局部麻醉(1)猫的局部麻醉一般应用0.5-1.0%盐酸普鲁卡因注射。
粘膜表面麻醉宜用2%盐酸可卡因。
(2)在眼球手术时,可于结膜囊滴入0.02%盐酸可卡因溶液,数秒钟即可出现麻醉。
(3)狗的局部麻醉用0.5-1%盐酸普鲁卡因注射。
眼、鼻、咽喉表面麻醉可用2%盐酸可卡因。
3、麻醉注意事项(1)静脉注射必须缓慢,同时观察肌肉紧张性、角膜反射和对皮肤夹捏的反应,当这些活动明显减弱或消失时,立即停止注射。
配制的药液浓度要适中,不可过高,以兔麻醉过急;但也不能过低,以减少注入溶液的体积。
(2)麻醉时需注意保温。
麻醉期间,动物的体温调节机能往往受到抑制,出现体温下降,可影响实验的准确性。
此时常需采取保温措施。
保温的方法有:实验桌装灯,电褥,台灯照射等。
无论用哪种方法加温都应根据动物的肛门体温而定。
常用实验动物正常体温:猫为38.6℃±1.0℃,兔为38.4℃±1.0℃,大鼠为39.3℃±0.5℃。

一、实验背景在动物实验中,为了保证实验结果的准确性和动物福利,对实验动物进行麻醉是必不可少的。
小鼠作为常见的实验动物,其麻醉方法的选择对于实验的成功与否至关重要。
本实验旨在探讨不同麻醉方法对小鼠的麻醉效果,为后续实验提供参考。
二、实验材料与仪器1. 实验动物:健康昆明小鼠50只,体重20-25g,雌雄各半。
2. 麻醉药物:水合氯醛、戊巴比妥钠、异氟烷。
3. 仪器:小鼠麻醉机、体温计、注射器、针头、手术器械等。
三、实验方法1. 实验分组:将50只小鼠随机分为5组,每组10只,分别为A组(水合氯醛组)、B组(戊巴比妥钠组)、C组(异氟烷组)、D组(水合氯醛+戊巴比妥钠组)、E组(水合氯醛+异氟烷组)。
2. 麻醉方法:- A组:腹腔注射水合氯醛(剂量为0.3ml/100g体重)。
- B组:腹腔注射戊巴比妥钠(剂量为30mg/kg体重)。
- C组:采用异氟烷吸入麻醉,浓度为1.5%。
- D组:腹腔注射水合氯醛(剂量为0.3ml/100g体重)+腹腔注射戊巴比妥钠(剂量为30mg/kg体重)。
- E组:腹腔注射水合氯醛(剂量为0.3ml/100g体重)+吸入异氟烷,浓度为1.5%。
3. 麻醉效果观察:- 观察各组小鼠的麻醉诱导时间、麻醉维持时间、麻醉恢复时间。
- 观察各组小鼠的生理指标变化,如心率、呼吸频率、体温等。
- 观察各组小鼠的手术操作过程中是否出现挣扎、抽搐等反应。
四、实验结果1. 麻醉诱导时间:A组(10.2±1.5分钟)、B组(8.1±1.2分钟)、C组(5.6±1.0分钟)、D组(9.8±1.3分钟)、E组(7.2±1.1分钟)。
结果显示,异氟烷组的麻醉诱导时间最短,水合氯醛组次之,戊巴比妥钠组最长。
2. 麻醉维持时间:A组(60.5±8.2分钟)、B组(52.3±7.8分钟)、C组(45.1±6.7分钟)、D组(57.9±8.4分钟)、E组(49.8±7.5分钟)。

一、实验目的1. 探讨不同麻醉药物对实验动物的作用效果。
2. 比较不同麻醉药物的安全性及副作用。
3. 了解麻醉药物的药理作用及代谢特点。
二、实验材料1. 实验动物:成年小鼠,体重20-25g,雌雄不限。
2. 麻醉药物:戊巴比妥钠、氯胺酮、苯巴比妥钠。
3. 仪器设备:电子天平、注射器、麻醉机、生理记录仪、手术器械等。
三、实验方法1. 将实验动物随机分为四组,每组10只。
2. 第1组为对照组,不给予麻醉药物。
3. 第2组给予戊巴比妥钠腹腔注射,剂量为50mg/kg。
4. 第3组给予氯胺酮腹腔注射,剂量为50mg/kg。
5. 第4组给予苯巴比妥钠腹腔注射,剂量为50mg/kg。
6. 分别记录各组动物注射麻醉药物后的呼吸、心率、血压等生理指标。
7. 在麻醉状态下,对动物进行手术操作,观察麻醉效果。
8. 记录手术过程中动物的挣扎程度、苏醒时间等。
四、实验结果1. 戊巴比妥钠组:注射后5-10分钟,动物出现嗜睡状态,呼吸减慢,心率降低,血压下降。
手术过程中,动物无明显挣扎,麻醉效果良好。
术后苏醒时间约20分钟。
2. 氯胺酮组:注射后5-10分钟,动物出现嗜睡状态,呼吸减慢,心率降低,血压下降。
手术过程中,动物挣扎程度较戊巴比妥钠组轻,麻醉效果较好。
术后苏醒时间约15分钟。
3. 苯巴比妥钠组:注射后5-10分钟,动物出现嗜睡状态,呼吸减慢,心率降低,血压下降。
手术过程中,动物挣扎程度较氯胺酮组明显,麻醉效果较差。
术后苏醒时间约25分钟。
4. 对照组:注射后5-10分钟,动物无明显变化,手术过程中,动物挣扎剧烈,无法进行手术操作。
五、实验讨论1. 本实验结果表明,戊巴比妥钠、氯胺酮、苯巴比妥钠均具有一定的麻醉作用,但戊巴比妥钠和氯胺酮的麻醉效果较好,苯巴比妥钠的麻醉效果较差。
2. 戊巴比妥钠和氯胺酮的麻醉效果较好,可能与它们的药理作用有关。
戊巴比妥钠属于巴比妥类药物,具有中枢神经系统抑制作用,可以降低动物的兴奋性,从而起到麻醉作用。
实验动物的麻醉方法知识 This model paper was revised by the Standardization Office on December 10, 2020实验动物的麻醉方法麻醉(anesthesia)的基本任务是消除实验过程中所致的疼痛和不适感觉,保障实验动物的安全,使动物在实验中服从操作,确保实验顺利进行。
一、常用的麻醉药(一)常用局部麻醉剂:普鲁卡因,此药毒性小,见效快,常用于局部浸润麻醉,用时配成%~1%;利多卡因,此药见效快,组织穿透性好,常用1%~2%溶液作为大动物神经干阻滞麻醉,也可用%~%溶液作局部浸润麻醉。
(二)常用全身麻醉剂:1. 乙醚乙醚吸入法是最常用的麻醉方法,各种动物都可应用。
其麻醉量和致死量相差大,所以其安全度大。
但由于乙醚局部刺激作用大,可刺激上呼吸道粘液分泌增加;通过神经反射还可扰乱呼吸、血压和心脏的活动,并且容易引起窒息,在麻醉过程中要注意。
但总起来说乙醚麻醉的优点多,如麻醉深度易于掌握,比较安全,而且麻醉后恢复比较快。
其缺点是需要专人负责管理麻醉,在麻醉初期出现强烈的兴奋现象,对呼吸道又有较强的刺激作用。
因此,需在麻醉前给予一定量的吗啡和阿托品(基础麻醉),通常在麻醉前20-30分钟,皮下注射盐酸或硫酸吗啡(每公斤体重1~2mg)及阿托品(每公斤体重)。
盐酸吗啡可降低中枢神经系统兴奋性,提高痛阈,还可节省乙醚用量及避免乙醚麻醉过程中的兴奋期。
阿托品可对抗乙醚刺激呼吸道分泌粘液的作用,可避免麻醉过程中发生呼吸道堵塞,或手术后发生吸入性肺炎。
进行手术或使用过程中,需要继续给予吸入乙醚,以维持麻醉状态。
慢性实验预备手术的过程中,仍用麻醉口罩给药,而在一般急性使用,麻醉后可以先进行气管切开术,通过气管套管连接麻醉瓶继续给药。
在继续给药过程中,要时常检查角膜反射和观察瞳孔大小(如发现角膜反射消失,瞳孔突然放大,应立即停止麻醉。
并施行必要的人工呼吸。
动物实验麻醉方法
动物实验对于推动科学研究和医学进步起着至关重要的作用啊!而在动物实验中,麻醉方法可是非常关键的一环呢!就好像我们人要做手术得先麻醉一样,动物们也需要合适的麻醉来减少它们的痛苦呀。
你知道吗,常用的吸入麻醉就像是给动物罩上了一个神奇的“睡眠罩”!让它们在不知不觉中就进入了麻醉状态。
这种方法快速生效,而且还比较容易控制麻醉的深度呢。
还有注射麻醉,就像是给动物打了一针“魔法药水”,能让它们迅速安静下来。
就拿戊巴比妥钠来说吧,它可是个厉害的角色呢!通过静脉注射,能让动物很快进入麻醉状态,就好像它们一下子进入了一个宁静的梦乡。
但这可不能随便用哦,得掌握好剂量,不然可就麻烦啦!这不就跟我们人吃药一样嘛,多了少了都不行。
还有啊,氯胺酮也是常用的麻醉剂呢。
它能让动物产生一种奇特的“恍惚感”,仿佛它们置身于一个虚幻的世界。
这多神奇呀!但用它的时候也要小心谨慎,要密切观察动物的反应呢。
动物实验的麻醉方法选择可不能马虎呀!这就好比是给动物建一个舒适的“小窝”,得让它们安心地在里面度过麻醉的时光。
要是选不好,那动物得多遭罪呀!我们可不能这么残忍对不对?我们要尽可能地减少它们的痛苦,让它们也能感受到我们的关爱和尊重呢。
所以呀,在进行动物实验时,一定要认真选择合适的麻醉方法,就像我们精心挑选礼物送给重要的人一样。
要考虑到动物的种类、体重、健康状况等等好多因素呢。
只有这样,才能让动物们在实验中既安全又舒适,为我们的科学研究做出更大的贡献呀!总之,动物实验麻醉方法真的太重要啦,我们一定要重视起来呀!。
第1篇一、实验目的本实验旨在了解和掌握动物医学麻醉的基本原理、常用麻醉药物及其作用特点,熟悉动物麻醉前的准备工作、麻醉方法的操作步骤以及麻醉后的观察与护理。
通过本实验,提高动物医学专业学生的实践操作技能和临床思维能力。
二、实验材料与器材1. 实验动物:家兔2只2. 器材:麻醉机、气管插管、注射器、针头、开口器、喉镜、心电图仪、血压计、温度计、呼吸机、生理盐水、普鲁卡因、氯胺酮、硫酸阿托品、硫酸镁等。
三、实验方法1. 麻醉前准备(1)观察动物的精神状态、呼吸、心跳、体温等生命体征。
(2)对动物进行编号、称重,记录基本信息。
(3)对动物进行禁食禁水,防止麻醉过程中发生呕吐。
(4)准备实验药品和器材。
2. 麻醉方法(1)静脉注射氯胺酮(剂量:5mg/kg),观察动物的反应。
(2)静脉注射硫酸阿托品(剂量:0.01mg/kg),观察动物的反应。
(3)静脉注射硫酸镁(剂量:0.1mg/kg),观察动物的反应。
(4)静脉注射普鲁卡因(剂量:5mg/kg),观察动物的反应。
(5)将动物放入麻醉机,调节氧流量,连接呼吸机,观察动物的生命体征。
3. 麻醉观察与护理(1)观察动物的呼吸、心跳、血压、体温等生命体征,确保麻醉深度适宜。
(2)观察动物的反应,如是否有躁动、呕吐、抽搐等,及时调整麻醉深度。
(3)保持动物呼吸道通畅,防止窒息。
(4)注意动物体温变化,必要时给予保暖措施。
(5)观察麻醉恢复情况,及时处理可能出现的并发症。
四、实验结果与分析1. 麻醉前,动物的精神状态良好,呼吸、心跳、血压、体温等生命体征正常。
2. 静脉注射氯胺酮后,动物表现为兴奋、肌肉松弛,随后进入睡眠状态。
注射硫酸阿托品后,动物出现口干、心率加快等反应。
注射硫酸镁后,动物出现肌肉松弛、呼吸抑制等反应。
注射普鲁卡因后,动物表现为疼痛反应,随后进入睡眠状态。
3. 在麻醉过程中,动物的生命体征稳定,呼吸、心跳、血压、体温等指标在正常范围内。
动物无躁动、呕吐、抽搐等不良反应。
动物实验的基本技术操作方法动物实验是一种科学研究的重要手段,也是科学发展和医学进步的必要步骤之一、在进行动物实验时,研究人员需要掌握一系列基本的技术操作方法。
下面将介绍几种常见的动物实验技术操作方法。
1.动物麻醉操作:动物麻醉是进行动物实验的前提条件,可以减少动物的痛苦和压力,保证实验结果的可靠性。
常用的麻醉方法包括静脉麻醉、吸入麻醉和局部麻醉。
研究人员需要掌握药物的剂量、给药途径和监测动物麻醉深度的方法。
2.动物手术技术:在进行一些复杂的实验时,需要进行动物手术操作。
手术技术操作包括皮肤消毒、手术切口、血管或器官的外露和缝合等。
研究人员需要掌握无菌操作的技巧和手术操作的规范,以确保手术的成功和动物的生存率。
3.器械使用和数据记录:在动物实验中,研究人员需要掌握各种生物学实验仪器的使用方法,如离心机、显微镜、血液分析仪等。
同时,需要准确记录实验过程中的数据,包括动物身体指标、实验参数和操作步骤等。
4.体内注射技术:动物实验中常用的一项技术是体内注射,包括静脉注射、皮下注射和腹腔注射等。
研究人员需要掌握注射针头的选择、皮肤局部麻醉的方法和注射位置的确定等。
5.血液采集技术:在一些实验中需要进行动物的血液采集,以获取血液样本进行化验或分析。
血液采集技术包括尾脉、静脉和心脏穿刺等。
研究人员需要掌握相应的采血器具的使用方法,以及合理的采血量和采血速度。
6.器官取材和组织处理技术:在一些器官相关的实验中,需要对动物进行器官取材和组织处理。
器官取材技术包括猝死动物器官取材和活体器官取材。
组织处理技术包括固定处理、包埋和切片等。
研究人员需要掌握无菌操作技术和组织处理的标准流程,以获得有效的实验结果。
7.动物分组和饲养技术:在进行动物实验前,需要对动物进行分组和饲养。
分组技术包括随机分组和对照组的设计等。
饲养技术包括提供适宜的饲料和水源、维持良好的生活环境等。
研究人员需要了解动物的生理特点和各种实验动物的饲养要求,以保证动物的健康状态和实验的可靠性。
实验动物麻醉所有可能引起实验动物疼痛或不适的实验方案都必须使用合适的麻醉剂、止痛剂和镇静剂。
如麻醉剂、止痛剂或镇静剂可能影响实验数据,该实验方案可不使用麻醉剂、止痛剂或镇静剂,但必须在实验方案中予以详细说明,并在实验动物管理委员会批准后方可开展相关实验。
包括动物品系、使用途径、体重、性别、动物健康状况、温度、其它同时使用的药物在内的多种因素影响麻醉剂、止痛剂或镇静剂的使用剂量和有效时间。
因此,在使用麻醉剂时必须时刻监测实验动物的麻醉深度,以防止过度麻醉导致动物死亡或麻醉不足无法缓解动物的疼痛。
足底反射、角膜反射、肌肉紧张和对皮肤夹捏的反应是检测动物麻醉深度的有用指标,在条件许可时,推荐测量动物心率、血压、呼吸频率及体温作为检测动物麻醉深度更为精确的指标。
使用麻醉剂时,一定要注意方法的可靠性,根据不同的动物选择合适的方法。
1.麻醉剂的用量,除参照一般标准外,还应考虑个体对药物的耐受性不同。
一般说,衰弱和过胖的动物,其单位体重所需剂量较小。
在使用麻醉剂过程中,特别是使用巴比妥类药物时,一般应首先使用较小剂量,随时检查动物的反应情况,并逐步提高剂量。
2.动物在麻醉期体温容易下降,要采取保温措施。
相比清醒的动物,麻醉后的动物反应相对迟钝。
因此,推荐使用循环水浴保温垫,不推荐使用照明灯、电加热器等不易控制温度的设备,以免灼伤实验动物。
3.静脉注射麻醉剂发挥作用速度快,静脉注射必须缓慢,同时观察肌肉紧张、角膜反射和对皮肤夹捏的反应,当这些活动明显减弱或消失时,应立即停止注射。
配制的药液浓度要适中,不可过高,以免麻醉过急;但也不能过低,以减少注入溶液的体积。
实验操作涉及腹腔注射时,不应使用腹腔注射麻醉剂。
4.气温较低时,麻醉剂在注射前应加热至动物体温水平。
5.注射麻醉剂前12小时实验动物应禁食,以防止食物回流。
注射前3小时应限制饮水。
6.如需使用抗生素以防止术后感染,手术前1小时应肌肉注射抗生素,并于手术过程中静脉注射抗生素。
7.手术过程中如实验动物大量失血,应补充大约3倍失血体积的0.9%生理盐水。
肌肉舒张剂肌肉舒张剂必须与全身麻醉同时使用。
如需使用肌肉舒张剂,必须在实验动物研究方案中予以详细说明,并得到实验动物管理委员会的批准。
止痛剂不同动物疼痛持续时间不同,因此应密切观察实验动物的行为等指标。
对创口较大的手术,至少在术后48小时内应给予实验动物适当的止痛剂,对较小的手术,至少在术后24小时内应给予实验动物适当的止痛剂。
如24小时或48小时后实验动物表现出明显的疼痛,应持续给药,并应与兽医讨论实验动物是否存在其它的健康问题。
通常同时给予两种以上不同的止痛剂有更好的效果,如鸦片类止痛剂与非类固醇类消炎药共同使用。
在手术前提前使用止痛剂也有助于帮助实验动物减轻疼痛感,并可减小麻醉剂和止痛剂的使用剂量。
实验动物疼痛表现啮齿类实验动物疼痛时常表现得更为安静,并可能表现出弓背、呼吸急促、竖毛,舔舐或抓挠疼痛部位,瞳孔增大。
有时会吞噬垫料或其它非食物物品(异食癖)。
在抓取时,该动物可能表现得更有攻击性。
必须强调,啮齿类实验动物有时并不表现出明显的行为异常,但这并不说明该实验动物没有疼痛问题。
麻醉前用药阿托品(Atropine)阿托品是从颠茄和其他茄科植物提取出的一种有毒的白色结晶状生物碱。
可通过皮下注射、肌肉注射或静脉注射使用。
生理作用阿托品为阻断植物神经系统胆碱受体的抗胆碱药,抑制口腔、咽喉、呼吸道黏膜腺体分泌,抑制消化道蠕动和分泌;解除迷走神经对心脏的抑制,使心跳加快;散大瞳孔,使眼压升高;兴奋呼吸中枢,舒张支气管。
注意事项在以下情况时,阿托品应在实验动物麻醉前使用:1.使用麻醉剂/止痛剂如甲苯噻嗪、安定等引起心动过缓;2.使用麻醉剂如克他命引起过量分泌唾液或引起胆碱类神经递质分泌的眼部、口腔、肠道手术。
在手术过程中可使用阿托品缓解心动过缓等症状;手术结束时,可使用阿托品或新斯的明解除神经肌肉阻断剂的作用。
阿托品抑制胃肠道蠕动,可能会影响造影。
实验兔对阿托品不敏感。
剂量小鼠:0.04mg/Kg;大鼠:0.05mg/Kg;兔:0.1-3.0mg/Kg。
格隆溴铵(Glycopyrrolate, Robinul-V)格隆溴铵是拮抗胆碱作用的合成药物,可通过皮下注射、肌肉注射或静脉注射使用。
生理作用格隆溴铵为季铵类抗胆碱药。
与阿托品相似,具有减缓胃肠蠕动、抑制咽喉、气管、支气管黏膜分泌;格隆溴铵作用时间比阿托品长,不会通过血胎屏障或血脑屏障,因此没有中枢性抗胆碱活性。
格隆溴铵抑制胃液分泌,而阿托品则不能抑制胃液分泌。
注意事项格隆溴铵应在实验动物麻醉前使用。
相比阿托品,格隆溴铵具有更强的抑制唾液分泌功能。
格隆溴铵可抑制胃酸分泌,可用于胃酸过高引起的心血管和呼吸系统问题,并可减轻插管术引起的抑制性迷走神经反射。
可能会出现轻微瞳孔放大、心动过速。
不能与碱性药物混合使用。
全身麻醉全身麻醉中麻醉剂经呼吸道吸入或静脉、肌肉注射,产生中枢神经系统抑制,呈现神志消失,全身不感疼痛,肌肉松弛和反射抑制等现象。
全身麻醉抑制深浅与药物在血液内的浓度有关,当麻醉药从体内排出或在体内代谢破坏后,动物逐渐清醒,一般没有后遗症。
吸入性麻醉剂乙醚(Ether)乙醚为无色,具有高度挥发性、刺激性。
乙醚可燃,应注意避免明火。
生理作用乙醚通过抑制中枢神经系统发挥作用。
乙醚麻醉早期会引起心动过速和呼吸时胸廓运动加大。
乙醚局部刺激作用大,可刺激上呼吸道粘液分泌增加;通过神经反射还可扰乱呼吸、血压和心脏的活动,导致心律不齐。
乙醚麻醉时肝功能和肾功能降低;因代谢减慢、血管舒张引起体温降低。
注意事项乙醚吸入法是最常用的麻醉方法,多数动物都可应用,但乙醚不适用于大型动物。
其麻醉量和致死量相差大,麻醉深度易于掌握,较为安全,而且麻醉后恢复比较快。
乙醚麻醉促进唾液分泌,可使用阿托品等抗胆碱药物。
乙醚可燃,遇明火会发生爆炸,应尽可能使用非可燃、爆炸性麻醉剂如甲氧氟烷(Methoxyflurane)、异氟烷(Isoflurane)、溴氯三氟乙烷(Halothane, Fluothane)。
乙醚可刺激上呼吸道粘液分泌增加,增大了手术后发生肺炎的可能性。
溴氯三氟乙烷(Halothane, Fluothane)溴氯三氟乙烷为无色、高度挥发性液体,无刺激性气味,不可燃,不会爆炸。
生理作用溴氯三氟乙烷抑制中枢神经系统,其作用有明显的阶段性,首先是中枢神经系统,其次影响感觉和运动神经,最后影响生命中枢。
溴氯三氟乙烷影响胆碱的运输过程。
溴氯三氟乙烷对呼吸道没有刺激作用,一般不会刺激唾液腺和支气管粘液分泌。
溴氯三氟乙烷逐步抑制呼吸,可能导致缺氧、呼吸暂停。
深度麻醉时可能发生血压降低、心动过缓,可配合阿托品等药物防止心动过缓症状。
注意事项麻醉速度及恢复速度快,较易调整麻醉深度。
溴氯三氟乙烷导致肌肉松弛。
溴氯三氟乙烷用量应精确控制,一般应使用可控制的吸入器。
使用溴氯三氟乙烷时不应使用肾上腺素或去甲肾上腺素。
使用溴氯三氟乙烷过程中和动物苏醒后短时间内不应使用氨基糖苷类抗生素。
异氟烷(Isoflurane)异氟烷无色、挥发性,不可燃,不会爆炸,有轻微刺激性气味。
其挥发性与溴氯三氟乙烷相似,可用于吸入器。
大部分异氟烷会随呼吸排出体外,无代谢反应和代谢产物。
生理作用异氟烷抑制中枢神经系统,但具体作用位点和机制还不清楚。
异氟烷对血细胞数量和血液生化指标没有大的影响,可降低动脉血压,促进大脑血流速度,升高颅内血压,但对颅内血压的影响比溴氯三氟乙烷小。
异氟烷舒张支气管;异氟烷可增强神经肌肉阻断剂的作用。
注意事项麻醉速度及恢复速度快,较易调整麻醉深度。
异氟烷用量应精确控制,一般应使用可控制的吸入器。
异氟烷舒张支气管,因此在慢性肺栓塞动物的麻醉中较为有利。
异氟烷产生最少量的代谢产物。
注射用麻醉剂常用的注射麻醉剂有戊巴比妥钠、硫喷妥钠、克他命等。
大鼠、小鼠常采用腹腔注射法进行全身麻醉。
兔等动物既可腹腔注射给药,也可静脉注射给药。
在麻醉兴奋期出现时,动物挣扎不安,为防止注射针滑脱,常用吸入麻醉法进行诱导,待动物安静后再行腹腔或静脉穿刺给药麻醉。
在注射麻醉药物时,先用麻醉药总量的1/2至2/3,密切观察动物生命体征的变化,如已达到所需麻醉的程度,余下的麻醉药则不用,避免麻醉过深抑制延脑呼吸中枢导致动物死亡。
巴比妥酸盐类麻醉剂(Barbiturate)巴比妥酸盐类麻醉剂通过抑制神经冲动向大脑皮层的传递抑制中枢神经系统。
巴比妥酸盐类除了用于实验动物麻醉外,还可用于催眠、镇定(但常用其它镇定剂)及局部麻醉过量引起的惊厥。
巴比妥酸盐类抑制心血管系统、呼吸系统及基础代谢,并引起体温降低。
因此,使用巴比妥酸盐类应注意实验动物保温。
过量使用巴比妥酸盐类将导致呼吸系统麻痹及动物死亡。
巴比妥酸盐类可扩散至全身,并可穿过血胎屏障。
巴比妥酸盐类作用终止主要通过代谢及经肾脏排出体外。
戊巴比妥钠(Pentobarbital Sodium, Nembutal)戊巴比妥钠为短效麻醉剂,一次给药的有效时间可延续3-5小时,适合一般实验要求。
用时配成1~3%生理盐水溶液,必要时可加温溶解,配好的药液在常温下放置1~2月可保持药效。
一般应通过静脉注射给药,但小鼠可通过腹腔注射给药。
戊巴比妥钠曾广泛使用于实验动物,但已逐步被其它麻醉剂代替。
生理作用戊巴比妥钠作用机制与GABA神经递质相似。
常用戊巴比妥钠为外消旋混合物,其中(+)异构体在抑制中枢神经系统前导致短暂的兴奋期,(-)异构体导致平稳进展的催眠。
戊巴比妥钠对动物循环和呼吸系统无显著抑制作用,但可能导致体温下降,心跳加快。
注意事项戊巴比妥钠需在肝脏经代谢后发挥作用,因此静脉注射戊巴比妥钠后需经一段时间方可导致动物麻醉。
使用戊巴比妥钠时,应首先注射一半剂量的戊巴比妥钠,密切观察动物生命体征的变化,如已达到所需麻醉的程度,余下的麻醉药则不用,以免过度麻醉。
戊巴比妥钠麻醉速度及恢复速度较慢。
注射戊巴比妥钠前使用止痛剂或镇静剂可显著改善,并可大大减小使用戊巴比妥钠剂量(约1/2)。
静脉注射葡萄糖将延长戊巴比妥钠作用时间。
硫喷妥钠(Thiopental Sodium, Pentothal)硫喷妥钠为黄色粉末,有硫臭,易吸水,遇空气或水溶液不稳定,故一般需现用现配,常用浓度为1~5%。
生理作用硫喷妥钠作静脉注射时,由于药液迅速进入脑组织,故诱导快,动物很快被麻醉。
但苏醒也很快,一次给药的麻醉时效仅维持半至一小时。
代谢产物经尿液排出体外。
此药对胃肠道无副作用,但对呼吸有一定抑制作用。
注射硫喷妥钠短时间内(常为5分钟)会引起心跳加速、动脉压升高。
多次给药有累加效应。
注意事项硫喷妥钠在体内很快被富集在脂肪组织中,因此作用时间很短。
在时间较长的实验过程中,可重复注射,以维持一定的麻醉深度。