高三化学一轮复习 第二章 化学物质及其变化 第二节 离子反应
- 格式:ppt
- 大小:1.50 MB
- 文档页数:44





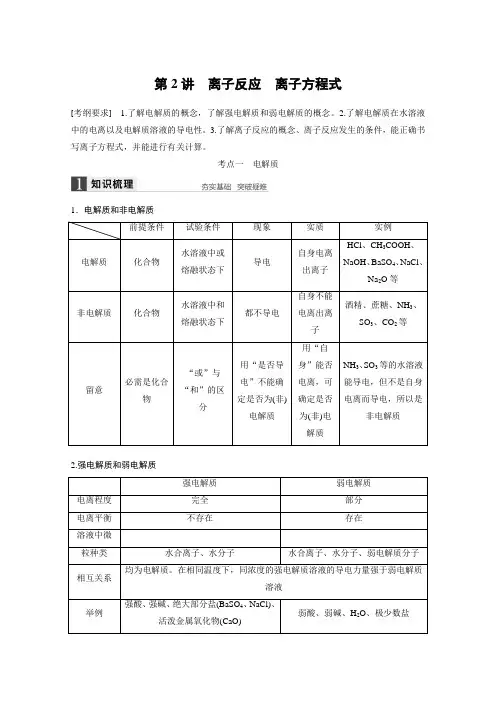
第2讲离子反应离子方程式[考纲要求] 1.了解电解质的概念,了解强电解质和弱电解质的概念。
2.了解电解质在水溶液中的电离以及电解质溶液的导电性。
3.了解离子反应的概念、离子反应发生的条件,能正确书写离子方程式,并能进行有关计算。
考点一电解质1.电解质和非电解质前提条件试验条件现象实质实例电解质化合物水溶液中或熔融状态下导电自身电离出离子HCl、CH3COOH、NaOH、BaSO4、NaCl、Na2O等非电解质化合物水溶液中和熔融状态下都不导电自身不能电离出离子酒精、蔗糖、NH3、SO3、CO2等留意必需是化合物“或”与“和”的区分用“是否导电”不能确定是否为(非)电解质用“自身”能否电离,可确定是否为(非)电解质NH3、SO3等的水溶液能导电,但不是自身电离而导电,所以是非电解质2.强电解质和弱电解质强电解质弱电解质电离程度完全部分电离平衡不存在存在溶液中微粒种类水合离子、水分子水合离子、水分子、弱电解质分子相互关系均为电解质。
在相同温度下,同浓度的强电解质溶液的导电力量强于弱电解质溶液举例强酸、强碱、绝大部分盐(BaSO4、NaCl)、活泼金属氧化物(CaO)弱酸、弱碱、H2O、极少数盐3.电离电解质在水溶液中或熔融状态下离解成自由移动离子的过程。
深度思考1.推断正误,正确的划“√”,错误的划“×”(1)强电解质溶液的导电性比弱电解质溶液的导电性强()(2)BaSO4投入水中,导电性较弱,故它是弱电解质()(3)弱电解质溶液中存在两种共价化合物分子()(4)强电解质都是离子化合物,弱电解质都是共价化合物()(5)CaO是强电解质,是由于它的水溶液能导电()(6)Cl2的水溶液能导电,所以Cl2是电解质()答案(1)×(2)×(3)√(4)×(5)×(6)×解析电解质溶液导电性的强弱与溶液中离子浓度的大小及所带电荷数的多少有关,与电解质强弱没有必定联系,(1)错误;尽管BaSO4难溶于水,但溶解的部分全部电离,故其为强电解质,(2)错误;弱电解质溶液中,有未电离的弱电解质和水这两种共价化合物分子,(3)正确;HCl、H2SO4都是共价化合物但却是强电解质,(4)错误;CaO是强电解质,是由于熔化时能完全电离,能导电,它的水溶液能导电,是由于CaO和H2O反应生成Ca(OH)2,Ca(OH)2能电离出自由移动的Ca2+和OH-,(5)错误;Cl2是单质,(6)错误。


新教材高考化学一轮复习:第2讲离子反应离子方程式[课程标准]1.认识酸、碱、盐等电解质在水溶液中或熔融状态下能发生电离。
通过实验事实认识离子反应及其发生的条件。
2.能用电离方程式表示某些酸、碱、盐的电离。
能用化学方程式、离子方程式正确表示典型物质的主要化学性质。
考点一电解质及其电离1.电解质及其电离的关系(1)常见的强酸、弱酸强酸HNO3、H2SO4、HClO4、HCl、HBr、HI弱酸H2CO3、H2SiO3、CH3COOH、H2C2O4、HClO、HF、H2S、H2SO3强碱NaOH、KOH、Ca(OH)2、Ba(OH)2、RbOH、CsOH弱碱NH3·H2O、Mg(OH)2、Fe(OH)3质也不是非电解质。
②本身电离而导电的化合物才是电解质,如虽然CO2、SO2、NH3的水溶液能导电,但CO2、SO2、NH3均是非电解质。
2.电解质导电的原因——电离(1)概念:电解质溶于水或受热熔化时,形成自由移动的离子的过程。
(2)电离条件:酸的电离条件是溶于水,盐和碱的电离条件是溶于水或受热熔化。
[点拨] ①电解质不一定能导电,如固态NaCl、液态HCl等都不导电。
②电解质的强弱与电解质溶液导电能力的强弱、溶解度的大小没有直接关系,如碳酸钙,其溶解度小,溶液导电能力弱,但其属于强电解质。
3.电离方程式的书写(1)强电解质的电离方程式中,用“===”连接,弱电解质(包括弱酸的酸式酸根)的电离方程式中,用“”连接。
例如:Na2SO4:Na2SO4===2Na++SO2-4;HClO:HClO H++ClO-。
(2)多元弱酸的电离分步书写,多元弱碱的电离一步书写。
例如:H2CO3:H2CO3H++HCO-3、HCO-3H++CO2-3;Fe(OH)3:Fe(OH)3Fe3++3OH-。
(3)酸式盐的电离,强酸酸式盐与弱酸酸式盐在水溶液中的电离方式不同。
例如:NaHSO4:NaHSO4===Na++H++SO2-4;NaHCO3:NaHCO3===Na++HCO-3、HCO-3H++CO2-3。

2018-2019学年高中化学第二章化学物质及其变化第二节第2课时《离子反应及其发生的条件》知识点归纳及例题解析新人教版必修1编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2018-2019学年高中化学第二章化学物质及其变化第二节第2课时《离子反应及其发生的条件》知识点归纳及例题解析新人教版必修1)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2018-2019学年高中化学第二章化学物质及其变化第二节第2课时《离子反应及其发生的条件》知识点归纳及例题解析新人教版必修1的全部内容。
第2课时离子反应及其发生的条件[学习目标定位] 1.了解离子反应的含义及离子方程式的书写方法.理解离子反应的本质。
2.掌握复分解型离子反应发生的条件。
掌握一些常见离子能否共存的判断方法。
一离子方程式完成下列实验,并填表:实验操作实验现象实验结论无明显变化K+、Cl-、Na+、SO错误!相互之间不发生化学反应产生白色沉淀Ba2+与SO错误!反应生成BaSO4,可表示为Ba2++SO2-,4===BaSO4↓归纳总结离子反应及离子方程式(1)离子反应是有离子参加或生成的反应。
(2)离子方程式是用实际参加反应的离子符号来表示反应的式子。
(3)离子方程式的书写步骤及要求(以BaCl2和Na2SO4反应为例)①“写"化学方程式,必须根据实验事实BaCl2+Na2SO4===BaSO4↓+2NaCl。
②“改”反应物和生成物,将易溶、易电离的物质改写成离子形式,其他物质写化学式[如单质、沉淀、气体、难电离物质(如H2O、CH3COOH)、氧化物等]2Cl-+Ba2++SO错误!+2Na+===2Cl-+BaSO4↓+2Na+。
