苯酚硫酸法测总糖
- 格式:doc
- 大小:32.00 KB
- 文档页数:2


苯酚-硫酸比色法测定多糖含量
苯酚-硫酸法是常用的多糖含量测定方法之一。
该方法基于多糖在硫酸的作用下,与苯酚产生颜色反应的原理,利用光度计测定反应产物的吸收值,从而计算出多糖的含量。
步骤如下:
1. 取样品0.1g,在50ml锥形瓶中加入5ml去离子水,振荡
20min溶解。
2. 加入2ml 5%苯酚水溶液,振荡均匀。
3. 加入5ml浓硫酸,使用磁力搅拌器搅拌1-2min。
4. 将混合物放置在冷水中冷却10min。
5. 用紫外分光光度计在490nm处测定吸光度A,同时以含有相同试验液体积的去离子水为对照。
6. 计算样品中多糖含量。
该方法测定简便,精度高,适用于多糖含量较高的样品。
但此法不能区分多糖的种类及其组成,不能应用于含非多糖的样品中。

总糖含量的测定苯酚硫酸法
总糖含量的测定苯酚-硫酸法的实验原理为:苯酚-硫酸试剂可与游离的或寡糖、多糖中的己糖、糖醛酸(或甲苯衍生物)起显色反应,己糖在490nm处(戊糖及糖醛酸在480nm)有最大吸收,吸收值与糖含量呈线性关系。
实验材料包括葡萄糖试剂、试剂盒、浓硫酸、苯酚等,实验步骤如下:
1. 材料处理:将0.5~1g所测的材料捣碎,用适量蒸馏水、玻璃碾磨器碾磨并分次抽提,混合液离心得抽提液即样品液。
2. 标准曲线制作:取50μg/ml的己糖标准溶液0ml,0.1ml,0.2ml,0.3ml,0.4ml,0.5ml于试管中,用水补足到0.5ml,加0.3ml 5%酚溶液,混匀后快速加入1.8ml浓硫酸,振荡混匀,室温放置20min即可出现橙黄色,以第一管调零点,可于490nm处比色测定读OD值。
以糖含量为横坐标,相应的OD值为纵坐标,绘制标准曲线。
3. 样品含量测定:取0.5ml内含2~25μg糖量,同样加入0.3ml 5%酚溶液,混匀后立刻沿管壁加入浓硫酸1.8ml,振荡混匀,达室温后,可测490nm处的OD值,从标准曲线上查相应糖含量。
该方法不需要沸水浴加热,且蛋白质的存在对显色反应影响不大,故也可用于糖蛋白中的己糖测定,还可用于己糖甲基化衍生物和6-脱氧核糖、戊糖的测定。
除此之外,该方法的热量来自浓硫酸与水的混合,因此加浓硫酸时反应快,且应立即混匀,试管应大一些,以免烫手。


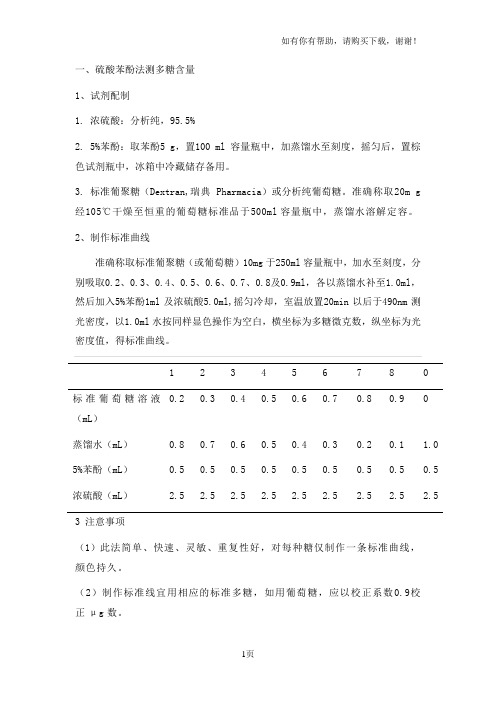
一、硫酸苯酚法测多糖含量1、试剂配制1. 浓硫酸:分析纯,95.5%2. 5%苯酚:取苯酚5 g,置100 ml容量瓶中,加蒸馏水至刻度,摇匀后,置棕色试剂瓶中,冰箱中冷藏储存备用。
3. 标准葡聚糖(Dextran,瑞典Pharmacia)或分析纯葡萄糖。
准确称取20m g经105℃干燥至恒重的葡萄糖标准品于500ml容量瓶中,蒸馏水溶解定容。
2、制作标准曲线准确称取标准葡聚糖(或葡萄糖)10mg于250ml容量瓶中,加水至刻度,分别吸取0.2、0.3、0.4、0.5、0.6、0.7、0.8及0.9ml,各以蒸馏水补至1.0ml,然后加入5%苯酚1ml及浓硫酸5.0ml,摇匀冷却,室温放置20min以后于490nm测光密度,以1.0ml水按同样显色操作为空白,横坐标为多糖微克数,纵坐标为光密度值,得标准曲线。
1 2 3 4 5 6 7 8 0 标准葡萄糖溶液0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 0 (mL)蒸馏水(mL)0.8 0.7 0.6 0.5 0.4 0.3 0.2 0.1 1.0 5%苯酚(mL)0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5 浓硫酸(mL) 2.5 2.5 2.5 2.5 2.5 2.5 2.5 2.5 2.5 3 注意事项(1)此法简单、快速、灵敏、重复性好,对每种糖仅制作一条标准曲线,颜色持久。
(2)制作标准线宜用相应的标准多糖,如用葡萄糖,应以校正系数0.9校正μg数。
(3)对杂多糖,分析结果可根据各单糖的组成比及主要组分单糖的标准曲线的校正系数加以校正计算(4)测定时根据光密度值确定取样的量。
光密度值最好在0.1——0.3之间。
比如:小于0.1之下可以考虑取样品时取2克,仍取0.2ml样品液,如大于0.3可以减半取0.1ml的样品液测定。
(5)正常的反应溶液是深棕色。
糖越多颜色越深。
注意硫酸的纯度。
空白的颜色很深,说明你的空白中的苯酚被氧化了深红是醌(苯酚氧化生成)的颜色颜色过深的话说明你的酚的难度过大,一般是5%但是没遇到你说的那么严重,不是深红色的做的好的时候颜色很浅,颜色深点也有肯能。
实验一硫酸-苯酚法测多糖含量1. 目的要求测量蒽酮硫酸法不能测量的血清型的过程样品中的多糖含量2•方法原理糖在浓硫酸作用下,水解生成单糖,并迅速脱水生成糖醛衍生物,然后与苯酚缩合成橙黄色化合物,且颜色稳定,在波长490 nm处和一定的浓度范围内,其吸光度与多糖含量呈线性关系正比,从而可以利用分光度计测定其吸光度,并利用标准曲线定量测定样品的多糖含量,本方法可用于多糖、单糖含量的测定。
3•主要实验仪器及材料浓硫酸,苯酚,蒸馏装置,分光光度计,电子天平,坐标纸或电脑等。
4.掌握要点硫酸显色的安全、准确操作,单糖到多糖的转换系数。
5 .试剂配制1)葡萄糖标准液的配制准确称取干燥恒重的葡萄糖100 mg,蒸馏水准确定容至100 mL的1 mg/L的葡萄糖液,摇匀后准确吸取10 mL该溶液,蒸馏水稀释定容至100 mL,即得100 ug/mL的葡萄糖标准液。
2)90%苯酚液的配制准确移取苯酚90mL,蒸馏水定容至100 mL,即得90 %苯酚液,棕色瓶中避光保存3)6%苯酚液的配制将90%苯酚液稀释至6%,即一体积储存液对应十四体积纯水,临用现配。
6.实验步骤表1标准曲线的制作步骤AvV 口吕号0 1 2 3 4 5 6葡萄糖0.0 0.1 0.2 0.3 0.4 0.6 0.8 1.0苯酚液0.5 0.5 0.5 0.5 0.5 0.5 0.5 0.5浓硫酸 3.0 3.0 3.0 3.0 3.0 3.0 3.0 3.0取8支干净的具塞试管按表 2方法在操作,先在冰水浴中加入 0.5ml的苯酚溶液,震荡摇匀后缓慢逐滴加入纯硫酸,以不放热或微量放热为宜,摇匀后恒温加塞沸水放置20mi n, 取出凉水冷却10min,以0号作为空白调零,在最大吸收波长处(490nm)测定吸光度。
以葡萄糖浓度X为横坐标(ug/mL),吸光度Y为纵坐标,从而来绘制标准曲线。
用 exceL软件求得回归方程2)待测样品多糖的测定与计算将提取得到的待测多糖用蒸馏水溶解,定容至100 mL,取溶解后的溶液,按标准曲线中的测定方法,以样液为参比液,测定溶液的吸光值,按回归方程计算待测溶液的多糖浓度,注意乘换算系数。
1.1原理
多糖可以被浓硫酸在适当高温下水解,产生单糖,并迅速脱水成糠醛衍生物,该衍生物在强酸条件下与苯酚起显色反应,生成橙黄色物质,在波长490nm处和一定浓度范围内,其吸光度值与糖含量呈线性关系,从而可用比色法测定其含量。
1.2实验步骤
1.2.1100μg/ml D-葡萄糖对照品溶液制备
精密称取10mg D-葡萄糖,加纯化水充分溶解,定容至100ml,作为对照品溶液。
1.2.26%苯酚溶液配制
称取6g苯酚,加入纯化水充分溶解,定容至100ml,备用。
1.2.3对照品管制备
取8支试管,按下表按下表加入100μg/ml D-葡萄糖对照品溶液:
1.2.4供试品管制备
将供试品采用纯化水稀释至D-葡萄糖标准曲线范围内,每步稀释应不超过10倍。
10倍及以内的稀释直接在玻璃试管中进行。
10倍稀释用移液器量取供试品100μl,加纯化水900μl,振荡混匀。
原倍稀释直接取供试品1.0ml加入玻璃试管中。
10倍以内稀释操作按下表在试管中加入相应溶液。
大于10倍的稀释需按下表操作在离心管中先做10倍或100倍稀释(2步10倍稀释)后,再在玻璃试管中按照下表量取稀释。
更高稀释倍数也按照上述原则进行。
1.2.5试验操作
向含有1ml标对照品和供试品的试管中加入0.6ml 6%苯酚溶液,混匀,迅速加入3ml浓硫酸,混匀,置沸水浴反应20分钟。
显色后,冷却至室温,依据紫外-可见分光光度计标准操。
硫酸苯酚法测可溶性总糖含量一、测定原理可溶性糖主要有能溶于水及乙醇的可溶性单糖和寡聚糖。
糖在浓硫酸作用下脱水生成糠醛或羟甲基糠醛能与苯酚所合成一种橙红色化合物,在10~100mg范围内其颜色深浅与糖的含量成正比,且在485nm波长下有最大吸收峰,因此可用比色法在此波长下测定。
硫酸苯酚法可以用于甲基化的糖、戊糖和多聚糖的测定,方法简单,灵敏度高且不受蛋白质存在的影响,产生的颜色稳定时间160min以上。
二、实验试剂1.90%苯酚溶液:称取90g苯酚,加蒸馏水定容至100ml。
2.9%苯酚溶液:取3ml 90%苯酚溶液,加蒸馏水至30ml,现配先用。
3.浓硫酸(比重)4.1%蔗糖标准液:将分析纯蔗糖在80 ℃下烘至恒重,精确称取1.000 g ,加少量水溶解,移入100ml 容量瓶中,加入浓硫酸,用蒸馏水定容至刻度。
5.100μg/L 蔗糖标准液:精确吸取1%蔗糖标准液lml加入100ml容量瓶中,加蒸馏水定容。
三、仪器设备分光光度计,50ml比色管7支,移液管四、实验步骤1.标准曲线的制作取20 ml刻度试管6支,从0~5分别编号,按表1加入溶液和水,然后按顺序向试管内加入1ml 9%苯酚溶液,摇匀,再从管液正面以5~20 s 时间加入5ml浓硫酸,摇匀。
比色液总体积为8ml,在室温下放置3 0 min ,显色。
然后以空白为参比,在485 nm波长下比色测定,以糖含量为横坐标,光密度为纵坐标,绘制标准曲线,求出标准直线方程。
表一2.可溶性糖的提取称取样品~0.3 g, 放入1支刻度试管中,加入5~10 ml蒸馏水,塑料薄膜封口,于沸水中提取30min(提取2次),提取液过滤入25 ml容量瓶中,反复冲洗试管及残渣,定容至刻度。
3.测定吸取样品液于试管中(重复2次),加蒸馏水1.5 ml,同制作标准曲线的步骤,按顺序分别加入苯酚、浓硫酸溶液,显色并测定光密度。
由标准线性方程求出糖的量,计算测试样品中糖含量。
总糖和还原糖的测定实验报告
实验目的,通过对食品中总糖和还原糖的测定,掌握测定方法和原理,了解不同食品中糖的含量。
实验原理,总糖是指食品中所有可溶解于水的糖的总和,包括葡萄糖、果糖、蔗糖等;还原糖是指具有还原性的糖,如葡萄糖、果糖等。
测定总糖的方法一般采用硫酸酚法,而测定还原糖的方法则是费林试剂法。
实验步骤:
1. 样品制备,将食品样品研磨成细粉,称取适量样品置于烘干器中,使其干燥后称取一定质量的样品备用。
2. 总糖的测定,取一定质量的样品,加入硫酸酚溶液,放入水浴中加热,再加入苯酚,用硫酸铜溶液滴定,记录滴定消耗的体积。
3. 还原糖的测定,取一定质量的样品,加入水和费林试剂,加热沸腾后立即加入硫酸,冷却后用蒸馏水定容至刻度线,用紫外分光光度计测定吸光度。
实验结果:
经过实验测定,得出样品中总糖的含量为10.5g/100g,还原糖的含量为
8.3g/100g。
实验分析:
通过对样品中总糖和还原糖的测定,可以了解到样品中糖的含量,为食品质量的评定提供了重要依据。
总糖的含量反映了食品的甜度,而还原糖的含量则反映了食品中具有还原性的糖的含量,对于不同类型的食品,其糖的含量也会有所不同。
实验总结:
通过本次实验,我们掌握了总糖和还原糖的测定方法和原理,了解了不同食品中糖的含量。
在实际生活中,我们可以通过这些方法对食品进行质量检测,保障食品安全和营养健康。
总糖和还原糖的测定实验报告到此结束。
苯酚-硫酸法
1. 原理
苯酚-硫酸法是利用多糖在硫酸的作用下先水解成单糖,并迅速脱水生成糖醛衍生物,然后与苯酚生成橙黄色化合物。
再以比色法测定。
2. 试剂
浓硫酸
6%苯酚:
先配置80%苯酚:80g苯酚(分析纯重蒸馏试剂)加20g水使之溶解,可置冰箱中避光长期储存。
再配置6%苯酚:取75ul的80%苯酚于烧杯中,加入960ul
水(每次测定均需现配)。
3. 操作步骤
(1) 制作标准曲线:准确称取标准葡聚糖(或葡萄糖)20mg于500ml容量瓶中,加水至刻度,分别吸取0.4、0.6、0.8、1.0、1.2、1.4、1.6及1.8ml,各以蒸馏水补至2.0ml,然后加入6%苯酚1.0ml及浓硫酸5.0ml,摇匀冷却,室温放置20分钟以后于490nm测光密度,以2.0ml水按同样显色操作为空白,横坐标为多糖微克数,纵坐标为光密度值,得标准曲线。
(2) 样品含量测定:
吸取1.0ml样品,补水至2.0ml,然后加入6%苯酚1.0ml及浓硫酸5.0ml,摇匀冷却室温放置30分钟以后于490nm测光密度。
每次测定取双样对照。
以标准曲线计算多糖含量。
注意事项:
1、苯酚是否重蒸、其溶液浓度、是否现配现用
2、加入硫酸后是否加热、显色时间的确定
3、所选波长:这个最为重要,因为已糖及其甲基化衍生物在490nm下有最大吸收峰,而戊糖、糠醛酸及其甲基化衍生物在480nm下有最大吸收峰。
如果阁下的多糖样品不是单一品而是数种混合(纯化也难一达到100%纯),则波长一定要扫描过再做
4、加浓硫酸前要摇匀,加之后也要摇匀。
(1)此法简单、快速、灵敏、重复性好,对每种糖仅制作一条标准曲线,颜色持久。
(2)制作标准线宜用相应的标准多糖,如用葡萄糖,应以校正系数0.9校正μg数。
(3)对杂多糖,分析结果可根据各单糖的组成比及主要组分单糖的标准曲线的校正系数加以校正计算
(4)测定时根据光密度值确定取样的量。
光密度值最好在0.1——0.3之间。
比如:小于0.1之下可以考虑取样品时取2克,仍取0.2ml样品液,如大于0.3可以减半取0.1ml的样品液测定。
(5)正常的反应溶液是深棕色。
糖越多颜色越深。
注意硫酸的纯度。
空白的颜色很深,说明你的空白中的苯酚被氧化了深红是醌(苯酚氧化生成)的颜色颜色过深的话说明苯酚的浓度过大。
操作的时候有几条你需要注意的,这些对你的检测结果影响极大
1、苯酚需要重蒸,配制的苯酚溶液需要妥善保存。
2、样品检测的时候,向样品中加了苯酚溶液需要迅速摇匀,加入硫酸基本操作:硫酸沿壁加,最好能旋转比色管,让硫酸能均匀的沿壁流下。
3、加完硫酸需要立即摇匀,前提是塞子要配套,不怕烫热、冷水浴,要准确。