高中化学竞赛有机部分讲义
- 格式:ppt
- 大小:1.29 MB
- 文档页数:39

第二节 胺一、分类和命名法定义:氨分子中的氢原子被氨基取代后所得到的化合物。
分类:根据氨分子中的一个、二个和三个氢原子被烃基取代分成伯胺(10胺)、仲胺(20胺)和叔胺(30胺)。
相当于氢氧化铵NH 4OH 和卤化铵NH 4X 的四个氢全被烃基取代所成的化合物叫做季铵碱和季铵盐。
NH 3 → R-NH 2 伯胺→ R 2NH 仲胺→ R 3N 叔胺NH 4OH → R 4NOH 季铵碱NH 4X → R 4NX 季铵盐根据氨基所连的烃基不同可分为脂肪胺(R-NH 2)和芳香胺(Ar-NH 2)。
根据氨基的数目又可分成一元胺和多元胺。
应当注意的是:1、伯、仲、叔胺与伯、仲、叔醇的分级依据不同。
胺的分级着眼于氮原子上烃基的数目;醇的分级立足于羟基所连的碳原子的级别。
例如叔丁醇是叔醇而叔丁胺属于伯胺。
叔丁醇 (30醇) 叔丁胺(10胺)2、要掌握氨、胺和铵的用法。
氨是NH 3。
氨分子从形式上去掉一个氢原子,剩余部分叫做氨基-NH 2,(去掉二个氢原子叫亚氨基=NH)。
氨分子中氢原子被烃基取代生成有机化合物的胺。
季铵类的名称用铵,表示它与NH 4的关系。
命名:对于简单的胺,命名时在“胺”字之前加上烃基的名称即可。
仲胺和叔胺中,当烃基相同时,在烃基名称之前加词头“二”或“三”。
例如:CH 3NH 2 甲胺 (CH 3)2NH 二甲胺 (CH 3)3N 三甲胺 C 6H 5NH 2 苯胺 (C 6H 5)2NH 二苯胺 (C 6H 5)3N 三苯胺而仲胺或叔胺分子中烃基不同时,命名时选最复杂的烃基作为母体伯胺,小烃基作为取代 基,并在前面冠以“N”,突出它是连在氮原子上。
例如:CH 3CH 2CH 2N (CH 3)CH 2CH 3 N-甲基-N-乙基丙胺(或甲乙丙胺)C 6H 5CH (CH 3)NHCH 3 N-甲基-1-苯基乙胺C 6H 5N (CH 3)2 N ,N-二甲基苯胺季铵盐和季铵碱,如4个烃基相同时,其命名与卤化铵和氢氧化铵的命名相似,称为卤化四某铵和氢氧化四某铵;若烃基不同时,烃基名称由小到大依次排列。


奥林匹克竞赛有机化学要义精讲一.有机物系统命名法根据IUPAC命名法及1980年中国化学学会命名原则,按各类化合物分述如下。
1.带支链烷烃主链选碳链最长、带支链最多者。
编号按最低系列规则。
从靠侧链最近端编号,如两端号码相同时,则依次比较下一取代基位次,最先遇到最小位次定为最低系统(不管取代基性质如何)。
例如,命名为2,3,5-三甲基己烷,不叫2,4,5-三甲基己烷,因2,3,5与2,4,5对比是最低系列。
取代基次序IUPAC规定依英文名第一字母次序排列。
我国规定采用立体化学中“次序规则”:优先基团放在后面,如第一原子相同则比较下一原子。
例如,称2-甲基-3-乙基戊烷,因—CH2CH3>—CH3,故将—CH3放在前面。
2.单官能团化合物主链选含官能团的最长碳链、带侧链最多者,称为某烯(或炔、醇、醛、酮、酸、酯、……)。
卤代烃、硝基化合物、醚则以烃为母体,以卤素、硝基、烃氧基为取代基,并标明取代基位置。
编号从靠近官能团(或上述取代基)端开始,按次序规则优先基团列在后面。
例如,3.多官能团化合物(1)脂肪族选含官能团最多(尽量包括重键)的最长碳链为主链。
官能团词尾取法习惯上按下列次序,—OH>—NH2(=NH)>C≡C>C=C如烯、炔处在相同位次时则给双键以最低编号。
例如,(2)脂环族、芳香族如侧链简单,选环作母体;如取代基复杂,取碳链作主链。
例如:(3)杂环从杂原子开始编号,有多种杂原子时,按O、S、N、P顺序编号。
例如:4.顺反异构体(1)顺反命名法环状化合物用顺、反表示。
相同或相似的原子或基因处于同侧称为顺式,处于异侧称为反式。
例如,(2)Z,E命名法化合物中含有双键时用Z、E表示。
按“次序规则”比较双键原子所连基团大小,较大基团处于同侧称为Z,处于异侧称为E。
次序规则是:(Ⅰ)原子序数大的优先,如I>Br>Cl>S>P>F>O>N>C>H,未共享电子对:为最小;(Ⅱ)同位素质量高的优先,如D>H;(Ⅲ)二个基团中第一个原子相同时,依次比较第二、第三个原子;(Ⅳ)重键分别可看作(Ⅴ)Z优先于 E,R优先于S。


有机化学第一讲高中化学竞赛有机化学第一讲高中化学竞赛第一课:基本有机化学概述一、有机化和物和有机化学的涵义有机化学是研究有机化合物的来源、制备、结构、性质、应用及相关理论和方法的科学。
它是化学的一个分支。
其研究对象是有机化合物。
什么是有机化合物呢?早期化学家将所有物质按其来源分为两类,人们把从生物体(植物或动物)中获得的物质定义为有机化合物,无机化合物则被认为是从非生物或矿物中得到的。
目前,绝大多数有机物不是从天然有机物中获得的,但由于历史和习惯之间的关系,“有机”一词仍然保留下来。
2、有机化合物的特性1。
成分和结构特征有机化合物:种类繁多、数目庞大(已知有七百多万种、且还在不但增加)但组成元素少(c,h,o,n,p,s,x等)原因:1)c原子自身相互结合能力强2)有很多种结合方式(单键、双键、三键、链、环)3)同分异构现象(构造异构、构型异构、构象异构)例如,c2h6o就可以代表乙醇和甲醚两种不同的化合物、2.物理特性1)高挥发性、低熔点和沸点2)水溶性差(大多不容或难溶于水,易溶于有机溶剂)3.化学性质方面的特点1)易燃烧2)热稳定性差,易热分解(许多化合物在200~300度下分解)3)反应速度慢4)反应复杂,副作用多三、有机化合物的分类1.按基本骨架分类(1)脂肪族化合物:分子中的碳原子相互结合形成碳链或碳环。
(2)芳香化合物:碳原子连接成特殊的芳香环。
(3)杂环化合物:这类化合物具有环状结构,但是组成环的原子除碳外,还有氧.硫.氮等其他元素的原子。
2.按官能团分类官能团是决定一类化合物主要性质的原子、原子团或特殊结构。
显然,含有相同官能团的有机化合物具有相似的化学性质。
常见的官能团及相应化合物的类别CC碳-碳双键烯烃碳碳叁键cc炔烃卤素原子―x卤代烃羟基―oh醇、酚醚基COC醚o醛、CHO羰基酮等co羧基羧酸椰酰化合物rc氨基氨硝基―no2硝基化合物磺酸基―so3h磺酸巯基sh硫醇、硫酚氰基CN腈四、有机化合物结构的表示方法凯库勒公式:扩展缩写hhhcccchcchhchch切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切切或键线式面向对象第二讲烷烃分子中只有C和H元素的有机化合物称为碳氢化合物由碳和氢两种元素组成的饱和烃称为烷烃。


第六章 醇、酚、醚醇和酚都含有相同的官能团羟基(-OH ),醇的羟基和脂肪烃、脂环烃或芳香烃侧链的碳原子相连。
而酚的羟基是直接连在芳环的碳原子上。
因此醇和酚的结构是不相同的,其性质也是不同的。
醇的通式为ROH ,酚的通式为ArOH 。
醚则可看作是醇和酚中羟基上的氢原子被烃基(-R 或-Ar )取代的产物,醚的通式为R-O-R 或Ar-O- Ar 。
第一节 醇一、醇的分类和命名醇分子可以根据羟基所连的烃基不同分为脂肪醇、脂环醇和芳香醇。
根据羟基所连的碳原子的不同类型分为伯醇、仲醇和叔醇。
根据醇分子中所含的羟基数目的不同可分为一元醇和多元醇。
结构简单的醇采用普通命名法,即在烃基名称后加一“醇”字。
如:CH 3CH 2OH (CH 3)2CHOH乙醇 异丙醇 苯甲醇(苄醇) 对于结构复杂的醇则采用系统命名法,其原则如下: 1、选择连有羟基的碳原子在内的最长的碳链为主链,按主链的碳原子数称为“某醇”。
2、从靠近羟基的一端将主链的碳原子依次用阿拉伯数字编号,使羟基所连的碳原子的位次尽可能小。
1、 命名时把取代基的位次、名称及羟基的位次写在母体名称“某醇”的前面。
如: 2,6-二甲基-3,5-二乙基-4-庚醇 1-乙基环戊醇2,6-二甲基-5-氯-3-庚醇2、 不饱和醇命名时应选择包括连有羟基和含不饱和键在内的最长的碳链做主链,从靠近羟基的一端开始编号。
例如:CH 2═CHCH 2CH 2OH 3-丁烯-1-醇6-甲基-3-环已烯醇3、 命名芳香醇时,可将芳基作为取代基加以命名。
例如:2-乙基-3-苯基-1-丁醇3-苯丙烯醇4、 多元醇的命名应选择包括连有尽可能多的羟基的碳链做主链,依羟基的数目称二醇、三醇等,并在名称前面标上羟基的位次。
因羟基是连在不同的碳原子上,所以当羟基CH 2OH CH 3OHCH 3CH 2CHCHCHCH 2CH 3CH CH CH 3CH 3CH 3CH 2CH 3OH Cl OH CH 3CH 3CH 3CHCHCH 2CHCHCH 3OH CH 3CH 3CH 2CH 3CH 2OH CH CH CH 2OH CH CH CH 2CH 2OH OH CH 2OH CH CH 2OH OH CH 2CH CH 3OH OH数目与主链的碳原子数目相同时,可不标明羟基的位次。
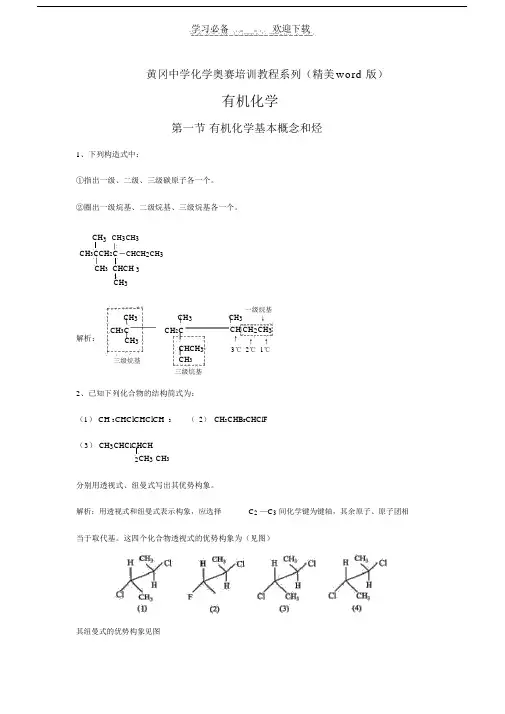
学习必备 欢迎下载黄冈中学化学奥赛培训教程系列(精美 word 版)有机化学第一节 有机化学基本概念和烃1、下列构造式中:①指出一级、二级、三级碳原子各一个。
②圈出一级烷基、二级烷基、三级烷基各一个。
CH 3 CH 3CH 3 CH 3CCH 2C CHCH 2CH 3CH 3 CHCH 3CH 3CH 3 CH 3 CH 3 一级烷基↓解析: CH 3CCH 2CCH CH 2CH 3CH 3CHCH 3↑ ↑ ↑3℃ 2℃ 1℃三级烷基CH 3三级烷基2、已知下列化合物的结构简式为: (1) CH 3CHClCHClCH 3 ( 2) CH 3CHBrCHClF( 3) CH 3CHClCHCH2CH 3 CH 3分别用透视式、纽曼式写出其优势构象。
解析:用透视式和纽曼式表示构象,应选择C 2 —C 3 间化学键为键轴,其余原子、原子团相当于取代基。
这四个化合物透视式的优势构象为(见图)其纽曼式的优势构象见图3、( 2000 年广东省模拟题)用烃 A 分子式为C10H16,将其进行臭氧化后,水解得到HCHO 和 A 催化加氢后得烃B, B 化学式为 C10H20,分子中有一个六元环,用键线式写出A,B 的结构。
解析:从 A 催化加氢生成的 B 的化学式可推知,原 A 分子中有两个C=C 键和一个六元环。
从水解产物可知, C1与 C6就是原碳环连接之处HCHO 的羰基,只能由C3支链上双键臭氧化水解生成。
所以 A 的结构为, B 的结构为。
4、下列化合物若有顺反异构,写出异构体并用顺、反及E、 Z 名称命名。
5、(河南省98 年竞赛题)写出符合C6H10的所有共轭二烯烃的异构体,并用E—Z命名法命名。
解析:6、用化学方法鉴别下列化合物:CH 3CH2CH2CH3,CH 3CH 2CH=CH 2, CH 3CH 2C≡ CH 。
解析:( 1)用 Br 2, CH 3CH 2CH=CH 2与 CH 3CH2 C≡ CH 可褪色, CH 3CH 2CH 2CH 3不反应。


高中化学竞赛讲义化学竞赛是一项旨在检验学生对化学知识和实验技能的综合能力的竞赛活动。
参加高中化学竞赛不仅可以提升学生的学科能力,还能促进学生的团队合作和创新思维。
本文将从理论知识、实验技能和应试技巧三个方面,为高中生参加化学竞赛提供详细的讲义。
一、理论知识在化学竞赛中,理论知识是考察的重点之一。
参加者需要熟悉化学元素周期表、化学键、化学反应、物质的性质等基础知识。
此外,对于一些常见的化学实验原理和操作方法也需要了解透彻。
1.1 元素周期表:元素周期表是化学竞赛的基础,参加者需要熟练掌握元素的周期性规律,理解元素周期表中各个区块的特点和规律,能够根据元素的位置和性质进行推理和分析。
1.2 化学键:化学键是物质中原子之间的连接方式,参加者需要了解共价键、离子键、金属键等不同类型的化学键的形成原理和特点,理解化学键的稳定性和反应性。
1.3 化学反应:化学反应是化学变化的过程,参加者需要熟悉常见的化学反应类型,掌握化学方程式的书写和平衡方法,能够根据反应条件和物质性质分析反应过程。
1.4 物质的性质:不同物质具有不同的性质,参加者需要了解物质的物理性质和化学性质,能够根据物质的性质进行分类和比较,推断物质的结构和性质。
二、实验技能实验技能是化学竞赛中的关键环节,参加者需要具备基本的实验操作能力和仪器使用技巧,能够准确、安全地进行化学实验,并获得准确的实验数据和结论。
2.1 实验操作:参加者需要掌握基本的实验室操作技能,包括溶液配制、试剂的使用和处理、仪器的操作等,保证实验过程的准确和规范。
2.2 仪器使用:化学实验通常需要借助各种仪器进行,参加者需要了解各种常见的化学实验仪器的使用原理和方法,掌握仪器的操作技巧,保证实验过程的顺利进行。
2.3 实验安全:化学实验存在一定的危险性,参加者需要了解常见的实验安全知识,遵守实验室的安全规定,正确使用个人防护装备,确保实验过程的安全性。
三、应试技巧除了理论知识和实验技能,参加者还需要具备一定的应试技巧,包括答题技巧、时间管理和心理调节等方面的技能。
2--烷烃所谓“烃”就是碳氢化合物(Hydrocarbon)的意思,它是一个有机化学专用的新字,“火”旁来自碳,表示它易着火,:“”来自氢。
碳氢两字读得快一些即成它的发音(听)。
烷烃是饱和烃。
饱和烃是含氢最多的烃。
烷(wan)有完满的意思,也就是饱和的意思。
§1. 烷烃的同系列和异构一、烷烃的同系列(Homologous series),n表示碳原子数目。
最简单的烷烃是甲烷,其次是烷烃的通式为:C nn2乙烷、丙烷……,凡具有同一个通式,结构相似,化学性质也相似,物理性质则随着碳原子数目的增加而有规律地变化的化合物系列,称为同系列。
同系列中的化合物互称为同系物(Homologs)。
相邻的同系物在组成上相差CH2,这个CH2称为系列差。
1.烷烃的同分异构现象烷烃同系列中,甲烷、乙烷、丙烷只有一种结合方式,没有异构现象,从丁烷起就有同分异构现象。
分子中碳原子的排列方式不同。
我们把分子式相同,而构造不同的异构体称为构造异构体。
实质上是由于碳干构造的不同而产生的,所以往往又称为碳干异构体。
(Skeletal isomer)在烷烃分子中随着碳原子数的增加,异构体的数目增加得很快。
对于低级烷烃的同分异构体的数目和构造式,可利用碳干不同推导出来。
以己烷为例其基本步骤如下:(1)写出这个烷烃的最长直链式:(省略了氢)(2)写出少一个碳原子的直链式作为主链把剩下的碳当作支链。
依次当取代基连在各碳原子上,就能写出可能的同分异构体的构造式。
(3)写出少二个碳原子的直链式作为主链。
把两个碳原子当作支链(2个甲基),连接在各碳原子上,或把两个碳原子当作(乙基),接在各碳上。
把重复者去掉。
这样己烷的同分异构体只有5个。
书写构造式时,常用简化的式子为:CH3CH2CH2CH2CH3或CH3(CH2)4CH3。
(4)伯、仲、叔和季碳原子。
如戊烷的三个同分异构体为:我们把直接与一个碳原子相连的称为“伯”(Primary)或一级碳原子,用1o表示;直接与二个碳原子相连的称为“仲”(Secondary)或二级碳原子,用2o表示;直接与三个碳原子相连的称为“叔”(Tertary)或三级碳原子,用3o表示;直接与四个碳原子相连的称为“季”(Quaternary)或四级碳原子,用4o表示;在伯、仲、叔碳上的氢分别叫伯、仲、叔氢。
高中化学竞赛大学有机化学课件6(附加条款版)高中化学竞赛大学有机化学课件6一、引言化学竞赛作为高中阶段学生提高化学素养、培养化学思维的重要途径,一直受到广泛关注。
有机化学作为化学竞赛的重要组成部分,对于参赛选手来说至关重要。
本课件旨在帮助高中化学竞赛选手更好地掌握大学有机化学知识,提高竞赛成绩。
二、有机化学基本概念1.有机化合物:含有碳元素的化合物,通常与生命活动密切相关。
2.有机反应:有机化合物在一定条件下发生的化学变化,包括合成、分解、取代、加成等。
3.有机化合物结构:碳原子之间的成键方式,包括单键、双键、三键以及环状结构等。
4.有机化合物的分类:根据分子结构、官能团、反应类型等不同特点进行分类。
三、有机化学基本反应1.烷烃的卤代反应:烷烃与卤素单质在光照条件下发生取代反应,卤代烷。
2.烯烃的加成反应:烯烃与卤素单质、水、卤化氢等发生加成反应,卤代烷、醇等化合物。
3.炔烃的加成反应:炔烃与卤素单质、水、卤化氢等发生加成反应,卤代烷、醛、羧酸等化合物。
4.醇的氧化反应:醇在酸性条件下与氧化剂如酸性高锰酸钾、铬酸等反应,醛、酮等化合物。
5.醛、酮的还原反应:醛、酮与还原剂如氢气、锂铝氢化剂等反应,醇。
6.羧酸的酯化反应:羧酸与醇在酸性条件下反应,酯。
7.芳香烃的取代反应:芳香烃在一定条件下与取代基发生取代反应,取代芳香烃。
四、有机化学合成策略1.反应途径的选择:根据目标产物的结构特点,选择合适的反应途径。
2.反应条件的优化:通过调整反应温度、压力、催化剂等条件,提高反应产率和选择性。
3.保护基的应用:在合成过程中,通过引入保护基,保护敏感官能团,提高反应可控性。
4.反应顺序的安排:合理安排反应顺序,避免不必要的副反应,提高合成效率。
五、有机化学竞赛实例分析1.合成题目分析:分析题目所给的反应物和产物,确定反应类型和合成路线。
2.反应机理探讨:根据反应类型,推导反应机理,理解反应过程。
3.实验操作注意事项:分析实验操作步骤,注意实验安全,提高实验技能。