乙醇水溶液物理特性比热密度粘度等
- 格式:docx
- 大小:295.63 KB
- 文档页数:7

乙醇的知识点总结一、结构乙醇的分子式为C2H5OH,其结构式为CH3CH2OH。
由于乙醇分子中含有羟基(—OH)它既具有醇的性质,又具有醚的性质,因此在化学性质上介于醇和醚之间。
乙醇的分子式中,氧原子与碳原子连接,共用了一个电子,形成一个共价键。
二、性质1. 物理性质乙醇是一种无色透明液体,有刺激性的气味,呈甘甜味,密度为0.789g/cm3,相对分子质量为46.07。
乙醇熔点为-114.14℃,沸点为78.24℃,可溶于水、乙醚、液体酮等有机物,但不溶于石油醚。
2. 化学性质乙醇是一种两性物质,在水中呈微弱的碱性,是一种良好的溶剂。
在氧气存在下,乙醇可以被氧化成乙醛,然后进一步被氧化成乙酸。
另外,乙醇也可以发生酯化反应,与酸酐反应生成酯类。
三、制备方法乙醇工业生产主要有合成法和发酵法两种方法:1. 合成法合成法是从石油煤炭等原料中生产乙醇的一种主要方法。
其中最为常用的方法是乙烯直接水合生成乙醇。
此法是利用水来加成乙烯中的双键,得到乙醇的方法。
此法具有操作简单、反应温度低、不需要能的特点。
2. 发酵法发酵法是指利用植物类生物质资源作为原料进行发酵酒精制备。
主要包括淀粉、果糖、麦芽糖、蔗糖或者纤维素等废渣等。
其中淀粉、果糖等可在酵母菌的催化下生产乙醇,而蔗糖和甜菜糖的水解物生产乙醇的方法。
四、应用1. 化工行业乙醇主要用作有机合成原料,可制取酯类,也可以用于合成脂肪醇、杀菌剂、润滑油、生成柔软剂和除油剂等。
此外,它还可作燃料、溶剂、原料等。
2. 食品工业乙醇在食品工业中主要用作增稠剂、香料及溶剂等。
在酒的生产中,餐饮业中,地道食品生产中也可以发挥其独特的作用。
3. 医药行业乙醇在医药行业中用于麻醉剂及用作杀菌剂。
近年来也存在为食物净化而使用的情形。
4. 古董保存用乙醇浸泡保存古董可以杀菌消毒及保持古董原样。
五、环境影响1. 乙醇的毒性乙醇对人体有一定的毒性。
当摄入过量乙醇会造成中枢神经系统的抑制。

乙醇的物理特征是什么原理乙醇是一种无色、易燃液体,具有特殊的物理特征。
下面将详细介绍乙醇的物理特征以及其背后的原理。
首先,乙醇的物理特征之一是其沸点和熔点相对较低。
乙醇的沸点为78.5摄氏度,熔点为-114.1摄氏度。
这是因为乙醇分子之间通过氢键进行相互作用。
氢键是一种弱的化学键,通常在分子间的电负性较高的原子(如氧、氮等)与氢原子之间形成。
乙醇分子中的氧原子与氢原子形成氢键,使得分子间的吸引力增强。
这种氢键相互作用的强度较弱,使得需要较低的能量用于克服分子间的吸引力,从而使乙醇分子比较容易从液体相变成气体相,即沸腾。
其次,乙醇具有较高的蒸汽压。
蒸汽压是指液体分子的逸出速率与液体表面上气体分子的逸出速率之间的动态平衡。
一般来说,温度越高,液体分子的平均动能越大,逸出速率也越快,从而蒸汽压越大。
乙醇分子之间的氢键相互作用较弱,因此分子间的吸引力较小,液体分子逸出速率较高,乙醇的蒸汽压相对较大。
这也是为什么乙醇能够在室温下迅速挥发。
此外,乙醇的密度相对较小,约为0.789 g/cm³。
密度是指物质单位体积内的质量。
乙醇分子由碳、氢、氧原子组成,相对分子质量为46.07 g/mol。
乙醇的分子量相对较小,使得单位体积内的分子数量也相对较多,从而导致乙醇的密度较小。
乙醇同时也具有一定的表面张力。
表面张力是指液体表面上分子间互相吸引产生的张力。
乙醇分子之间通过氢键相互吸引,因此在液体表面上形成一层较为稳定的分子层。
这种分子层使得液体表面的分子比内部分子间的吸引力更强,导致液体表面收缩,形成球状或凸面。
这就是为什么水珠在表面上形成球状,而不是扁平。
最后,乙醇的溶解性较好。
乙醇是一种亲水性溶剂,与水分子之间可以通过氢键形成相互作用。
由于乙醇分子具有氧原子,可以与水分子的氧原子形成氢键。
这种氢键相互作用使得乙醇可以溶解在水中,同时也使得乙醇可以溶解许多极性或部分极性的物质,如醛、酮、脂肪酸等。
然而,乙醇与非极性物质的相容性较差。

乙醇的结构简式为CH3CH2OH,俗称酒精、无水酒精、火酒、无水乙醇。
乙醇的用途很广,可用乙醇来制造醋酸、饮料、香精、染料、燃料等。
医疗上也常用体积分数为70%——75%的乙醇作消毒剂等。
乙醇的物性数据:1.性状:无水透明、易燃易挥发液体。
有酒的气体和刺激性辛辣味。
2. 密度:0.78945g/cm^3; (液) 20°C3. 熔点:-114.3 °C (158.8 K)4. 沸点:78.4 °C (351.6 K)5. 在水中溶解时:p Ka =15.96. 黏度:1.200 mpa·s(cp),20.0 °C7. 分子偶极矩:5.64 fC·fm (1.69 D) (气)8. 折光率:1.36149. 相对密度(水=1): 0.7910.相对蒸气密度(空气=1): 1.5911.饱和蒸气压(kPa): 5.33(19℃)12.燃烧热(kJ/mol): 1365.513.临界温度(℃): 243.114.临界压力(MPa): 6.13715.辛醇/水分配系数的对数值: 0.3216.闪点(℃,开口): 16.017.闪点(℃,闭口): 14.018.引燃温度(℃): 36319.爆炸上限%(V/V): 19.020.爆炸下限%(V/V): 3.321.燃点(℃):390~43022.蒸发热:(kJ/mol,b.p):38.9523.熔化热:(kJ/kg) :104.724.生成热:(kJ/mol,液体):-277.825.比热容:(kJ/(kg·k),20°C,定压):2.4226.沸点上升常数:1.03~1.0927.电导率(s/m):1.35×10-1928.热导率(w/(m·k)):18.0029.体膨胀系数(k-1, 20°C):0.0010830.气相标准燃烧热(kJ/mol):1410.0131.气相标准声称热(kJ/mol):-234.0132.气相标准熵(J/mol·k):280.6433.气相标准生成自由能(kJ/mol):-166.734.气相标准热熔(J/mol·k):65.2135. 液相标准燃烧热(kJ/mol):-1367.5436.液相标准声称热(kJ/mol):-276.9837. 液相标准熵(J/mol·k):161.0438.液相标准生成自由能(kJ/mol):-174.1839.液相标准热熔(J/mol·k):112.6乙醇生态学数据:乙醇蒸汽对眼和呼吸道粘膜有轻微的刺痛作用。

一.乙醇的物理性质乙醇液体密度是0.789g/cm?,乙醇气体密度为1.59kg/m?,相对密度(d15.56)0.816,式量(相对分子质量)为46.07g/mol。
沸点是78.2℃,14℃闭口闪点,熔点是-114.3℃。
纯乙醇是无色透明的液体,有特殊香味,易挥发。
乙醇的物理性质主要与其低碳直链醇的性质有关。
分子中的羟基可以形成氢键,因此乙醇黏性大,也不及相近相对分子质量的有机化合物极性大。
[2]20℃下,乙醇的折射率为1.3611。
溶解性能与水以任意比互溶;可混溶于醚、氯仿、甲醇、丙酮、甘油等多数有机溶剂。
潮解性由于存在氢键,乙醇具有较强的潮解性,可以很快从空气中吸收水分。
羟基的极性也使得很多离子化合物可溶于乙醇中,如氢氧化钠、氢氧化钾、氯化镁、氯化钙、氯化铵、溴化铵和溴化钠等;但氯化钠和氯化钾微溶于乙醇。
此外,其非极性的烃基使得乙醇也可溶解一些非极性的物质,例如大多数香精油和很多增味剂、增色剂和医药试剂。
二.乙醇用途可用乙醇制造醋酸、饮料、香精、染料、燃料等。
医疗上也常用体积分数为70%~75%的乙醇作消毒剂等,在国防化工、医疗卫生、食品工业、工农业生产中都有广泛的用途。
三.乙醇主要种类1、按生产使用的原料可分为淀粉质原料发酵酒精、糖蜜原料发酵酒精、亚硫酸盐纸浆废液发酵生产酒精。
淀粉质原料发酵酒精(一般有薯类、谷类和野生植物等含淀粉质的原料,在微生物作用下将淀粉水解为葡萄糖,再进一步由酵母发酵生成酒精);糖蜜原料发酵酒精(直接利用糖蜜中的糖分,经过稀释杀菌并添加部分营养盐,借酵母的作用发酵生成酒精);亚硫酸盐纸浆废液发酵生产酒精(利用造纸废液中含有的六碳糖,在酵母作用下发酵成酒精,主要产品为工业用酒精。
也有用木屑稀酸水解制作的酒精)。
2、按生产的方法来分,可分为发酵法、合成法两大类。
3、按产品质量或性质来分,又分为高纯度酒精、无水酒精、普通酒精和变性酒精。
4、按产品系列(BG384-81)分为优级、一级、二级、三级和四级。
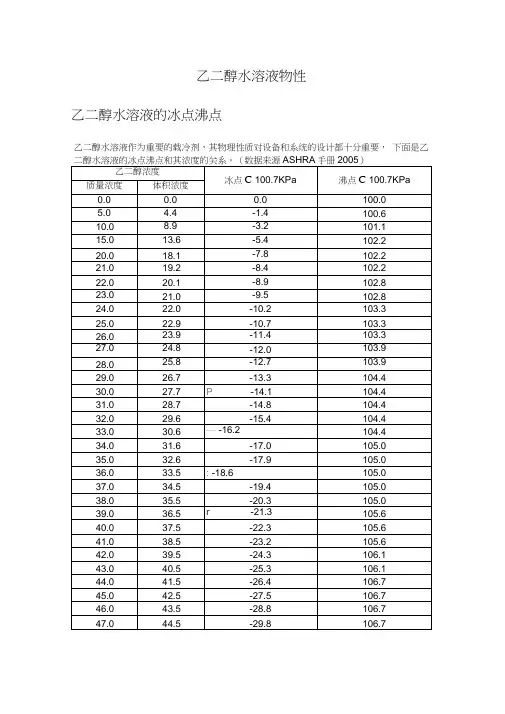
乙二醇水溶液物性
乙二醇水溶液的冰点沸点
乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要,下面是乙
乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要,下面是乙
乙二醇水溶液的密度
乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要, 下面是乙二醇水溶液的密度(kg/m3)和其浓度的关系。
(数据来源ASHRA手册
乙二醇水溶液的比热
乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要,下面是乙
乙二醇水溶液导热系数
乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要,
下面是乙二醇水溶液的导热系数(W/m.K)和其浓度的关系。
(数据来源ASHRAE 手册2005)。

乙醇的物理常数乙醇的物理常数:一、性质外观与性状:无色液体,有特殊香味.密度:0.789 g/cm^3; (液)熔点:117.3 °C (158.8 K)沸点:78.3 °C (351.6 K)在水中的溶解度:pKa 15.9黏度:1.200 mPa·s (cP),20.0 °C分子偶极矩:5.64 fC·fm (1.69 D) (气)折射率:1.3614相对密度(水=1):0.79相对蒸气密度(空气=1):1.59饱和蒸气压(kPa):5.33(19℃)燃烧热(kJ/mol):1365.5临界温度(℃):243.1临界压力(MPa):6.38辛醇/水分配系数的对数值:0.32闪点(℃):12引燃温度(℃):363爆炸上限%(V/V):19.0爆炸下限%(V/V):3.3溶解性:与水混溶,可混溶于醚、氯仿、甘油等多数有机溶剂.电离性:非电解质无色、透明,具有特殊香味的液体(易挥发),密度比水小,能跟水以任意比互溶(一般不能做萃取剂).是一种重要的溶剂,能溶解多种有机物和无机物.二、物理性质乙醇的物理性质主要与其低碳直链醇的性质有关.分子中的羟基可以形成氢键,因此乙醇黏度[1]很大,也不及相近相对分子质量的有机化合物极性大.室温下,乙醇是无色易燃,且有特殊香味的挥发性液体.λ=589.3nm和18.35°C下,乙醇的折射率为1.36242,比水稍高.作为溶剂,乙醇易挥发,且可以与水、乙酸、丙酮、苯、四氯化碳、氯仿、乙醚、乙二醇、甘油、硝基甲烷、吡啶和甲苯等溶剂混溶.此外,低碳的脂肪族烃类如戊烷和己烷,氯代脂肪烃如1,1,1-三氯乙烷和四氯乙烯也可与乙醇混溶.随着碳数的增长,高碳醇在水中的溶解度明显下降.由于存在氢键,乙醇具有潮解性,可以很快从空气中吸收水分.羟基的极性也使得很多离子化合物可溶于乙醇中,如氢氧化钠、氢氧化钾、氯化镁、氯化钙、氯化铵、溴化铵和溴化钠等.氯化钠和氯化钾则微溶于乙醇.此外,其非极性的烃基使得乙醇也可溶解一些非极性的物质,例如大多数香精油和很多增味剂、增色剂和医药试剂.。

乙醇的物理性质知识点内容乙醇分子是由是由C、H、O 三种原子构成(乙基和羟基两部分组成),可以看成是乙烷分子中的一个氢原子被羟基取代的产物,也可以看成是水分子中的一个氢原子被乙基取代的产物。
下面给大家带来一些关于乙醇的物理性质知识内容,希望对大家有所帮助。
一.乙醇的物理性质乙醇液体密度是0.789g/cm?,乙醇气体密度为1.59kg/m?,相对密度(d15.56)0.816,式量(相对分子质量)为46.07g/mol。
沸点是78.2℃,14℃闭口闪点,熔点是-114.3℃。
纯乙醇是无色透明的液体,有特殊香味,易挥发。
乙醇的物理性质主要与其低碳直链醇的性质有关。
分子中的羟基可以形成氢键,因此乙醇黏性大,也不及相近相对分子质量的有机化合物极性大。
[2]20℃下,乙醇的折射率为1.3611。
溶解性能与水以任意比互溶;可混溶于醚、氯仿、甲醇、丙酮、甘油等多数有机溶剂。
潮解性由于存在氢键,乙醇具有较强的潮解性,可以很快从空气中吸收水分。
羟基的极性也使得很多离子化合物可溶于乙醇中,如氢氧化钠、氢氧化钾、氯化镁、氯化钙、氯化铵、溴化铵和溴化钠等;但氯化钠和氯化钾微溶于乙醇。
此外,其非极性的烃基使得乙醇也可溶解一些非极性的物质,例如大多数香精油和很多增味剂、增色剂和医药试剂。
二.乙醇用途可用乙醇制造醋酸、饮料、香精、染料、燃料等。
医疗上也常用体积分数为70%~75%的乙醇作消毒剂等,在国防化工、医疗卫生、食品工业、工农业生产中都有广泛的用途。
三.乙醇主要种类1、按生产使用的原料可分为淀粉质原料发酵酒精、糖蜜原料发酵酒精、亚硫酸盐纸浆废液发酵生产酒精。
淀粉质原料发酵酒精(一般有薯类、谷类和野生植物等含淀粉质的原料,在微生物作用下将淀粉水解为葡萄糖,再进一步由酵母发酵生成酒精);糖蜜原料发酵酒精(直接利用糖蜜中的糖分,经过稀释杀菌并添加部分营养盐,借酵母的作用发酵生成酒精);亚硫酸盐纸浆废液发酵生产酒精(利用造纸废液中含有的六碳糖,在酵母作用下发酵成酒精,主要产品为工业用酒精。

乙醇的结构简式为CH3CH2OH,俗称酒精、无水酒精、火酒、无水乙醇。
乙醇的用途很广,可用乙醇来制造醋酸、饮料、香精、染料、燃料等。
医疗上也常用体积分数为70%——75%的乙醇作消毒剂等。
乙醇的物性数据:1.性状:无水透明、易燃易挥发液体。
有酒的气体和刺激性辛辣味。
2. 密度:0.78945g/cm^3; (液) 20°C3. 熔点:-114.3 °C (158.8 K)4. 沸点:78.4 °C (351.6 K)5. 在水中溶解时:p Ka =15.96. 黏度:1.200 mpa·s(cp),20.0 °C7. 分子偶极矩:5.64 fC·fm (1.69 D) (气)8. 折光率:1.36149. 相对密度(水=1): 0.7910.相对蒸气密度(空气=1): 1.5911.饱和蒸气压(kPa): 5.33(19℃)12.燃烧热(kJ/mol): 1365.513.临界温度(℃): 243.114.临界压力(MPa): 6.13715.辛醇/水分配系数的对数值: 0.3216.闪点(℃,开口): 16.017.闪点(℃,闭口): 14.018.引燃温度(℃): 36319.爆炸上限%(V/V): 19.020.爆炸下限%(V/V): 3.321.燃点(℃):390~43022.蒸发热:(kJ/mol,b.p):38.9523.熔化热:(kJ/kg) :104.724.生成热:(kJ/mol,液体):-277.825.比热容:(kJ/(kg·k),20°C,定压):2.4226.沸点上升常数:1.03~1.0927.电导率(s/m):1.35×10-1928.热导率(w/(m·k)):18.0029.体膨胀系数(k-1, 20°C):0.0010830.气相标准燃烧热(kJ/mol):1410.0131.气相标准声称热(kJ/mol):-234.0132.气相标准熵(J/mol·k):280.6433.气相标准生成自由能(kJ/mol):-166.734.气相标准热熔(J/mol·k):65.2135. 液相标准燃烧热(kJ/mol):-1367.5436.液相标准声称热(kJ/mol):-276.9837. 液相标准熵(J/mol·k):161.0438.液相标准生成自由能(kJ/mol):-174.1839.液相标准热熔(J/mol·k):112.6乙醇生态学数据:乙醇蒸汽对眼和呼吸道粘膜有轻微的刺痛作用。

工业乙醇的物理常数表
工业乙醇是一种常见的有机化合物,具有广泛应用的价值。
在工业生产过程中,工业乙醇的物理常数具有重要的参考价值。
下面是工业乙醇的物理常数表:
一、密度相关常数
1.密度:0.787-0.789 g/cm³(20℃)
2.比重:0.789 (20℃/水)
3.平均速度:213.5 m/s
二、蒸汽压相关常数
1.蒸汽压:5.95 kPa (20℃)
2.饱和蒸汽压:5.95 kPa (20℃)
3.活泼度:1.00
三、热力学相关常数
1.热值:29.7 MJ/kg
2.热容:2.44 J/g·K (25℃)
3.热导率:0.1651 W/m·K (25℃)
4.粘度:1.2 mPa·s (20℃)
5.表面张力:22.39 mN/m (20℃)
四、其他常数
1.溶解性:在水中易溶,在乙醚、乙酸、苯等有机溶剂中不易溶解。
2.相对介电常数:24.5 (20℃)
3.凝固点:-11
4.1℃
4.熔点:-114.3℃
以上是工业乙醇的物理常数表,这些常数对于工业生产和应用过程中的计算和评估都非常重要。
同时也可以为研究和开发新的应用提供基础数据支持。

乙二醇水溶液物理特性(比热、密度、粘度等)乙二醇水溶液物性乙二醇水溶液的冰点沸点乙二醇浓度质量浓度体积浓度0.00.05.04.410.08.915.013.620.018.121.019.222.020.123.021.024.022.025.022.926.023.927.024.828.025.829.026.730.027.731.028.732.029.633.030.634.031.635.032.636.033.537.034.538.035.539.036.540.037.541.038.542.039.543.040.544.041.545.042.546.043.547.044.5冰点℃100.7KPa 0.0-1.4-3.2-5.4-7.8-8.4-8.9-9.5-10.2-10.7-11.4-12.0-12.7-13.3-14.1-14.8-15.4-16.2-17.0-17.9-18.6-19.4-20.3-21.3-22.3-23.2-24.3-25.3-26.4-27.5-28.8-29.8沸点℃100.7KPa 100.0100.6101.1102.2102.2102.2102.8 102.8 103.3 103.3 103.3 103.9 103.9 104.4 104.4 104.4 104.4 104.4 105.0 105.0 105.0 105.0 105.0 105.6 105.6 105.6106.1 106.1 106.7 106.7 106.7 106.748.049.050.051.052.053.054.055.056.057.058.059.060.0 65.070.0 75.0 80.0 85.0 90.0 95.045.546.547.648.649.650.651.652.753.754.755.756.857.8 62.868.3 73.6 78.9 84.3 89.7 95.0 -31.1 -32.6 -33.8 -35.1 -36.4 -37.9 -39.3 -41.1 -42.6 -44.2 -45.6 -47.1 -48.3 -46.8-36.9 -29.8 -19.4 106.7 106.7 107.2 107.2 107.2 107.8 107.8 108.3 108.3 108.9 108.9 109.4 110.0 112.8 116.7 120.0 123.9133.9140.6158.3乙二醇水溶液粘度温度℃乙二醇水溶液浓度(体积浓度)10%20%30%40%50%–3566.93–3043.98–2530.5–2015.7522.07–1511.7416.53–106.199.0612.74-53.655.037.1810.052.083.024.155.838.0951.792.543.484.826.63101.562.182.954.045.5151.371.892.533.444.63201.211.652.22.963.94251.081.461.922.573.3960% 93.44 65.25 46.75 34.28 25.69 19.62 15.25 12.05 9.66 7.85 6.46 5.38 4.52 70% 133.53 96.57 70.38 51.94 38.8829.53 22.76 17.79 14.09 11.31 9.18 7.53 6.24 80% 191.09 141.02 102.21 74.53 55.09 41.36 31.56 24.44 19.2 15.29 12.3310.05 8.29 90% 196.87 128.43 87.52 61.85 45.08 33.74 25.84 20.18 16.04 12.95 10.5930 35404550556065 70 75 80 85 90 95 100 105 110 115 120 125 0.97 0.88 0.8 0.73 0.67 0.62 0.570.53 0.5 0.47 0.44 0.41 0.39 0.37 0.35 0.33 0.32 0.3 0.290.281.3 1.17 1.06 0.96 0.88 0.81 0.740.69 0.64 0.59 0.55 0.52 0.49 0.46 0.43 0.4 0.38 0.36 0.340.331.69 1.5 1.34 1.21 1.09 0.99 0.90.83 0.76 0.7 0.65 0.6 0.56 0.52 0.49 0.46 0.43 0.41 0.38 0.36 2.26 1.99 1.77 1.59 1.43 1.29 1.171.06 0.97 0.89 0.82 0.76 0.7 0.65 0.6 0.56 0.53 0.49 0.46 0.432.94 2.56 2.26 2 1.78 1.59 1.431.29 1.17 1.07 0.98 0.89 0.82 0.76 0.7 0.65 0.6 0.56 0.53 0.49 3.84 3.292.84 2.47 2.16 1.91 1.691.51 1.35 1.22 1.1 1 0.92 0.84 0.77 0.71 0.66 0.61 0.57 0.53 5.23 4.42 3.76 3.232.8 2.43 2.131.88 1.67 1.49 1.33 1.2 1.09 0.99 0.9 0.82 0.76 0.7 0.64 0.6 6.9 5.79 4.91 4.19 3.61 3.122.722.39 2.11 1.87 1.66 1.49 1.34 1.21 1.1 1 0.91 0.83 0.77 0.71 8.77 7.34 6.21 5.3 4.563.95 3.453.032.672.372.121.91.711.541.41.271.161.070.980.9乙二醇水溶液的密度温度℃-35-30-25-20-15-10-55101520251018.731017.571016.281014.871013.341011.69乙二醇水溶液浓度(体积浓度)10%1036.851035.671034.361032.941031.39 1029.72 1027.93 20% 1054.31 1053.11 1051.78 1050.33 1048.76 1047.07 1045.25 1043.32 30% 1071.98 1070.87 1069.63 1068.28 1066.80 1065.21 1063.491061.65 1059.68 1057.60 40%50% 1089.94 1089.04 1088.01 1086.87 1085.61 1084.22 1082.71 1081.08 1079.33 1077.46 1075.46 1073.35 1071.11 60% 1104.60 1103.541102.36 1101.06 1099.64 1098.09 1096.43 1094.64 1092.73 1090.70 1088.54 1086.27 1083.87 70% 1118.61 1117.38 1116.04 1114.58 1112.99 1111.28 1109.45 1107.501105.43 1103.23 1100.92 1098.48 1095.92 80% 1132.11 1130.72 1129.21 1127.57 1125.82 1123.94 1121.94 1119.82 1117.58 1115.22 1112.73 1110.13 1107.40 1141.871140.07 1138.14 1136.09 1133.91 1131.62 1129.20 1126.67 1124.01 1121.23 1118.32 90% 3035404550556065707580859095100 105 110 115 120 125 1009.92 1008.02 1006.01 1003.87 1001.61 999.23 996.72 994.10 991.35988.49 985.50 982.39 979.15 975.80 972.32 968.73 965.01 961.17 957.21 953.12 1026.02 1023.99 1021.83 1019.55 1017.16 1014.64 1011.99 1009.23 1006.351003.34 1000.21 996.96 993.59 990.10 986.48 982.75 978.89 974.91 970.81 966.59 1041.26 1039.08 1036.78 1034.36 1031.81 1029.15 1026.36 1023.45 1020.421017.27 1014.00 1010.60 1007.09 1003.45 999.69 995.81 991.81 987.68 983.43 979.07 1055.39 1053.07 1050.62 1048.05 1045.35 1042.54 1039.61 1036.55 1033.371030.07 1026.65 1023.10 1019.44 1015.65 1011.74 1007.71 1003.56 999.29 994.90 990.38 1068.75 1066.27 1063.66 1060.94 1058.09 1055.13 1052.04 1048.83 1045.041042.04 1038.46 1034.77 1030.95 1027.01 1022.95 1018.76 1014.46 1010.03 1005.48 1000.81 1081.35 1078.71 1075.95 1073.07 1070.06 1066.94 1063.69 1060.32 1056.831053.22 1049.48 1045.63 1041.65 1037.55 1033.33 1028.99 1024.52 1019.94 1015.23 1010.40 1093.24 1090.43 1087.51 1084.46 1081.30 1078.01 1074.60 1071.06 1067.411063.64 1059.74 1055.72 1051.58 1047.32 1042.93 1038.43 1033.80 1029.05 1024.18 1019.19 1104.55 1101.58 1098.48 1095.27 1091.93 1088.48 1084.90 1081.20 1077.371073.43 1069.36 1065.18 1060.87 1056.44 1051.88 1047.21 1042.41 1037.46 1032.46 1027.30 1115.30 1112.15 1108.89 1105.50 1101.99 1098.36 1094.60 1090.73 1086.731082.611078.371074.011069.531064.921060.201055.351050.381045.291040.081034.74乙二醇水溶液的比热乙二醇水溶液作为紧张的载冷剂,其物理性子对装备和体系的设想都非常紧张,上面是乙二醇水溶液的比热(kJ/kg.K)和其浓度的干系。

酒精的物理化学性质乙醇俗称酒精,是一种有机物,结构简式CHCHOH或CHOH,分子式CHO,是最常见的一元醇。
紧接着我们为你整理了酒精的物理化学性质,一起来看看吧。
酒精的物理性质溶解性能与水以任意比互溶;可混溶于醚、氯仿、甲醇、丙酮、甘油等多数有机溶剂。
无色透明液体,有特殊香味,易挥发。
相对密度0.816。
乙醇液体密度是0.789g/cm,乙醇气体密度为1.59kg/m,沸点是78.4℃,熔点是-114.3℃。
易燃,其蒸气能与空气形成爆炸性混合物,能与水以任意比互溶。
乙醇是一种非常不错的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分;也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提升反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相中充分接触,加快反应速率。
乙醇的物理性质主要与其低碳直链醇的性质有关。
分子中的羟基可以形成氢键,因此乙醇黏性大,也不及相近相对分子水平的有机化合物极性大。
室温下,乙醇是无色、易燃、有特殊香味的挥发性液体。
=589.3nm和18.35℃下,乙醇的折射率为1.36242,比水稍高。
挥发性作为溶剂,乙醇易挥发,且可以与水、乙酸、丙酮、苯、四氯化碳、氯仿、乙醚、乙二醇、甘油、硝基甲烷、吡啶和甲苯等溶剂混溶。
此外,低碳的脂肪族烃类如戊烷和己烷,氯代脂肪烃如1,1,1-三氯乙烷和四氯乙烯也可与乙醇混溶。
潮解性由于存在氢键,乙醇具有潮解性,可以很快从空气中吸收水分。
羟基的极性也使得大量离子化合物可溶于乙醇中,如氢氧化钠、氢氧化钾、氯化镁、氯化钙、氯化铵、溴化铵和溴化钠等。
氯化钠和氯化钾则微溶于乙醇。
此外,其非极性的烃基使得乙醇也可溶解一些非极性的物质,例如大部分香精油和大量增味剂、增色剂和医药试剂。
乙醇溶液密度每含有乙醇水平g浓度(体积比%)=度含有乙醇重量g浓度(体积比%)=度例如:密度为0.791g/cm每含有乙醇重量:0.79199.5%=0.787045g浓度:99.7%=99.7度酒精的化学性质酸碱性酸性乙醇的各种化学式乙醇分子中含有极化的氧氢键,电离时生成烷氧基负离子和质子。
乙二醇水溶液物性乙二醇水溶液的冰点沸点乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要,下面是乙二醇水溶液的冰点沸点和其浓度的关系。
(数据来源ASHRAE手册2005)乙二醇浓度冰点℃ 100.7KPa沸点℃ 100.7KPa 质量浓度体积浓度0.00.00.0100.05.0 4.4-1.4100.610.08.9-3.2101.115.013.6-5.4102.220.018.1-7.8102.221.019.2-8.4102.222.020.1-8.9102.823.021.0-9.5102.824.022.0-10.2103.325.022.9-10.7103.326.023.9-11.4103.327.024.8-12.0103.928.025.8-12.7103.929.026.7-13.3104.430.027.7-14.1104.431.028.7-14.8104.432.029.6-15.4104.433.030.6-16.2104.434.031.6-17.0105.035.032.6-17.9105.036.033.5-18.6105.037.034.5-19.4105.038.035.5-20.3105.039.036.5-21.3105.640.037.5-22.3105.641.038.5-23.2105.642.039.5-24.3106.143.040.5-25.3106.144.041.5-26.4106.745.042.5-27.5106.746.043.5-28.8106.747.044.5-29.8106.748.045.5-31.1106.749.046.5-32.6106.750.047.6-33.8107.251.048.6-35.1107.252.049.6-36.4107.253.050.6-37.9107.854.051.6-39.3107.855.052.7-41.1108.356.053.7-42.6108.357.054.7-44.2108.958.055.7-45.6108.959.056.8-47.1109.460.057.8-48.3110.0 65.062.8112.8 70.068.3116.7 75.073.6120.0 80.078.9-46.8123.9 85.084.3-36.9133.9 90.089.7-29.8140.6 95.095.0-19.4158.3乙二醇水溶液粘度乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要,下面是乙二醇水溶液的粘度(mPa.s)和其浓度的关系。
95%乙醇的物理性质
相对密度(20℃/4℃):0.793
凝固点:-114℃,
沸点:78.32℃
闪点(开口):16℃
燃点:390-430 ℃
折射率:1.3614
粘度(20℃):1.41mPa·s
表面张力(20 ℃):22.27×10ˆ-3N/m
比热容(20 ℃):2.42kJ/(kgK)
蒸气压(20 ℃):5.732kPa
溶解度参数δ=12.7。
无色透明、易燃易挥发液体。
有酒的气味和刺激性辛辣味。
溶于水、甲醇、乙醚和氯仿。
能溶解许多有机物和若干无机物。
具有吸湿性,能与水形成共沸混合物。
与铬酸、次氯酸钙、过氧化氢、硝酸、硝酸铂、过氮酸盐及氧化剂反应剧烈,有发生爆炸的危险。
易挥发,极易燃烧,火焰淡蓝色。
蒸气与空气形成爆炸性混合物,爆炸极限4.3-19.0%(体积)。
微毒,有麻醉性,饮入乙醇中毒剂量75-80g。
致死剂量
为250-500g。
空气中最高容许浓度1880mg/m3。
乙醇的物理性质知识点内容乙醇分子是由是由C、H、O 三种原子构成(乙基和羟基两部分组成),可以看成是乙烷分子中的一个氢原子被羟基取代的产物,也可以看成是水分子中的一个氢原子被乙基取代的产物。
下面给大家带来一些关于乙醇的物理性质知识内容,希望对大家有所帮助。
一.乙醇的物理性质乙醇液体密度是0.789g/cm?,乙醇气体密度为1.59kg/m?,相对密度(d15.56)0.816,式量(相对分子质量)为46.07g/mol。
沸点是78.2℃,14℃闭口闪点,熔点是-114.3℃。
纯乙醇是无色透明的液体,有特殊香味,易挥发。
乙醇的物理性质主要与其低碳直链醇的性质有关。
分子中的羟基可以形成氢键,因此乙醇黏性大,也不及相近相对分子质量的有机化合物极性大。
[2]20℃下,乙醇的折射率为1.3611。
溶解性能与水以任意比互溶;可混溶于醚、氯仿、甲醇、丙酮、甘油等多数有机溶剂。
潮解性由于存在氢键,乙醇具有较强的潮解性,可以很快从空气中吸收水分。
羟基的极性也使得很多离子化合物可溶于乙醇中,如氢氧化钠、氢氧化钾、氯化镁、氯化钙、氯化铵、溴化铵和溴化钠等;但氯化钠和氯化钾微溶于乙醇。
此外,其非极性的烃基使得乙醇也可溶解一些非极性的物质,例如大多数香精油和很多增味剂、增色剂和医药试剂。
二.乙醇用途可用乙醇制造醋酸、饮料、香精、染料、燃料等。
医疗上也常用体积分数为70%~75%的乙醇作消毒剂等,在国防化工、医疗卫生、食品工业、工农业生产中都有广泛的用途。
三.乙醇主要种类1、按生产使用的原料可分为淀粉质原料发酵酒精、糖蜜原料发酵酒精、亚硫酸盐纸浆废液发酵生产酒精。
淀粉质原料发酵酒精(一般有薯类、谷类和野生植物等含淀粉质的原料,在微生物作用下将淀粉水解为葡萄糖,再进一步由酵母发酵生成酒精);糖蜜原料发酵酒精(直接利用糖蜜中的糖分,经过稀释杀菌并添加部分营养盐,借酵母的作用发酵生成酒精);亚硫酸盐纸浆废液发酵生产酒精(利用造纸废液中含有的六碳糖,在酵母作用下发酵成酒精,主要产品为工业用酒精。
乙醇水溶液物理特性比
热密度粘度等
GE GROUP system office room 【GEIHUA16H-GEIHUA GEIHUA8Q8-
乙二醇水溶液物性
乙二醇水溶液的冰点沸点
乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要,下面是乙二醇水溶液的冰点沸点和其浓度的关系。
(数据来源ASHRAE手册2005)
乙二醇水溶液粘度
乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要,下面是乙二醇水溶液的粘度(mPa.s)和其浓度的关系。
(数据来源ASHRAE手册2005)
乙二醇水溶液的密度
乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要,下面是乙二醇水溶液的密度(kg/m3)和其浓度的关系。
(数据来源ASHRAE手册2005)
乙二醇水溶液的比热
乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要,下面是乙二醇水溶液的比热(kJ/kg.K)和其浓度的关系。
(数据来源ASHRAE手册2005)
乙二醇水溶液导热系数
乙二醇水溶液作为重要的载冷剂,其物理性质对设备和系统的设计都十分重要,下面是乙二醇水溶液的导热系数(W/m.K)和其浓度的关系。
(数据来源ASHRAE手册2005)。