§6-3溶剂萃取分离法
- 格式:pdf
- 大小:128.05 KB
- 文档页数:20


溶剂萃取法操作规程溶剂萃取法是一种常用的物质分离技术,广泛应用于化学、生物、环境等领域。
在进行溶剂萃取法操作时,需要遵循一些规程以确保实验的顺利进行和结果的准确性。
下面是溶剂萃取法操作的一般规程:1. 实验前的准备:(1)仔细阅读实验操作指南和相关文献,了解所要分离的物质的性质和操作流程。
(2)检查所使用的设备和器材是否完好,并保持清洁。
(3)准备所需的试剂和溶剂,并确保其纯度和保存状态。
(4)佩戴实验防护设备,如实验手套、护目镜等。
2. 样品的准备:(1)根据实验要求,将待分离物质进行适当的前处理,如破碎、粉碎、溶解等。
(2)根据不同的实验目的,选择合适的试剂和溶剂,将样品溶解在溶剂中。
3. 萃取液的制备:(1)根据实验的需要,选择合适的有机溶剂和水相溶剂,并在试管或烧瓶中混合。
(2)根据实验要求,调整萃取液的pH值,可以使用酸碱溶液进行调整。
4. 萃取操作:(1)将样品溶液添加到萃取液中,摇匀混合。
(2)根据实验要求,冷却或加热反应体系,控制溶质的分配行为。
(3)静置一段时间,使两相之间分相,并待两相分离。
5. 分离和收集:(1)使用分离漏斗或离心机等工具,将两相分离。
(2)根据实验需要,分离出有机相或水相,并将其收集至不同的容器中。
6. 萃取溶剂的回收:(1)对于有机溶剂,可以进行蒸馏回收,以减少溶剂的消耗和对环境的影响。
(2)对于水相溶液,可以进行浓缩或其他方法进行溶剂的回收。
7. 清洗和处理废液:(1)清洗使用过的玻璃仪器和设备,确保下次实验的准确性。
(2)处理废液时,必须按照环保要求进行处理,以避免对环境造成污染。
8. 实验记录和数据处理:(1)详细记录实验条件、操作步骤、结果等相关信息,并做好标记和编号。
(2)对实验结果进行分析和处理,计算各分析物的相对含量或其他物理化学参数。
9. 实验后的清理和整理:(1)将实验室设备和器材清理干净,并恢复原样。
(2)将实验结果和数据整理好,并准备实验报告和相关文献资料。


萃取分离法的操作流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!萃取分离法是一种常用的分离和提纯技术,广泛应用于化学、生物、制药等领域。


溶剂萃取分离法萃取分离法包括液相-液相、固相-液相和气相-液相等几种方法,但应用最广泛的为液-液萃取分离法(亦称溶剂萃取分离法)。
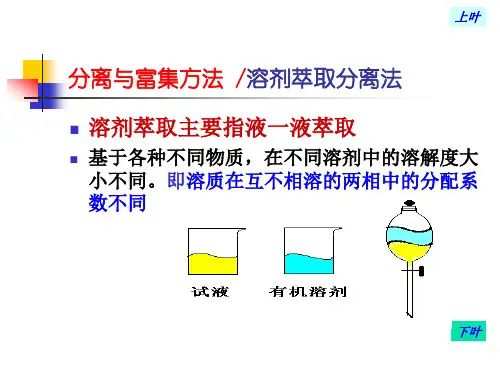
该法常用一种与水不相溶的有机溶剂与试液一起混合振荡,然后搁置分层,这时便有一种或几种组分转入有机相中,而另一些组分则仍留在试液中,从而达到分离的目的。
溶剂萃取分离法既可用于常量元素的分离又适用于痕量元素的分离与富集,而且方法简单、快速。
如果萃取的组分是有色化合物,便可直接进行比色测定,称为萃取比色法。
这种方法具有较高的灵敏度和选择性。
一、萃取分离的基本原理(一)萃取过程的本质根据相似相溶规则,将物质由亲水性转化为疏水性。
极性化合物易溶于极性的溶剂中,而非极性化合物易溶于非极性的溶剂中,这一规律称为“相似相溶原则”。
例如I2是一种非极性化合物、CCl4是非极性溶剂,水是极性溶剂,所以I2易溶于CCl4而难溶于水。
当用等体积的CCl4从I2的水溶液中提取I2时,萃取百分率可达98.8%。
又如用水可以从丙醇和溴丙烷的混合液,萃取极性的丙醇。
常用的非极性溶剂有:酮类、醚类、苯、CCl4和CHCl3等。
无机化合物在水溶液中受水分子极性的作用,电离成为带电荷的亲水性离子,并进一步结合成为水合离子,而易溶于水中。
如果要从水溶液中萃取水合离子,显然是比较困难的。
为了从水溶液中萃取某种金属离子,就必须设法脱去水合离子周围的水分子,并中和所带的电荷,使之变成极性很弱的可溶于有机溶剂的化合物,就是说将亲水性的离子变成疏水性的化合物。
为此,常加入某种试剂使之与被萃取的金属离子作用,生成一种不带电荷的易溶于有机溶剂的分子,然后用有机溶剂萃取。
例如Ni2+在水溶液中是亲水性的,以水合离子Ni(H2O)62+的状态存在。
如果在氨性溶液中,加人丁二酮肟试剂,生成疏水性的丁二酮肟镍螯合物分子,它不带电荷并由硫水基团取许代了水合离子中的水分子,成为亲有机溶剂的硫水性化合物,即可用CHCl3萃取。
(二)分配系数设物质A在萃取过程中分配在不互溶的水相和有机相中:A有= A水在一定温度下,当分配达到平衡时,物质A在两种溶剂中的活度(或活度)比保持恒定,即分配定律可用下式表示:K D=[A]有/[A]水式中K D称为分配系数。



10 溶剂萃取法在液体混合物溶液中加入某种溶剂,使溶液中的组分得到全部或部分分离的过程称为萃取。
溶剂萃取法是从稀溶液中提取物质的一种有效方法。
广泛地应用于冶金和化工行业中。
在黄金行业中,用溶剂萃取法提取纯金、银已有许多研究[1~3],在国外,其成熟技术已经工业应用多年。
用萃取法从含氰废水中提取铜、锌的研究也多有报导[5~6]。
在我国,直到1997年才由清华大学和山东省莱州黄金冶炼厂合作完成了萃取法从氰化贫液中分离铜的工业试验,取得了较好的效果。
9.1 溶剂萃取法的基本原理溶剂萃取法也称液—液萃取法,简称萃取法。
萃取法由有机相和水相相互混合,水相中要分离出的物质进入有机相后,再靠两相质量密度不同将两相分开。
有机相一般由三种物质组成,即萃取剂、稀释剂、溶剂。
有时还要在萃取剂中加入一些调节剂,以使萃取剂的性能更好。
从氰化物溶液中萃取有色金属氰络物一般用高分子有机胺类,如氯化三烷基甲胺(N 263)、稀释剂为高碳醇、溶剂是磺化煤油。
水相即是要处理的废水。
与吸收操作相似,萃取法以相际平衡为过程极限。
这与离子交换法和液膜法也是相近的。
但离子交换法使用固体离子交换树脂做吸收物质;而液膜法使用的是油包水(碱溶液用于吸收氰化氢)组成的吸收物质。
萃取法所用的吸收剂均由有机物组成,其质量密度一定要与水溶液或称萃取原料液有相当大的差别,以使两相靠重力就能较容易地分离开,有机相还要有较高的沸点,以保证有机物在使用过程中不至于损失太大。
萃取过程是一个传质过程,溶质从水相传递到有机相中,直到平衡。
因此要求萃取设备能充分地使水相中的物质在较短时间内扩散到有机相中,而且要求有机相的粘度不要过大,以免被吸收物质在有机相内产生较大浓度梯度而阻碍吸收进程。
萃取过程得到的富集了水相中某种物质或几种物质的有机相叫萃取相。
经过萃取分离出某种物质或几种物质的水相叫萃余液。
通过反萃将萃取相的被萃取物分离出去才能使有机相循环使用。
对于含铜氰络离子的萃取相,可用烧碱溶液将铜络离子从萃取相中反萃出来,得到含铜氰络合物浓度极高的溶液。