保护基团方法大全
- 格式:pdf
- 大小:1.20 MB
- 文档页数:41



12.4 基团的保护(P209)保护基应满足下列3点要求(李209):(1) 保护基在温和条件下容易引入所要保护的分子。
(2) 保护基与被保护基形成的结构能够经受住保护阶段所发生的反应的条件,而不起反应。
(3) 保护基易于在温和条件下除去,即可以在不损及分子其余部分的条件下除去,而且对反应物分子不起其他作用(如不会因空间效应而引起立体结构的变化)。
一、羟基的保护醇与酚都容易被氧化、烷基化和酰基化(酚羟基使苯环易于氧化)。
但有不同,仲醇和叔醇常易脱水,有时要加以阻止。
保护醇类ROH 的方法一般是将羟基制成醚类ROR ′或酯类ROCOR ′,前者对氧化剂或还原剂都有相当的稳定性。
这是羟基保护的主要方法。
(一)形成甲醚类(讲)先用碱脱去羟基的质子,再与合成子+CH 3作用,如使用试剂NaH /(CH 3)2SO 4、CH 3I/OH -或(CH 3)2SO 4/OH -。
ROH ROCH 3333对RMgX 、LiAlH 4、CrO 3、碱稳定。
C 6H 5OH C 6H 5OCH 3C 6H 5OH CH 3I 或(CH 3)2SO 4-HI对RMgX 、LiAlH 4、CrO 3、碱稳定。
(二)形成混合型缩醛⑴ 四氢吡喃醚ROTHP (Tetrahydropyranyl )(讲)制备时,使用二氢吡喃与醇类在酸催化下进行加成作用。
对RMgX 、LiAlH 4、CrO 3、碱、金属氢化物稳定。
(前讲义)ROH O ,TsOH,Et O ROH +2欲恢复到醇类,则在酸性水溶液中进行水解,即可脱去保护基团。
(三)形成乙酸酯类(ROCOCH 3)用乙酐在吡啶中将一级、二级醇转变为乙酸酯,吡啶是用来吸收生成的乙酸(巨167):ROH ROCOCH 3K 2CO 3溶液(CH 3CO)2O 吡啶-CH 3OH ROH二、二醇的保护三、羰基的保护 最重要的是形成缩醛和缩酮。
缩醛和缩酮的保护基不与碱、氧化试剂或亲核试剂(如H -,RMgBr)作用,而通常以酸水解回复到羰基。


word 格式-可编辑-感谢下载支持
举例说明保护基团的作用,并用绿色化学的观点来说明其优缺点。
答: 在有机合成中,为达到最终合成目的常常采用“以退为进”的策略,先把有用的官能团位置有目的的保护起来再在适当的位置使它复原。
例如我们常见的羟基、羰基、氨基的保护。
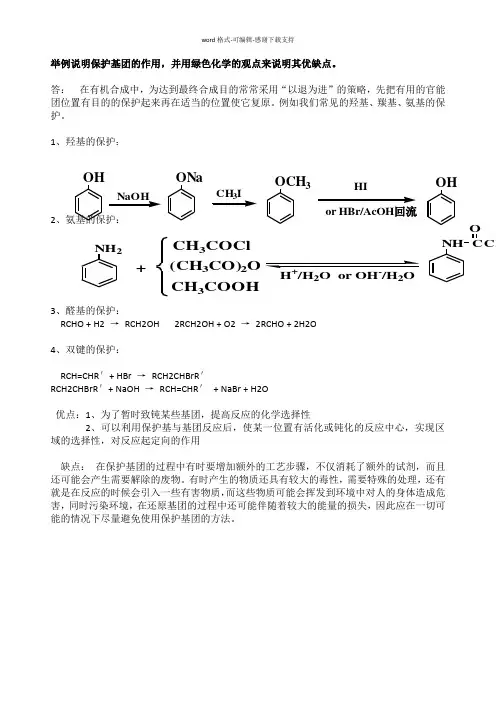
1、羟基的保护:
2
、氨基的保护:
3、醛基的保护:
RCHO + H2 →
RCH2OH 2RCH2OH + O2 → 2RCHO + 2H2O
4、双键的保护:
RCH=CHR '+ HBr → RCH2CHBrR ' RCH2CHBrR '+ NaOH → RCH=CHR ' + NaBr + H2O
优点:1、为了暂时致钝某些基团,提高反应的化学选择性
2、可以利用保护基与基团反应后,使某一位置有活化或钝化的反应中心,实现区域的选择性,对反应起定向的作用
缺点: 在保护基团的过程中有时要增加额外的工艺步骤,不仅消耗了额外的试剂,而且还可能会产生需要解除的废物。
有时产生的物质还具有较大的毒性,需要特殊的处理,还有就是在反应的时候会引入一些有害物质,而这些物质可能会挥发到环境中对人的身体造成危害,同时污染环境,在还原基团的过程中还可能伴随着较大的能量的损失,因此应在一切可能的情况下尽量避免使用保护基团的方法。
NH 2+CH 3COCl (CH 3CO)2O CH 3COOH NH CCH
O H /H 2O or OH /H 2O OH ONa OCH 3HI or HBr/AcOH 回流OH。


基团保护方法
以下是 8 条关于基团保护方法的内容:
1. 嘿,你知道吗,有一种基团保护方法叫酯化保护!就像给基团穿上一件坚固的盔甲。
比如在合成复杂分子时,为了不让某个基团捣乱,我们就可以把它变成酯呀。
这多神奇!
2. 哇塞,还有醚化保护呢!这就好比给基团罩上一个保护罩。
举个例子,在一些反应里,我们把基团醚化,让它乖乖待着,不影响我们想要的反应进行。
3. 听我说呀,酰胺化保护也很厉害哟!就如同给基团找了个安全的小窝。
比如说,特定情况下,把基团变成酰胺,它就安稳啦。
4. 嘿呀,你晓得不,硅烷化保护超有用的呀!它简直是基团的超级保镖。
就像在某些精细合成中,用硅烷化给基团提供强大保护。
5. 哇哦,苄基化保护可是不能小瞧的呢!这就好像给基团围了一道篱笆。
想想看,特定反应需要的时候,苄基化保护能发挥大作用呢。
6. 咦,酰基化保护也很棒呀!它像是给基团戴上了一顶特别的帽子。
比如在某些合成路线里,酰基化保护让反应顺顺利利的。
7. 嘿,还有烷氧基甲基化保护呢!这不就是给基团安排了一个专属房间嘛。
在一些复杂反应体系中,这种保护方法太实用啦。
8. 哎呀呀,卤代保护也不容忽视啊!简直是基团的秘密武器。
像在一些情况下,卤代一下,起到的保护作用可大着呢!总之,基团保护方法多种多样,各有各的神奇之处,我们可得好好掌握呀!。

基团的保护方式一:使基团先参与反应又释放出方式二:反应的先后顺序问题(1)基团保护①醛基的保护如:②双键的保护如:③羟基的保护如:R--OH R--OCH3R--OCH3R--OH④羧基的保护如:⑤氨基的保护如:练习1、(氨基的保护)苄佐卡因是一种医用麻醉药品,学名对氨基苯甲酸乙酯,它以对硝基甲苯为主要起始原料经下列反应制得:请回答下列问题:(1)写出A、B、C的结构简式:A____________,B______________,C______________。
(2)用1H核磁共振谱可以证明化合物C中有____种氢处于不同的化学环境。
(3) ①与②能否颠倒位置,为什么2、(酚羟基的保护)工业上用甲苯生产对- 羟基苯甲酸乙酯HO ——COOC 2H 5(一种常用的化妆品防霉剂),其生产过程如下(反应条件未全部注明)所示:按上图填空: (1)有机物A 的结构简式为(2)写出反应⑤的化学方程式(有机物写结构简式,注明反应条件)(3)反应②和反应④的反应类型分别是(选填编号) 、 a .取代反应,b .加成反应,c .消去反应,d .酯化反应,e .氧化反应(4)写出反应③的化学方程式(有机物写结构简式,不用写反应条件,但要配平)(5)在合成线路中设计③和⑥两步反应的目的是 。
3、(醛基的保护)化合物A 是石油化工的一种重要原料,用A 和水煤气为原料经下列途径合成化合物D (分子式为C 3H 6O 3).已知:请回答下列问题:(1).写出下列物质的结构简式:A B COOH OCH 3③ 一定条件 ② Cl 2 ①催化剂 CH 3I CH 3CH 3OHC 2H 5OH⑤ CH 3OCH 3 ④ COOC 2H 5OCH 3 HI ⑥H CH 3A:__________;B:____________;C:_____________;D:___________.(2).指出反应②的反应类型______________________.(3).写出反应③的化学方程式_______________.(4).反应④的目的是___________________________________________________.(5).化合物D’是D的一种同分异构体,它最早发现于酸牛奶中,是人体内糖类代谢的中间产物.D’在浓硫酸存在的条件下加热,既可以生成能使溴水褪色的化合物E(C3H4O2),又可以生成六原子环状化合物F(C6H8O4).请分别写出D’生成E和F的化学方程式:D’→E:______________________________ D’→F:________________________.4、(氨基的保护)所给信息:①②苯胺,弱碱性,易氧化③利用这些反应,按以下步骤可从某烃A合成一种染料中间体DSD酸。

保护醇类 ROH 的方法一般是制成醚类(ROR′) 或酯类(ROCOR′),前者对氧化剂或还原剂都有相当的稳定性。
1. 形成甲醚类 ROCH3可以用碱脱去醇ROH质子,再与合成子+CH3作用,如使用试剂NaH / Me2SO4。
也可先作成银盐 RO-Ag+ 并与碘甲烷反应,如使用 Ag2O / MeI;但对三级醇不宜使用这一方法。
醇类也可与重氮甲烷CH2N2,在Lewis酸(如BF3·Et2O)催化下形成甲醚.脱去甲基保护基,回复到醇类,通常使用Lewis酸,如BBr3及Me3SiI,也就是引用硬软酸碱原理(hard-soft acids and bases principle),使氧原子与硼或硅原子结合(较硬的共轭酸),而以溴离子或碘离子(较软的共轭碱)将甲基(较软的共轭酸)除去。
2. 形成叔丁基醚类 ROC(CH3)3醇与异丁烯在Lewis 酸催化下制备。
叔丁基为一巨大的取代基(bulky group),脱去时需用酸处理3. 形成苄醚 ROCH2Ph:制备时,使醇在强碱下与苄溴 (benzyl bromide)反应,通常以加氢反应或锂金属还原,使苄基脱除,并回复到醇类。
4. 形成三苯基甲醚 (ROCPh3)制备时,以三苯基氯甲烷在吡啶中与醇类作用,而以 4-二甲胺基吡啶(4-dimethyl aminopyridine, DMAP)为催化剂。
5. 形成甲氧基甲醚 ROCH2OCH3制备时,使用甲氧基氯甲烷与醇类作用,并以三级胺吸收生成的HCl。
甲氧基甲醚在碱性条件下和一般质子酸中有相当的稳定性,但此保护基团可用强酸或Lewis酸在激烈条件下脱去。
7. 形成四氢吡喃 ROTHP制备时,使用二氢吡喃与醇类在酸催化下进行加成作用。
欲回收恢复到醇类时,则在酸性水溶液中进行水解,即可脱去保护基团。
有机合成中常引用这种保护基团,其缺点是增加一个不对称碳(缩酮上的碳原子),使得NMR谱的解析较复杂。

常见有机合成中的保护基与去保护方法【常见有机合成中的保护基与去保护方法】有机合成化学是一个极具挑战性和创造性的科学领域。
在有机合成中,保护基(也称作保护基团)是一种化学基团,通常用于保护某些反应中的特定官能团,以防止其发生不必要的化学反应。
而去保护方法则是指在有机合成反应中,将保护基去除的方法。
本文将介绍一些常见的保护基以及它们的去保护方法。
一、醇保护基1.脂肪醇保护基:脂肪醇是有机合成中常用的保护基。
常见的脂肪醇保护基有烷基、苄基、戊二烯基等。
去保护方法可以是加热反应物或者在酸性条件下加入还原剂。
2.酯保护基:酯保护基通常用于保护羟基。
去保护方法可通过加入酸性条件或加热反应物来去除。
二、羧酸保护基1.酯保护基:酯保护基用于保护羧酸官能团,常用的酯保护基有甲基、乙基、苄基等。
去保护方法可通过加入碱性条件或加热反应物来去除。
2.酰氯保护基:酰氯保护基也是常见的羧酸保护基。
去保护方法可以是加入水或碱来水解酰氯基团。
三、氮保护基1.苄基保护基:苄基保护基通常用于保护胺官能团。
去保护方法通常是加入酸性条件或氧化剂,使其发生脱保护反应。
2.甲基保护基:甲基保护基也是常见的氮保护基。
去保护方法可以是加入酸性条件或还原剂。
四、硫保护基1.烷基硫基保护基:烷基硫基保护基通常用于保护硫氧化物。
去保护方法可以通过加入酸性条件或氧化剂。
2.苄基硫基保护基:苄基硫基保护基也是常见的硫保护基。
去保护方法通常是加入酸性条件或还原剂。
五、氧保护基1.苄基保护基:苄基保护基常用于保护醛官能团。
去保护方法可以通过加入酸性条件或还原剂。
2.乙酸保护基:乙酸保护基也是常见的氧保护基。
去保护方法可以通过加入碱性条件或加热反应物。
在有机合成中,保护基和去保护方法的选择是非常关键的。
不同的有机合成反应需要使用不同的保护基,而去保护方法则取决于保护基的性质和条件。
在合成中选择合适的保护基和去保护方法,对反应物的稳定性、产率和纯度有着重要的影响。
常见的羟基的保护与脱保护方法常见的羟基保护与脱保护方法概述:在有机合成中,羟基(-OH)是一种常见的官能团。
然而,由于其活泼性和反应性,羟基在某些情况下需要被保护。
保护羟基可以防止其在反应中发生不必要的副反应或失活,同时也可以控制反应的选择性。
本文将介绍几种常见的羟基保护与脱保护方法。
一、羟基保护方法:1. 酯保护:酯是常用的羟基保护基团。
通过与羟基反应,可以将醇转化为酯。
酯保护的优势在于其稳定性和易于去除。
常用的酯保护试剂有二甲基亚砜(DMS)和四氢噻吩-1-氧化物(THF)等。
2. 醚保护:醚也是一种常见的羟基保护基团。
通过与羟基反应,可以将醇转化为醚。
醚保护的优势在于其稳定性和容易操作。
常用的醚保护试剂有二甲基二甲酰胺(DMF)和三甲基硅氧烷(TMS)等。
3. 硅保护:硅是一种常用的羟基保护基团,通过与羟基反应,可以形成硅醚。
硅保护的优势在于其稳定性和容易去除。
常用的硅保护试剂有三甲基氧硅烷(TMS)和二甲基氟硅烷(DMFS)等。
二、羟基脱保护方法:1. 酸性脱保护:酸性条件下,羟基保护基团可以被去除。
常用的酸性脱保护试剂有无水氢氟酸(HF),三氟甲磺酸(TfOH)和三氯化硼(BCl3)等。
酸性脱保护条件需要控制好反应的温度、时间和酸的浓度,以避免不必要的副反应。
2. 还原性脱保护:还原剂可以将羟基保护基团还原为醇。
常用的还原剂有氢化钠(NaH)和氢化铝锂(LiAlH4)等。
还原性脱保护条件需要控制好反应的温度和还原剂的浓度,以避免不必要的副反应。
3. 碱性脱保护:碱性条件下,羟基保护基团可以被去除。
常用的碱性脱保护试剂有氢氧化钠(NaOH)和氢氧化钾(KOH)等。
碱性脱保护条件需要控制好反应的温度、时间和碱的浓度,以避免不必要的副反应。
总结:在有机合成中,羟基的保护与脱保护是常见的操作。
通过选择合适的保护基团和脱保护条件,可以实现对羟基的保护和去保护,从而实现有机合成的目标。
不同的保护基团和脱保护条件具有不同的适用范围和反应条件,需要根据具体的合成需求进行选择。
有机合成中的保护基团在有机化学合成中,保护基团是一种重要的工具,用于保护化合物中的特定官能团或功能基团,以防止其在反应条件下发生不必要的变化或分解。
通过使用适当的保护基团,有机化学家能够实现高选择性和高收率的合成反应,从而有效地构建复杂的有机分子。
本文将介绍一些常见的保护基团及其在合成过程中的应用。
一、醇的保护基团1. 苄基(Bn)- 苄基是最常用的醇保护基团之一,它通过醇和苄溴化物反应制备。
苄基在碱性条件下可以容易地被去除,因此是一个理想的保护基团。
它广泛应用于糖类、多羟基醇和其他含醇化合物的合成中。
2. 丙二酰基(Ac)- 丙二酰基是另一种常用的醇保护基团。
丙二酰基化反应通常在醇和丙酰氯或丙二酸酐的存在下进行。
这个保护基团可以在碱性和酸性条件下容易去除,适用于多数醇类化合物的保护。
二、羧酸的保护基团1. 甲酯基(MeO)- 甲酯基是最常用的羧酸保护基团,在碱性或酸性条件下都可以容易去除。
甲酯化反应通常在酸催化下进行,可以实现选择性地保护羧酸基。
2. 苄基(Bn)- 苄基也可以用作羧酸的保护基团,它通过羧酸和苄溴化物反应制备。
苄基保护基团在碱性条件下容易去除,适用于一些特殊的有机合成反应。
三、胺的保护基团1. 丙酰胺基(AcNH)- 丙酰胺基是最常用的胺保护基团之一。
它通过胺和丙酰氯反应制备,可以在酸性条件下容易去除。
丙酰胺基在多肽合成和其他涉及胺基反应的有机合成中广泛应用。
2. 苄基(Bn)- 苄基也可以用作胺的保护基团,它通常通过胺和苄溴化物反应制备。
苄基在碱性条件下可以容易去除,适用于一些特殊的有机合成反应。
四、醛和酮的保护基团1. 乙二醇基(EG)- 乙二醇基是最常用的醛和酮的保护基团,它通过醛或酮和乙二醇反应制备。
乙二醇基在酸性条件下可以容易去除,适用于多数醛酮化合物的保护。
2. 氧代硅基(Si OR)- 氧代硅基是另一种常用的醛和酮保护基团,通过醛或酮和硅醇反应制备。
氧代硅基在酸性条件下可以容易去除,并可以通过适当的硅硫化剂在碱性条件下去除。
有机合成中的重要保护基团和去保护方法在有机合成中,保护基团扮演着至关重要的角色。
它们可以保护反应中的特定功能团,以防止其与其他试剂发生不必要的反应。
保护基团的引入和去除成为了有机合成中的两个关键步骤。
在本文中,我们将探讨一些有机合成中的重要保护基团,以及去除它们的方法。
1. 醇保护基团醇保护基团是有机合成中最常用的保护基团之一。
它可以通过与醇反应生成醚来引入。
常用的醇保护基团包括醇酯、醚和醇醚。
在选取保护基团时,需要考虑其稳定性和去保护的条件。
去除醇保护基团的方法有很多种。
常用的方法包括酸处理和还原。
酸处理通常使用强酸,如硫酸、盐酸或三氟甲磺酸。
还原方法则是使用还原试剂,如铝醇盐或氢化钠。
2. 酰基保护基团酰基保护基团是保护羧酸的常用基团。
它可以通过与酸反应生成酯来引入。
常用的酰基保护基团包括乙酰基、苄酰基和丙酰基。
选择合适的酰基保护基团需要考虑其稳定性和易于去除的条件。
去除酰基保护基团的方法主要有碱处理和酸处理。
碱处理通常使用碱性试剂,如碳酸氢钠或氢氧化钠。
酸处理则使用酸性试剂,如盐酸或三氟甲磺酸。
3. 氨基保护基团氨基保护基团常用于保护胺官能团。
常用的氨基保护基团包括铺地基(Boc)、苄基、三甲基硅基(TMS)和甲酰基。
选择保护基团需要考虑其稳定性和去除的条件。
去除氨基保护基团的方法有多种。
常用的方法包括酸处理和碱处理。
酸处理通常使用强酸,如三氟甲磺酸或盐酸。
碱处理通常使用氢氧化钠或氢氧化铯。
4. 硅基保护基团硅基保护基团常用于保护醇和酚官能团。
常用的硅基保护基团包括二甲基氧硅基(TBS)、二异丙基氧硅基(TIPS)和三甲基硅基(TMS)。
选择硅基保护基团需要考虑其稳定性和去除的条件。
去除硅基保护基团的方法主要是酸处理。
常用的酸处理试剂包括氢氟酸、三氟甲磺酸和硼氟酸。
总结起来,有机合成中的保护基团起着至关重要的作用。
正确选择保护基团可以有效地保护特定的功能团,而去除保护基团则是合成目标化合物的关键步骤。
有机合成中的基团保护在有机合成中,某些不希望起反应的官能团,在反应试剂或反应条件的影响下而产生副反应,这样就不能达到预计的合成目标,因此,必须采取措施保护某些官能团,待完成反应后再除去保护基,使其复原。
1、保护措施必须符合如下要求①只对要保护的基团发生反应,而对其它基团不反应;②反应较易进行,精制容易;③保护基易脱除,在除去保护基时,不影响其它基团。
2、常见的基团保护措施①羟基的保护在进行氧化或某些在碱性条件下进行的反应,往往要对羟基进行保护。
a.防止羟基受碱的影响,可用成醚反应。
b.防止羟基氧化可用酯化反应。
②对羧基的保护羧基在高温或碱性条件下,有时也需要保护。
对羧基的保护最常用的是酯化反应。
③对不饱和碳碳键的保护碳碳双键易被氧化,对它们的保护主要用加成反应使之达到饱和。
;④对羰基的保护(以信息题出现)羰基,特别是醛基,在进行氧化反应或遇碱时,往往要进行保护。
对羰基的保护一般采用生成缩醛或缩酮的反应。
(缩醛或缩酮)(缩酮)生成的缩醛或缩酮水解又变成原来的醛或酮。
3、题例解析例1、已知下列信息:①烯键在一定条件下氧化可生成二元醇:②醛能发生如下反应生成缩醛:缩醛比较稳定,与稀碱和氧化剂均难起反应,但在稀酸中温热,会水解为原来的醛。
现有如下合成路线:试回答下列问题:(1)写出A、B的结构简式:________、________。
(2)写出反应Ⅲ的化学方程式:________。
解析:由题给信息知,欲使CH2=CH—CHO变为CH2OH—CHOH—CHO,需将C=C双键氧化,而—CHO对氧化剂敏感,故应先进行保护,待C=C双键氧化完毕,再将醛基还原出来,故合成路线为:答案:(1)A:CH2=CH=CH(OC2H5)2 B:CH2OH—CHOH—CH(OC2H5)(2)CH2OH—CHOH—CH(OC2H5) CH2OH—CHOH—CHO+2C2H5OH例2、已知胺(R—NH2)具有下列性质:−R—NHCOCH3+CH3COOH(Ⅰ)R—NH2+(CH3CO)2O−→−R—NH2+CH3COOH(Ⅱ)R—NHCOCH3+H2O−→硝基苯胺是重要的化工原料,其合成路线如下:(1)a、c、e分别为________。
有机化学中的保护基团和去保护反应保护基团在有机化学中具有重要的作用,它们可以保护特定的官能团,防止其被其他反应所干扰。
同时,去保护反应则能够将保护基团去除,使被保护的官能团重新恢复活性。
本文将探讨有机化学中的保护基团和去保护反应,并介绍一些常见的实例。
一、保护基团的种类及其应用1. 硅醚保护基团硅醚保护基团由于其稳定性和易去除性而在有机化学中得到广泛应用。
硅醚保护基团可以保护醇、酚等羟基化合物。
典型的硅醚保护基团有三甲基硅基(TMS)、甲基三乙基硅基(SEM)、四甲基硅基(TBS)等。
去除硅醚保护基团常用的方法是用强酸或碱溶液处理。
2. 酯保护基团酯保护基团可以保护羧酸和酮等官能团。
合成中常使用的酯保护基团有甲酯、乙酯等。
酯保护基团可以通过酸催化或碱催化条件下的酯水解反应去除。
3. 酰基保护基团酰基保护基团可以保护胺基化合物中的氨基,常用的酰基保护基团有苯甲酰基(Boc)、三甲基乙酰基(TFA)、甲氧羰基(Fmoc)等。
去除酰基保护基团需要使用相应的去保护试剂,如氢氟酸、三氟乙酸等。
二、去保护反应的应用1.硅醚的去保护硅醚保护基团可以通过酸或碱处理去除。
常用的去保护试剂是氟化银(AgF)和氟化铵(NH4F),它们可以有效去除硅醚保护基团,还原羟基的反应活性。
2. 酯的去保护酯保护基团可以通过酸催化的水解或酸催化的醇ysis反应去除。
常用的去保护试剂是浓氢氧化钠(NaOH)、甲醇、乙醇等。
在合适的条件下,酯保护基团可以选择性地去除,而不影响其他官能团。
3. 酰基的去保护酰基保护基团可以通过使用酸或碱去保护试剂去除。
例如,苯甲酰基(Boc)保护基团可以使用三氟乙酸或氢氟酸处理去除。
甲氧羰基(Fmoc)保护基团可以通过用碱处理去除。
这些去保护反应一般是在温和的条件下进行。
三、实例展示1. 硅醚保护例如,对于芳香醇类化合物,可以使用TMS作为保护基团,合成过程中保护羟基,避免其在反应中被氧化或其他官能团干扰。
Protecting Groups in Organic Synthesis选择保护基的原则:(1) 保护基的供应来源,包括经济程度。
(2) 保护基团必须能容易进行保护,且保护效率高。
(3) 保护基的引入对化合物的结构论证不致增加过量的复杂性, 如保护中忌讳产生新的手性中心。
(4) 保护以后的化合物必须承受的起以后进行的反应和后处理过 程。
(5) 保护基以后的化合物对分离、纯化、各种层析技术要稳定。
(6) 保护基团在高度专一的条件下能选择性、高效率地被除去。
(7) 去保护过程的副产物和产物能容易被分离。
呼之即来, 呼之即来,挥之即去。
挥之即去。
切莫请神容易, 切莫请神容易,送神难。
送神难。
羟基的保护基1). 酯类保护基 t-BuCO (Piv); PhCO; MeCO; ClCH2CO et al.OH HO OH OHPivCl (1eq) Py-CH2Cl2 0-25 oCHOOO90% Nicolaou, K. C.; Webber, S. E. Synthesis, 1986, 453酯类保护基的除去(cleavage) 碱性条件下水解, 水解能力: t-BuCO(Piv) < PhCO < MeCO < ClCH2CO 常用的碱:K2CO3, NH3, NH2NH2, Et3N, i-Pr2NEt et al 去除Piv一般用较强的强碱体系,如 KOH/H2O, LiAlH4, DIBAL, KBHEt3OTBDMS TBDMSO O O OTBDMSDIBAL(2.5eq) CH2Cl2, -78 oCTBDMSOOH95% Nicolaou, K. C.; Webber, S. E. Synthesis, 1986, 453ClCH2CO的去除可以用硫脲,氨/甲醇,苯,吡啶水溶液, NH2CH2CH2SH, NH2CH2CH2NH2, PhNHCH2CH2NH2 等除去。
O O O O O OBnClOBnOBn HOOBnOBnAcOOBnOBnNH2NH2 (15eq) HOAc-HOMe rt, 12 hAcO OOOBnOBnAcHNAcHNO OBn74% Cook, A. F.; Maichuk, D. T. J. Org. Chem., 1970, 35, 1940.OR AcO O RO O O O OR Ph O O O O H2NHN S SH HO AcOOH O O O O O OH Ph O O ODioxane, i-Pr2NEtAcOAcOR = ClCH2CO40%Smith, A.B.; Hale, K. J.; Vaccaro, H. A.; Rivero, R. A. J. Am. Chem. Soc, 1991, 113, 2112.2). 硅醚保护基 硅醚保护基主要有: Me3Si (trimethylsilyl, TMS); (triethylsilyl, TES); Et3Si t-BuMe2Si (tert-butyldimethylsilyl, TBDMS or TBS) i-Pr3Si (triisopropylsilyl, TIPS) t-BuPh2Si (tert-butyldiphenylsilyl, TBDPS) 酸水解相对稳定性: TMS(1) < TES(64) < TBDMS(20,000) < TIPS(700,000) < TBDPS (5,000,000) 碱水解相对稳定性: TMS(1) < TES(50) < TBDMS = TBDPS (20,000) < TIPS(100,000) 硅醚保护基的除去: (F-Si 142 kcal/mol; O-Si 112 kcal/mol) 通常用 HF / CH3CN; TBAF / THF; HF.Py / CH3CNTMS ether: TMSCl or TMSOTf in pyridine, NEt3, I-Pr2NEt, imidazole, DBUOOHCO2Me COOBu-tO OTMS CO2MeMe3SiCl-Im 100 C, 90 min.oO O OH OTBSCOOBu-t O O O H OTBS100% Kerwin, S. M.; Paul, A. G.; Heathcock, C. H. J. Org. Chem., 1987, 52, 1686TES ether:TESCl/Imid. DMAP; TESOTf / Py. or 2,6-dimethylpyridineOH O H OTES OTESOTf (1.1eq) Py, MeCN, o -50 C, 10 min. 79%HHeathcook, C. H.; Young, S. D.; Hagen, J. P.; Pilli, R.; Badertscher, U. J. Org. Chem., 1985, 50, 2095TBDMS ether: TBDMSCl / imid. / DMF; TBDMSOTf / 2,6-dimethylpyridineOH OBz OBMP O OTBDMSOTf 2,6-di-tert-buylepyridine CH2Cl2, rt, 24 hOTBS OBz OBMP O OHikota, M.; Tone, H., Horita, K.; Yonemitsu, O. J. Org. Chem., 1990, 55, 7.OH OHOH OHDMF, rt,80%Nicolaou, K. C.; Pavia, M. R.; Seitz, S. P. J. Am. Chem. Soc., 1981, 103, 1224.imidazole(2.5 eq)DMF, rt, 48 hJ. Chem. Soc. Perkin. Trans. I , 1991, 1543.87%Marshell, J. A.; Sedrani, R. J. Org. Chem., 1991, 56, 5496.87%, 1989, 111, 2967.85%2MeOO Nakata, T.; Fukui, M.; Oishi, T. Tetrahedron Lett., 1988, 29, 2219.90%OHOTBSCollington, E. W.; Finch, H. Smith, I. J. Tetrahedron Lett., 1985, 26, 681.83%OFK-506, 73%Nakatsuka, M.; Ragan, J. A.; Sammakia, T.; Smith, D. B.; Uehling, D. E.; Schreiber, S. L.J. Am. Chem. Soc., 1990, 112, 5583.reagent: PMBCl; p-MeOC 6H 4CH 2O-C(=NH)CCl 3 cleavage: DDQ, CANTr (三苯甲基醚) reagent: TrCl/Py/DMAP; TrOTf/2,6-dimethylpyridineclaevage: HCO 2H-H 2O; HCO 2H-tert -BuOH; HCl/MeCN; Na/NH 3tert -butyl (叔丁基醚) reagent: isopropene/CH 2Cl 2; t -BuO-C(=NH)CCl 3cleavage: HCO 2H; CF 3CO 2H; HBr-HOAc, FeCl 3; TiCl 4; TMSIallyl (烯丙基醚) reagent: Allyl bromidecleavage: t -BuOK/DMSO/NaOHcleavage : MOM HCl/THF/H 2O(1:2:1); Lewis acid: Me 3SiBr/CH 2Cl 2; Me 2BBr/CH 2Cl 2MTM AgNO 3/2,6-dimethylpyridine; HgCl 2/CaCO 3MEM ZnBr 2/CH 2Cl 2;HBr/THF;TiCl 4/CH 2Cl 2; MeBBr/CH 2Cl 2BOM Na/NH 3/EtOH, H 2/Pd(OH)2/C;Raney-Ni/EtOH;BF 3/PhSH/CH 2Cl 2 SEM HCl/MeOH; Lewis acid;THP(四氢吡喃) tetrahydropyrane etherreagents : DHP(3,4-dihydro-2H -pyran)cleavage : HOAc/THF/H 2O (4:2:1)Silylene derivatives(硅烯衍生物硅烯衍生物)DTBS (d i-tert-butylsilylene)reagent: t-Bu 2SiCl 2/Et 3N/HOBT/MeCN; (HOBT 1-hydroxybenzotriazole )t-Bu 2Si(OTf)2/2,6-dimethylpyridine/CH 2Cl 2Cleavage: HF-Py/THF-Pyridine, rtHO(CH 2)3OHp-TsOH91%Okawara, H.; Nakai, H.; Ohno, M. Tetrahedron lett., 1982, 23, 1087.J. A. J. Am. Chem. Soc., 1990, 112, 1607.HOCH 2CH 2OH TMSCl, rt, 16 hCO 2MeOOOO+ (TMS)2OChan, T. H.; Schwerdtfeger, A. E. J. Org. Chem., 1991, 56, 3294.76%Gerspacher, M.; Rapoport, H. J. Org. Chem., 1991, 56, 3700Me2Me2H2MeKOH (0.95 eq.)MeOH / H 2O95%Tetrahedron Lett., 1991, 22, 2679.Valerio, R. M.; Alewood, P. F.; Johns, R. B. Synthesis , 1988, 786.HOAc-i -PrOH-H 2OH2Me100%J. Org. Chem., 1990, 55, 3068.4:4:1100C, 15 hTsE (2-tosylethyl) Bn (benzyl)allyl (allyl) ester78-87%Org. Synthesis , 1988, Coll. Vol. VI, 418.2H BocO NPhCN80-83%Itoh, M.; Hagiwara, D.; Kamiya, T. Bull. Chem. Soc. Jpn ., 1977, 50, 718.rt, 3 hEt 3N, H 2O,dioxaneOO2 TFA100%Yamashiro, D.; Blake, J.; Li, C. H. J. Am. Chem. Soc., 1972, 94, 2855.NCOOMe CbzCOOMe 100%Sakaitani, M., Ohfune, Y. J. Org. Chem ., 1990, 55, 870.Et 3N, rt, 30 minEt 3SiH, PdCl 2Bergman, M.; Zervas, L. Ber. Deutsch. Chem. Ges., 1932, 65, 1192.N H 91%Hoogerhout, P.; Guis, C. P.; Erkelens, C.; van Boom, J. H.Recl. Trav. Chim. Pays-Bas , 1985, 104, 54.dioxane-H 2O, 0 o C, 4 h, rt. 8 h97%Schultheiss-Reimann, P.; Kunz, H. Angew. Chem. Int. Ed. Engl., 1983, 22, 62.CODcyclooctadiene CODcyclooctadiene Cp cyclopentadieneO SO 3H CSA camphorsulfonic acidCl NC DDQ 2,3-dichloro-5,6-dicyano -1,4-benzoquinone N N OC 2H 5O O C 2H 5O DEAD diethyl azodicarboxylate NIS N -iodosuccinimide O N N O O O DIAD diisopropyl azodicarboxylateoxideClCrO 3N O 3S PPTs pyridinium p -toluenesulfonate SO 3H PTS p -toluenesulfonic acid N Py pyridine TBAF tetrabutylammonium florideN F3ClS OCF 3DIBALH diisobutylaluminium hydride AlH DMAP4-N,N -dimethylaminopyridine N N DMF N,N -dimethylformamide DMPU N,N'-dimethylpropyleneurea 1,3-dimethyl-3,4,5,6-tetrahydro -2(1H)-pyrimidinoneN Im imidazol-1-yl LDA lithium diisopropylamide N NCS N -chlorosuccinimide N O Cl TFA trifluoroacetic acidO OH F F FF TIPSCl triisopropylsilyl chloride TIPSOTf triisopropylsilyl triflate Si O S O O F F F TMSBr trimethylsilyl bromide Si Br TMSCl trimethylsilyl chlorideSi ClO RuO 4Tr trityl triphenylmethyl Ph Bnbenzyl BOM benzyloxymethyl Cbz benzyloxycarbonyl O O Fmoc 9-fluorenylmethoxycarbonyl O Troc 2,2,2-trichloroethoxycarbonyl O O Cl Cl Cl辛烷99壬烷8。