2CO(g)
K
C (s) + H2O (g)
CO (g) + H2 (g) K1
CO (g) +H2O (g)
CO2 (g) + H2 (g) K2
K = K1/K2
可编辑ppt
8
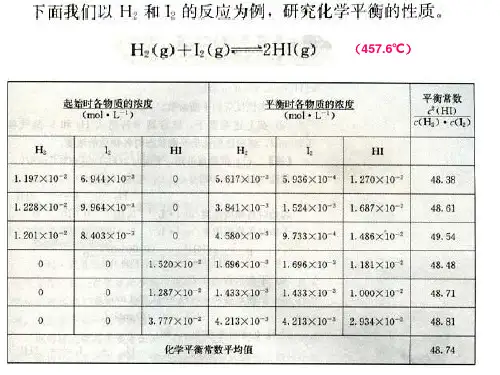
三、化学平衡常数意义
①判断反应进行的程度:K值越大,表示反应进行的程度越大,
反应物转化率也越大。
一般来说,K >105,认为正反应进行得较完全 K <10-5 认为 正反应很难进行(逆反应较完全) 10-5 ≤K ≤ 105 认为是可逆反应
可编辑ppt
16
解(1)根据题意得: H2 +
起始浓度mol/L: 0.01
I2 ≒ 2HI 0.01 0
平衡浓度mol/L: 0.0080 0.0080 0.0040
K= C(HI)2 =0.25
C(H2)C(I2)
解(2)设H2的消耗浓度为x
H2 +
I2 ≒ 2HI
起始浓度mol/L: 0.02 0.02 0
已知平衡浓度求平衡常数和初始浓度
例1:合成氨的反应N2+3H22NH3在某温度下 各物质的浓度平衡是: [N2]=3mol·L-1, [H2]=9mol·L-1, [NH3] =4mol·L-1
求该反应的平衡常数和N2、H2的初始浓度。
可编辑ppt
14
解:①求平衡常数K
Kc=[NH3]2/([N2][H2]3)=16/(3×93)=7.32×10-3
解:设达到平衡时氢气的浓度为X
CO + H2O H2+CO2
初始 0.02 0.02
00
平衡时 0.02-x 0.02-x x x