高一化学必修二原子结构
- 格式:doc
- 大小:92.00 KB
- 文档页数:4


高一化学元素周期律知识点归纳高一的化学学习十分重要,高一的化学知识掌握情况将会直接影响以后高年级的化学学习,其中化学元素周期律是一个最基础的知识点。
下面是店铺为大家整理的高一化学必备的知识,希望对大家有用! 高一化学元素周期律知识1.原子结构所有的元素的原子核都由质子和中子构成。
正例:612C、613C、614C三原子质子数相同都是6,中子数不同,分别为6、7、8.反例:只有氕(11H)原子中没有中子,中子数为0。
2.所以原子的中子数都大于质子数正例:613C 、614C 、13H 等大多数原子的中子数大于质子数。
绝大多数元素的相对原子质量(近似等于质子数与中子数之和)都大于质子数的2倍。
反例1.氕(11H)没有中子,中子数小于质子数。
2.氘(11H)、氦(24He)、硼(510B)、碳(612C)、氮(714N)、氧(816O)、氖(1020Ne)、镁(1224Mg)、硅(1428Si)、硫(1632S)、钙3.具有相同质子数的微粒一定属于同一种元素正例:正例:同一元素的不同微粒质子数相同:H+ 、H- 、H等。
反例1:不同的中性分子可以质子数相同,如:Ne、HF、H2O、NH3、CH4 。
反例2:不同的阳离子可以质子数相同,如:Na+、H3O+、NH4+ 。
反例3:不同的阴离子可以质子数相同,如:NH4+ 、OH-和F-、Cl和HS。
4.电子云氢原子电子云图中,一个小黑点就表示有一个电子。
含义纠错:小黑点只表示电子在核外该处空间出现的机会。
5.元素周期律元素周期律是指元素的性质随着相对原子质量的递增而呈周期性变化的规律。
概念纠错:元素周期律是指元素的性质随着原子序数的递增而呈周期性变化的规律。
6.元素周期律难失电子的元素一定得电子能力强。
概念纠错:反例1:稀有气体元素很少与其它元素反应,即便和氟气反应也生成共价化合物,不会失电子,得电子能力也不强。
反例2:IVA的非金属元素,既不容易失电子,也不容易得电子,主要形成共价化合物,也不会得失电子。


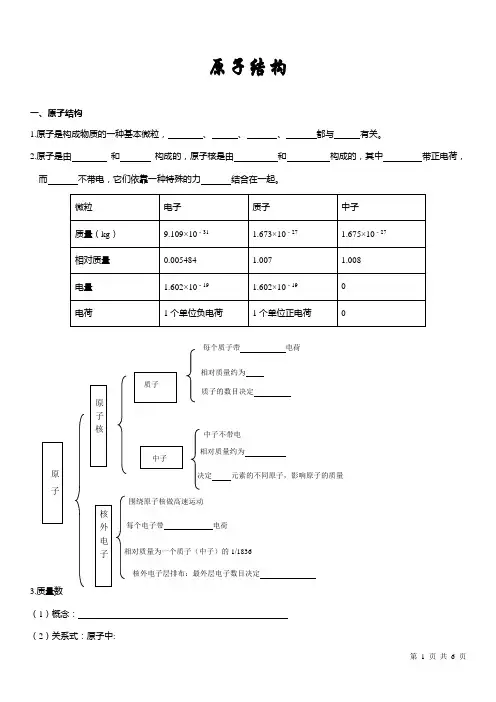
原子结构一、原子结构1.原子是构成物质的一种基本微粒,、、、都与有关。
2.原子是由和构成的,原子核是由和构成的,其中带正电荷,而不带电,它们依靠一种特殊的力结合在一起。
3.质量数(1)概念:(2)关系式:原子中:相对质量约为质子的数目决定中子不带电相对质量约为决定元素的不同原子,影响原子的质量围绕原子核做高速运动每个电子带电荷相对质量为一个质子(中子)的1/1836核外电子层排布:最外层电子数目决定每个质子带电荷核电荷数(Z )= =质量数(A )= ( )+ ( ) 4.原子结构的表示方法:AZX【思考】①阳离子中A Z X n +:核外电子数=质量数(A )= + ②阴离子中A Z X m -:核外电子数= 质量数= + 二、元素、核素、同位素1.元素是 , 元素的种类由 决定。
填写下表并思考:①分别写出氕、氘、氚的原子符号表达式:氕 氘 氚 ②氕、氘、氚的原子结构有什么异同?它们是同一种元素吗?它们是同一种原子吗? ③原子核都是由质子和中子组成的吗?2.核素: 。
几种常见的核素(写出相应的核素符号)氢 ,碳 ,氧 ,氯 ,铀目前已经发现了112种元素,是否表示发现了112种原子?理由是什么?3.同位素: 。
它分为和两种,放射性同位素最常见的应用是制造氢弹原料的是,制造原子弹和核反应堆燃料的是。
三、核外电子排布1.核外电子运动的特征2.核外电子的分层排布看表2总结每层最多可以排布的电子数目?元素的性质与元素原子的最外层电子排布的关系(1)稀有气体原子最外层电子数为8(氦除外),结构稳定,性质;金属原子最外层电子数一般少于4个,易电子;表现性;非金属原子最外层电子数4个,较易获得电子,表现性。
(2)化合价是的一种重要性质。
元素化合价的数值,与特别是有关。
题型一:有关原子结构、元素、核素、同位素练习题例1.对于A Z X 和A+1Z X+ 两种粒子,下列叙述正确的是( ) A .质子数一定相同,质量数和中子数一定不同 B .化学性质几乎相同C .一定都由质子、中子、电子构成D .核电荷数,核外电子数一定相同 例2.、、、H +、H 2是 可以表示为 ( )。

[键入文字]
高一必修2 化学元素周期律知识点梳理
世界由物质组成,化学则是人类用以认识和改造物质世界的主要方法和手段之一。
精品小编准备了高一必修2 化学元素周期律知识点,希望你喜欢。
一.元素周期表的结构
周期序数=核外电子层数主族序数=最外层电子数
原子序数=核电荷数=质子数=核外电子数
二.元素的性质和原子结构
(一)碱金属元素:
2.碱金属化学性质的递变性:
递变性:从上到下(从Li 到Cs),随着核电核数的增加,碱金属原子的电子层数逐渐增多,原子核对最外层电子的引力逐渐减弱,原子失去电子的能力增强,即金属性逐渐增强。
所以从Li 到Cs 的金属性逐渐增强。
结论:
1)原子结构的递变性导致化学性质的递变性。
1。

第2课时核外电子排布整体构思教学目标1.课标要求了解原子核外电子排布。
2.三维目标知识与技能使学生了解关于原子核外电子运动特征的常识;了解原子核外电子排布的初步知识,能画出1~18号元素的原子结构示意图。
培养学生的空间想象能力、抽象思维能力和科学的分析推理能力。
过程与方法采用对比的方法分析核外电子的运动特征;通过学生的探究活动,完成对核外电子的分层排布的剖析。
情感态度与价值观通过对原子核外电子排布规律的分析,了解物质运动的复杂性和特殊性,培养学生“结构决定性质”的化学思想。
教学重点、难点1.重点:原子核外电子的排布规律。
2.难点:原子结构与元素性质间的联系。
教学方法本节采用“交流研讨”“自学探究”“学以致用”的教学方式,以“提出问题―→探究问题―→自学分析―→得出结论―→学以致用―→知识深化”等环节组织教学活动,帮助学生了解原子结构模型,体验假说和模型在科学研究中不可替代的作用,并掌握原子核外电子排布规律。
并通过老师引导,初步认识到原子结构与元素性质的关系,利用所学知识对元素的某些性质进行合理解释。
【教材学析】本节课是学生在学习了原子的结构之后,进一步向化学反应的实质迈进的一步。
它为必修Ⅰ教材中氧化剂、还原剂提供理论支持又为接下来学习元素周期律知识打下良好的基础,因此,从教材的前后关系来看,本节课具有承上启下的作用。
同时这节课涉及了化学上原子的发现史,所以本节课又是培养学生人文涵养的良好教材。
【学情分析】学生在初中已经初步接触了核外电子分层排布的思想,但初中各学校教学的程度不同以及学生之间的差异是客观存在的。
因此,教师只有全面地了解学生之间的差异,才能结合实际,有的放矢。
【教学流程】课前准备(一)学生准备:上网查阅,搜集有关原子结构模型的资料。
(二)教师准备:教学媒体、课件、相关资料。
板书设计二、核外电子的排布1.核外电子排布的规律:(1)电子是在原子核外距核由近及远、能量由低至高的不同电子层上分层排布,并分别命名为K、L、M、N、O、P、Q;(2)每层最多容纳的电子数为2n2(n代表电子层数);(3)电子一般总是尽先排在能量最低的电子层里,即最先排第一层,当第一层排满后,再排第二层,等等;(4)最外层电子数则不超过8个(第一层为最外层时,电子数不超过2个)。




高中化学必修2知识点归纳总结第一单元原子核外电子排布与元素周期律一、原子结构质子(Z个)原子核注意:中子(N个)质量数(A)=质子数(Z)+中子数(N)Z1.原子数 A X 原子序数=核电荷数=质子数=原子的核外电子核外电子(Z个)★熟背前20号元素,熟悉1~20号元素原子核外电子的排布:H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。
电子层:一(能量最低)二三四五六七对应表示符号:K L M N O P Q3.元素、核素、同位素元素:具有相同核电荷数的同一类原子的总称。
核素:具有一定数目的质子和一定数目的中子的一种原子。
同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。
(对于原子来说)二、元素周期表1.编排原则:①按原子序数递增的顺序从左到右排列②将电子层数相同的各元素从左到右排成一横行。
(周期序数=原子的电子层数)③把最外层电子数相同的元素按电子层数递增的顺序从上到下排成一纵行。
主族序数=原子最外层电子数2.结构特点:核外电子层数元素种类第一周期 1 2种元素短周期第二周期 2 8种元素周期第三周期 3 8种元素元(7个横行)第四周期 4 18种元素素(7个周期)第五周期 5 18种元素周长周期第六周期 6 32种元素期第七周期 7 未填满(已有26种元素)表主族:ⅠA~ⅦA共7个主族族副族:ⅢB~ⅦB、ⅠB~ⅡB,共7个副族(18个纵行)第Ⅷ族:三个纵行,位于ⅦB和ⅠB之间(16个族)零族:稀有气体三、元素周期律1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属性)随着核电荷数的递增而呈周期性变化的规律。
高一化学教案原子结构9篇原子结构 1教学目标1.常识性了解原子的核式结构.2.常识性了解通常情况下原子是中性的、物体不显电性的原因.3.常识性了解摩擦起电的原因.4.通过观察实物模型、各种媒体资料,建立原子及电子得失的微观图景,培养学生的抽象思维能力.教学建议教材分析本节的教学内容有:原子的微观结构、原子核外电子的得失及物体带电、摩擦起电的原因.是对第一节“摩擦起电两种电荷”的进一步分析和解释,在知识结构上二者是一个有因果关系的整体.教法建议关于原子结构的知识,通过教学要使学生认识到以下几点:原子是由位于中心的原子核和核外电子组成的;原子核带正电,电子带负电;在通常情况下,原子核所带的正电荷与核外电子总共所带的负电荷在数量上相等,整个原子呈中性.关于摩擦起电的原因,可以充分利用电教手段,帮助学生初步建立原子结构的微观图景,确立电子可以转移,从而使物体可以带两种电荷的观点,培养学生的抽象思维能力.在解释摩擦起电现象时,应抓住以下四点:(1)在通常情况下,原子呈中性,由原子组成的物体也呈中性.(2)不同物质的原子核束缚电子的本领不同.(3)两个物体相互摩擦时,哪个物体的原子核束缚电子的本领弱,它的一些电子就会转移到另一个物体上,失去电子的物体带正电,得到电子的物体带等量的负电.(4)强调“摩擦起电的原因是电荷从一个物体转移到另一个物体上,并不是摩擦创造了电荷.”教学设计方案教学过程应突出以下几个方面:一是在复习上一节知识的基础上引入新课.二是充分利用电教手段,帮助学生初步建立一个原子结构的微观图景,确立电子可以转移,从而使物体可以带两种电荷的观点,培养学生的抽象思维能力.三是多启发、多诱导,使教学过程真正成为学生的学习过程.1. 在复习上一节知识的基础上引入新课演示:用玻璃棒与丝绸摩擦吸引轻小物体.提问1:为什么玻璃棒会吸引碎纸屑?提问2:若将与玻璃棒摩擦过的丝绸靠近碎纸屑,会出现什么现象?提问3:自然界里存在几种电荷?提问4:被丝绸摩擦过的玻璃棒带什么电荷?摩擦起电的原因是什么?2.进行新课(1)物质的原子结构①物质由分子组成.简单介绍人类对物质微观世界的认识,并举例说明原子大小的数量级:经过科学家世世代代的研究,现在已经认识到,一切物质都是由分子构成的,分子又是由原子构成的.若把原子看作球形,一般原子的半径只有10-10米左右.设想把1亿个氧原子一个挨着一个地排成一行,也只有几厘米长.原子并不是组成物质的最小微粒,人们认识原子的结构,经历了漫长的时间,直到19世纪末叶,英国科学家汤姆生用实验证明了比原子小得多的带负电的粒子电子的存在,从此才揭示出原子是具有结构的.②原子的核式结构.原子是由位于中心的原子核和核外绕核高速运转的电子所组成;原子核半径约相当于原子半径的十万分之一,原子核几乎集中了原子的全部质量;原子核带正电,电子带负电.电子是带有最小负电荷的粒子,实验证明:一个电子所带电量为1.6×10-19库.一个电子也可叫做一个元电荷,用符号e表示.任何带电体带的电量都是e的整数倍.请同学们计算一下,多少个电子所带的电量是1库?(6.25×1018个)提问:那么通常情况下,物体为什么不显电性呢?(原子核所带的正电荷与核外电子总共所带的负电荷在数量上相等,整个原子呈中性.)不同物质中的原子核所带的电量并不相同,核外电子的数目也不相同.(利用氢原子、氧原子的原子挂图,讲解氢原子、氧原子的原子结构.)了解物质的原子结构.(2)摩擦起电的原因利用电教手段,帮助学生初步建立原子结构模型和原子得失电子的微观图景,并进一步归纳出结论:①不同物质的原子核束缚电子的本领不同.②失去部分电子的物体带正电,得到多余电子的物体带等量的负电.讨论:玻璃棒与丝绸摩擦后,玻璃棒带什么电?为什么带正电?(3)摩擦起电的实质电荷从一个物体转移到另一个物体上,并不是摩擦创造了电荷.探究活动上物理课时,老师精心准备的静电仪器,用丝绸摩擦玻璃棒,常常效果不明显,而满教室静观实验的学生却被自己的衣服不时电一下.因为学生的运动衣裤或其他外衣面料常常用尼龙织物的,比较结实,里面再穿件毛衣比较保暖.查一下起电顺序表就会发现,羊毛(羊皮)排最前面,尼龙排后,这是最容易起电的一套配置.每个人穿戴一套天然的静电起电设备.人的一举一动都造成摩擦,起电过程一刻也不停止.同样我们也可以理解过去的人穿不起毛衣,也没有这些化纤织物,棉布对棉布当然摩擦不出电来.为什么面粉厂车间总要洒水以保持空气潮湿?油罐车为什么要拖一条铁链?手握金属棒用丝绸摩擦能不能带电?化纤衣服面料中加一些金属线有什么用?原子结构 2教学目标1.常识性了解原子的核式结构.2.常识性了解通常情况下原子是中性的、物体不显电性的原因.3.常识性了解摩擦起电的原因.4.通过观察实物模型、各种媒体资料,建立原子及电子得失的微观图景,培养学生的抽象思维能力.教学建议教材分析本节的教学内容有:原子的微观结构、原子核外电子的得失及物体带电、摩擦起电的原因.是对第一节“摩擦起电两种电荷”的进一步分析和解释,在知识结构上二者是一个有因果关系的整体.教法建议关于原子结构的知识,通过教学要使学生认识到以下几点:原子是由位于中心的原子核和核外电子组成的;原子核带正电,电子带负电;在通常情况下,原子核所带的正电荷与核外电子总共所带的负电荷在数量上相等,整个原子呈中性.关于摩擦起电的原因,可以充分利用电教手段,帮助学生初步建立原子结构的微观图景,确立电子可以转移,从而使物体可以带两种电荷的观点,培养学生的抽象思维能力.在解释摩擦起电现象时,应抓住以下四点:(1)在通常情况下,原子呈中性,由原子组成的物体也呈中性.(2)不同物质的原子核束缚电子的本领不同.(3)两个物体相互摩擦时,哪个物体的原子核束缚电子的本领弱,它的一些电子就会转移到另一个物体上,失去电子的物体带正电,得到电子的物体带等量的负电.(4)强调“摩擦起电的原因是电荷从一个物体转移到另一个物体上,并不是摩擦创造了电荷.”教学设计方案教学过程应突出以下几个方面:一是在复习上一节知识的基础上引入新课.二是充分利用电教手段,帮助学生初步建立一个原子结构的微观图景,确立电子可以转移,从而使物体可以带两种电荷的观点,培养学生的抽象思维能力.三是多启发、多诱导,使教学过程真正成为学生的学习过程.1. 在复习上一节知识的基础上引入新课演示:用玻璃棒与丝绸摩擦吸引轻小物体.提问1:为什么玻璃棒会吸引碎纸屑?提问2:若将与玻璃棒摩擦过的丝绸靠近碎纸屑,会出现什么现象?提问3:自然界里存在几种电荷?提问4:被丝绸摩擦过的玻璃棒带什么电荷?摩擦起电的原因是什么?2.进行新课(1)物质的原子结构①物质由分子组成.简单介绍人类对物质微观世界的认识,并举例说明原子大小的数量级:经过科学家世世代代的研究,现在已经认识到,一切物质都是由分子构成的,分子又是由原子构成的.若把原子看作球形,一般原子的半径只有10-10米左右.设想把1亿个氧原子一个挨着一个地排成一行,也只有几厘米长.原子并不是组成物质的最小微粒,人们认识原子的结构,经历了漫长的时间,直到19世纪末叶,英国科学家汤姆生用实验证明了比原子小得多的带负电的粒子电子的存在,从此才揭示出原子是具有结构的.②原子的核式结构.原子是由位于中心的原子核和核外绕核高速运转的电子所组成;原子核半径约相当于原子半径的十万分之一,原子核几乎集中了原子的全部质量;原子核带正电,电子带负电.电子是带有最小负电荷的粒子,实验证明:一个电子所带电量为1.6×10-19库.一个电子也可叫做一个元电荷,用符号e表示.任何带电体带的电量都是e的整数倍.请同学们计算一下,多少个电子所带的电量是1库?(6.25×1018个)提问:那么通常情况下,物体为什么不显电性呢?(原子核所带的正电荷与核外电子总共所带的负电荷在数量上相等,整个原子呈中性.)不同物质中的原子核所带的电量并不相同,核外电子的数目也不相同.(利用氢原子、氧原子的原子挂图,讲解氢原子、氧原子的原子结构.)了解物质的原子结构.(2)摩擦起电的原因利用电教手段,帮助学生初步建立原子结构模型和原子得失电子的微观图景,并进一步归纳出结论:①不同物质的原子核束缚电子的本领不同.②失去部分电子的物体带正电,得到多余电子的物体带等量的负电.讨论:玻璃棒与丝绸摩擦后,玻璃棒带什么电?为什么带正电?(3)摩擦起电的实质电荷从一个物体转移到另一个物体上,并不是摩擦创造了电荷.探究活动上物理课时,老师精心准备的静电仪器,用丝绸摩擦玻璃棒,常常效果不明显,而满教室静观实验的学生却被自己的衣服不时电一下.因为学生的运动衣裤或其他外衣面料常常用尼龙织物的,比较结实,里面再穿件毛衣比较保暖.查一下起电顺序表就会发现,羊毛(羊皮)排最前面,尼龙排后,这是最容易起电的一套配置.每个人穿戴一套天然的静电起电设备.人的一举一动都造成摩擦,起电过程一刻也不停止.同样我们也可以理解过去的人穿不起毛衣,也没有这些化纤织物,棉布对棉布当然摩擦不出电来.为什么面粉厂车间总要洒水以保持空气潮湿?油罐车为什么要拖一条铁链?手握金属棒用丝绸摩擦能不能带电?化纤衣服面料中加一些金属线有什么用?原子结构 3教学目标1.常识性了解原子的核式结构.2.常识性了解通常情况下原子是中性的、物体不显电性的原因.3.常识性了解摩擦起电的原因.4.通过观察实物模型、各种媒体资料,建立原子及电子得失的微观图景,培养学生的抽象思维能力.教学建议教材分析本节的教学内容有:原子的微观结构、原子核外电子的得失及物体带电、摩擦起电的原因.是对第一节“摩擦起电两种电荷”的进一步分析和解释,在知识结构上二者是一个有因果关系的整体.教法建议关于原子结构的知识,通过教学要使学生认识到以下几点:原子是由位于中心的原子核和核外电子组成的;原子核带正电,电子带负电;在通常情况下,原子核所带的正电荷与核外电子总共所带的负电荷在数量上相等,整个原子呈中性.关于摩擦起电的原因,可以充分利用电教手段,帮助学生初步建立原子结构的微观图景,确立电子可以转移,从而使物体可以带两种电荷的观点,培养学生的抽象思维能力.在解释摩擦起电现象时,应抓住以下四点:(1)在通常情况下,原子呈中性,由原子组成的物体也呈中性.(2)不同物质的原子核束缚电子的本领不同.(3)两个物体相互摩擦时,哪个物体的原子核束缚电子的本领弱,它的一些电子就会转移到另一个物体上,失去电子的物体带正电,得到电子的物体带等量的负电.(4)强调“摩擦起电的原因是电荷从一个物体转移到另一个物体上,并不是摩擦创造了电荷.”教学设计方案教学过程应突出以下几个方面:一是在复习上一节知识的基础上引入新课.二是充分利用电教手段,帮助学生初步建立一个原子结构的微观图景,确立电子可以转移,从而使物体可以带两种电荷的观点,培养学生的抽象思维能力.三是多启发、多诱导,使教学过程真正成为学生的学习过程.1. 在复习上一节知识的基础上引入新课演示:用玻璃棒与丝绸摩擦吸引轻小物体.提问1:为什么玻璃棒会吸引碎纸屑?提问2:若将与玻璃棒摩擦过的丝绸靠近碎纸屑,会出现什么现象?提问3:自然界里存在几种电荷?提问4:被丝绸摩擦过的玻璃棒带什么电荷?摩擦起电的原因是什么?2.进行新课(1)物质的原子结构①物质由分子组成.简单介绍人类对物质微观世界的认识,并举例说明原子大小的数量级:经过科学家世世代代的研究,现在已经认识到,一切物质都是由分子构成的,分子又是由原子构成的.若把原子看作球形,一般原子的半径只有10-10米左右.设想把1亿个氧原子一个挨着一个地排成一行,也只有几厘米长.原子并不是组成物质的最小微粒,人们认识原子的结构,经历了漫长的时间,直到19世纪末叶,英国科学家汤姆生用实验证明了比原子小得多的带负电的粒子电子的存在,从此才揭示出原子是具有结构的.②原子的核式结构.原子是由位于中心的原子核和核外绕核高速运转的电子所组成;原子核半径约相当于原子半径的十万分之一,原子核几乎集中了原子的全部质量;原子核带正电,电子带负电.电子是带有最小负电荷的粒子,实验证明:一个电子所带电量为1.6×10-19库.一个电子也可叫做一个元电荷,用符号e表示.任何带电体带的电量都是e的整数倍.请同学们计算一下,多少个电子所带的电量是1库?(6.25×1018个)提问:那么通常情况下,物体为什么不显电性呢?(原子核所带的正电荷与核外电子总共所带的负电荷在数量上相等,整个原子呈中性.)不同物质中的原子核所带的电量并不相同,核外电子的数目也不相同.(利用氢原子、氧原子的原子挂图,讲解氢原子、氧原子的原子结构.)了解物质的原子结构.(2)摩擦起电的原因利用电教手段,帮助学生初步建立原子结构模型和原子得失电子的微观图景,并进一步归纳出结论:①不同物质的原子核束缚电子的本领不同.②失去部分电子的物体带正电,得到多余电子的物体带等量的负电.讨论:玻璃棒与丝绸摩擦后,玻璃棒带什么电?为什么带正电?(3)摩擦起电的实质电荷从一个物体转移到另一个物体上,并不是摩擦创造了电荷.探究活动上物理课时,老师精心准备的静电仪器,用丝绸摩擦玻璃棒,常常效果不明显,而满教室静观实验的学生却被自己的衣服不时电一下.因为学生的运动衣裤或其他外衣面料常常用尼龙织物的,比较结实,里面再穿件毛衣比较保暖.查一下起电顺序表就会发现,羊毛(羊皮)排最前面,尼龙排后,这是最容易起电的一套配置.每个人穿戴一套天然的静电起电设备.人的一举一动都造成摩擦,起电过程一刻也不停止.同样我们也可以理解过去的人穿不起毛衣,也没有这些化纤织物,棉布对棉布当然摩擦不出电来.为什么面粉厂车间总要洒水以保持空气潮湿?油罐车为什么要拖一条铁链?手握金属棒用丝绸摩擦能不能带电?化纤衣服面料中加一些金属线有什么用?原子结构 41.3 原子结构的模型教学目标:1、了解原子的构成、原子结构模型及其在历史上的发展过程,体验建立模型的思想。
高一化学原子结构试题
1、简单原子的原子结构可用下图形象地表示( )
其中表示质子或电子,表示中子。
则下列有关①②③的叙述中,正确的是
A.①②③互为同位素 B.①②③互为同素异形体
C.①②③是三种物理性质相同的粒子 D.①②③具有相同的质量数
2、下列说法中肯定错误的是( )
A.某原子K层上只有一个电子
B.某原子M层上电子数为L层上电子数的4倍
C.某离子M层上和L层上的电子数均为K层的4倍
D.某离子的核电荷数与最外层电子数相等
3、已知R2+核外有a个电子,b个中子,表示R原子符号正确的是()
A. B. C. D. .
4、16O和18O是氧元素的两种核素, N A表示阿伏加德罗常数,下列说法正确的是( )
A.16O2与18O2互为同分异构体 B.16O与18O核外电子排布方式不同
C.通过化学变化可以实现16O与18O间的相互转化 D.标准状况下,1.12 L16O2和1.12 L18O2均含0.1N A个氧原子
5、质子数和中子数相同的原子A,其阳离子A n+核外共有X个电子,则A的质量数为()
A.2(x+n) B.2(x-n) C.2x D.n+2
6、核电荷数为1~18的元素中,下列叙述正确的是( )
A最外层只有1个电子的原子一定是金属元素的原子 B最外层只有2个电子的原子一定是金属元素的原子
C原子核外各电子层电子数相等的原子一定是金属元素的原子 D最外层电子数最多的原子最容易获得电子
7、下列说法中正确的是( )
A.某微粒核外电子排布为2、8、8,则该微粒一定是氩原子 B.最外层电子达到稳定结构的微粒只能是稀有气体元素的原子C.F-、Na+、Mg2+、Al3+是与Ne原子具有相同电子层结构的离子
D.既不容易获得电子形成阴离子,也不容易失去电子形成阳离子的原子,最外层电子已达稳定结构
8、某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成H m X分子。
在a g H m X中所含质子的物质的量是( )
A.a
A+m (A-N+m) mol B.
a
A
(A-N) C.
a
A+m
(A-N) D.
a
A
(A-N+m)
9、有a X n-和b Y m+两种简单离子(a、b均小于18),已知a X n-比b Y m+多两个电子层,下列关系和说法正确的是
A.X只能是含有三个电子层的元素
B.a-b+n+m等于10或等于16
C.Y是质子数不小于5的元素
D.Y不可能是含有两个电子层的元素
10、下列说法中不正确的是( )
①质子数相同的粒子一定属于同一种元素②同位素的性质几乎相同③质子数相同电子数也相同的两种粒子,不可能是一种分子和一种离子④同一种元素的核素种类由中子数决定
A.②③
B.①②
C.①④
D.③④
11.下列说法正确的是( )
A.只含一种元素的物质一定是纯净物
B.质量数和电子数相同的微粒,一定是同位素
C.质量数相同的两种原子一定属于同种元素
D.质量数不同的两种微粒的化学性质可能相同
12、某元素构成的双原子单质分子只有3种,其相对分子质量分别为158、160、162,在天然单质中,此3种单质的物质的量之比为1∶1∶1,由此推断,以下结论中正确的是( )
A.此元素有3种同位素
B.其中一种同位素的质量数为80
C.此元素有2种同位素
D.此元素的单质的平均相对分子质量为158
13、下面是某同学所画的各原子的原子结构示意图,你认为正确的是( )
14、已知R 2+离子核外有a 个电子,b 个中子。
表示R 原子符号正确的是( )
A .b a R
B .
a+b-2a-2R C .a+b+2a+2R D .a+b a-2R 15、13C —NMR(核磁共振)、15N —NMR 可用于测定蛋白质、核酸等生物大分子的空间结构,瑞士科学家库尔特、维特里希等人为此获得2002年诺贝尔化学奖。
下列有关13C 、15N 的叙述正确的是( )
A .15N 与14N 互为同位素
B .13
C 与C 60互为同素异形体
C .13C 、15N 具有相同的中子数
D .15N 的核外电子数与中子数相同
16、X 、Y 、Z 、R 分别代表四种元素,如果+m a X 、+n b Y 、-n c Z 、-m d R 四种离子的电子层结构相同,则下列关系正确的是( )
A 、a-c=m-n
B 、a-b=n-m
C 、c+d=m+n
D 、b-d=n+m
17某元素原子R 的质量数为A ,R m-的核外电子数为x ,则Wg R m-
离子所含中子的物质的量为( )
A. (A-x+m) mol
B. (A-x-m) mol
C.
D.
18.在离子RO 3n-中共有x 个核外电子,R 原子的质量数A ,则R 原子核内含有的中子数是( ) A. A-x+n+48 B. A-x-n-24 C. A-x+n+24 D. A+x-n-24
19.最新科技报导,美国夏威夷联合天文中心的科学家发现了新型氢微粒,这种新微粒是由3个氢原子核(只含质子)和2个电子构成,对于这种微粒,下列说法中正确的是( )
A .是氢的一种新的同素异形体
B .是氢的一种新的同位素
C .它的组成可用H 3表示
D .它比一个普通H 2分子多一个氢原子核
20.Na和Na+两种粒子中,不相同的是()
①核内质子数②核外电子数③最外层电子数④核外电子层数
A.①②
B.②③
C.③④
D.②③④
21.下列关于核外电子排布的说法中不正确的是()
A.第n层电子层最多可容纳的电子数为2n2
B.第二电子层中最多可容纳的电子数为8
C.最多可容纳8个电子的电子层一定是第二电子层
D.最多可容纳2个电子的电子层一定是第一电子层
22.两种元素原子的核外电子层数之比与它们的最外层电子数之比相等。
在周期表中的前10号元素中,满足上述关系的元素共有()
A.1对
B.2对
C.3对
D.4对
23、有下列微粒:①11H;②21H;③31H;④16O;⑤18O;⑥12C;⑦14C;⑧40K;⑨40Ca;⑩35Cl2;⑾37Cl2,回答以下问题(填序号):
(1)以上11种微粒共含有________种核素,属于________种元素。
(2)互为同位素的是________;________;________。
(3)质量数相等的微粒是____________。
(4)形成的水分子共有________种。
24、根据下列叙述,写出微粒符号。
(1)原子核外有2个电子层,核外有10个电子的原子:___________。
(2)原子核外有3个电子层,最外层有7个电子的原子:___________。
(3)质量数为24,质子数等于中子数的原子:___________。
(4)最外层电子数是次外层电子数的4倍的二价阴离子:_________。
(5)电子总数为18的一价简单阳离子:___________。
25、有A、B、C、D、E五种微粒,已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到一个电子后,其电子层结构与氩原子相同;
③C微粒带有两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。
(1)写出这五种微粒的符号:A________B______C_______D________E_________。
(2)B微粒的结构示意图为___________________,C微粒的结构示意图为__________________。
(3)A的单质与EB溶液反应的离子方程式为______________________________________。
26.A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次递增,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍。
试推断它们各是什么元素,写出它们的元素符号:
A _____ ,
B ______ ,
C _______ ,
D ______ 。