第二章 单级平衡过程
- 格式:pdf
- 大小:376.39 KB
- 文档页数:16
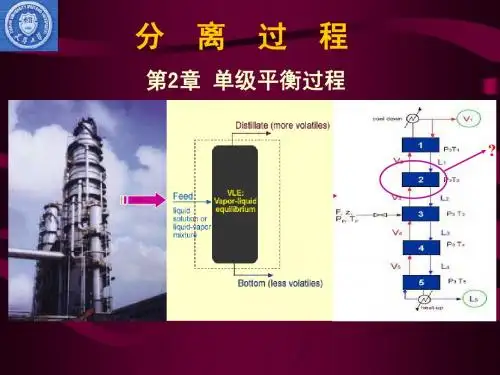

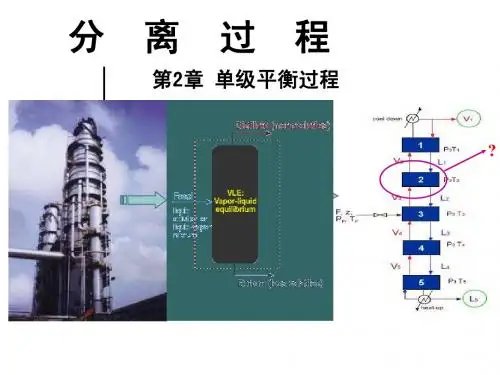
第二章 单级平衡过程Chapter2 Single stage balance process单级平衡分离是指两相经一次紧密接触达到平衡后随即引离的过程,由于平衡两相的组成不同,因而可起到一个平衡级的分离作用。
其相平衡用于阐述混合物分离原理、传质推动力和设计计算。
§2-1汽液相平衡(Vapour-liquid phase equilibrium )所谓相平衡是指两个或两个以上的相处于平衡状态。
“平衡”的意思是指:在宏观上系统的性质随时间而改变的趋势已达到零。
而所谓“相”,是指任何数量的物质在其所占据的空间内宏观性质是均匀一致的,没有不连续的地方。
一定数量的物质,即使被分割成若干部分,但只要它们的性质和组成完全一样,则可把它们称为一个“均相”。
若有两个或两个以上的均相,虽然它们互相紧密接触,但它们各自的性质并不随时间而改变,通常,就用“相平衡“这一词来表达这一状态。
对于双组分系统温度—压力—组成的平衡关系,常常利用实验来测得,而多组分系统的相平衡关系用实验方法来测定就比较复杂。
随着相平衡理论研究的深入,对双组分和多组分系统的汽液相平衡已建立了一些定量的关系式,利用这些关系式,它只需用少量的双组分的实验数据,这就大大地减轻了实验工作量。
一、汽液相平衡关系(Vapour-liquid phase equilibrium ) 1. 基本关系式相平衡条件:组分i 在汽液两相中的化学位相等,L i V i μμ= 也可表示为组分i 在汽液两相中的逸度相等,L iV i f f ˆˆ= i V i V i i V i V i y f y P f 0ˆˆγφ== iL i L i i L i L i x f x P f 0ˆˆγφ== i L i i V i x P y P φφˆˆ= 或 ii L i i V i x f y P γφ0ˆ= ()RTP P V P f Si i S iSi Li-=ex p 0φ2. 相平衡常数i k ①定义工程中常用相平衡常数来表示相平衡关系iii x y k =i k 表示了i 组分在平衡的汽液两相中的分配情况,俗称分配系数。




化工分离过程教师:教师:孙章化学工程学院目录第二章单级平衡过程第五章分离设备的处理能力和效率第二章单级平衡过程第三节闪蒸过程的计算第三节闪蒸过程的计算汽液平衡常数与组成有关的闪蒸计算同时收敛法2.3 闪蒸过程的计算2.3.1 等温闪蒸和部分冷凝过程2.3.2 绝热闪蒸过程底部产物L ,x顶部产物V ,y加热器节流阀闪蒸过程描述普通精馏塔中的平衡级就是一简单绝热闪蒸级。
2个∑i ∑i LV LH VH Q FH +=+2C+3变量数:3C+8个C+3C +5(F, T F , P F , T, p,V, L, Q, z i , y )2分为如下五类:Q, T(或p), L,y i ,x i部分汽化p(或T),V(或ψ)i i p,T表2-4 闪蒸计算类型√*进行闪蒸计算之前,需要核实闪蒸问题是否成立!ΣK i z i =1ΣK i z i >1,Σ(z i /K i )=1,Σ(z i /K i )>1 只有当T B <T<T D 时,才构成闪蒸问题。
反之,若ΣK i z i <1, 则为过冷液体;若Σ(z i /K i )<1, 则为过热蒸汽。
T>T B T<T D2.3.1 等温闪蒸规定:p 、T一、汽液平衡常数与组成无关),(P T f K i =值容易确定,所以联立求解上述(2C+3)个方程比较简单。
具体步骤如下:,...C,i Vy Lx Fz i i i 21 =+=Ci x K y i i i ,...2,1 ==Ci x VK Lx Fz i i i i ,...2,1 =+=V F L -=C i VK V F Fz x i ,...2,1 =+−=(2-66)/V Fψ=汽化率)1(1−+=i i i K z x ψ(2-68))1(1−+==i i i K z K x K y ψ1)1(11=−+∑=C i i i K z ψ(2-69)(1)1(11=−+∑=Ci i i i K z K ψ0)1(1)1()(1=−+−=∑=i i i K z K f ψψ(2-71)方程通过闪蒸方程(2-71)求出汽化率ψ后,由()和(2-68)式可分别求出x i 和y i ,进而由总物料衡算式(2-64)可求出V 和L ,由热量衡算式(2-65)可求出Q 。


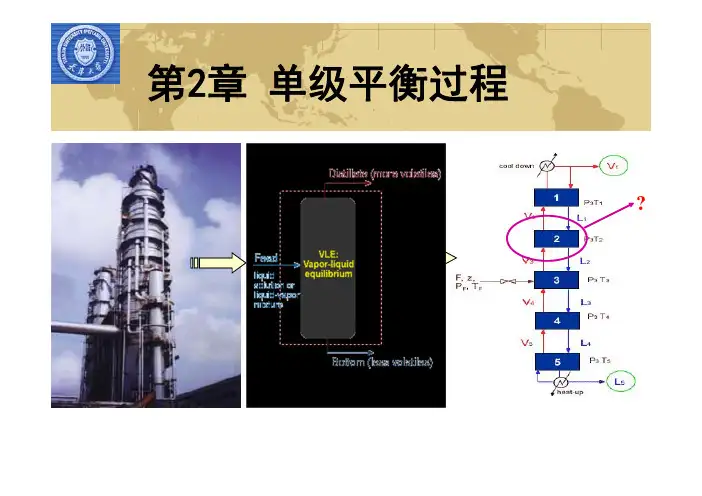
第二章单级平衡过程2.2 多组分物系的泡点和露点计算1要点(1)泡点、露点的概念;(2)泡点温度和压力的计算方法;(3)露点温度和压力的计算方法。
23名词解释:①泡点温度(Bubble-point temperature):液体混合物在一定压力下开始沸腾时的温度,称为在这压力下的泡点温度。
泡点温度随液体组成不同而改变,随压力不同而变化。
对于纯液体, 泡点温度即是该压力下的沸点。
=(,)b i T f P x T--XT--Y X, Y TP4名词解释:①泡点温度(Bubble-point temperature):液体混合物在一定压力下开始沸腾时的温度,称为在这压力下的泡点温度。
泡点温度随液体组成不同而改变,随压力不同而变化。
对于纯液体, 泡点温度即是该压力下的沸点。
=(,)b i T f P x T--XT--Y X, Y TP5名词解释:①泡点温度(Bubble-point temperature):液体混合物在一定压力下开始沸腾时的温度,称为在这压力下的泡点温度。
泡点温度随液体组成不同而改变,随压力不同而变化。
对于纯液体, 泡点温度即是该压力下的沸点。
=(,)b i T f P x T--XT--Y X, Y TP②泡点压力(Bubble-point pressure):液体混合物在一定温度下开始沸腾时的压力,称为在这温度下的泡点压力。
泡点压力随液体组成不同而改变, 随温度不同而变化。
对于纯液体,泡点压力即是该温度下的饱和蒸汽压。
=(,)b iP f T xP--YPX, Y TP--X67③露点温度(Dew-point temperature):汽体混合物在一定压力下达到饱和开始结成液滴时的温度,称为在这压力下的露点温度。
露点温度随汽体组成不同而改变,随压力不同而变化。
(,)d i T f P y =T--XT--Y X, YTP8④露点压力(Dew-point pressure):汽体混合物在一定温度下达到饱和开始结成液滴时的压力,称为在这温度下的露点压力。