一级反应---过氧化氢分解
- 格式:xls
- 大小:28.00 KB
- 文档页数:3
一级反应——过氧化氢的催化分解
1.数据记录
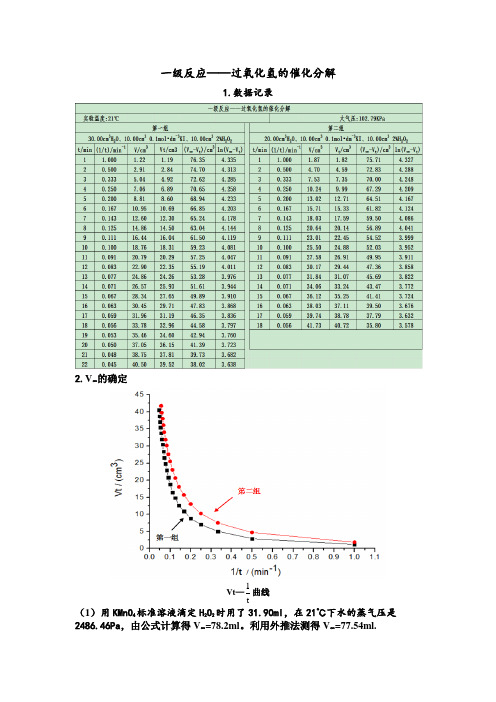
2.V ∞的确定
Vt —t
1
曲线
(1)用KMnO4标准溶液滴定H2O2时用了31.90ml,在21℃下水的蒸气压是2486.46Pa,由公式计算得V∞=78.2ml。
利用外推法测得V∞=77.54ml.
3.求k1.
ln(V∞-Vt)
第一组
第二组
t / min
ln(V∞-Vt)—t曲线
第一组
第二组
由图表可知:第一组中k1=-0.0333;第二组中k1=-0.0439.
4.求k.
根据k1=kc KI求算k。
则第一组中k=-0.333;第二组中k=-0.439.
注意事项及思考题
(1)摇晃过氧化氢分解瓶是应注意不要用手握住瓶身及瓶底,避免温度对实验
造成的影响。
(2)读取氧气体积时,使量气管及水准瓶中水面处于同一水平面,就是继续保持内外的压力相等,有利于准确读取在t时刻产生氧气的体积。
(3)摇晃分解瓶的快慢对试验会产生影响吗?
答:搅拌对实验也有影响。
为进行比较,搅拌要适当,每次实验的搅拌情况尽量一致。
(4)H2O2和KI溶液的初始浓度对实验结果是否有影响?应根据什么条件选择它们?
答:有影响;因为V∞与H2O2的初始浓度C0成正比,而k又与催化剂KI 溶液的浓度成正比,所以说它们对实验结果是有影响的。

过氧化氢的催化分解一、实验目的1、了解不同催化剂对过氧化氢(H2O2)催化分解速率的影响。
2、认知能催化分解H2O2的不同催化剂。
二、实验原理过氧化氢催化分解是一级反应:H2O2→H2O+1/2O2.。
(凡是反应速度只与反应浓度的一次方成正比的反应称为一级反应。
)实验证明,过氧化氢的反应机理为一级反应.化学反应速度取决于反应物的浓度、温度、反应压力、催化剂、搅拌速度等许多因素。
许多催化剂如Pt、Ag、Cr、MnO2、FeCl3、CuO、血液、铁丝、炭粉、土豆丝等都能加速H2O2分解。
用土豆丝来催化分解H2O2溶液,说明生物体内不断产生的过氧化氢酶,可促使H2O2迅速分解,这种酶广泛存在于动植物组织中。
三、实验仪器与药品仪器:试管(2个)、具支试管(1个)、锈铁丝、气球、土豆丝、药品:H2O2溶液,四、实验步骤1,过氧化氢溶液的制备用移液管吸取30℅H2O2溶液5ml,置于50ml容量瓶中,稀释至刻度线,摇匀定容,即得实验用的H2O2溶液。
2,酶催化作用的验证实验取两只试管,在一支试管中放入切成细条状的土豆丝。
分别向两支试管中注入3%的H2O2 5ml,注意观察现象(放入土豆丝的试管中迅速产生大量的气泡,泡沫很快充满试管;用玻璃棒桶开泡沫,)插入带火星的木条,则木条立即复燃,而另一支试管中无明显现象。
3,用抽动法做“催化剂对H2O2分解速度的影响”的实验①取一支具支试管,在具支试管中加入10ml浓度30%H2O2溶液,在支管上装上小气球,通过橡皮塞插入一根已生锈的绕成螺旋状的粗铁丝。
②将螺旋状的锈铁丝向下插入H2O2溶液中是,注意观察现象的变化。
(H2O2迅速分解,锈铁丝表面上,有大量气泡产生。
气球鼓起;把铁丝向上拉,离开H2O2溶液,则反应不明显。
)③取下塞子,用带火星木条放在试管口,注意观察现象变化。
(则木条立即复燃,说明有O2生成。
)五、注意事项1、实验过程中注意安全2、玻璃仪器轻拿轻放六、思考题1,催化剂对反应速度有何影响?2,常用催化剂有哪些?。

积分后得浓度与时间关系:(12-5)式中,k-一级速率常数,S-1,min-1或h-1,d-1等。
以lgC与t作图呈直线,直线的斜率为-k/2.303,截距为lgC0。
通常将反应物消耗一半所需的时间为半衰期(half life),记作t1/2,恒温时,一级反应的t1/2与反应物浓度无关。
(12-6)对于药物降解,常用降解10%所需的时间,称十分之一衰期,记作t0.9,恒温时,t0.9也与反应物浓度无关。
(12-7)反应速率与两种反应物浓度的乘积成正比的反应,称为二级反应。
若其中一种反应物的浓度大大超过另一种反应物,或保持其中一种反应物浓度恒定不变的情况下,则此反应表现出一级反应的特征,故称为伪一级反应。
例如酯的水解,在酸或碱的催化下,可按伪一级反应处理。
3温度对反应速率的影响与药物稳定性预测编辑阿仑尼乌斯(Arrhenius)方程大多数反应温度对反应速率的影响比浓度更为显著,温度升高时,绝大多数化学反应速率增大。
Arrhenius根据大量的实验数据,提出了著名的Arrhenius经验公式,即速率常数与温度之间的关系式(12-8)。
k=Ae-E/RT (12-8)式中,A-频率因子;E-为活化能;R-为气体常数。
上式取对数形式为:(12-9)或(12-10)一般说来,温度升高,导致反应的活化分子分数明显增加,从而反应的速率加快。
对不同的反应,温度升高,活化能越大的反应,其反应速率增加得越多。
药物稳定性的预测在药剂学中阿仑尼乌斯方程可用于制剂有效期的预测。
根据Arrhenius方程以1gk对1/T作图得一直线,此图称Arrhenius图,直线斜率为-E/(2.303R),由此可计算出活化能E,若将直线外推至室温,就可求出室温时的速度常数(k25)。
由k25可求出分解10%所需的时间(即t0.9)或室温贮藏若干时间以后残余的药物的浓度。
实验时,首先设计实验温度与取样时间,然后将样品放入各种不同温度的恒温水浴中,定时取样测定其浓度(或含量),求出各温度下不同时间药物的浓度变化。

过氧化氢的催化分解一、实验原理过氧化氢水溶液在室温下,没有催化剂存在时,分解反应进行得很慢,但在含有催化剂I –的中性溶液中,其分解速率大大加快,反应式为:2H 2O 2 == 2H 2O + O 2(g)反应机理为: H 2O 2 + I – → H 2O + IO – k 1 (慢) (1) H 2O 2 + IO – → H 2O + O 2(g) + I – k 2 (快) (2) 整个分解反应的速率由慢反应(1)决定,速率方程为: 22-22H O 1H O I dc k c c dt-=因反应(2)进行得很快且很完全,I –的浓度始终保持不变,故上式可写成: 2222H O H O dc kc dt-=式中,-1I k k c =,k 为表观反应速率常数。
将上式积分得 0lnc kt c= 此式表明,反应速率与H 2O 2浓度的一次方成正比,故称为一级反应。
将上式积分得:01ln ln c t k c t +-=式中c 0、c t 分别为反应物过氧化氢在起始时刻和t 时刻的浓度。
反应半衰期为: 112/1693.02ln k k t ==设H 2O 2完全分解时放出O 2的体积为V ∞,反应t 时放出O 2的体积为V , 则c 0∝V ∞,c ∝(V ∞ – V ),故 lnV kt V V ∞∞=-ln-V Vkt V ∞∞-= ln -+ln V V kt V ∞∞-=()以ln(V ∞ – V )对t 作图应得一直线,从直线斜率(– k )即可求得H 2O 2分解反应的速率常数。
故实验需测定反应不同时刻O 2的体积V 及H 2O 2完全分解时O 2的体积V ∞。
V ∞可用下法之一求出。
(a) 加热法 在测定若干个V 数据后,将H 2O 2溶液加热至50~60 ℃ 约15 min ,可以认为H 2O 2已分解完全,待冷却至室温后,记下量气管的读数,即为V ∞。
(b) 浓度标定法 用KMnO 4标准溶液对H 2O 2原始浓度进行标定,O 2近似按理想气体处理,则有2222222H O H O O O O 2c V RT RT V n p p ∞⋅=⋅=⋅ 式中,2O p 为O 2的分压,是外界大气压与实验温度下水的饱和蒸气压之差。

过氧化氢催化分解速率常数的测定一、实验原理过氧化氢(H2O2)在存在催化剂的情况下,能够催化分解成水和氧气。
该反应速率与催化剂种类、催化剂浓度、温度等因素有关。
过氧化氢的分解反应可以用如下反应式表示:2H2O2 → 2H2O + O2在一定的反应条件下,反应速率的快慢可以通过测定反应的速率常数来确定。
速率常数k的单位是mol/(L/s),表示单位时间内单位体积溶液中反应物的消耗量。
二、实验目的1. 了解催化剂对过氧化氢分解反应速率的影响;2. 能够通过实验测定速率常数k。
三、实验仪器和试剂1. 50 mL锥形瓶、滴定管、分液漏斗、实验管夹等;2. 过氧化氢(H2O2)、氯化铁铵六水合物(NH4Fe(SO4)2·6H2O)。
四、实验步骤1. 实验前准备(1)空气中存在的灰尘和微生物等会影响实验结果,因此需先将仪器、试剂及其他必需的物品仔细清洗干净。
(2)将50 mL锥形瓶放入水浴中,加热至50℃。
2. 实验操作(1)将实验管夹夹住滴定管,用滴定管分别向50 mL锥形瓶中加入10 mL的H2O2溶液和2 mL的NH4Fe(SO4)2·6H2O溶液。
(2)迅速将实验管夹取下,并立即开始计时。
(3)记时,每隔30秒取出一个样品到冷水中浸泡降温。
(4)将样品移入滴定管中,加入一滴甲基橙指示剂,用已知浓度的Na2S2O3标准溶液滴定至淡黄色为止。
(5)按相同方法进行4次实验数据采集。
五、实验结果与分析序号时间t(min)[H2O2](mol/L)实验室温度T(℃)Na2S2O3消耗量V (mL)1 0.5 0.020 21.8 22.02. 计算速率常数k值过氧化氢的分解反应速率遵循一级反应速率方程,即:-rate/k = d[H2O2]/dt = k[H2O2]根据速率方程,可用ln[H2O2]关于时间t的直线斜率来表示反应的速率常数k,其表达式是:其中,[H2O2]0为反应体系初始浓度,kt为反应时的ln[H2O2]的变化量。

过氧化氢催化分解反应速率常数的测定标签:分类:药学资料化学实验报告过氧化氢反应速率常数教育一、实验目的(1)了解过氧化氢催化分解反应速率常数的测定方法。
(2)熟悉一级反应的特点,了解催化剂对反映速率的影响。
(3)掌握用图解计算法求反应速率常数。
二、实验用品1、仪器玻璃反应容器1个、水准瓶1个、50mL量气管1个、超级恒温槽1套、三通活塞1个、秒表1块、10mL量筒1个、5mL吸量管2支、胶管3m。
2、药品-1KI溶液。
质量分数为2%的H2O2溶液(新鲜配制)、0.1mol·L三、实验原理与技术过氧化氢很不稳定,在常温下的分解反应式为:H2O2→H2O+1/2O2(Ⅰ)在KI作用下的分解反应机理为:H2O2+KI→KIO+H2O(慢)(Ⅱ)KIO→KI+1/2O2(快)(Ⅲ)(Ⅱ)式是H2O2分解的速控步骤,H2O2分解反应的反应速率方程为:-dc H2O2/dt=k′c H2O2·c KI(Ⅳ)因为c KI近似不变,(Ⅳ)式可简化为:-dc H2O2/dt=kc H2O2(Ⅴ)(其中k=k′c KI)。
H2O2的催化分解反应为一级反应,对(Ⅴ)式积分可得:ln(c/c0)=-kt(Ⅵ)(其中c0为H2O2的初始浓度;c为反应至t时刻H2O2的浓度;k为H2O2的催化分解反应的速率常数)。
反应的半衰期为:t1/2=ln2/k=0.693/k(Ⅶ)在等温等压条件下,在H2O2的分解反应中,氧气体积增长速率反映了H2O2的分解速率,本实验就是通过测定不同时刻放出的氧气的体积,间接地求出H2O2在相应时刻的浓度,这种方法称为物理法。
令ⅴ∞表示H2O2全部分解放出的O2的体积;ⅴt表示反应至t时刻放出的O2的体积;则由(Ⅰ)式可看出:定温定压下反的O 2的体积ⅴt 与被消耗的H 2O 2的浓度成正比,而ⅴ∞则与H 2O 2的初始浓度成正比,且两者比例系数,则:c 。
∝ⅴ∞;c ∝(ⅴ∞-ⅴt )。
实验31 一级反应动力学—H 2O 2催化分解速率系数的测定 预习要求1. 本实验中使用什么物质作为催化剂;其使用时的注意事项。
2. 本实验反应过程中反应物浓度的变化的表示方法。
3. 反应速率系数的概念及影响因素。
实验目的1.了解催化剂在催化反应中的作用特征。
2.测量H 2O 2催化分解反应的速率系数及表观活化能。
实验原理对于反应: a A + b B = y Y + z Z其反应速率与反应物的量浓度的关系可通过实验测定得到。
多数反应的速率方程的形式为:υA = k A c Aα c B β 若实验确定某反应物A 的消耗速率与反应物A 的浓度的一次方成正比,则该反应对A 为一级反应。
其反应速率方程为:—d c A / d t = k A c A (3-19) 以过氧化氢分解反应为例,H 2O 2 → H 2O + ½O 2实验证明过氧化氢分解反应的反应速率与H 2O 2(A )浓度的关系符合式(3-19)。
将式(3-19)积分得:ln (c A / c A ,0)= -k A t (3-20) 式中:k A ——反应速率系数;c A ——反应时刻为t 时H 2O 2的浓度;c A,0——反应开始前H 2O 2的浓度。
在反应不同时刻测得H 2O 2的浓度,代入式(3-20)即可求出反应速率系数k A 。
H 2O 2分解过程中有O 2放出。
若保持生成O 2的温度、压力不变,可通过测量放出O 2的体积,经过代换得到溶液中H 2O 2的浓度。
设浓度为c A ,0的H 2O 2全部分解放出的氧气体积为V ∞,反应时刻t 时H 2O 2分解放出的氧气体积为V t ,则c A ,0∝V ∞ ; c A ∝(V ∞ – V t )将以上关系式代入式(3-20)得:t k V V V t A ∞∞-=-ln(3-21) 或 V t k )V V (t ∞A ∞lg +2.303-=-lg (3-22) 以lg (V ∞-V t )对t 作图。
五.实验结果及数据处理(1)H2O2分解反应速率常数的测定与计算本次实验采用差减法处理实验数据可分别得t及+∆t时刻方程为由k1=ln V∞V∞−V ttV∞−V t=V∞exp−k1tV∞−V t+∆t=V∞exp−k1t+∆t取∆t为恒等时间,则上两式相减得V t+∆t−V t=Aexp−k1t式中A=V∞1−exp−k1t为常数。
令B=ln A,上式又可写为ln V t+∆t−V t=−k1+B将数据测定分为前段与后段,以后段各数据分别对相等时间间距∆t的前段数据相减可得V t+∆t的一组数据,利用ln V t+∆t−V t对t作图而得到k1。
(2)半衰期的计算半衰期t=ln2k1①25mL0.05mol∙dm−3KI+10mL约1mol∙dm−3H2O2溶液。
取∆t为1.5min,得到如下数据。
表1利用ln V t+∆t−V t对t作图,得到如下图表。
故k 1=0.0136t =ln 20.0136=50.97②25mL0.1mol ∙dm −3KI +10mL 约1mol ∙dm −3H 2O 2溶液。
取∆t 为1.0min ,得到如下数据。
表2利用ln V t +∆t −V t 对t 作图,得到如下图表。
故k 1=0.0262t =ln 20.0262=26.46③25mL0.1mol∙dm−3KI+5mL约1mol∙dm−3H2O2溶液+10mL约1mol∙dm−3H2O。
取∆t为1.5min,得到如下数据。
表3利用ln V t+∆t−V t对t作图,得到如下图表。
=25.96故k1=0.0267t=ln20.0267。
过氧化氢催化分解实验目的:1. 测定KI催化H2O2分解反应的速率常数和反应级数。
2. 掌握一级反应的特性,考察反应物浓度、催化剂浓度等对反应速率常数的影响。
3. 掌握由动力学数据确定反应速率常数及反应级数的方法。
实验内容:1.测定不同反应条件下H2O2分解产生氧气的速率,以产生一定体积的氧气所对应的时间计算。
2.准确标定H2O2溶液的初始浓度c0。
3.计算V∞的数值。
4.做ln(V∞-V t)-t图,由直线斜率求表观反应速率常数及相对应的半衰期。
实验进程:一、讲解内容1. 做好实验准备,在实验开始前要求学生将恒温水浴温度调节到(25±0.10)℃并打开循环水泵进行恒温。
2. 实验原理:过氧化氢是一种很不稳定的化合物,在没有催化剂存在时,分解很慢,加入催化剂可以加速其分解。
(1)提问:大家肯定已经学习过过氧化氢的分解反应,反应产物为?(1)在加入催化剂KI的条件下,H2O2的反应进程加快,讲解反应步骤:慢(2)快(3)由以上机理可知,KI和H2O2生成的中间产物改变了反应途径,降低了反应的活化能,从而加速了反应进程。
研究表明,反应(2)的速率远慢于反应(3),反应(2)为整个分解过程的控速步骤,而总反应(1)的速率就等于(2)的反应速率,故H2O2分解反应速率方程可表示为:(4)式中,c表示各物质浓度(mol / L);t为反应时间;k为反应速率常数,其职与温度、催化剂等有关。
反应中KI作为催化剂,浓度不发生改变,可令k=,式(4)可简化为:(5)k为表观反应速率常数,量纲为[时间]-1。
由式(5)可以看出,反应速率与反应物浓度的一次方成正比,故H2O2催化分解反应为一级反应,其表观反应速率常数k将随温度和KI浓度变化而变化。
将式(5)积分得:+(6)式中,c0为H2O2的初始浓度;c t为t时刻H2O2的浓度。
以对t作图若为一直线,则确定H2O2催化分解反应为一级反应,并可由直线斜率求出反应速率常数k。