硫酸锌溶液的电解.ppt
- 格式:ppt
- 大小:916.62 KB
- 文档页数:21

电解硫酸锌方程式
电解硫酸锌方程式是指将硫酸锌溶液通过电解分解反应转化为锌金属和氧气的化学反应。
该反应可以用如下方程式表示:
ZnSO4 -> Zn + O2
在该方程式中,ZnSO4代表硫酸锌,Zn代表锌金属,O2代表氧气。
电解是一种通过外加电流使溶液中的化学物质发生氧化还原反应的方法。
在电解过程中,正极(阳极)会发生氧化反应,负极(阴极)会发生还原反应。
在电解硫酸锌中,硫酸锌溶液被电解时,硫酸锌分解成锌金属和氧气。
具体来说,硫酸锌是一种离子化合物,它在溶液中会完全离解成锌离子(Zn2+)和硫酸根离子(SO42-)。
在电解过程中,阳极上的氧化反应将发生,硫酸根离子(SO42-)会被氧化为氧气(O2),同时释放出电子。
而在阴极上的还原反应将发生,锌离子(Zn2+)会被还原为锌金属,并吸收电子。
总体来说,电解硫酸锌的反应方程式描述了硫酸锌溶液中的离子被电解分解为锌金属和氧气的过程。
通过电解,硫酸锌被分解成了其组成离子,并在阳极和阴极上发生了相应的氧化和还原反应。
这样的电解反应在实际应用中有一定的重要性。
例如,在电镀工业中,电解硫酸锌可以被用来镀锌。
在这个过程中,锌金属可以被沉
积在其他材料表面上,起到保护和防腐的作用。
此外,电解硫酸锌还可以用于制备其他锌化合物,如硫酸锌的盐类。
总结起来,电解硫酸锌方程式描述了硫酸锌溶液在电解过程中分解为锌金属和氧气的反应。
这个反应在电镀和制备锌化合物等领域有一定的应用价值。


硫酸锌水溶液的电积过程一、实验目的通过锌电积的实验过程,了解电积有关的仪器设备及操作,掌握槽电压、电流密度、电流效率以及电能消耗的测试与计算方法。
二、基本原理锌电积一般采用Pb-Ag( 1%)合金作阳极,纯铝板作阴极,以酸性硫酸锌溶液作电解液。
当通以直流电时,阴、阳极发生以下电化学反应:阴极 Zn 2++2e=Zn E o =-0.763V阳极 H 2O-2e=1/2O 2+2H + E o =-1.229V总反应 2221Zn H O Zn 2H O 2+++=++直流电三、实验方法、试剂和仪器设备实验方法如图示:试剂:硫酸锌,硫酸,铝板,铅板,抽水泵仪器设备:直流稳压稳流电源,万用电表,电解槽四、实验操作步骤1、先将铝阴极置于天平称重并记下重量,然后将铝阴极放入电解槽内,取出测量其浸入溶液的实际尺寸并计算面积,再根据已确定的铝阴极电流密度计算出所需电流强度。
2、接线:将直流稳压稳流电源、电解槽、阴阳极等仪器联结好,即可通电,并记下通电起始时间、电流强度及槽电压。
3、通电开始实验正常进行,可按规定项目进行记录。
4、电解进行30~45分钟实验结束,关闭所有电源。
同时取出铝阴极置于沸水中置2分钟,以除去硫酸盐结晶,然后放入烘箱烘干再取出称重,记下电解后阴极的重量。
五、安全措施及应注意的事项1、线路联结必须严格按操作步骤进行,经检查后方可通电,否则易损坏仪器设备并造成实验中断。
2、实验过程中,不得任意摆弄仪器开关、旋钮以及各接触点,以免因接触不良断电影响实验。
3、如遇仪器设备发生故障或因接触不良而引起断电,应立即报告认真检查原因及时处理。
六、数据的整理与分析1、记录内容:实验日期、题目名称A 、技术条件:a 、温度:室温b 、阴极面积: m 2c 、阴极电流密度:D K = 350~500A/m 2d 、电流强度: Ae 、同名极距:4~6cmf 、电解液成分(g/L):硫酸锌 0.75~0.8mol/L ,硫酸 1.0mol/LB 、电解前后铝阴极重量的变化。


电解硫酸锌溶液制锌的原理
锌电解的电解液系浸出净化后的含锌约150g/L的中性硫酸锌水溶液和从电解槽中排出的含锌约50g/L、硫酸约170g/L的废电解液的混合液。
两者的体积比称为电解液的循环体积比。
增大循环体积比中废电解液的比例,即增大循环量,可以消除浓差极化,降低槽电压,提高电流效率,但循环量过大会使阳极析出的二氧化锰进入阴极,影响阴极析出锌的质量,同时也增大了电能消耗。
通常控制电解液循环体积比为1:(10~25)。
锌电解过程中,由于电解液等的电阻产生的焦耳热超过因蒸发、辐射而散发的热量,为维持电解液的温度在35~40℃,必须对电解液业进行冷却,普遍采用空气冷却塔。
以铅银合金板为阳极(不溶阳极),铝板为阴极,含有硫酸的硫酸锌水溶液为电解液,在电解槽中通直流电电解。
在阴、阳极上发生如下电化学反应:
阴极Zn+2e→Zn 析出金属锌。
阳极H2O-2e→2H+1/2O2 。
电解槽槽电压为3.4~3.6V,电流密度为300~600A/m,每吨电解锌消耗直流电能2900-3100kWV・h。
电解锌的纯度可达99.9%以上。
锌电解能耗较高。
电解过程中,阳极除析出氧外,还析出二氧化锰,作为氧化剂返回到浸出工序。

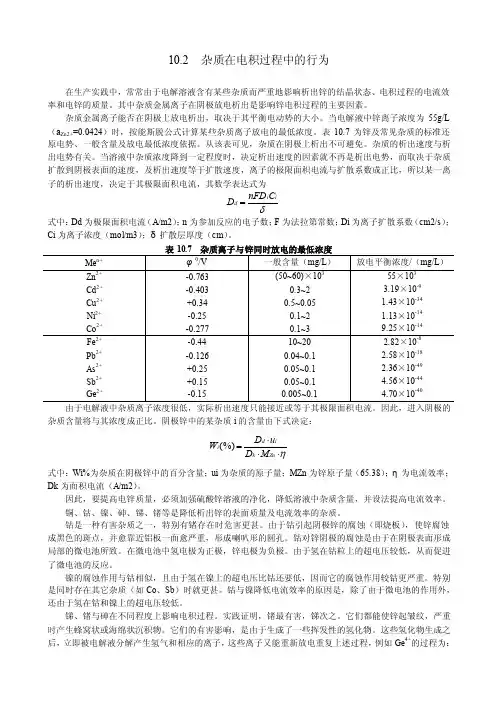
10.2 杂质在电积过程中的行为在生产实践中,常常由于电解溶液含有某些杂质而严重地影响析出锌的结晶状态、电积过程的电流效率和电锌的质量。
其中杂质金属离子在阴极放电析出是影响锌电积过程的主要因素。
杂质金属离子能否在阴极上放电析出,取决于其平衡电动势的大小。
当电解液中锌离子浓度为55g/L (a Zn2+=0.0424)时,按能斯脱公式计算某些杂质离子放电的最低浓度。
表10.7为锌及常见杂质的标准还原电势、一般含量及放电最低浓度依据。
从该表可见,杂质在阴极上析出不可避免。
杂质的析出速度与析出电势有关。
当溶液中杂质浓度降到一定程度时,决定析出速度的因素就不再是析出电势,而取决于杂质扩散到阴极表面的速度,及析出速度等于扩散速度,离子的极限面积电流与扩散系数成正比,所以某一离子的析出速度,决定于其极限面积电流,其数学表达式为δii d C nFD D =式中:Dd 为极限面积电流(A/m2);n 为参加反应的电子数;F 为法拉第常数;Di 为离子扩散系数(cm2/s );Ci 为离子浓度(mol/m3);δ扩散层厚度(cm )。
杂质含量将与其浓度成正比。
阴极锌中的某杂质i 的含量由下式决定:η⋅⋅⋅=Zn k id i M D u D W (%)式中:Wi%为杂质在阴极锌中的百分含量;ui 为杂质的原子量;MZn 为锌原子量(65.38);η为电流效率;Dk 为面积电流(A/m2)。
因此,要提高电锌质量,必须加强硫酸锌溶液的净化,降低溶液中杂质含量,并设法提高电流效率。
铜、钴、镍、砷、锑、锗等是降低析出锌的表面质量及电流效率的杂质。
钴是一种有害杂质之一,特别有锗存在时危害更甚。
由于钴引起阴极锌的腐蚀(即烧板),使锌腐蚀成黑色的斑点,并愈靠近铝板一面愈严重,形成喇叭形的圆孔。
钴对锌阴极的腐蚀是由于在阴极表面形成局部的微电池所致。
在微电池中氢电极为正极,锌电极为负极。
由于氢在钴粒上的超电压较低,从而促进了微电池的反应。



5硫酸锌溶液的电解沉积原理(2)5.2.2阴极过程5.2.2.1在工业生产条件下,锌电积液中含有Zn2+50~60g/L和H2SO4120-180g/L。
如果不考虑电积液中的杂质,则通电时,在阴极上仅可能发生两个过程。
(1)锌离子放电,在阴极上析出金属锌:Zn2++2e=Zn φ?(18)=―0.763V (18)(2)氢离子放电,在阴极上放出氢气:2H++2e=H2 φ?(19)=0.000V (19)在这两个放电反应中,究竟哪一种离子优先放电,对于湿法炼锌而言是至至关重要的。
从各种金属的电位序(见表4―4)来看,氢具有比锌更大的正电性,氢将从溶液中优先析出,而不析出金属锌。
但在工业生产中能从强酸性硫酸锌溶液中电积锌,这是因为实际电积过程中,存在由于极化所产生的超电压。
金属的超电压一般较小,约为0.03伏,而氢离子的超电压则随电积条件的不同而变。
塔费尔通过实验和推导总结出了超电压与电流密度的关系式,即著名的塔费尔公式:ηH=a+blgD K式中ηH——氢的超电压,a——常数,即电极上通过单位电流密度时的超电压值,随阴极材料、表面状态、溶液组成和温度而变;b——;只随电解液温度而变。
D k——阴极电流密度。
因此,电积时可创造一定条件,由于极化作用氢离子的放电电位会大大地改变,使得氢离子在阴极上的析出电位值比锌更负而不是更正,因而使锌离子在阴极上优先放电析出。
这就是锌电积技术赖以成功的理论依据。
5.2.2从以上分析可见,氢的超电压在锌电积实际生产中具有重要意义。
根据塔费尔公式,影响氢在阴极析出的超电压的主要因素有:由塔费尔公式可见,a值改变,氢的超电压就改变,即氢的超电压随阴极材料而定。
表5—1列出了在不同金属阴极上析出氢的超电压值。
从表中可以看出,在不同金属的阴极上氢析出超电压值相差较大。
大体上可分为三类:高超电压金属:Pb、Cd、Hg、T1、Zn、Sn;中超电压金属:Fe、Co、Ni、Cu、Au。

5硫酸锌溶液的电解沉积在ZnSO4和H2SO4水溶液中,采用Pb-Ag合金为阳极,纯铝作阴极,通以直流电进行电解,在阴极析出锌,在阳极产生氧气,与此同时,湿法炼锌工艺锌焙砂浸出过程所消耗的硫酸在此电解液中得到再生。
5.1锌电解液成分及锌电积生产过程5.1.1锌电解液锌电解液除主要成分硫酸锌、硫酸和水外,还存在少量杂质金属的硫酸盐及部分阴离子(主要为氯离子和氟离子)。
目前锌电解液中锌的浓度一般波动在40~60g/L范围内,而硫酸浓度则趋于逐步提高,已从110~140g/L提高到170~200g/L。
对于杂质的含量各厂也有不同要求。
加拿大一家锌厂在进行改造时曾做过调查,为了适应电流密度大幅度提高,对电解液中杂质含量(mg/L)要求更严格:Cd<0.3,CO<0.3,Sb<0.03,Ge<0.03,Fe<10,CL<50~100,F<10,Mn<1.8g/L5.1.2锌电积生产过程硫酸锌溶液的电积过程是将已经净化好的硫酸锌溶液(新液)以一定比例同废电解液混合后连续不断地从电解槽的进液端送入电解槽内。
铅银合金板(含银量约1%)阳极和压延铝板阴极,并联交错悬挂于槽内,通以直流电,在阴极析出金属锌(称阴极锌或析出锌),在阳极则放出氧气。
随着电积过程的不断进行电解液含锌量逐渐减少,而硫酸含量则逐渐增多,为保证电积条件的稳定,必须不断地补充新液以维持电解液成分稳定不变。
电积一定时间后,提出阴极板,剥下压延铝板上的析出锌片送往熔铸工序。
5.2锌电积过程的理论基础锌电解液的主要成分是硫酸锌、硫酸和水,当通以直流电时带正电荷的离子移向阴极,带负电荷的离子移向阳极,并分别在阴、阳极上放电。
阴极主要反应:Zn2++2e=Zn阳极主要反应:2OH--2e=0.5O2+H2O(或H2O-2e=0.5O2+2H+)电极过程总反应:ZnSO4+H2O=Zn+H2SO4+0.5O25.3锌电解车间的主要生产设备及布置5.3.1电解槽电积锌用的电解槽是一种长方形的槽子。
硫酸锌溶液的电解沉积-原理(1)5.1概述硫酸锌溶液的电解沉积是湿法炼锌流程中四个重要工序中的最后一个。
其目的主要是从硫酸锌溶液中提取纯度高的金属锌。
电积的技术经济指标不仅反映出整个炼锌工艺的好坏,而且因直接消耗大量电能,在很大程度上影响着电锌厂的生产成本。
硫酸锌溶液的电解沉积是湿法炼钟的最后一个生产工序。
其目的主要是从硫酸锌溶液中提取纯度高的金属锌。
硫酸锌溶液电解沉积就是:以净化的硫酸锌溶液作电解液,以铅银合金板(含银1%)做阳极,压延铝板做阴极,在直流电的作用下,阴极上析出金属锌(称阴极锌),在阳极上放出氧气。
随着过程的不断进行,电解液中的含锌量不断减少,硫酸含量不断增加,至一定程度后就不能再供正常电积之用。
这时的电解液叫做废电解液(电积废液)。
废电解液连续不断地从电解槽的出液端溢出,一部分与新液混合供电解液循环用,一部分送往浸出车间供浸出用。
每隔一定时问取出阴极将析出锌剥下进去熔化铸锭,成为锌成品。
阴极铝板经过清刷处理以后,再装入电解槽中,继续进行电解沉积。
电解沉积锌的过程一般可以分为三种方法:标准法、中酸中电流密度法、和高酸高电流密度法。
标准法采用300~400A/m2的电流密度,电解液含酸100~130g/L,中酸中电流密度法采用400~600A/m2的电流密度,电解液含酸130~160g/L;高酸高电流密度法采用600~1000A/m2的电流密度,电解液含酸220~300g/L。
三种方法原理是一样的,只不过是所用的电流密度和电积液酸度有较大差别而已。
增加电流密度,可提高电积槽的锌产量,但电积液必须除去更多的热量,纯度要求也更严格。
过去采用低酸低电流密度法的电锌厂较普遍,但它限制了生产过程的强化。
因此,现在的电锌厂多使用中酸中电流密度法,在操作良好的条件下,可以获得高于90%的电流效率。
采用高酸高电流密度法的电锌厂(如美国克洛格电锌厂,采用960A/m2,H2SO4260g/L的作业条件)必须在高锌含量下作业,以保证溶液中的锌酸比高于足以避免析出锌反溶的程度,返回的废液由于含酸高,更容易溶解焙砂中的铁酸锌。
如果使用铜作为正极,硫酸锌作为电解质,这样的原电池是无法正常工作的。
因为负极锌和电解质硫酸锌不能发生自发的氧化还原反应,即锌无法置换出溶液中的锌。
所以,这种配置无法实现电子从负极流向正极的流动。
如果使用硫酸铜作为电解质,这样的原电池就可以正常工作。
因为负极锌和电解质硫酸铜可以发生自发的氧化还原反应。
所以,铜锌原电池的电解质溶液应该是可以与锌发生自发的氧化还原反应的电解质,比如硫酸铜、硫酸等。