-常见晶体结构举例
- 格式:ppt
- 大小:84.00 KB
- 文档页数:8

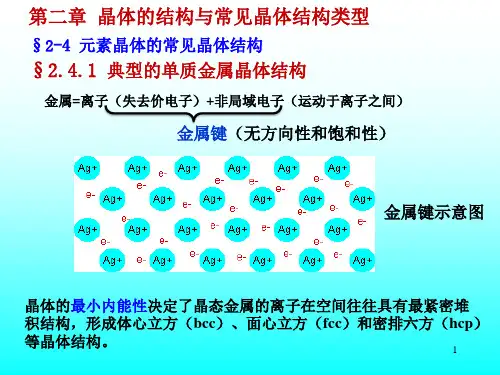



晶体与非晶体的例子晶体与非晶体是固体材料中两种常见的结构类型,它们在原子或分子排列上存在着显著的不同。
下面将分别从晶体和非晶体的角度举例说明它们的特点和应用。
晶体是具有长程有序结构的固体材料,其原子或分子呈周期性排列,形成具有特定几何形状和面向的晶体结构。
晶体的结构稳定、有序,具有明确的晶体学方向性。
以下是几种常见的晶体材料:1. 钻石:钻石是一种由碳原子构成的晶体材料,具有极高的硬度和光泽。
它的晶体结构是由碳原子以sp3杂化形式排列而成的,使得钻石成为非常耐磨的材料,被广泛用于珠宝和工业领域。
2. 盐类晶体:如氯化钠(NaCl)、碳酸钙(CaCO3)等,这类晶体由正负离子以离子键结合形成。
氯化钠是一种典型的离子晶体,其晶体结构呈立方对称,被广泛应用于食品加工和化工生产中。
3. 金属晶体:金属材料的晶体结构多为紧密堆积结构,如面心立方、体心立方等。
金属晶体具有良好的导电性和导热性,被广泛应用于电子、汽车等领域。
4. 半导体晶体:如硅(Si)、锗(Ge)等,这类晶体结构介于金属和非金属之间,具有一定的导电性和带隙能量。
半导体晶体在电子器件制造中发挥着关键作用。
非晶体是没有规则周期结构的固体材料,其原子或分子呈无序排列状态,缺乏明显的晶体学方向性。
以下是几种常见的非晶体材料:5. 玻璃:玻璃是一种非晶体材料,其原子排列呈无序状态。
玻璃具有透明、硬度高、不导电等特点,被广泛用于建筑、容器、光学器件等领域。
6. 塑料:塑料是一种由高分子化合物构成的非晶体材料,其分子链呈无序排列。
塑料具有轻质、耐腐蚀、易加工等特点,广泛应用于包装、建材等领域。
7. 液晶:液晶是一种介于液体和固体之间的非晶体材料,其分子呈液态有序排列。
液晶具有电光响应性,被广泛应用于液晶显示器、电子书等领域。
8. 胶体:胶体是一种由固体颗粒悬浮在液体中形成的非晶体材料,具有粒径小、表面活性大等特点。
胶体在生物医药、食品加工等领域有着重要应用。





举例说明单晶体多晶体和非晶体的结构下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!单晶体、多晶体与非晶体的结构比较1. 单晶体的结构单晶体是指由同一种化学物质构成的晶体,其原子或分子排列呈现高度有序的结构。
典型的晶体结构范文晶体是由原子、分子或离子按照一定的规律排列而组成的固体物质。
晶体结构是指晶体中原子、分子或离子的空间排列方式。
不同的晶体结构决定了晶体的物理性质和化学性质。
下面将介绍几种典型的晶体结构。
1.离子晶体结构:离子晶体是由带正电荷的阳离子和带负电荷的阴离子构成的晶体。
它们之间通过离子键相互结合。
典型的离子晶体如氯化钠(NaCl)。
在氯化钠晶体中,钠离子和氯离子按照八面体配位的方式排列。
每个钠离子被六个氯离子包围,每个氯离子被六个钠离子包围。
2.共价晶体结构:共价晶体是由原子通过共用电子而形成的晶体。
原子之间的共价键保持着晶体的稳定性。
典型的共价晶体如金刚石(C),其中每个碳原子通过共价键与周围四个碳原子相连。
金刚石晶体的结构是由不同的碳原子和碳原子之间的关系构成的。
3.金属晶体结构:金属晶体是由金属原子构成的晶体,金属原子之间通过金属键相互结合。
金属晶体的典型例子是铁(Fe)和铜(Cu)。
在金属晶体中,金属原子形成密堆积结构,具有非常高的导电性和热导性。
4.分子晶体结构:分子晶体是由分子构成的晶体,分子之间通过范德华力相互结合。
分子晶体的典型例子是冰(H2O)。
在冰晶体中,水分子通过氢键连接在一起,形成六角形密堆积结构。
5.网络共价晶体结构:网络共价晶体是由原子通过共价键形成复杂的网状结构的晶体。
典型的例子是二硫化碳(CS2)。
在二硫化碳晶体中,碳原子通过共价键和硫原子形成复杂的网状结构。
以上是一些典型的晶体结构,每种晶体结构都有其独特的特点和性质。
了解晶体的结构对于研究晶体的物理性质和化学性质具有重要意义。
晶体结构3-1-1 晶体的宏观特征通常人们说的“固体”可分为晶态和非晶态两大类。
晶态物质, 即晶体,是真正意义的固体。
在宏观上,晶体有别于橡胶、玻璃、琥珀、树脂等非晶态的最普遍的本质特征是它的“自范性”,即:晶体能够自发地呈现封闭的规则凸多面体的外形。
非晶态物质则没有自范性1。
单一的晶体多面体叫做单晶。
有时两个体积大致相当的单晶按一定规则生长在一起,叫做双晶;许多单晶以不同取向连在一起,叫做晶簇。
有的晶态物质(例如用于雕塑的大块“汉白玉”),看不到规则外形,是多晶,是许多肉眼看不到的微小晶体的集合体。
有的多晶压成粉末,放到光学显微镜或电子显微镜下观察,仍可看到整齐规则的晶体外形(图3-1)。
a.水晶单晶b。
石膏双晶和晶簇c。
水晶晶簇d。
蛋白质显微照片图3-1 晶体自发呈现规则凸多面体外形举例2配制明矾饱和溶液,在容器中央挂一条线,浸入溶液的线端悬一小块明矾晶体(晶种),尽量保持恒温令溶液慢慢挥发,数天后,你会发现线端的晶种长大了,呈现八面体外形。
你再把得到的明矾晶体放进饱和铬钾矾溶液,不久,会发现呈八面体外形的铬钾矾晶体在明矾晶体上生长。
这个实验不仅说明晶体会自发呈现规则凸多面体外形,还告诉我们,明矾和铬钾矾是类质同晶的——KAl(SO4)2·12H2O和KCr(SO4)2·12H2O组成和结构类同, 有相同的外形。
早在1669年,丹麦科学家斯丹诺(N. Steno)就发现,晶体,例如水晶(SiO2),在自然条件下形成的单晶的形状丰富多样, 然而,借助几何学知识,却可找到相同的晶面(如图3-2中用R、r、m…标记的晶面),而且,确定的晶面之间的二面角——“晶面夹角”是不变的。
这叫做晶面夹角不变定律。
图3-2 自然生长的水晶晶体1固体物质除晶体和称为玻璃态的非晶态外,还有液晶、类晶等介乎晶态与非晶态之间的状态。
液晶和类晶也有某种整齐排列的特性,但在宏观外形和微观结构上却与理想晶体不完全相同。
十二晶体结构
是一种特殊的结晶形态,也被称作十二面体晶胞。
这种结构的
晶胞由十二个六角形构成,看起来非常美丽。
但是除了其美观,
对于材料科学和化学领域来说也是非常重要的。
最早发现的实例是铝石墨烯(Al13C4)的分子团簇。
这种分子
团簇的晶胞由13个铝原子和4个碳原子构成,形状类似于一个球。
这种结构是一种几何立体的体系,具有极高的强度和超弹性。
这
些特性使得其在纳米材料和生物医学领域有着广泛的应用。
除了铝石墨烯,还在其他材料中被广泛应用。
比如氢化物、卤
素化合物和碱金属化合物等。
在这些材料中,的特性主要体现在
其高度对称性和其调节热导率的能力。
这在材料的制造和应用过
程中都有着非常重要的意义。
举例来说,氢化镧(LaH10)和氢化铈(CeH10)这两种化合
物都具有。
这种结构中的La和Ce原子占据了中心位置,而氢原
子则填充在晶胞的角落处。
这种结构的特性使得氢化镧成为了一
种具有潜力的超导材料,并能够用于制造高温超导电缆和超导磁体。
而氢化铈则可以用于制造高强度的磁体,因为能够调节热传导,从而使得其在高温下仍能保持磁场的稳定性。
总的来说,是一种具有非常特殊性质的结晶形态。
除了在材料
科学和化学领域的应用之外,在生物医学领域也有着潜在的应用。
拥有这种结构之后,材料可以具有极高的强度,超弹性和优异的
传热性能。
可以预见,在以后的发展中,将会在各种领域发挥着
更加重要的作用。