石灰石石膏湿法烟气脱硫工艺的化学原理
- 格式:docx
- 大小:19.98 KB
- 文档页数:9

石灰石-石膏湿法脱硫原理分析烟气脱硫发生在吸收塔吸收区内,装液有循环泵抽出,经喷淋层喷嘴雾化喷出,细小的聚液液滴充满整个吸收塔吸收区域,与逆流而上的烟气接触发生传质和化学吸收反应,脱除SO2.整个吸收过程可以假设由两部分组成,一是气态的SO2溶解在装液中的传质过程;而是溶解的SO2在浆液中所发生的化学吸收过程。
(1)气液相间传质过程系数塔内气液相间的传质过程可用Whitman(1923)提出的双模理论来描述。
该理论假设当气液两相接触时,在气体和液体之间存在稳定的相界面,相界面两侧各存在很薄的气模和液膜。
气体一份子括但形势从气相主体穿过气模和液膜进入液相主体,在相界面气液两相平衡,且遵循亨利定律;在两膜层以外的中心区,流体勋在充分的湍流,分子浓度均匀。
(2)化学吸收反应过程1)SO2水解烟气中的SO2通过喷淋液相后,首先与浆液发生水解反应,反应的方程式:O2+H2O→H+ + HSO3-HSO3-→H+ + SO32-SO2的水解使得液相中的SO2分子减少,破坏了气液相间的分子平衡,以推动S02分子气相主体输送到液相主体,而从上面的方程式S02的水解和H2SO3的电离均是可逆过程,只消耗掉反应生成物,才能推动反应不断的进行,从而不断断的吸收气相中的S02分子,以到烟气脱的目的。
2)氧化反应SO2水解后,脱硫浆液中会存在大量的HSO3-,由于其具有强还原性,在吸收塔浆液区,易于氧化风机以及烟气中带来的溶解氧反应,氧化反应过程为:HSO3-+O2=HSO4-HSO4-=H++SO42-氧化反应将HSO3-氧化为SO42-,减少了水解反应的生成物,促进水解反应的进行和气态SO2的吸收,而且将化学特性较不稳定的SO32-氧化成为特性较稳定的SO42-,为下部与CaCO3的结晶反应提供了基础。
3)石膏结晶在氧化反应阶段后,浆液中存在的SO42-与浆液的Ca2+离子反应生成难溶于水的二水硫酸钙(石膏),这些石膏会被石膏排出泵送出脱硫塔,降低脱硫塔内石膏的浓度,这使得石膏结晶的反应能够源源不断的进行下去。

石灰石石膏湿法脱硫化学反应原理
石灰石石膏湿法脱硫是一种常用的烟气脱硫技术,其原理主要包括以下几个步骤:
1. 石膏浆液的制备:将石灰石(CaCO3)与水反应生成石灰石浆液,同时加入一定量的氧化剂如空气,将部分CaCO3氧化
成氧化钙(CaO),形成钙离子(Ca2+)和氢氧根离子(OH-)。
2. 脱硫反应:将石膏浆液与含有二氧化硫(SO2)的烟气接触,二氧化硫会与钙离子和氢氧根离子发生反应,生成固态的硫酸钙(CaSO4·2H2O)。
反应方程式如下:
Ca2+ + SO2 + 2H2O → CaSO4·2H2O
3. 生成石膏:反应产生的硫酸钙会以颗粒状悬浮在石膏浆液中,形成石膏。
4. 脱水:通过脱水设备,将石膏浆液中的水分去除,使石膏凝固成固体。
整个过程中,石膏浆液充当了吸收剂的角色,能够吸收并固定烟气中的二氧化硫,从而实现脱硫的目的。
生成的石膏可以作为工业原料或用于土壤改良等方面的应用。

热电厂多是以燃烧煤作为发电的能源,煤中含有硫,燃烧出二氧化硫,会污染空气产生酸雨,所以常用的脱硫方法是石灰石—石膏湿法脱硫。
石灰石被磨碎,制成石灰石浆液,石灰石浆液与烟气中的二氧化硫反应生成石膏,这个过程就脱除了二氧化硫,接下来就为大家详细的讲解一下,希望对大家有所帮助。
1、脱硫原理。
石灰石—石膏湿法脱硫技术是将石灰石粉加水制成浆液作为吸收剂泵入吸收塔与烟气充分接触混合,烟气中的二氧化硫与浆液中的碳酸钙以及从塔下部鼓入的空气进行氧化反应生成硫酸钙,硫酸钙达到一定饱和度后,结晶形成二水石膏。
经吸收塔排出的石膏浆液经浓缩、脱水,使其含水量减小,然后用输送机送至石膏贮仓堆放,脱硫后的烟气经过除雾器除去雾滴,再经过换热器加热升温后,由烟囱排入大气。
由于吸收塔内吸收剂浆液通过循环泵反复循环与烟气接触,吸收剂利用率很高,钙硫比较低,脱硫效率高。
2、技术和经济性。
石灰石—石膏法脱硫工艺流程简单、技术先进又可靠,脱硫效率高以上,是
目前国内外烟气脱硫应用广泛的脱硫工艺。
但是系统复杂、设备庞大、耗水量大、一次性投资高,一般适用于大型电厂。
3、适用范围。
单塔处理脱硫量大,适用于任何含硫量的煤种的烟气脱硫,对锅炉的适应性强,一般在大型电厂或大功率锅炉使用。
正如上文所介绍的,使用石灰石—石膏湿法脱硫技术更加适合大型电厂等废弃排放量大的惬意,而且脱硫原料石灰石的价格也很便宜。
浙江钙科机械设备有限公司,于2014年三月注册成立,注册资金4500万元。
本公司与合肥水泥设计院合作,致力于石灰生产工艺研究,以改革目前我国石灰生产工艺为研究目标,为配套企业提供石灰原料。

一、石灰石/石灰-石膏法脱硫工艺一)、工作原理石灰石/石灰-石膏法烟气脱硫采用石灰石或石灰作为脱硫吸收剂,石灰石经破碎磨细成粉状与水混合搅拌成吸收浆液,当采用石灰为吸收剂时,石灰粉经消化处理后加水制成吸收剂浆液。
在吸收塔内,吸收浆液与烟气接触混合,烟气中的二氧化硫与浆液中的碳酸钙以及鼓入的氧化空气进行化学反应从而被脱除,最终反应产物为石膏。
二)、反应过程1、吸收SO2+ H2O—>H2SO3SO3+ H2O—>H2SO42、中和CaCO3+ H2SO3—>CaSO3+CO2+ H2OCaCO3+ H2SO4—>CaSO4+CO2+ H2OCaCO3+2HCl—>CaCl2+CO2+ H2OCaCO3+2HF—>CaF2+CO2+ H2O3、氧化2CaSO3+O2—>2 CaSO44、结晶CaSO4+ 2H2O—>CaSO4·2H2O三)、系统组成脱硫系统主要由烟气系统、吸收氧化系统、石灰石/石灰浆液制备系统、副产品处理系统、废水处理系统、公用系统(工艺水、压缩空气、事故浆液罐系统等)、电气控制系统等几部分组成。
四)、工艺流程锅炉/窑炉—>除尘器—>引风机—>吸收塔—>烟囱来自于锅炉或窑炉的烟气经过除尘后在引风机作用下进入吸收塔,吸收塔为逆流喷淋空塔结构,集吸收、氧化功能于一体,上部为吸收区,下部为氧化区,经过除尘后的烟气与吸收塔内的循环浆液逆向接触。
系统一般装3-5台浆液循环泵,每台循环泵对应一层雾化喷淋层。
当只有一台机组运行时或负荷较小时,可以停运1-2层喷淋层,此时系统仍保持较高的液气比,从而可达到所需的脱硫效果。
吸收区上部装二级除雾器,除雾器出口烟气中的游离水份不超过75mg/Nm3。
吸收SO2后的浆液进入循环氧化区,在循环氧化区中,亚硫酸钙被鼓入的空气氧化成石膏晶体。
同时,由吸收剂制备系统向吸收氧化系统供给新鲜的石灰石浆液,用于补充被消耗掉的石灰石,使吸收浆液保持一定的pH值。

石灰石膏法脱硫原理石灰石膏法脱硫是一种常用的烟气脱硫技术,其原理是利用石灰石膏(CaSO4)与烟气中的二氧化硫(SO2)发生反应,形成硫酸钙(CaSO3),从而达到脱除烟气中二氧化硫的目的。
本文将详细介绍石灰石膏法脱硫的原理及其工作过程。
石灰石膏法脱硫的原理可以分为两个步骤:吸收和再生。
在吸收步骤中,石灰石膏与烟气中的二氧化硫发生反应生成硫酸钙,反应方程式如下:CaCO3 + SO2 + 1/2O2 + H2O → CaSO4·2H2O + CO2。
在这个过程中,石灰石膏被转化为硫酸钙,而二氧化硫则被吸收。
在再生步骤中,通过加热硫酸钙,将其分解为二氧化硫和石灰石膏,反应方程式如下:CaSO4·2H2O + 1/2O2 → CaSO3 + 1/2H2O + 1/2O2。
通过这个过程,硫酸钙被再生,生成二氧化硫和石灰石膏。
这样,石灰石膏可以循环使用,而硫酸钙则可以被收集、处理或转化为其他有用的化合物。
石灰石膏法脱硫的工作过程可以分为干法和湿法两种。
在干法石灰石膏法脱硫中,石灰石膏直接喷入烟气中,与二氧化硫发生反应。
而在湿法石灰石膏法脱硫中,石灰石膏首先与水形成石灰乳,然后喷入烟气中进行反应。
两种方法各有优缺点,选择时需要根据具体情况进行考虑。
石灰石膏法脱硫技术具有成熟、稳定、经济、环保等优点,被广泛应用于燃煤电厂、钢铁厂、水泥厂等工业领域。
通过合理的工艺设计和操作控制,可以实现高效脱硫,减少二氧化硫排放,保护环境,符合现代工业可持续发展的要求。
总的来说,石灰石膏法脱硫利用石灰石膏与烟气中的二氧化硫发生反应,通过吸收和再生步骤实现脱硫的目的。
该技术在工业应用中具有重要意义,对减少大气污染、保护环境、促进工业可持续发展具有积极作用。
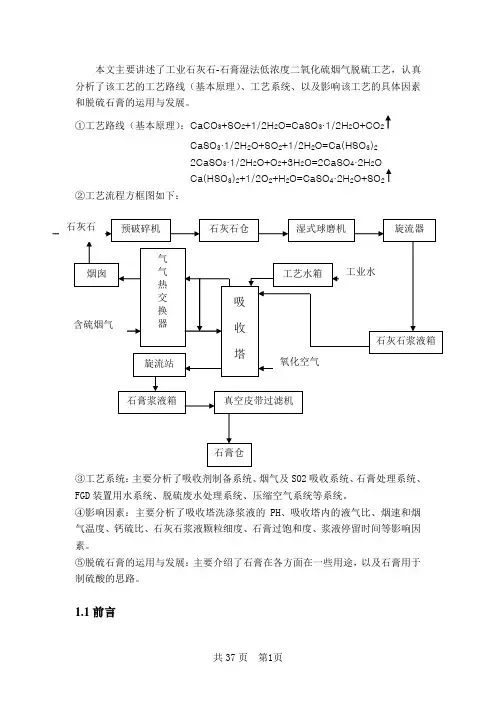
本文主要讲述了工业石灰石-石膏湿法低浓度二氧化硫烟气脱硫工艺,认真分析了该工艺的工艺路线(基本原理)、工艺系统、以及影响该工艺的具体因素和脱硫石膏的运用与发展。
①工艺路线(基本原理):CaCO3+SO2+1/2H2O=CaSO3·1/2H2O+CO2CaSO3·1/2H2O+SO2+1/2H2O=Ca(HSO3)22CaSO3·1/2H2O+O2+3H2O=2CaSO4·2H2OCa(HSO3)2+1/2O2+H2O=CaSO4·2H2O+SO2②工艺流程方框图如下:③工艺系统:主要分析了吸收剂制备系统、烟气及SO2吸收系统、石膏处理系统、FGD装置用水系统、脱硫废水处理系统、压缩空气系统等系统。
④影响因素:主要分析了吸收塔洗涤浆液的PH、吸收塔内的液气比、烟速和烟气温度、钙硫比、石灰石浆液颗粒细度、石膏过饱和度、浆液停留时间等影响因素。
⑤脱硫石膏的运用与发展:主要介绍了石膏在各方面在一些用途,以及石膏用于制硫酸的思路。
1.1前言二氧化硫是主要大气污染物之一,严重影响环境,威胁人们的生活健康。
削减二氧化硫的排放量,保护大气环境质量,是目前及未来相当长时间内我国环境保护的重要课题之一。
目前,国内外处理低浓度二氧化硫烟气的方法有许多,如氨法、钙法、钠法、铝法、氧化法、吸附法、催化法及电子束法等。
但由于受到技术可靠性、经济合理性、及行业生产特点等限制,当前比较成熟且广泛运用的方法主要有三种,即氨法、钙法和钠法。
氨法是烟气脱硫方法中较传统的工艺,该法采用液氨或氨水作为吸收剂,吸收效率高、脱硫彻底。
钙法是采用石灰水或石灰乳洗涤含二氧化硫的烟气,技术成熟,生产成本低,但吸收速率慢、吸收能力小、装置运行周期短。
钠法是使用碳酸钠或氢氧化钠等碱性物质吸收含二氧化硫的烟气,具有吸收能力大、吸收速率快、脱硫效率高、设备简单、操作方便等优势,但最大的问题是原料钠碱较贵,生产成本高。

石灰石-石膏湿法烟气脱硫工艺石灰石(石灰)-石膏湿法脱硫工艺是湿法脱硫的一种,是目前世界上应用范围最广、工艺技术最成熟的标准脱硫工艺技术。
是当前国际上通行的大机组火电厂烟气脱硫的基本工艺。
它采用价廉易得的石灰石或石灰作脱硫吸收剂,石灰石经破碎磨细成粉状与水混合搅拌成吸收浆液,当采用石灰为吸收剂时,石灰粉经消化处理后加水制成吸收剂浆液。
在吸收塔内,吸收浆液与烟气接触混合,烟气中的二氧化硫与浆液中的碳酸钙以及鼓入的氧化空气进行化学反应被脱除,最终反应产物为石膏。
脱硫后的烟气经除雾器除去带出的细小液滴,经换热器加热升温后排入烟囱。
脱硫石膏浆经脱水装置脱水后回收。
由于吸收浆液循环利用,脱硫吸收剂的利用率很高。
最初这一技术是为发电容量在100MW以上、要求脱硫效率较高的矿物燃料发电设备配套的,但近几年来,这一脱硫工艺也在工业锅炉和垃圾电站上得到了应用.根据美国EPRI统计,目前已经开发的脱硫工艺大约有近百种,但真正实现工业应用的仅10多种。
已经投运或正在计划建设的脱硫系统中,湿法烟气脱硫技术占80%左右。
在湿法烟气脱硫技术中,石灰石/石灰—石膏湿法烟气脱流技术是最主要的技术,其优点是:1、技术成熟,脱硫效率高,可达95%以上。
2、原料来源广泛、易取得、价格优惠3、大型化技术成熟,容量可大可小,应用范围广4、系统运行稳定,变负荷运行特性优良5、副产品可充分利用,是良好的建筑材料6、只有少量的废物排放,并且可实现无废物排放7、技术进步快。
石灰石/石灰—石膏湿法烟气脱硫工艺,一般布置在锅炉除尘器后尾部烟道,主要有:工艺系统、DCS控制系统、电气系统三个分统。
基本工艺过程在石灰石一石膏湿法烟气脱硫工艺中,俘获二氧化硫(SO2)的基本工艺过程:烟气进入吸收塔后,与吸收剂浆液接触、进行物理、化学反应,最后产生固化二氧化硫的石膏副产品。
基本工艺过程为:(1)气态SO2与吸收浆液混合、溶解(2)SO2进行反应生成亚硫根(3)亚硫根氧化生成硫酸根(4)硫酸根与吸收剂反应生成硫酸盐(5)硫酸盐从吸收剂中分离用石灰石作吸收剂时,SO2在吸收塔中转化,其反应简式式如下:CaCO3+2 SO2+H2O ←→Ca(HSO3)2+CO2在此,含CaCO3的浆液被称为洗涤悬浮液,它从吸收塔的上部喷入到烟气中。

石灰石——石膏湿法烟气脱硫技术石灰石——石膏湿法烟气脱硫技术石灰石——石膏湿法烟气脱硫技术是已经开发和推广的烟气脱硫技术中的主流技术,占国内外安装烟气脱硫装置总容量的85%以上。
特点是商业应用时间长,工艺技术成熟,配套设备完善,工作稳定,操作简单,脱硫效率可达到95%以上,可靠性高达95%以上。
吸收剂为石灰石粉,资源丰富,价格低廉,使用安全;副产品为脱硫石膏,可用作水泥添加剂、农业土壤调节剂,或进一步清洗、均化、除杂后,生产建筑用石膏板等。
石灰石——石膏湿法烟气脱硫技术广泛应用于火电厂、冶金、各种工业锅炉、窑炉、水泥工业、玻璃工业、化工工业、有色冶炼等行业大型燃烧设备烟气中SO2的排放控制。
一、工艺流程石灰石——石膏湿法烟气脱硫装置主要由烟气系统、石灰石浆液制备系统、烟气吸收及氧化系统、石膏脱水系统、烟气排放连续监测系统(CEMS)以及自动控制系统和公用工程系统等组成。
工艺流程如图示。
一定浓度的石灰石浆液连续从吸收塔顶部喷入,与经过增加风机增压后进入吸收塔的烟气发生接触。
在烟气被冷却洗涤的过程中,烟气中的SO2被浆液中的碳酸钙吸收生成亚硫酸钙而成为净化烟气,净化后的烟气经除雾器除去烟气中的小雾滴,从吸收塔上部排出,进入大气。
向吸收塔底部的溶液中鼓入空气,溶液中的亚硫酸钙被氧化成为硫酸钙结晶物——石膏。
吸收塔底部的溶液是石灰石、石膏组成的浆状混合物,其部分被强制在塔内循环,部分作为产物排出而成为脱水石膏。
二、工艺原理石灰石——石膏湿法烟气脱硫系统中主要的化学反应包括:1. SO2的吸收2.与石灰石的反应3.氧化反应4.CaSO4晶体生成总的反应方程式为:SO2(g)+ CaCO3(s)+2H2O(l)+1/2O2(g)→CaSO4·2H2O(s)+CO2(g)三、脱硫系统的主要设备1.烟气系统烟气系统由进口烟气挡板门、旁路烟气挡板门、钢制烟道、脱硫增压风机等组成。
原烟气经烟道、烟气进口挡板门进入增压风机,经增压风机升压后进入吸收塔。

石灰石-石膏湿法烟气脱硫工艺的化学原理一、概述:脱硫过程就是吸收,吸附,催化氧化和催化还原,石灰石浆液洗涤含SO烟气,产生化学反应分离出脱硫副产物,化学吸收速率较快与扩散速率有关,2又与化学反应速度有关,在吸收过程中被吸收组分的气液平衡关系,既服从于相平衡(液气比L/G,烟气和石灰石浆液的比),又服从于化学平衡(钙硫比Ca/S,二氧化硫与炭酸钙的化学反应)。
1、气相:烟气压力,烟气浊度,烟气中的二氧化硫含量,烟尘含量,烟气中的氧含量,烟气温度,烟气总量2、液相:石灰石粉粒度,炭酸钙含量,黏土含量,与水的排比密度,-,它们与溶解了的CaCO和SOHSO的反应3、气液界面处:参加反应的主要是323是瞬间进行的。
二、脱硫系统整个化学反应的过程简述:1、 SO在气流中的扩散,22、扩散通过气膜3、 SO被水吸收,由气态转入溶液态,生成水化合物24、 SO水化合物和离子在液膜中扩散25、石灰石的颗粒表面溶解,由固相转入液相6、中和(SO水化合物与溶解的石灰石粉发生反应)27、氧化反应8、结晶分离,沉淀析出石膏,三、烟气的成份:火力发电厂煤燃烧产生的污染物主要是飞灰、氮氧化物和二氧化硫,使用静电除尘器可控制99%的飞灰污染。
四、二氧化硫的物理、化学性质:①. 二氧化硫SO的物理、化学性质:无色有刺激性气味的有毒气体。
密度比2空气大,易液化(沸点-10℃),易溶于水,在常温、常压下,1体积水大约能溶解40体积的二氧化硫,成弱酸性。
SO为酸性氧化物,具有酸性氧化物的通性、2还原性、氧化性、漂白性。
还原性更为突出,在潮湿的环境中对金属材料有腐蚀性,液体SO无色透明,是良好的制冷剂和溶剂,还可作防腐剂和消毒剂及还原2剂。
②. 三氧化硫SO的物理、化学性质:由二氧化硫SO催化氧化而得,无色易挥23发晶体,熔点16.8℃,沸点44.8℃。
SO为酸性氧化物,SO极易溶于水,溶于33水生成硫酸HSO,同时放出大量的热,42③. 硫酸HSO的物理、化学性质:二元强酸,纯硫酸为无色油状液体,凝固点423,浓硫酸溶于水会放出大量的热,密度为1.84g/cm具有10.4℃,沸点338℃,为强氧化性(是强氧化剂)和吸水性,具有很强的腐蚀性和破坏性,五、石灰石湿-石膏法脱硫化学反应的主要动力过程:1、气相SO被液相吸收的反应:SO经扩散作用从气相溶入液相中与水生成亚硫22-+,当PHH 亚硫酸迅速离解成亚硫酸氢根离子HSO值较高时,和氢离子酸HSO3232-,要使SO吸收不断进行下去,必须中和HSO二级电离才会生成较高浓度的SO233++当,即降低吸收剂的酸度,碱性吸收剂的作用就是中和氢离子电离产生的HH 吸收液中的吸收剂反应完后,如果不添加新的吸收剂或添加量不足,吸收液的酸度迅速提高,PH值迅速下降,当SO溶解达到饱和后,SO的吸收就告停止,脱22硫效率迅速下降2、吸收剂溶解和中和反应:固体CaCO 的溶解和进入液相中的CaCO的分解,33+浓度(PH固体石灰石的溶解速度,反应活性以及液相中的H值)影响中和反应2+2+的形CaCa的氧化反应,以及其它一些化合物也会影响中和反应速度。

石灰石石膏湿法脱硫的工艺【石灰石石膏湿法脱硫的工艺】导语:石灰石石膏湿法脱硫是一种常见的烟气脱硫技术,通过将石灰石与石膏反应,可以高效地去除燃煤发电厂和工业锅炉烟气中的二氧化硫。
本文将深入探讨石灰石石膏湿法脱硫的工艺原理、优势以及相关问题。
一、工艺原理1. 石灰石石膏湿法脱硫原理:石灰石与石膏发生反应生成硬石膏,将烟气中的二氧化硫转化为硫酸钙,并形成可回收利用的石膏产物。
主要反应方程式如下所示:CaCO3 + SO2 + 2H2O → CaSO4·2H2O + CO22. 脱硫反应的特点:该反应是一个快速的液相反应,在一定反应温度、气体流速和石膏浆液浓度下进行。
反应速率受碱性、反应温度、质量浓度等因素的影响。
二、工艺步骤1. 石灰石石膏湿法脱硫的基本步骤:(1)石灰石破碎、磨细:将原料石灰石经过破碎和磨细处理,提高其活性和反应速率。
(2)制备石膏浆液:将石灰石与水混合,形成石灰石浆液。
为了提高脱硫效果,还可加入一定量的添加剂。
(3)脱硫反应:将石灰石浆液喷入脱硫塔,通过与烟气的接触和反应,使二氧化硫转化为硫酸钙。
(4)石膏产物处理:将脱硫过程中生成的硬石膏经过脱水、干燥等处理后,得到成品石膏。
2. 工艺改进:为了提高脱硫效率和经济性,石灰石石膏湿法脱硫工艺进行了多方面的改进。
例如引入喷雾器、增加反应塔数目、采用高效填料等,以增加烟气与石灰石浆液的接触面积,加强反应效果。
三、工艺优势1. 脱硫效率高:石灰石石膏湿法脱硫工艺能够高效地将烟气中的二氧化硫转化为重质石膏产物,脱硫效率可达到90%以上。
2. 石膏产物可回收利用:脱硫过程中生成的硬石膏可以用于建材、石膏板等行业,实现资源的循环利用。
3. 工艺成熟可靠:石灰石石膏湿法脱硫工艺经过多年的实践应用,技术成熟可靠,广泛应用于燃煤发电厂和工业锅炉等领域。
四、问题与挑战1. 石膏处理与排放:脱硫过程中生成的硬石膏需要进行后续的脱水、干燥等处理,同时还需要解决石膏产物的长期存储和排放问题。

烟气脱硫方法的原理
烟气脱硫是一种常用的空气污染治理方法,其原理主要通过化学反应将烟气中的二氧化硫(SO2)转化为无害的硫酸盐(如石膏)或硫酸。
以下是常用的烟气脱硫方法及其原理:
1. 湿法烟气脱硫(湿法脱硫工艺):
- 石灰石-石膏法:石灰石(CaCO3)与含SO2的烟气反应生成石膏(CaSO4·2H2O),反应方程式为:CaCO3 + SO2 + H2O →CaSO4·2H2O + CO2。
石膏可以作为一种资源利用或废物处理。
- 石灰石-氨法:石灰石与氨气反应生成氯化钙(CaCl2)和硫酸(H2SO4),反应方程式为:CaCO3 + 2NH3 + H2O →CaCl2 + (NH4)2SO4 + CO2。
- 浆液喷射法:通过将喷雾剂(如石膏浆液)喷射到烟气中,使烟气中的SO2与喷射剂中的钙离子发生反应,生成硫酸钙(CaSO4)。
2. 半干法烟气脱硫(喷射吸收法):
- 以一种含碱的废气液滴(吸收剂)通过喷射装置,由烟气顺流吹入反应器中,烟气中的SO2与吸收剂中的碱发生反应生成不溶性硫酸盐。
3. 干法烟气脱硫(干法脱硫工艺):
- 活性炭吸附法:通过将烟气中的SO2吸附到活性炭表面上,从而减少烟气中的SO2含量。
- 活性氧化催化剂法:通过加入活性氧化催化剂(如二氧化钛)到烟气中,
促进SO2与氧气的氧化反应生成二氧化硫(SO3),再与水反应生成硫酸。
这些方法的原理主要是通过化学反应将烟气中的SO2转化成无害的化合物,从而达到脱除烟气中SO2的目的。
不同的脱硫方法适用于不同的工业领域和排放条件,选择合适的脱硫方法可以有效减少SO2对环境的污染。
石灰石-石膏湿法烟气脱硫工艺原理
石灰石-石膏湿法烟气脱硫工艺原理是一种常用于烟气脱硫的方法。
它基于石灰石(CaCO3)与烟气中的二氧化硫(SO2)反应生成石膏(CaSO4·2H2O)的化学原理。
该工艺主要包括石灰石粉碎、石膏湿法吸收、石膏浆液处理及循环系统等步骤。
首先,石灰石经过粉碎成为合适的颗粒大小。
然后,烟气通过脱硫塔,与石灰石颗粒接触,其中的SO2与石灰石中的CaCO3反应生成钙亚硫酸钙(CaSO3)。
接着,钙亚硫酸钙在脱硫塔中的湿环境下与氧气氧化为石膏(CaSO4·2H2O)。
石膏与水形成的浆液通过脱硫塔下部的排出管道排出。
为了保持反应的持续进行,石膏浆液需要循环使用。
因此,排出的石膏浆液经过处理后,再被送回脱硫塔进行再次使用。
处理包括石膏浆液的浓缩、滤液的回收以及过滤液的处理等步骤。
石灰石-石膏湿法烟气脱硫工艺的原理是利用石灰石作为反应剂,将烟气中的二氧化硫与石灰石反应生成石膏,从而达到脱硫的目的。
石膏是一种无害且可以回收利用的产物,因此该工艺具有环保和资源利
用的双重优势。
总结起来,石灰石-石膏湿法烟气脱硫工艺原理是通过石灰石与烟气中的二氧化硫反应生成石膏,再将石膏浆液进行循环利用,以达到脱硫的效果。
这种工艺在工业生产中被广泛应用,为减少大气污染做出了重要贡献。
石灰石-石膏湿法烟气脱硫工艺的化学原理一、概述:脱硫过程就是吸收,吸附,催化氧化和催化还原,石灰石浆液洗涤含SO2烟气,产生化学反应分离出脱硫副产物,化学吸收速率较快与扩散速率有关,又与化学反应速度有关,在吸收过程中被吸收组分的气液平衡关系,既服从于相平衡(液气比L/G,烟气和石灰石浆液的比),又服从于化学平衡(钙硫比Ca/S,二氧化硫与炭酸钙的化学反应)。
1、气相:烟气压力,烟气浊度,烟气中的二氧化硫含量,烟尘含量,烟气中的氧含量,烟气温度,烟气总量2、液相:石灰石粉粒度,炭酸钙含量,黏土含量,与水的排比密度,3、气液界面处:参加反应的主要是SO2和HSO3-,它们与溶解了的CaCO3的反应是瞬间进行的。
二、脱硫系统整个化学反应的过程简述:1、 SO2在气流中的扩散,2、扩散通过气膜3、 SO2被水吸收,由气态转入溶液态,生成水化合物4、 SO2水化合物和离子在液膜中扩散5、石灰石的颗粒表面溶解,由固相转入液相6、中和(SO2水化合物与溶解的石灰石粉发生反应)7、氧化反应8、结晶分离,沉淀析出石膏,三、烟气的成份:火力发电厂煤燃烧产生的污染物主要是飞灰、氮氧化物和二氧化硫,使用静电除尘器可控制99%的飞灰污染。
四、二氧化硫的物理、化学性质:①. 二氧化硫SO2的物理、化学性质:无色有刺激性气味的有毒气体。
密度比空气大,易液化(沸点-10℃),易溶于水,在常温、常压下,1体积水大约能溶解40体积的二氧化硫,成弱酸性。
SO2为酸性氧化物,具有酸性氧化物的通性、还原性、氧化性、漂白性。
还原性更为突出,在潮湿的环境中对金属材料有腐蚀性,液体SO2无色透明,是良好的制冷剂和溶剂,还可作防腐剂和消毒剂及还原剂。
②. 三氧化硫SO3的物理、化学性质:由二氧化硫SO2催化氧化而得,无色易挥发晶体,熔点16.8℃,沸点44.8℃。
SO3为酸性氧化物,SO3极易溶于水,溶于水生成硫酸H2SO4,同时放出大量的热,③. 硫酸H2SO4的物理、化学性质:二元强酸,纯硫酸为无色油状液体,凝固点为10.4℃,沸点338℃,密度为1.84g/cm3,浓硫酸溶于水会放出大量的热,具有强氧化性(是强氧化剂)和吸水性,具有很强的腐蚀性和破坏性,五、石灰石湿-石膏法脱硫化学反应的主要动力过程:1、气相SO2被液相吸收的反应:SO2经扩散作用从气相溶入液相中与水生成亚硫酸H2SO3亚硫酸迅速离解成亚硫酸氢根离子HSO3-和氢离子H+,当PH值较高时,HSO3二级电离才会生成较高浓度的SO32-,要使SO2吸收不断进行下去,必须中和电离产生的H+,即降低吸收剂的酸度,碱性吸收剂的作用就是中和氢离子H+当吸收液中的吸收剂反应完后,如果不添加新的吸收剂或添加量不足,吸收液的酸度迅速提高,PH值迅速下降,当SO2溶解达到饱和后,SO2的吸收就告停止,脱硫效率迅速下降2、吸收剂溶解和中和反应:固体CaCO3的溶解和进入液相中的CaCO3的分解,固体石灰石的溶解速度,反应活性以及液相中的H+浓度(PH值)影响中和反应速度和Ca2+的氧化反应,以及其它一些化合物也会影响中和反应速度。
石灰石-石膏湿法脱硫工艺的基本原理一、石灰石-石膏湿法脱硫工艺的基本原理石灰石——石膏湿法烟气脱硫工艺的原理是采用石灰石粉制成浆液作为脱硫吸收剂,与经降温后进入吸收塔的烟气接触混合,烟气中的二氧化硫与浆液中的碳酸钙,以及加入的氧化空气进行化学反应,最后生成二水石膏。
脱硫后的净烟气依次经过除雾器除去水滴、再经过烟气换热器加热升温后,经烟囱排入大气。
由于在吸收塔内吸收剂经浆液再循环泵反复循环与烟气接触,吸收剂利用率很高,钙硫比较低(一般不超过1.1),脱硫效率不低于95%,适用于任何煤种的烟气脱硫。
石灰石——石膏湿法烟气脱硫工艺的化学原理:烟气中的SO2溶解于水中生成亚硫酸并离解成氢离子和HSO 离子;烟气中的氧(由氧化风机送入的空气)溶解在水中,将 HSO 氧化成SO ; ? 吸收剂中的碳酸钙在一定条件下于水中生成Ca2+;在吸收塔内,溶解的二氧化硫、碳酸钙及氧发生化学反应生成石膏(CaSO4?2H2O)。
由于吸收剂循环量大和氧化空气的送入,吸收塔下部浆池中的HSO或亚硫酸盐几乎全部被氧化为硫酸根或硫酸盐,最后在CaSO4达到一定过饱和度后结晶形成石膏—CaSO4?2H2O,石膏可根据需要进行综合利用或抛弃处理。
二、工艺流程及系统湿法脱硫工艺系统整套装置一般布置在锅炉引风机之后,主要的设备是吸收塔、烟气换热器、升压风机和浆液循环泵我公司采用高效脱除SO2的川崎湿法石灰石,石膏工艺。
该套烟气脱硫系统(FGD)处理烟气量为定洲发电厂,1和,2机组(2×600MW)100,的烟气量,定洲电厂的FGD系统由以下子系统组成:(1)吸收塔系统(2)烟气系统(包括烟气再热系统和增压风机)(3)石膏脱水系统(包括真空皮带脱水系统和石膏储仓系统)(4)石灰石制备系统(包括石灰石接收和储存系统、石灰石磨制系统、石灰石供浆系统) (5)公用系统(6)排放系统(7)废水处理系统1、吸收塔系统吸收塔采用川崎公司先进的逆流喷雾塔,烟气由侧面进气口进入吸收塔,并在上升区与雾状浆液逆流接触,处理后的烟气在吸收塔顶部翻转向下,从与吸收塔烟气入口同一水平位置的烟气出口排至烟气再热系统。
石灰石/石膏湿法烟气脱硫技术概述摘要:本文主要对烟气脱硫工艺中的石灰石/石膏湿法烟气脱硫技术进行介绍。
首先介绍其工艺原理,烟气中的二氧化硫与浆液中的碳酸钙以及从塔下部浆池鼓入的氧化空气进行反应生成硫酸钙,硫酸钙达到一定饱和度后,结晶形成二水石膏。
关键词:FGD;石灰石/石膏湿法;烟气系统;吸收系统1 烟气脱硫工艺概述烟气脱硫(FGD)是目前燃煤电厂控制气体排放最有效和应用最广的技术。
20世纪60年代后期以来,烟气脱硫技术发展迅速,根据美国电力研究院的统计,大约有200种不同流程的FGD工艺进行了小试或工业性试验,但最终被证实在技术上可行、经济上合理并且在燃煤电厂得到采用的成熟技术仅有十多种。
2. 石灰石/石膏湿法烟气脱硫工艺石灰石/石膏湿法脱硫工艺是目前世界上应用最广泛、技术最为成熟的脱除技术,约占全部安装FGD 容量的70%。
它是以石灰石为脱硫吸收剂,通过向吸收塔内喷入吸收剂浆液,使之与烟气充分接触、混合,并对烟气进行洗涤,使得烟气中的与浆液中的碳酸钙以及鼓入的强制氧化空气发生化学反应,最后生成石膏,从而达到脱除的目的。
2.1 工艺原理石灰石粉加水制成重量浓度约为30%的浆液作为脱硫吸收剂,泵入吸收塔与烟气充分接触混合,烟气中的二氧化硫与浆液中的碳酸钙以及从塔下部浆池鼓入的氧化空气进行反应生成硫酸钙,硫酸钙达到一定饱和度后,结晶形成二水石膏。
脱硫后的烟气依次经过除雾器除去雾滴,再经过加热器升温至大于80℃后,由烟囱排入大气。
2.2.1工艺流程采用价廉易得的石灰石或石灰做脱硫吸收剂,石灰石经破碎磨成粉状与水混合搅拌成吸收浆液。
当采用石灰为吸收剂时,石灰经消化处理加水搅拌成吸收浆液。
锅炉的烟气从电除尘器或布袋除尘后(除尘效率大于97%),经烟气换热器降温后从吸收塔下部进入吸收塔(经过气-气换热器后的烟气温度下降到100℃左右)。
脱硫净化后的烟气依次经过除雾器除去雾滴然后再经气-气换热器升温后,从烟囱排放到大气空中。
火电厂石灰石∕石灰-石膏湿法烟气脱硫系统运行导则概述及解释说明1.1 概述:烟气脱硫是指通过对石灰石或石灰-石膏湿法进行处理,去除火电厂烟气中的硫化物,以减少大气污染和保护环境。
该系统运行导则旨在提供指导和规范,确保火电厂石灰石/石灰-石膏湿法的脱硫系统能够高效、安全地运行。
1.2 文章结构:本文将按以下结构进行描述: 引言、正文、火电厂石灰石/石灰-石膏湿法烟气脱硫系统运行导则概述、解释说明和结论等。
1.3 目的:本文的主要目的是详细介绍火电厂石灰石/石灰-石膏湿法烟气脱硫系统运行导则,并提供相应的解释说明。
通过了解该系统的运行原理和注意事项,可以加强对其重要性和操作技术要求的认识,并有效地应用于实践中。
这一部分主要对文章引言部分进行了概述,简要介绍了文章所涉及的内容和目标。
2. 正文在火电厂中,烟气脱硫系统是一项关键的环保设备,用于降低燃煤过程中产生的二氧化硫(SO2)排放。
其中,火电厂石灰石/石灰-石膏湿法是一种广泛应用的技术,在全球范围内被广泛采用。
2.1 火电厂石灰石/石灰-石膏湿法的基本原理火电厂使用石灰石或者活性石灰作为脱硫剂,并与进入脱硫系统的废气相接触。
这些脱硫剂会与废气中的二氧化硫发生化学反应,生成硫酸钙或者其他低水溶性物质。
这些物质会被捕集并沉积在吸收塔中的喷射层上。
通过周期性地从喷射层上刮走含有脱除硫酸盐沉淀物的污泥,并将其送至富含二氧化碳的稀释乳液中,就可以得到可回收的CaCO3或Ca(OH)2溶液,并继续循环使用于吸收塔的喷射装置中。
2.2 石灰石/石灰-石膏湿法系统运行导则为确保火电厂石灰石/石灰-石膏湿法系统的高效稳定运行,以下是一些运行导则:2.2.1 控制废气流量和温度:废气流量和温度对于脱硫反应的进行至关重要。
必须通过合适的调节措施确保进入吸收塔的废气流量和温度在合适的范围内,以保证反应能够顺利进行。
2.2.2 确保脱硫剂供应充足:火电厂需要确保有足够的石灰石或者活性石灰供应给脱硫系统,以满足脱硫反应所需。
石灰石-石膏湿法烟气脱硫工艺的化学原理一、概述:脱硫过程就是吸收,吸附,催化氧化和催化还原,石灰石浆液洗涤含SO2烟气,产生化学反应分离出脱硫副产物,化学吸收速率较快与扩散速率有关,又与化学反应速度有关,在吸收过程中被吸收组分的气液平衡关系,既服从于相平衡(液气比L/G,烟气和石灰石浆液的比),又服从于化学平衡(钙硫比Ca/S,二氧化硫与炭酸钙的化学反应)。
1、气相:烟气压力,烟气浊度,烟气中的二氧化硫含量,烟尘含量,烟气中的氧含量,烟气温度,烟气总量2、液相:石灰石粉粒度,炭酸钙含量,黏土含量,与水的排比密度,3、气液界面处:参加反应的主要是SO2和HSO3-,它们与溶解了的CaCO3的反应是瞬间进行的。
二、脱硫系统整个化学反应的过程简述:1、? SO2在气流中的扩散,2、? 扩散通过气膜3、? SO2被水吸收,由气态转入溶液态,生成水化合物4、? SO2水化合物和离子在液膜中扩散5、? 石灰石的颗粒表面溶解,由固相转入液相6、? 中和(SO2水化合物与溶解的石灰石粉发生反应)7、? 氧化反应8、? 结晶分离,沉淀析出石膏,三、烟气的成份:火力发电厂煤燃烧产生的污染物主要是飞灰、氮氧化物和二氧化硫,使用静电除尘器可控制99%的飞灰污染。
四、二氧化硫的物理、化学性质:①.?二氧化硫SO2的物理、化学性质:无色有刺激性气味的有毒气体。
密度比空气大,易液化(沸点-10℃),易溶于水,在常温、常压下,1体积水大约能溶解40体积的二氧化硫,成弱酸性。
SO2为酸性氧化物,具有酸性氧化物的通性、还原性、氧化性、漂白性。
还原性更为突出,在潮湿的环境中对金属材料有腐蚀性,液体SO2无色透明,是良好的制冷剂和溶剂,还可作防腐剂和消毒剂及还原剂。
②.?三氧化硫SO3的物理、化学性质:由二氧化硫SO2催化氧化而得,无色易挥发晶体,熔点16.8℃,沸点44.8℃。
SO3为酸性氧化物,SO3极易溶于水,溶于水生成硫酸H2SO4,同时放出大量的热,③.?硫酸H2SO4的物理、化学性质:二元强酸,纯硫酸为无色油状液体,凝固点为10.4℃,沸点338℃,密度为1.84g/cm3,浓硫酸溶于水会放出大量的热,具有强氧化性(是强氧化剂)和吸水性,具有很强的腐蚀性和破坏性,五、石灰石湿-石膏法脱硫化学反应的主要动力过程:1、气相SO2被液相吸收的反应:SO2经扩散作用从气相溶入液相中与水生成亚硫酸H2SO3亚硫酸迅速离解成亚硫酸氢根离子HSO3-和氢离子H+,当PH值较高时,HSO3二级电离才会生成较高浓度的SO32-,要使SO2吸收不断进行下去,必须中和电离产生的H+,即降低吸收剂的酸度,碱性吸收剂的作用就是中和氢离子H+当吸收液中的吸收剂反应完后,如果不添加新的吸收剂或添加量不足,吸收液的酸度迅速提高,PH值迅速下降,当SO2溶解达到饱和后,SO2的吸收就告停止,脱硫效率迅速下降2、吸收剂溶解和中和反应:固体CaCO3的溶解和进入液相中的CaCO3的分解,固体石灰石的溶解速度,反应活性以及液相中的H+浓度(PH值)影响中和反应速度和Ca2+的氧化反应,以及其它一些化合物也会影响中和反应速度。
Ca2+的形成是一个关键步骤,因为SO2正是通过Ca2+与SO32-或与SO42-化合而得以从溶液中除去,3、氧化反应:亚硫酸的氧化,SO32-和HSO3-都是较强的还原剂,在痕量过渡金属离子(如锰离子Mn2+)的催化作用下,液相中的溶解氧将它们氧化成SO42-。
反应的氧气来源于烟气中的过剩空气和喷入浆液池的氧化空气,烟气中洗脱的飞灰和石灰石的杂质提供了起催化作用的金属离子。
4、结晶析出:当中和反应产生的Ca2+、SO32-以及氧化反应产生的SO42-,达到一定浓度时这三种离子组成的难溶性化合物就将从溶液中沉淀析出。
沉淀产物:①.?或者是半水亚硫酸钙CaSO3·1/2H2O、亚硫酸钙和硫酸钙相结合的半水固溶体、二水硫酸钙CaSO4·2H2O。
这是由于氧化不足而造成的,系统易产生硬垢。
②.?或者是固溶体和石膏的混合物。
氧化充足的硫酸钙饱和溶液,不会形成二水硫酸钙硬垢石灰石湿法工艺过程的脱硫反应速率取决于上述四个控制步骤: 七、吸收塔内的化学反应化学总反应式:CaCO 3+2SO 2+H 2O Ca(HSO 3)2+CO 2 (吸收反应)Ca(HSO 3)2+O 2+CaCO 3+3H 2O 2CaSO 4·2H 2O+CO 2(氧化中和结晶) 1.?吸收区的吸收反应:1)?在吸收区主要发生的化学反应为: SO 2+H 2O →H 2SO 3????? H 2SO 3-→H ++HSO 3- 部分发生的化学反应为: H ++HSO 3-+1/2O 2→2H ++SO 42-2H ++SO 42-+CaCO 3+ H 2O →CaSO 4·2H 2O+CO 22)?气态二氧化硫SO 2溶解于水H 2O 中发生反应生成液态亚硫酸H 2SO 3溶液, H 2SO 3迅速离解生成氢离子和亚硫酸氢根离子H +、HSO 3-,部分H +、HSO 3-与烟气中的过剩氧和水中的溶解氧发生氧化反应,生成氢离子2H +和硫酸根离子SO 42-,由于喷淋的石灰石浆液在吸收区停留的时间很短,约5S 左右,只有部分固态石灰石颗粒溶解形成的CaCO 3溶液,分解出钙离子Ca 2+与氢离子2H +,它们和硫酸根离子SO 42-发生中和反应,中和了H +离子,生成硫酸钙CaSO 4,相对过饱和结晶析出二水石膏CaSO 4·2H 2O 。
3)在上述同时进行的化学反应过程中,在吸收区上部(PH 值高),逆流上升被吸收的SO 2基本被吸收,烟气中的过剩氧和水中的溶解氧也逐渐降低,H +、HSO 3-与烟气中的过剩氧和水中的溶解氧发生的氧化反应,在生成硫酸根离子SO 42-的同时,由于氧量的减少生成了大量的亚硫酸根离子SO 32-,它与石灰石浆液中的钙离子Ca 2+中和反应生成亚硫酸钙CaSO 3,若在氧化区内不能充分氧化,在中和区易析出难以溶解的半水石膏CaSO 3·1/2H 2O 。
4)烟气中的SO 2溶入石灰石吸收浆液的过程几乎全部发生在吸收区,但由于石灰石浆液和烟气在吸收区的接触时间仅数秒钟,浆液中的CaCO 3仅中和了部分已氧化的亚硫酸H 2SO 3(以及少量被烟气中的过剩氧O 2氧化的硫酸H 2SO 4)。
即在吸收区内,石灰石浆液只有少量的CaCO 3参与了化学反应。
5)吸收区吸收SO 2的控制:①.控制石灰石的品质、纯度和粒度:1.?石灰石中的杂质对石灰石颗粒的消溶起阻碍作用,石灰石品质高,石灰石颗粒的消溶性越好。
2.?石灰石颗粒的粒度越小,质量比面积就越大,石灰石的消溶性越好;3.?增强石灰石的消溶速率,浆液吸收SO2的反应速率越快,即提高了脱硫效率,也提升了石灰石粉的利用率;②.控制进入吸收塔的烟气的飞灰:飞灰阻碍石灰石的消溶,降低石灰石的消溶速率,导致脱硫效率下降。
PH值降低而无法调高,一般经过静电除尘器后,烟气飞灰浓度在100~300mg/Nm3。
电除尘电场退出超过规定,FGD保护退出运行。
③.根据进入FGD的SO2浓度,控制Ca/S比和L/G比:进入FGD的SO2浓度降低,应向吸收塔送入较低密度的石灰石浆液,而在进入FGD的SO2浓度很高时,应向吸收塔送入较高密度的石灰石浆液。
如果进入FGD的SO2浓度很高,石灰石浆液供浆流量已达到最大,PH值仍然下降,净烟气浓度超过设计保证值,脱硫效率下降,应加开备用循环泵增加液气比,2.?氧化区的氧化反应:1)?发生在氧化区的主要化学反应:H++HSO3-+1/2O2→2H++ SO42-CaSO3+ 2H+→ Ca2++H2O+CO2Ca2++SO42-+ H2O→CaSO4·2H2O2)?氧化区的范围大致从浆液池液面至固定管网氧化装置喷咀下方300mm处,即吸收塔约10米以上的液位,在氧化区氧化池内,从吸收区吸收SO2后喷淋落下的浆液,主要是大量未被氧化的亚硫酸氢根离子HSO3-溶液。
氧化风机将大量氧化空气沿吸收塔径向圆周均匀的喷入氧化区下部,将HSO3-氧化成氢离子H+和硫酸根SO42-,迅速中和洗涤浆液中剩余的CaCO3,以及在吸收区由于氧量不足而生成的亚硫酸钙CaSO3,最终生成溶解状态的硫酸钙CaSO4,当钙离子Ca2+和硫酸根SO42-浓度达到一定饱和时,结晶生成二水硫酸钙CaSO4·2H2O(二水石膏)。
3)?氧化控制:保证氧化区的液位,保证氧化风机的正常运行和供风量。
HSO3-离子在PH值为4.5时氧化速率最大,通过增加强制氧化控制PH值可控制在4.5-5.5之间,可将大量的HSO3-离子强制氧化成硫酸根SO42-,而SO42-与钙离子Ca2+发生反应生成硫酸亚硫酸氢钙的危害性:无色或微黄色固体或液体,有强烈的二氧化硫气味。
具有还原性。
接触酸或酸气能产生有毒气体。
(如硫化氢是一种有毒气体,人吸入后会引起昏迷甚至于死亡)受高热分解放出有毒的气体。
具有腐蚀性、刺激性。
有毒。
误服会中毒。
蒸气刺激眼睛和粘膜。
液体能腐蚀眼睛、皮肤和粘膜。
对环境可能有危害,对水体可造成污染。
高浓度可致人体灼伤。
空气中浓度超标时,必须佩戴自吸过滤式防毒面具(半面罩)。
应该佩戴空气呼吸器。
戴化学安全防护眼镜。
直接接触者应穿橡胶耐酸碱服。
戴橡胶耐酸碱手套。
吸收塔氧化空气严重不足,浆液会携带大量的有毒气体从脱水系统中分解出来。
4)?吸收塔浆液获得氧的途径主要是:烟气中的过剩氧气,水中的溶解氧和主要由氧化风机强制喷入浆液池的氧化空气。
另外烟气飞灰中和石灰石杂质中,对吸收的氧化反应也提供了起催化作用的金属离子,如:?5)?避免过多的新鲜石灰石浆液进入氧化区。
这将不利于HSO3-的氧化,存在过量的CaSO3有助于形成CaSO3·1/2H2O,而溶解氧很难氧化CaSO3·1/2H2O。
除非有过量的H+才能使其重新溶解为HSO3-。
3.?中和区的中和反应:1)?吸收浆液落入浆液池,缓缓经过氧化区,进入中和区,氧化区的下面一般视为中和区,循环泵入口至吸收塔喷淋层喷咀之间的管道、泵体空间也是中和区的一部分。
经过强制氧化,浆液中过剩的亚硫酸钙CaSO3浓度降至最低值,此时浆液中结晶生成二水硫酸钙CaSO4·2H2O的浓度最高,从吸收塔底部一侧排出浆液至脱水系统。
即可获得较高品位的石膏。
2)?经过吸收区吸收反应,氧化区强制氧化反应,进入在中和区的浆液,仍然有未中和完的H+,从2#、3#循环泵的入口加入新鲜的石灰石浆液,可以中和剩余H+,分解出Ca2+,活化浆液,提升和保持PH值。
使浆液在下一个循环中与硫酸根离子SO42-直接发生中和反应,生成硫酸钙CaSO4,结晶沉淀析出二水石膏CaSO4·2H2O。