卡尔费休水分测定---原始记录
- 格式:docx
- 大小:20.42 KB
- 文档页数:1
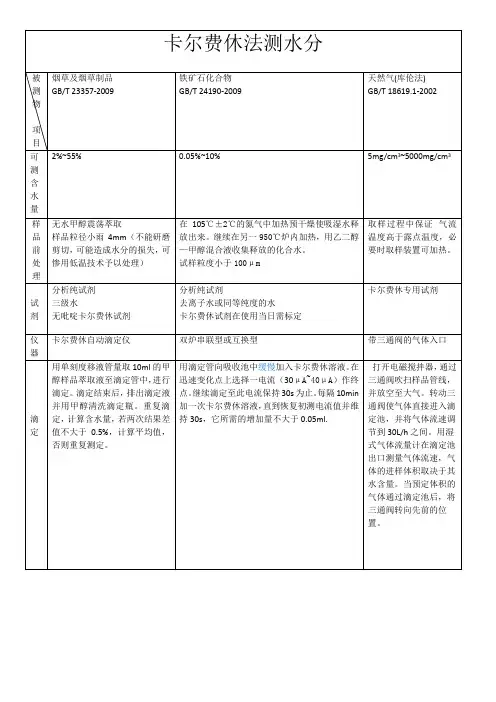


卡尔费休氏水分测定法对样品中水分的含量测定建立在R.W.Bunsen描述的下面这个反应上:I2+SO2+2H2O 2HI+H2SO4Karl Fischer首先发现这个反应可以在非水环境中用来测定水分含量,反应系统中包含有过量的SO2,甲醇可以被选作理想的溶剂。
但反应是可逆的,为了使反应向右进行,Karl Fischer用吡啶来吸收反应生成的HI和H2SO4.Smith,Bryanz 和 Mitchell 将这个反应描述成两步:I2+SO2+H2O+3B5C5N → 2B5C5NH+I- + B5C5N.SO3B 5C5N.SO3+CH3OH → B5C5N H+CH3SO4-在第一步反应中,KF试剂和水反应生成的B5C5N.SO3不稳定,容易分解成吡啶和二氧化硫,甲醇可以和其反应生成稳定的B5C5N H+CH3SO4-。
由此可见,甲醇作溶剂有防止副反应发生的作用。
在醇溶剂中,碘和水反应的化学计量数为1:1。
在无醇的溶剂中,碘和水反应的化学计量数为1:2:I 2+SO2+H2O+3 B5C5N → 2 B5C5N H+I- + B5C5N.SO3(不稳定)B 5C5N.SO3+H2O → B5C5N H+HSO4-(稳定)卡尔.费休试剂的基本成份是碘、二氧化硫、溶剂和有机碱,溶剂主要是醇类。
通常,试剂中二氧化硫、有机碱和醇类物质都是过量的,试剂中碘与水以固定的化学计量数1:1进行反应,所以我们在进行实验前应先确定滴定剂中碘的浓度,也即对滴定剂进行标定,这是本实验定量的基础。
用已知浓度的卡氏试剂滴定样品中的水分,由消耗滴定剂的体积和称样量,即可求出样品的含水量。
以前,卡氏试剂中用的有机碱主要是有毒、恶臭的吡啶,但更重要的是如果我们不能确定反应到底受那些方面的影响的话,我们就无法用其来进行定量分析。
后来,E.Barenrecht和J.Cverhoff对Karl Fisher反应进行了更进一步的研究后,得出了如下结论:◎吡啶不直接参加反应,也就是说它只起调节PH值和缓冲剂的作用,可以用其它的有机碱替代。

FNCPFL0025 液体无水氨水分的测定卡尔·费休法F_NCP_FL_ 0025液体无水氨-水分的测定-卡尔·费休法1 范围本方法适用于由氢、氧在高温、高压下直接催化合成制得的液体无水氨(液氨)中水分含量的测定。
本方法适用于水分等于或大于50mg/ kg的液体无水氨产品。
2 原理在乙二醇存在下,蒸发液氨试样后,利用水和卡尔 · 费休试剂(碘、二氧化硫、吡啶和甲醇组成的溶液)进行的定量反应。
H2O+I2+SO2+3C5H5N+ROH→2C5H5N · HI+C5H5NH · OSO2OR由直接电量法测定蒸发残留物的水分。
3 试剂3.1 冰乙酸,ρ约1.05g/ L3.2 二水酒石酸钠(Na2C4H4O6·2H2O)或水3.3 硫酸溶液,质量分数约为10%3.4 乙二醇,水分不大于0.1%(质量分数)如含水量超过0.1%(质量分数),可于500ml乙二醇中加入5A分子筛选约50g,塞上瓶塞,摇动后,放置过夜,吸取上层清液使用。
乙二醇极易吸湿,须防止大气中湿气影响。
3.5 甲醇,水分不大于0.03%(质量分数)如含水量超过0.03%(质量分数),可于500ml乙二醇中加入5A分子筛选约50g,塞上瓶塞,摇动后,放置过夜,吸取上层清液使用。
3.6 甲醇-乙酸溶液将100ml冰乙酸和900ml甲醇相混匀。
3.7 卡尔 · 费休试剂置670mL甲醇或乙二醇甲醚于干燥的1 L带塞的棕色玻璃瓶中,加约85g碘。
塞上瓶塞,振荡至碘全部溶解后,加入270mL吡啶,盖紧瓶塞,再振动至完全混匀。
用下述方法溶解65g 二氧化硫于溶液中。
通入二氧化硫时,用橡皮塞取代瓶塞,橡皮塞上装有温度计,进气玻璃管(离瓶底10mm,管径为6mm)和通大气毛细管。
将整个装置及冰浴置于台秤上,称量,称准至1g,通过软管使二氧化硫钢瓶(或二氧化硫发生器出口)与填充干燥剂(活性硅胶)的干燥塔及进气玻璃管连接,缓缓打开进气开关。

412 PCO2 垂直分布:在船上在20 ℃浴温下做平衡,得出的PCO2 ( 20 ℃) 垂直分布如图2a 。
换算到现场温度下PCO2 如图2b 。
PCO2 ( 现场) 随深度变化与TC O2 相似, 也在300 —400m 达最大值。
由温度降低造成向下减少,在135°E 以西与TC O2 一致。
从表层到1000m TCO2 值小于停泊点值。
停泊点上: 0 —100m , PCO2 ( 20 ℃) 在400m 可达1000uat m 左右,500m 出现个最小值, 以后又增加, 从600m 以下变化不大。
11 月26 日—11 月30 日, 再到2 月份, PCO2 值逐步减少。
垂直分布规律与以前相同。
从PCO2 (现场温度) 与TCO2 的关系图(图略) 可见在现场温度下当PCO2 大于μat m , TCO2 小于μmo l/ kg , 即对应着400m 以下深度时, PCO2 与TCO2 呈正相关趋势。
400m 以上与TCO2 不成正相关且PCO2 变化范围很大,显然是由于上层水温度变化影响增大的缘故。
参考文献:1 David W. Chip man and Jo hn G o ddard , Tachnical manual f o r ga schro matograp hic syst em f o r high p recisio n measurement of carbo n dio xide partical p ressures in discret e ocean wat er and air samples , R , New Y o r k , L amo nt - D o hert y G e ological Observato ry of Columb.马黎明,热带西太平洋海—气C02 交换与碳化学量的分布〈, 热带西太平洋海气相互作用综合研究〉M , 北京, 海洋出版社, 1993 ,156 - 173 .乔然, 马黎明, 张滨, 高精度测量海水和大气二氧化碳分压( PC02) 气相色谱系统的完善和应用, C , 微量元素研究进展( 1995 . 07) ,北京,化学工业出版社,1995 ,229 - 234 .乔然,海水二氧化碳分压的取样手段和分析计算方法, J , 北京, 海洋预报,1993 ,1 ( 1) 1 ,77 - 79 .234卡尔2费休法测定丙酮中微量水分代丽斌(北京燕山石油化工公司研究院,北京102500)摘要:本文采用乙二醇甲醚、吡啶、二氧化硫和碘配制成卡尔2费休试剂,在以乙二醇甲醚与吡啶( 4¬1) 的混和液作为本底溶剂的条件下,用其测定丙酮中的水分。

容量法卡尔费休法测定硬糖样品中水分的含量
目的:
本实验用甲醇和甲酰胺的混合溶液作为溶剂增加硬糖样品在溶剂中的溶解度,使用AKF-1水分仪直接测定硬糖中水分的含量,验证AKF-1在硬糖样品中水分检测的可行性、准确度和重复性。
仪器配置:
1、AKF-1卡尔费休水份测定仪主机;
2、全封闭安全滴定池组件;
3、双铂片电极
4、滴定池搅拌台
5、10μL微量进样针
6、电子天平(0.1mg)
试剂:
1、滴定剂:容量法单组份卡尔费休试剂
2、溶剂:无水甲醇
3、辅助试剂:甲酰胺
测定方法:
1、向滴定池内加入甲醇和甲酰胺的混合溶液(甲醇:甲酰胺=2:1);
2、使用仪器中“标定”选项的“打空白”功能滴定至终点,彻底除去滴定池和
溶剂中的水分;
3、选择“试剂标定”功能,用经过干燥处理的微量进样针精确抽取10 μL纯水,
拭干针头后将针头插入滴定池内加样,加样结束后输入加样质量为10 mg,开始标定;
4、重复步骤3,反复测量3-5次,仪器后自动保存标定结果并计算出平均值作为
试剂的滴定度;
5、将硬糖样品用研钵粉碎细化后,称取硬糖样品约0.3 g加入滴定池,将样品的
进样质量输入仪器,并开始测量。
仪器参数
1、计量管体积:20 mL
2、终点电流值:60 μA
3、最小进液量:0.002 mL
4、滴定延时:90 s
5、终点延时:10 s
6、漂移扣除:On
7、终点保持:On
卡尔费休水份测定仪样品测定记录。

卡尔费休水分测定仪操作方法一、测定仪器简介卡尔费休水分测定仪是一种用于测定物质中水分含量的仪器。
它采用卡尔费休法,通过化学反应将水分转化为氢气,并通过气体体积变化来计算样品中的水分含量。
二、操作步骤1. 准备工作a. 将样品粉碎并均匀混合,以保证测定的准确性。
b. 打开测定仪的电源开关,并连接氢气和氧气气源。
c. 确保仪器的温度和压力显示正常。
2. 样品称量a. 取一个干净的称量瓶,并记录其质量。
b. 将约5克的样品放入称量瓶中,并将其质量重新称量,记录下样品的质量。
3. 滴定操作a. 打开测定仪的滴定阀门,并将样品放入仪器中。
b. 关闭滴定阀门,并将仪器密封。
确保密封完好,避免气体泄漏。
c. 打开氢气阀门,使氢气进入仪器中。
d. 同时打开燃烧器,并点燃氢气。
确保燃烧器安全可靠。
e. 观察滴定管中的气泡,当气泡停止产生时,关闭氢气阀门。
4. 计算水分含量a. 将滴定管中的气体体积读数记录下来。
b. 根据卡尔费休法的原理,计算样品中的水分含量。
公式为:水分含量(%)= (气体体积 - 氢气体积)/ 样品质量 * 100%5. 清洁与关闭a. 关闭燃烧器和气源阀门,断开氢气和氧气的连接。
b. 清洁测定仪器,并确保其处于干燥的状态。
c. 关闭测定仪器的电源开关。
三、注意事项1. 操作过程中需注意安全,确保仪器和气源的正常运行。
2. 严禁在仪器运行时离开,以免发生意外。
3. 使用前应检查仪器的正常工作状态,如温度和压力显示。
4. 测定仪器的滴定管需保持清洁,避免阻塞。
5. 滴定操作中需确保样品完全燃烧,以保证测定结果的准确性。
6. 操作结束后,应及时清洁仪器,以保持其正常运行。
通过以上操作步骤,我们可以使用卡尔费休水分测定仪准确地测定样品中的水分含量。
这种仪器操作简单、准确度高,广泛应用于食品、化工、制药等领域。
希望本文能对读者了解卡尔费休水分测定仪的操作方法有所帮助。

卡尔费休法及其样品中微量水分测定方法一、背景:1935 年德国人卡尔费休(Karl Fischer发明了一种测定水分的新方法:利用碘和二氧化硫的氧化还原反应,在有机碱和甲醇的环境下,与水发应定量反应。
CH3OH + SO2 + RN —— [RNH]SO2CH3 RN为有机碱,例如吡啶。
这一步反应是二氧化硫与甲醇反应生成一种酯,而酯被碱中和。
I2 + H2O + [RNH]SO3CH3 + 2RN ——2HI + [RNH]SO4CH3 + 2(RNH)I 这一步反应是与水的定量发应:硫醚阴离子在水作用下被碘氧化成烷基硫酸盐,碘与水1:1定量反应。
用含碘的试剂不断滴定样品,判断终点的方法是观察碘过量时的颜色变化。
这就是最初的卡尔费休水分滴定法。
发展历:1.手动滴定、肉眼判断终点。
这是最初的卡尔费休滴定法。
2.手动滴定、电极极化判断终点。
在浸入溶液的双铂电极间加上一适当电压,因溶液中存在水而使阴极极化,电极间无电流通过。
滴定终点无水时,阴极去极化,电流突然增加至一最大值,并长久保持(电流表指针突然由0打到max,并保持在这个位置)。
这就是所谓的“永停法”判断终点。
3.自动滴定、自动判断终点。
所谓的全自动滴定仪,仪器内部都由精密的电路控制,滴定自动控制,漂移自动补偿,终点自动判断。
4.卡尔费休库仑法:这次测量方法本质的一个改进。
1959 年Meyer 和Boyd 将库仑法与卡尔费休法联立起来,改变试剂的成分,用碘离子替换了碘单质。
通过电解产生碘2I-— 2e —— I2。
其他过程不变。
10.71库仑电流相当于1mg的水。
由于计量方式由计量试剂体积到计量电流量,精确度大幅提高,可达1ppm。
而且不用预先确定试剂的滴定度,可以直接测量,也被称为一种“绝对方法”。
另外具有消耗试剂少,反应时间短等优点。
所以狭义的微量水分测定仪就是指的卡尔费休库仑法水分测定仪。
5.技术成熟的后仪器时代。
基本测量方法已经非常成熟了,相应的附加改进技术以及相关衍生产品层出不穷。

AKF-1容量法卡尔费休水分滴定仪
报告:上海禾工科学仪器有限公司
数据档案:2017042801 ---案例名称---
卡尔费休水分滴定仪直接进样测定N-甲基吡咯烷酮中的水分
---仪器参数---
计量管体积:20mL
控制精度:3μL(20ml高精度计量管)
搅拌速度:30
吸排试剂:自动
辅助功能:方法保存,结果自动计算存储,设备检定,废液瓶满警示功能滴定延时:10秒
终点延时:8秒
漂移扣除:开
终点保持:开
漂移值更新:自动
延时设置:可根据需要设置延时滴定、终点延时功能应对难溶样品
卡尔费休水份测定仪样品测定记录样品来源:客户寄样环境温度:20℃
样品名称:N-甲基吡咯烷酮滴定度:3.557mg/mL 环境湿度:45%。

模块二:食品营养成分检测操作及规范项目一水分测定任务食品中水分的测定第一法直接干燥法一、工作准备1、试剂(1)盐酸溶液(6 mol/L):量取50 mL盐酸,加水稀释至100 mL。
(2)氢氧化钠溶液(6mol/L):称取24 g氢氧化钠,加水溶解并稀释至100 mL。
(3)海砂:取用水洗去泥土的海砂或河砂,先用盐酸(6 mol/L)煮沸0.5 h,用水洗至中性,再用氢氧化钠溶液(6 mol/L)煮沸0.5 h,用水洗至中性,经105℃干燥备用。
2、仪器(1)扁形铝制或玻璃制称量瓶(2)电热恒温干燥箱(3)干燥器:内附有效干燥剂(4)天平:感量为0.1 mg3、参考标准GB 5009.3-2016食品安全国家标准食品中水分的测定二、检验程序见图2-1:101℃~105℃干燥箱,称量瓶恒重称取样品样品处理101℃~105℃干燥箱,样品及称量瓶恒重数据记录及处理出具报告图2-1 直接干燥法测定食品中水分检验流程图三、操作规程 1.固体样品取洁净铝制或玻璃制的扁形称量瓶,置于101℃~105℃干燥箱中,瓶盖斜支于瓶边,加热1.0h ,取出盖好,置干燥器内冷却0.5h ,称量,并重复干燥至前后两次质量差不超过2 mg ,即为恒重。
将混合均匀的试样迅速磨细至颗粒小于2 mm ,不易研磨的样品应尽可能切碎,称取2g ~10g 试样(精确至0.0001g ),放入此称量瓶中,试样厚度不超过5mm ,如为疏松试样,厚度不超过10mm ,加盖,精密称量后,置101℃~105℃干燥箱中,瓶盖斜支于瓶边,干燥2h ~4 h 后,盖好取出,放入干燥器内冷却0.5h 后称量。
然后再放入101℃~105℃干燥箱中干燥1h 左右,取出,放入干燥器内冷却0.5h 后再称量。
并重复以上操作至前后两次质量差不超过2mg ,即为恒重。
2.半固体或液体试样取洁净的称量瓶,内加10g 海砂及一根小玻棒,置于101℃~105℃干燥箱中,干燥1.0h 后取出,放入干燥器内冷却0.5h 后称量,并重复干燥至恒重。
1.前言卡尔·费休水分测定法是以甲醇为介质以卡氏液为滴定液进行样品水分测量的一种方法。
此方法操作简单,准确度高,广泛应用于医药、石油、化工、农药、染料、粮食等领域。
尤其适用于遇热易被破坏的样品。
一般情况下,产品中水分的含量异常会严重地影响产品的质量和使用效果。
例如:药品、日用品、食品中所含水分过高会影响其稳定性、理化性状、及使用效果和保质期,化学试剂中所含水分过多会影响其化学特性等。
因此,对产品中的水分进行检查并控制其限度非常重要。
以前,人们普遍应用加热干燥法,此种方法不但繁琐、费时,而且系统误差较大不能满足现代化生产中对产品检验的需要。
1935年,Karl Fischer发现了一种用滴定法测定含水量从1ppm 到100%的样品的方法。
该方法测定水分含量的用途广泛、结果准确可靠、重复性好,能够最大限度的保证分析结果的准确性。
而且该方法滴定时间短,一般情况下测定一个样品仅需2到5分钟,适应现代化生产中快速检测的要求。
因而卡尔·费休氏水分测定法得到了各界的一致认可,现在已成为国际上通用的经典水分测定法。
2.基本原理卡尔·费休水分测定法是一种非水溶液中的氧化还原滴定法,其滴定的基本原理是碘氧化二氧化硫时需要一定量的水参与反应,化学反应方程式如下:I2+SO2+2H2O → 2HI+H2SO4 (2-1)I2+SO2+H2O+3RN+R1OH → 2RNHI+RNSO4R1 (2-2)卡氏试剂中含有分子碘而呈深褐色,当含有水的试剂或样品加入后,由于化学反应,生成甲基硫酸化合物(RNSO4R1)而使溶液变成黄色,由此可用目测法判断终点,即由浅黄色变成橙色.但是目测法误差教大而且在测定有颜色的物质时会遇到麻烦。
国家标准大都规定用“永停法”来判定卡氏反应的终点,其原理为:在反应溶液中插入双铂电极,在两电极之间加上一固定的电压,若溶剂中有水存在时,则溶液中不会有电对存在,溶液不导电,当反应到达终点时,溶液中存在I2和I-电对,即:2I-= I2+2e (2-3)因此,溶液的导电性会突然增大,在设有外加电压的双铂电极之间的电流值突然增大,并且稳定在我们事先设定一个阈值上面,即可判断到了滴定终点,机器便会自动停止滴定,从而通过消耗KF试剂的体积计算出样品的含水量。
FCLHCQT0004 化工产品水分含量的测定卡尔·费休法电量反滴定法F_CL_HC_QT0004化工产品—水分含量的测定—卡尔·费休法-电量反滴定法1范围本方法适用于大部分有机和无机固、液体化工产品游离水或结晶水含量的测定。
在某些情况下,样品需要采取预处理措施,预处理方法在相应的方法中作规定。
2原理2.1卡尔·费休法原理存在于试样的任何水分(游离水或结晶水)与已知水当量的卡尔·费休试剂(电、二氧化硫、吡啶和甲醇组成的溶液)进行定量反应。
反应式如下:H2O+I2+SO2+3C5H5N 2C5H5N·HI+C5H5N·SO3C5H5N·SO3+ROH C5H5NH·OSO2OR注:甲醇可用乙二醇甲醚代替。
用此试剂,可得更为恒定的滴定体积,而且可在不使用任何专门技术下测定某些醛和酮类化工产品的水分。
2.2直接电量滴定法终点滴定原理使侵入溶液中的两铂电极有一电位差,当溶液中存在水时,阴极极化反抗电流通过,有阴极去极化伴随着突然增加的电流(由适合的电装置示出)指示滴定终点。
3试剂3.1甲醇:水含量低于0.05%(m/m)。
如试剂水含量大于0.05%,于500mL甲醇中加入5A 分子筛(3.11.1)约50g,塞上瓶塞,放置过夜,吸取上层清液使用。
3.2乙二醇甲醚:水含量低于0.05%(m/m),如试剂水含量大于0.1%,按3.1方法处理。
3.3碘3.4吡啶:水含量低于0.05%(m/m),如试剂水含量大于0.1%,按3.1方法处理。
3.5冰乙酸3.6氯仿:水含量低于0.05%(m/m),如试剂水含量大于0.1%,按3.1方法处理。
3.7硫酸:化学纯3.8无水亚硫酸钠:化学纯3.9二氧化硫:钢瓶装二氧化硫或用硫酸(3.7)分解饱和亚硫酸钠溶液(3.8)制得的二氧化硫,均需经脱水干燥处理。
二氧化硫发生装置见图1。
1. 二氧化硫气体发生器;2. 空洗气瓶;3. 浓硫酸洗气瓶;4. 分离器5. 接水泵;6. 温度计;7. 盛有甲醇、碘、吡啶溶液的吸收瓶;8. 冰浴图1 二氧化硫发生装置3.10样品溶剂:含4体积甲醇(3.1)和1体积吡啶(3.4)的混合物,或含4体积乙二醇甲醚(3.2)和1体积吡啶(3.4)的混合物(尤适用于某些含羰基化合物)。
微量水分测定仪校验规程1.0目的规范微量水分测定仪的校准操作,确保微量水分测定仪的有效性和准确性。
2.0范围本规程适用于卡尔·费休微量水分测定仪(库仑法)的首次检定、后续检定和使用中检验。
3.0通用技术要求3.1 仪器外观3.1.1 仪器上应有仪器的名称、型号、制造厂名、产品系列号、出厂日期等内容的标牌,国产仪器应有制造计量器具许可证标志。
3.1.2 仪器外观不应有影响仪器正常工作的机械损伤。
3.1.3 仪器的各紧固件均应紧固,工作正常。
3.2 仪器的电解池系统仪器的电解池系统应密封良好,无电极、干燥管、磨塞卡死现象。
3.3 仪器的电路系统3.3.1 仪器电源线、信号线等插件紧密,各开关、旋钮、按键等功能正常,指示灯灵敏,显示器清晰。
3.3.2 电解池搅拌系统正常,能调速。
4.0计量性能要求4.1 显示系统4.1.1 正常显示水分的绝对值μg4.1.2 正常显示电解速度的变化值或变化趋势4.1.3 具有用文字、代码、指示灯或声音提示仪器处于调零、空白测试、样品测量和测试结果等状态的功能。
4.1.4 具有指示卡尔·费休试剂过碘、过水的功能。
4.2 示值误差对不同测量范围,其测得的平均值与标准值之差(称示值误差)不得超过表l规定。
表l4.3 测量重复性:3%4.4 电解速度:电解1000μg水≤3min。
4.5 零点平衡时间:≤2min。
4.6 绝缘电阻:仪器的电源相、中连线与机壳间的绝缘电阻不低于20MΩ4.7 绝缘强度:仪器的电源相、中连线与机壳间的绝缘强度能承受50Hz、1500V 正弦交流电压历时1min,无击穿及飞弧现象。
4.8 泄漏电流:仪器的电源相、中连线与机壳间的泄漏电流不大于5mA(峰值)。
5.0内容5.1 环境条件5.1.1 检定室应清洁无尘,无易燃、易爆和腐蚀性气体,排风良好。
5.1.2 环境温度:5~30℃5.1.3 相对湿度:不大于80%。
5.1.4 供电电源:(220±10%)V,(50±1)Hz5.1.5 仪器应平稳放在工作台上,周围无强烈机械振动和电磁干扰源,仪器接地良好。
.微量水分测定仪检定规程1 范围本规程适用于卡尔·费休微量水分测定仪(库仑法)的首次检定、后续检定和使用中检验。
2 概述卡尔·费休微量水分测定仪(以下简称仪器)主要用于测定石油、化工、轻工、电力、医药、农药、环保、地质、食品等行业产品中的水分含量,其仪器的工作原理如下:卡尔·费休试剂同水反应为:I 2+SO 2+3C 5H 5N+H 20→2C 5H 5N ·HI+C 5H 5N ·SO 3C 5H 5N ·SO 3+CH 3OH →C 5H 5N ·HSO 4CH 3所用试剂溶液是由一定浓度的单质碘和充有二氧化硫的吡啶、甲醇等混合而成,通过电解在阳极上形成碘,碘又与水反应生成氢碘酸,直至水全部反应完毕为止。
反应终点用一铂电极来检测指示。
在电解过程中,电极反应如下:阳极:2I --2e →I 2 阴极:I 2+2e →2I -2H ++2e →H 2↑在整个过程中,二氧化硫有所消耗,其消耗量与水的克分子数相等。
依据法拉第电解定律,电解1克分子碘,需要二倍的96493C 电量,即电解1毫克当量水需要电量为96493mC 。
样品中的水分含量计算式为:96493210181036⨯⨯=⨯--Q W即722.10QW =式中:W ——样品中的水分含量,μg ; Q ——电解电量,mC ; 18——水的分子量;图1 卡尔·费休库仑法微量水分测定仪组成方框图3 通用技术要求3.1 仪器外观3.1.1 仪器上应有仪器的名称、型号、制造厂名、产品系列号、出厂日期等内容的标牌,国产仪器应有制造计量器具许可证标志。
3.1.2 仪器外观不应有影响仪器正常工作的机械损伤。
3.1.3 仪器的各紧固件均应紧固,工作正常。
3.2 仪器的电解池系统仪器的电解池系统应密封良好,无电极、干燥管、磨塞卡死现象。
3.3 仪器的电路系统3.3.1 仪器电源线、信号线等插件紧密,各开关、旋钮、按键等功能正常,指示灯灵敏,显示器清晰。