物理化学8.5电动势产生的机理与电极电势
- 格式:ppt
- 大小:1.60 MB
- 文档页数:21

化学反应中的电极电势与电池电动势实例在化学反应中,电极电势和电池电动势是两个重要的概念。
电极电势指的是在电化学反应中,电极与溶液中某种溶质之间建立的电势差。
而电池电动势则是指整个电池中两个电极之间的电势差。
本文将结合实例介绍化学反应中的电极电势与电池电动势的概念与相关原理。
实例一:铜与铁电池在铜与铁电池中,铜离子是从铜电极溶解产生的,这个反应可以表示为:Cu(s) → Cu²⁺(aq) + 2e⁻而在铁电极上,则是铁离子发生还原反应:Fe²⁺(aq) + 2e⁻ → Fe(s)根据这两个半反应的标准电极电势可以计算出它们之间的电势差。
在标准状态下,铜电极的标准电极电势为+0.34V,而铁电极的标准电极电势为-0.44V。
所以,在这个铜与铁电池中,电池电动势可以计算为:Ecell = E(铜) - E(铁) = +(0.34V) - (-0.44V) = +0.78V这个正值表示铜与铁电池是一个可行的电池反应,并且产生正向的电势差。
这意味着当铜与铁电池连接成电路时,电子会从铁电极流向铜电极,而离子则会在溶液中迁移,从而产生电流。
实例二:锌与铜电池在锌与铜电池中,锌离子会溶解,并且金属锌会被氧化为锌离子,这个反应可以表示为:Zn(s) → Zn²⁺(aq) + 2e⁻与之相对应的是铜电极上的还原反应:Cu²⁺(aq) + 2e⁻ → Cu(s)通过比较这两个半反应的标准电极电势,可以计算出锌与铜电池的电动势。
在标准状态下,锌电极的标准电极电势为-0.76V,而铜电极的标准电极电势为+0.34V。
因此,锌与铜电池的电动势可以计算为:Ecell = E(锌) - E(铜) = (-0.76V) - (+0.34V) = -1.1V这个负值表示锌与铜电池是一个不可行的电池反应,不能产生正向的电势差。
因此,在锌与铜电池中,电子从铜电极流向锌电极,但离子却会在溶液中迁移,从而产生反向的电流。

化学反应中的电极电势与电池电动势化学反应是一种涉及原子和分子之间重组的过程,而电池则是利用化学反应产生电能的装置。
电极电势和电池电动势是描述电化学反应中电子转移能力的重要参数。
本文将介绍电极电势和电池电动势的概念、影响因素以及它们之间的关系。
一、电极电势的概念与测量电极电势是指电极与溶液或气体之间的电势差。
在电化学反应中,电极上电子的转移产生电势差,进而影响反应的进行。
电极电势能够反映电子在电极上的活动程度,是判断电极是氧化还是还原的参数。
电极电势通常用标准电极电势(E°)来表示,单位为伏特(V)。
测量电极电势的方法有很多种,其中最常用的方法是通过比较电池。
比较电池由两个半电池组成,可以产生一个已知电势差的电池。
通过将待测电极与比较电池相连,测量它们之间的电势差,从而确定待测电极的电势差。
二、电极电势的影响因素1. 温度:电极电势随温度的变化而变化。
温度升高会导致电极电势升高或降低,具体取决于反应的热力学性质。
2. 浓度:电极电势与参与反应的物质浓度有关。
当参与反应的物质浓度发生改变时,电极电势也会发生变化。
3. 压力:对于气体电极,电极电势随气体的分压变化而变化。
增大气体分压会导致电极电势升高。
4. pH 值:对于溶液电极,电极电势会受到 pH 值的影响。
改变溶液pH 值能够改变电极电势。
三、电池电动势的概念与计算电池电动势是指电池两个电极之间的电势差,表征了电化学反应产生的电能。
电池电动势通常用电池电动势(Ecell)来表示,单位为伏特(V)。
计算电池电动势的方法是通过测量两个电极的电极电势,并利用Nernst 方程进行计算。
Nernst 方程是描述电极电势与反应物浓度之间关系的数学方程。
Ecell = E°cell - (RT/nF)ln(Q)其中,E°cell 是标准电动势,R 是气体常数,T 是温度,n 是电子转移的摩尔数,F 是法拉第常数,Q 是反应物的活度积。


电极电势详细资料大全为了获得各种电极的电极电势数值,通常以某种电极的电极电势作标准与其它各待测电极组成电池,通过测定电池的电动势,而确定各种不同电极的相对电极电势( electrode potential)E值。
1953年国际纯粹化学与套用化学联合会(IUPAC)的建议,采用标准氢电极作为标准电极,并人为地规定标准氢电极的电极电势为零。
基本介绍•中文名:电极电势•外文名:electrode potential•提出者:能斯特•提出时间:1953年•套用学科:电化学等•适用领域范围:化学滴定分析,电池等定义来源,标准状态,影响因素,相关套用,判断氧化剂和还原剂的相对强弱,判断氧化还原反应的方向,判断反应进行的限度,电势图,定义来源双电层理论德国化学家能斯特(H.W.Nernst)提出了双电层理论(electrical double layers theory)解释电极电势的产生的原因。
当金属放入溶液中时,一方面金属晶体中处于热运动的金属离子在极性水分子的作用下,离开金属表面进入溶液。
金属性质愈活泼,这种趋势就愈大;另一方面溶液中的金属离子,由于受到金属表面电子的吸引,而在金属表面沉积,溶液中金属离子的浓度愈大,这种趋势也愈大。
在一定浓度的溶液中达到平衡后,在金属和溶液两相界面上形成了一个带相反电荷的双电层(electrical double layers),双电层的厚度虽然很小(约为10 -8厘米数量级), 但却在金属和溶液之间产生了电势差。
通常人们就把产生在金属和盐溶液之间的双电层间的电势差称为金属的电极电势(electrode potential),并以此描述电极得失电子能力的相对强弱。
电极电势以符号E(M n+/M)表示, 单位为V(伏)。
如锌的电极电势以E( /Zn) 表示, 铜的电极电势以E( /Cu) 表示。
电极电势的大小主要取决于电极的本性,并受温度、介质和离子浓度等因素的影响。
标准状态电极符号:Pt|H 2(100kPa)|H +(1mol/L) 电极反应: 右上角的符号“⊖”代表标准态。

电动势和电极电势的关系引言:在电学领域中,电动势和电极电势是两个重要的概念。
电动势是指电源推动单位正电荷沿闭合回路移动所做的功,而电极电势则是指电池两极之间的电位差。
本文将探讨电动势和电极电势之间的关系,并介绍它们在电路中的应用。
一、电动势的定义和特点电动势是电源内能量转化为电能的能力,通常用字母E表示。
电动势的单位是伏特(V),它的大小与电池内部化学反应的能量转化有关。
电动势可以通过以下公式计算:E = W / q其中,E代表电动势,W代表电源对电荷做的功,q代表单位正电荷。
二、电极电势的定义和特点电极电势是指电池两极之间的电位差,通常用字母V表示。
电极电势是电荷在电路中移动时,由于电场力做功而使电位能发生变化的结果。
电极电势的大小与电池内部电化学反应有关,它可以通过以下公式计算:V = W / q其中,V代表电极电势,W代表电场力对电荷做的功,q代表单位正电荷。
三、电动势与电极电势的关系电动势和电极电势之间存在着密切的关系。
在理想情况下,电动势等于电极电势之和。
也就是说,电动势E等于正极电势V+和负极电势V-之差。
这个关系可以用以下公式表示:E = V+ - V-这个公式表明了电动势和电极电势之间的直接联系。
电动势可以看作是电池内部化学反应的驱动力,而电极电势则是电池两极之间的电压差。
四、电动势和电极电势在电路中的应用电动势和电极电势在电路中起着至关重要的作用。
电动势可以决定电流的大小和方向,它是电路中电流的驱动力。
电极电势则决定了电路中各个元件之间的电压差,它是电路中电压的来源。
在闭合电路中,电动势源通过电极电势差推动电荷的流动,从而产生电流。
而在开路电路中,电动势和电极电势之间的差别会导致电场力的存在,这个力使电荷在电路中产生电场,但不会导致电流的流动。
电动势和电极电势还可以用于判断电池的正负极。
根据电动势的定义,正极电势大于负极电势时,电流从正极流向负极;反之,电流从负极流向正极。
这个规律被广泛应用于电路设计和电池的连接。
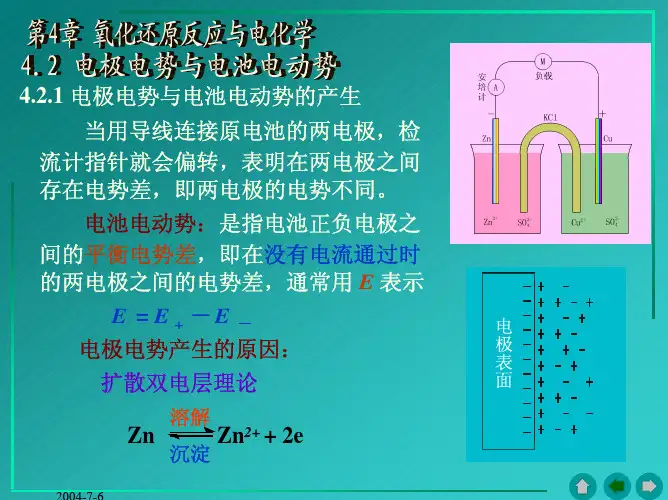
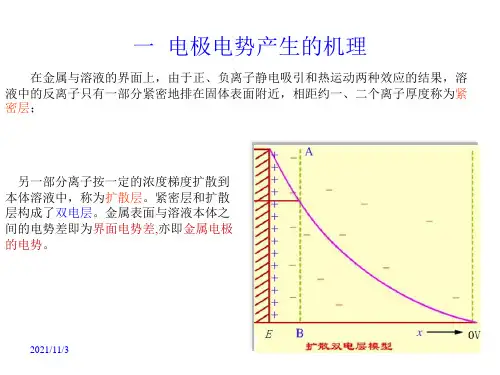



电池电动势产生的机理
锂离子电池中电动势的产生是物理反应最基本的机理,是电池正常运行的重要部分。
锂离子电池的工作原理建立在电势的基础之上,下面就来探讨锂离子电池电动势的产生机理。
锂离子电池中的电势,是指当负极引入外来的电荷的时候,形成电势,这种电势使离子能够在电池壳内作用,引起电荷的交换。
电位的产生主要是由于电池电解质的物理化学反应,以及负极和正极头极间的离子荷载差异造成,所以当前通过负极进入电池时,负极会先消费离子溶液区的离子,此时正极头上的离子负荷量会比负极头极高。
此时,由于离子负荷差异,就会在正极头极和负极头极之间产生一个电位。
另外,电解质也会引起电池电动势的产生,当电解质从正极进入负极时,由于前者是离子,后者是原子,它们之间的电子数量差异,就会在正极和负极之间产生一个电势。
最后,当锂离子电池连接到外部电路后,由于外部电路中集电极节点的势能不等,就会使离子在电池壳内流动,从而产生电势。
总之,锂离子电池电动势的产生机理主要是由电解质的物理化学反应、离子负荷差异和外部电路中电势差异引起。
此外,流动的电荷也会改变电位的大小,从而影响电池的运行。
因此,要提高电池的效率和稳定性,非常重要的一点就是要保持电势的稳定,也就是要控制电解质、离子负荷和外部电路环境。

电极电势与电池电动势的计算解读电极电势和电池电动势是电化学中重要的概念,用于描述电化学反应中的电势变化和电能的转化。
它们的计算和解读对于理解电化学反应的机理和性质具有重要意义。
首先,我们来解释电极电势的概念。
电势是一种能量形式,可以理解为单位电荷在电场中所具有的能量。
在电化学反应中,电极是通过将电子转移给或从溶液或电解质中的离子来参与反应的地方。
电极电势是指电极上电子的能量与电荷相对位置的差异,即电荷从电极内部到电极外部或反之所需的能量。
计算电极电势需要使用标准氢电极(SHE)作为参考电极。
标准氢电极的电势被定义为0V。
其他电极的电势可以通过与标准氢电极进行电位差测量来确定。
根据电极电势的正负差异,可以判断电极是否是氧化还是还原,以及其与参考电极之间的电势差,进而推断电化学反应的方向和性质。
电极电势的计算基于如下公式:E = E° - (RT/nF)lnQ其中,E是电极电势,E°是标准电堆电动势,R是气体常量,T是温度,n是反应物的电子数,F是法拉第常数,Q是反应物的反应物的活度。
通过这个公式,我们可以计算电极电势,并了解电极上电子转移的驱动力。
正值的电极电势表示自发反应,即电子从电极内部向外部移动,这种反应称为还原反应。
负值的电极电势表示非自发反应,电子从外部移动到电极内部,这种反应称为氧化反应。
与电极电势相对应的是电池电动势。
电池电动势是指电化学反应在电池中转化为电能的能力,可以通过连接两个电极并测量它们之间的电势差来测量。
电池电动势的正负差异也可以判断电化学反应的方向和性质。
在电池中,正极(或称为阳极)是发生氧化反应的地方,负极(或称为阴极)是发生还原反应的地方。
电池电动势可以通过将正极电势减去负极电势来计算。
相对于电极电势,电池电动势更加稳定,因为它不受电池中各种电化学反应的影响。
电池电动势的计算基于如下公式:Ecell = Ered - Eox其中,Ecell是电池电动势,Ered是还原反应的电极电势, Eox是氧化反应的电极电势。
电极电势与电池电动势电极电势和电池电动势是电化学中重要的概念,它们贯穿于电学和化学的交叉领域,对于理解电化学反应和电池工作原理具有重要意义。
一、电极电势电极电势是指在电化学反应中,电极与电解质溶液之间的电位差。
电极电势的大小取决于反应物质在电极上的活性和电解质溶液中的离子浓度。
按照惯例,电极电势被定义为标准氢电极与待测电极之间的电位差。
在电池中,一个电极受到氧化反应,被称为氧化电极(或阳极),而另一个电极则进行还原反应,被称为还原电极(或阴极)。
这两个电极之间的电位差即为电极电势。
二、电池电动势电池电动势是指电池在开路状态下的电位差,也可以理解为电池输出电能的能力。
电池中的电荷通过化学反应在电池内部产生电势差,从而驱动电流的流动。
常见的两种电池类型是原电池和电解池。
原电池是一种能将化学能转化为电能的电池,如干电池。
电解池是一种利用外加电源提供能量让非自发反应发生的电池,在这种情况下电动势可以是负值。
三、关系与计算电极电势与电池电动势存在一定的关系。
对于任意一个电池来说,电池电动势等于正极电极电势减去负极电极电势。
也就是说,一个电池的电动势等于其正极电极的电势减去负极电极的电势。
对于某些单质或者物种在标准状态下的电极电势,可以利用标准电极电势表来查找。
标准电极电势表列出了各种物质在标准状态下相对于标准氢电极的电势差。
通过查表,我们可以计算出两个电极的电势差,从而得到电池的电动势。
四、结论与应用电极电势和电池电动势是研究电化学反应和电池性能的重要工具。
了解电极电势和电池电动势可以帮助我们理解电化学反应速率、电流的产生和电池的工作原理。
在实际应用中,电极电势和电池电动势的概念广泛应用于能源领域、锂电池、燃料电池等电化学系统的设计和优化。
通过调节电极材料、电解质浓度等因素,可以改变电极电势和电池电动势,从而提高电池性能和能量转化效率。
综上所述,电极电势和电池电动势是电化学中的重要概念,它们相互关联并共同决定着电池的性能。
高中化学电极电势计算方法与原理化学电势是化学反应发生时产生的电能与电荷之间的关系。
在化学反应中,电子的转移会引起电势的变化,而电极电势则是用来描述这种变化的物理量。
在高中化学学习中,电极电势的计算是一个重要的考点。
本文将介绍电极电势的计算方法与原理,并通过具体的例子来说明。
一、电极电势的计算方法电极电势的计算方法主要有两种:标准电极电势法和Nernst方程法。
1. 标准电极电势法标准电极电势是指在标准状态下,电极与溶液中的氢离子浓度为1mol/L时的电极电势。
标准电极电势可以通过测量电池的电动势来确定。
在标准电极电势法中,电极电势的计算公式为:E°cell = E°cathode - E°anode其中,E°cell为电池的标准电动势,E°cathode为还原电极的标准电极电势,E°anode为氧化电极的标准电极电势。
举例说明:计算以下电池的标准电动势。
Cu(s) | Cu2+(aq, 0.1M) || Ag+(aq, 0.01M) | Ag(s)根据标准电极电势表,Cu2+/Cu的标准电极电势为0.34V,Ag+/Ag的标准电极电势为0.80V。
代入计算公式:E°cell = 0.80V - 0.34V = 0.46V因此,该电池的标准电动势为0.46V。
2. Nernst方程法Nernst方程是用来计算非标准电极电势的方法。
根据Nernst方程,非标准电极电势的计算公式为:Ecell = E°cell - (RT/nF) * ln(Q)其中,Ecell为非标准电极电势,E°cell为标准电极电势,R为理想气体常数,T为温度(单位为开尔文),n为电子转移数,F为法拉第常数,Q为反应物浓度的乘积与生成物浓度的乘积的比值。
举例说明:计算以下电池在25°C下的电动势。
Zn(s) | Zn2+(aq, 0.1M) || Cu2+(aq, 0.01M) | Cu(s)根据标准电极电势表,Zn2+/Zn的标准电极电势为-0.76V,Cu2+/Cu的标准电极电势为0.34V。