确定有机化合物的一般步骤和方法
- 格式:ppt
- 大小:976.00 KB
- 文档页数:46



研究有机化合物的一般步骤和方法①蒸馏、重结晶等分离提纯有机物的实验操作②通过具体实例了解某些物理方法如何确定有机化合物的相对分子质量和分子结构③确定有机化合物实验式、相对分子质量、分子式的有关计算从天然资源中提取有机物成分或者是工业生产、实验室合成的有机化合物不可能直接得到纯净物,因此,必须对所得到的产品进行分离提纯,如果要鉴定和研究未知有机物的结构与性质,必须得到更纯净的有机物。
1(1)分离、提纯(蒸馏、重结晶、升华、色谱分离);(2)元素分析(元素定性分析、元素定量分析)──确定实验式;(3)相对分子质量的测定(质谱法)──确定分子式;(4)分子结构的鉴定(化学法、物理法)。
2一、分离、提纯1.蒸馏蒸馏是分离、提纯液态有机物的常用方法。
当液态有机物含有少量杂质,而且该有机物热稳定性较强,与杂质的沸点相差较大时(一般约大于30ºC),就可以用蒸馏法提纯此液态有机物。
定义:利用混合液体或液-固体系中各组分沸点不同,使低沸点组分蒸发,再冷凝以分离整个组分的操作过程。
要求:含少量杂质,该有机物具有热稳定性,且与杂质沸点相差较大(大于30℃)。
所用仪器:铁架台(铁圈、铁夹)、酒精灯、石棉网、蒸馏烧瓶、温度计、冷凝管、接受器等。
如图所示:特别注意:冷凝管的冷凝水是从下口进上口出。
蒸馏的注意事项1、注意仪器组装的顺序:“先下后上,由左至右”;2、不得直接加热蒸馏烧瓶,需垫石棉网;3、蒸馏烧瓶盛装的液体,最多不超过容积的1/3;不得将全部溶液蒸干;4、需使用沸石(防止暴沸);5、冷凝水水流方向应与蒸汽流方向相反(逆流:下进上出);6、温度计水银球位置应与蒸馏烧瓶支管口齐平,以测量馏出蒸气的温度;2.重结晶定义:重结晶是使固体物质从溶液中以晶体状态析出的过程,是提纯、分离固体物质的重要方法之一。
重结晶常见的类型(1)冷却法:将热的饱和溶液慢慢冷却后析出晶体,此法适合于溶解度随温度变化较大的溶液。
(2)蒸发法:此法适合于溶解度随温度变化不大的溶液,如粗盐的提纯。
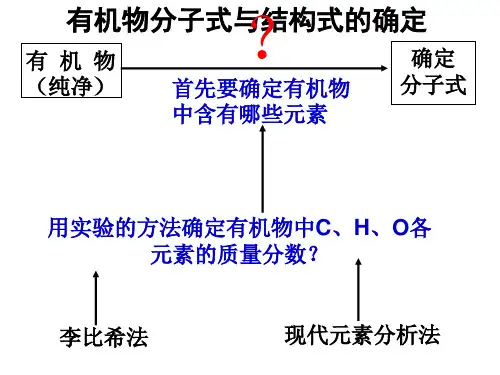

研究有机化合物的一般步骤和方法用第一步是确定问题。
在研究有机化合物之前,需要明确研究的目标和问题。
这可能是合成其中一种化合物,研究其化学性质或探索其应用等。
第二步是实验设计。
基于确定的问题,研究者需要设计实验方案。
这包括选择适当的合成方法、合成试剂和条件,以及确定适当的分析方法。
第三步是合成。
根据实验设计,研究者将开始合成目标化合物。
有机合成可以采用多种方法,如传统的有机合成反应、催化反应等。
在合成中需要考虑合成路线的选择、反应条件的优化等。
第四步是分离和纯化。
合成后的产物中通常会存在未反应试剂和副产物等杂质。
因此,需要对产物进行分离和纯化。
分离可以采用物理方法,如萃取、析出、晶体化等。
纯化则可以采用重结晶、柱色谱、高效液相色谱等分离技术。
第五步是表征。
对于合成后的纯化产物,需要对其进行表征。
这包括确定物质的外观、熔点、沸点、密度等物理性质,以及测定其元素成分、功能团等化学性质。
第六步是谱图分析。
对于有机化合物的结构确定,谱图分析是非常重要的。
常用的谱图包括核磁共振谱(NMR)、红外光谱(IR)、质谱(MS)等。
这些谱图可以提供有机分子的结构信息。
最后一步是结构确定。
基于前面的实验结果和谱图分析,研究者可以准确确定化合物的结构。
这通常包括通过利用谱图数据的结构解析软件进行计算预测,与数据库对比进行验证等手段。
除了上述步骤和方法外,研究中还需要注意实验过程中的安全操作,确保实验的可重复性和结果的可靠性。
此外,如果合成的目标化合物具有潜在的应用价值,还需要进行相关的应用评价和实验验证。
总之,研究有机化合物的一般步骤和方法涉及到确定问题、实验设计、合成、分离和纯化、表征、谱图分析以及结构确定等多个方面。
通过系统的实验和分析,可以准确确定有机化合物的结构,并进一步开展相关的性质和应用研究。





1.2 研究有机化合物的一般方法基本步骤:分离和提纯→元素定量分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式一、分离和提纯1、蒸馏:利用有机物与杂质沸点的差异(一般温度差大于30℃),将有机物以蒸汽的形式蒸出,然后冷凝得到产品(1)适用条件:①分离提纯互溶的液体混合物,也可用于分离液体和可溶性固体②被提纯的有机物的稳定性较强③有机物与杂质的沸点相差较大(一般大于30℃)(2)仪器:铁架台、酒精灯、温度计、蒸馏烧瓶、冷凝管、尾接管、锥形瓶、石棉网(3)装置:(4)注意事项:①蒸馏烧瓶中所盛液体体积:1/3≤V≤2/3②蒸馏烧瓶加热时要垫上石棉网③蒸馏烧瓶中加入沸石,防止暴沸④温度计的水银球应位于蒸馏烧瓶的支管口处⑤冷水从下口进,上口出⑥检查装置气密性:用酒精灯对蒸馏烧瓶微热,伸入到水槽的牛角管有连续均匀的气泡冒出,且停止加热后,牛角管口形成一段水柱,说明不漏气⑦操作顺序:实验前:先通水,再加热;实验后:先停止加热,再停水2、萃取:(1)分类:①液液萃取:利用待分离组分在两种不互溶的溶剂中的溶解性不同,将其从一种溶剂转移到另一种溶剂的过程。
②固液萃取:用溶剂从固体物质中溶解出待分离组分的过程。
例:用水浸取甜菜中的糖类;用酒精浸取黄豆中的豆油以提高产量(2)萃取剂:萃取用的溶剂称为萃取剂。
萃取剂的选择原则:①萃取剂与原溶剂互不相溶,且密度相差较大,易于静置分层②萃取剂与原溶剂、原溶质均不发生反应③被萃取物质在萃取剂中的的溶解度要比在原溶剂中的溶解度大得多常见与水互不相溶的有机溶剂:乙醚、石油醚、二氯甲烷、苯(密度小于水)、四氯化碳(密度大于水)3、分液:把两种互不相溶的液体分开的操作(1)仪器:分液漏斗(2)步骤:验漏→装液→振荡(排气)→静置分层→分液(上上,下下)(3)注意事项:①通过打开其上方的玻璃塞和下方的活塞可将两层液体分离②下层液体从下口放出,上层液体从上口倒出③萃取和分液是两个不同的概念,分液可以单独进行,但萃取之后一定要进行分液④萃取或分液之前必须检查分液漏斗是否漏液。

研究有机化合物的一般步骤和方法1.化合物合成:有机化合物的合成是研究有机化合物的首要步骤。
化合物的合成通常基于已有的化合物合成路线,也可以根据需要进行新的合成路径的设计。
常用的有机合成方法包括:催化反应、导向合成、环化反应、加成反应、氧化还原反应等。
2. 结构鉴定:鉴定有机化合物的结构是研究有机化合物的重要环节。
常用的结构鉴定方法包括:核磁共振波谱(NMR)、红外光谱(FT-IR)、质谱(MS)、紫外可见光谱(UV-Vis)等。
这些技术可以提供有关分子中原子连接方式和官能团的信息。
3.形态表征:除了结构鉴定外,有机化合物的形态表征也是研究的重要内容。
常用的表征方法包括:X射线衍射(XRD)、扫描电子显微镜(SEM)、透射电子显微镜(TEM)、原子力显微镜(AFM)等。
这些手段可以提供关于化合物的晶体结构、形貌和尺寸信息。
4. 性质研究:有机化合物的研究还包括对其性质的研究。
例如,热稳定性、溶解性、热导率、光学性质等。
这些性质的研究通常通过热重分析、差示扫描量热法(DSC)、循环伏安法(CV)、紫外可见光谱(UV-Vis)等方法来完成。
5.反应机理研究:了解有机化合物的反应机理对于研究其应用有重要意义。
反应机理研究通常通过实验和计算化学手段来实现。
实验方法包括动力学研究、反应中间体的生成和检测等。
计算化学方法包括分子轨道理论、密度泛函理论等。
综上所述,研究有机化合物的一般步骤和方法包括合成化合物、结构鉴定、形态表征、性质研究和反应机理研究。
这些方法的选用根据研究目的和化合物的特性而定,综合运用这些方法可以为有机化合物的研究提供全面的信息。