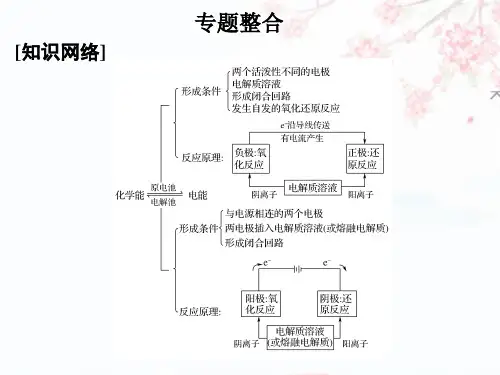
化学专题五《电化学问题研究》(苏教版选修6)PPT课件
- 格式:ppt
- 大小:3.22 MB
- 文档页数:65







课题2 电解与电镀一、判断电解过程中的电极产物判断电解过程中电极产物的依据是:电极材料和离子放电顺序。
阴离子失去电子和阳离子得到电子的过程叫放电。
放电顺序取决于离子本身的性质,也与离子浓度及电极材料有关。
电解时所使用的电极分为两类:一类为惰性电极,只起导体的作用(如铂、石墨等),并不参与反应;另一类为活性电极(除铂、金以及在电解时很易钝化的铅、铬以外的金属),活性电极若作阴极,只起导体的作用;若为阳极,发生氧化反应的往往是电极本身。
电极上物质的变化情况以及电子的转移情况用电极反应式来表明。
当电解质溶液中存在多种阳离子或者多种阴离子时,电解质溶液中各种离子在两极上得失电子是有一定顺序的,称之为放电顺序。
放电顺序涉及多种因素,在中学阶段只要求掌握:阳极——①若为惰性电极,则阴离子放电(失电子,发生氧化反应),放电顺序为: S 2->I ->Br ->Cl ->OH ->含氧酸根离子>F -②若为活性电极,则电极本身失去电子而放电,电极溶解。
因为活性电极的还原性几乎大于一切的阴离子。
阴极——无论是惰性电极,还是活性电极,阴极总是受到保护,不会参与电极反应,始终为阳离子放电(得电子,发生还原反应),放电顺序为:Ag +>Hg 2+>Fe 3+>Cu 2+>H +(酸)>Pb 2+>Sn 2+>Fe 2+>Zn 2+>H +(H 2O)>Al 3+>Mg 2+>Na +>Ca 2+>K +因此,判断电解过程中电极产物的步骤可以概括为:①分析电解质溶液的组成,找全离子(包括水电离出的H +及OH -)并分为阴、阳两组;②分析离子的放电顺序;③确定电极,写出电极反应式。
【例1】某同学按下图所示的装置进行电解实验。
下列说法正确的是( )A .电解过程中,铜电极上不会有H 2产生B .电解初期,主反应方程式为Cu +H 2SO 4=====通电CuSO 4+H 2↑ C .电解一定时间后,石墨电极上不会有铜析出D .整个电解过程中,H +的浓度不断增大解析:从装置图可以看出铜接电源正极作阳极,石墨作阴极,应在阴极区产生H 2,且H +浓度应逐渐减小,故A 、D 错。