实验-锂离子电池电极制备
- 格式:docx
- 大小:903.74 KB
- 文档页数:3

锂离子电池的制作流程1.负极材料的制备:2.正极材料的制备:锂离子电池的正极材料有多种选择,常见的有锂铁磷酸盐(LiFePO4)和三元材料(如锰酸锂、钴酸锂和镍酸锂的复合物)。
正极材料的制备通常采用固态反应或湿法合成。
然后,将正极材料与导电剂和粘结剂混合,并添加适量的溶剂,制成正极材料浆料。
3.电解液的制备:电解液是锂离子电池中起电导和传递锂离子作用的重要组成部分。
一般采用有机溶剂和锂盐混合制备电解液。
有机溶剂通常是碳酸酯、环状碳酸酯或甘醇醚等。
锂盐主要有氟化锂、磷酸锂或六氟磷酸锂等。
制备电解液时需要注意溶剂和锂盐的纯度和配比,以及获得高电导率的条件。
4.卷绕和层叠:卷绕和层叠是组装锂离子电池的关键步骤。
首先,在电解液中混合正负极材料与导电剂的浆料,制备正负极片。
然后,将正负极片和隔膜交替层叠在一起,形成电池芯。
层叠过程中需要注意电极片之间的对齐和紧密贴合,以及避免正负极短路。
5.紧凑和封装:将层叠好的电池芯放在压力机中,经过一定的压力和温度下进行紧凑处理。
这一步骤有助于提高电池芯的紧凑度和一致性。
然后,将电池芯封装在铝塑复合膜或铝箔袋中,并进行密封。
封装过程中需要注意避免氧气和水分的进入,以提高电池的安全性和稳定性。
6.电池性能测试和整理:整理是指将制作好的电池按照一定的标准进行测试和分类整理。
主要测试项包括电池容量、内阻、循环寿命、温度特性等。
根据测试结果,将电池按照性能等级进行分类。
以上就是锂离子电池的制作流程。
锂离子电池的制作过程需要严格的操作和控制,以确保电池的性能和安全性。
同时,不同厂商和应用场景可能有所差异,上述流程仅为一般制作流程的概述。

锂离子电池三电极制作
锂离子电池的三电极包括正极、负极和隔膜。
1. 正极:
正极通常由锂化合物(如LiCoO2、LiFePO4等)和导电剂(如碳黑)组成。
首先,将锂化合物和碳黑混合,并在此基础上添加粘合剂(如PVDF),形成均匀的浆料。
然后,将浆料在导电铝箔片上涂布,并在室温下烘干,形成正极片。
2. 负极:
负极主要由石墨材料组成。
首先,将石墨粉末与粘结剂混合,形成糊状浆料。
然后,将浆料涂布在铜箔片上,并进行烘干,形成负极片。
3. 隔膜:
隔膜通常由聚合物材料制成,目的是隔离正极和负极,防止直接接触。
隔膜表面具有微孔结构,以允许锂离子的传输。
制作隔膜的方法包括湿法和干法。
湿法制作隔膜时,聚合物溶液通过浸渍或涂布的方式涂覆在聚乙烯或聚丙烯基质上,然后经过烘干和拉伸等处理。
而干法制备隔膜则是通过将聚合物材料熔融,然后经过拉伸、冷却和固化等工艺制成。
这些正极、负极和隔膜片通过卷绕或层叠等方式组装在一起,并与电解液一起封装在金属壳体或软包装中,制成锂离子电池的三电极结构。

以磷酸亚铁为原料制备锂离子电池的电极材料磷酸亚铁锂的流程如下磷酸亚铁锂作为一种重要的锂离子电池正极材料,具有较高的比容量和较长的循环寿命,被广泛应用于电动汽车和便携式电子设备。
制备磷酸亚铁锂的流程主要包括原料准备、材料研磨、混合反应、煅烧、中和、成品分选等步骤。
首先,原料准备阶段。
制备磷酸亚铁锂的原料主要包括磷酸亚铁和锂源。
磷酸亚铁可以通过磷酸和亚铁盐反应制得。
锂源一般选择采用碳酸锂或氢氧化锂。
这些原料需要经过精细的筛选和测量,以保证纯度和质量的稳定。
其次,材料研磨阶段。
原料在粉体研磨机中进行研磨,以增加材料的比表面积,提高反应速率和均匀度。
研磨过程中要注意研磨时间和研磨介质的选择,以控制研磨粒度和保证产品的质量。
接下来,混合反应阶段。
将研磨好的磷酸亚铁和锂源粉末按一定的比例混合均匀。
混合反应可以通过干法反应或湿法反应进行。
干法反应中,将混合粉末放入煤气化炉中进行高温反应。
湿法反应中,将混合粉末悬浮于溶液中进行反应。
反应过程需要严格控制反应温度、反应时间和反应压力,以确保反应的完全和产物的纯度。
然后,煅烧阶段。
反应完成后,将产物进行高温煅烧,以提高产物的结晶度和电化学性能。
煅烧温度一般在600~800摄氏度之间,时间根据具体情况而定。
煅烧时要注意控制气氛和煅烧速度,避免产生杂质和过度烧结。
之后,中和阶段。
煅烧后的产物需要进行中和处理,去除杂质和调节pH值。
常用的中和剂包括盐酸和硫酸等。
中和过程中要注意对产物的搅拌和加热,并严格控制中和剂的用量和中和时间。
最后,成品分选阶段。
经过中和处理后的产物需要进行过滤、洗涤和干燥,以得到纯净的磷酸亚铁锂成品。
成品分选时要注意控制过滤速度和滤饼的厚度,以及干燥温度和时间,以确保产品的质量和稳定性。
总之,制备磷酸亚铁锂的流程复杂且需要严格的控制条件。
在每个步骤中,都需要注意原料的选择和处理、反应条件的控制、产物的分离和纯化等方面,以确保最终制得的磷酸亚铁锂具有优良的电化学性能。

实验-锂离子电池电极制备背景锂离子电池作为一种高性能的电池,被广泛用于移动电源和电动车等领域。
其中锂离子电池的正负极材料直接影响着电池的性能。
在锂离子电池中,阳极主要由碳材料和锂合金材料制备,而阴极则通常由钴、镍、锰、铁、钒等过渡金属氧化物或氢氧化物制备。
为了提高锂离子电池的性能,研究人员致力于开发新型材料和提高材料的制备工艺。
本实验旨在通过简单的制备方法,教大家如何制备一个锂离子电池电极,同时探究不同制备条件对电极性能的影响。
实验流程实验材料•钴酸锂(LiCoO2)•聚乙二醇(PEG 400)•黄原酸(C3H4O2)•丙二醇(C3H8O2)•纯净水实验步骤1.制备钴酸锂浆料将0.3g的钴酸锂粉末加入50ml的PEG400溶液中,并加入适量的黄原酸及丙二醇,搅拌均匀,加入纯净水调整浓度至10wt%。
2.制备电极片将铝箔切成10mm × 20mm大小的片状,并用砂纸打磨,通过烤箱在120℃下烘烤30分钟,使铝箔表面更加平整。
将刚制备好的钴酸锂浆料均匀涂在铝箔表面,烤箱烘烤制备完整的电极片。
3.测试电极性能将制备好的电极片置于电池板中,并用测试仪器测试其静态电容,并通过循环伏安法测试其循环性能。
实验结果经过实验,我们得到了如下结果:•制备出来的电极表面均匀且平整,厚度约为20 µm。
•循环伏安测试结果显示,制备出的电极片在0-3 V电压范围内能够提供较高的比容量和较好的循环性能。
分析与讨论通过实验结果,我们可以看出,在制备电极过程中,各种材料和条件都对电极性能产生了重要影响。
其中,钴酸锂浆料的配方比例、烤箱的温度和时间等因素都能够影响电极片的均匀性和表面平整度,从而影响电极的比容量和循环性能。
此外,这种制备方法可以适用于制备其他类型的锂离子电池正负极材料。
但需要注意的是,不同材料的制备条件可能有所差别,需要进行适当的调整和优化。
通过本实验,我们顺利制备出了钴酸锂电极片,并测试了其性能。

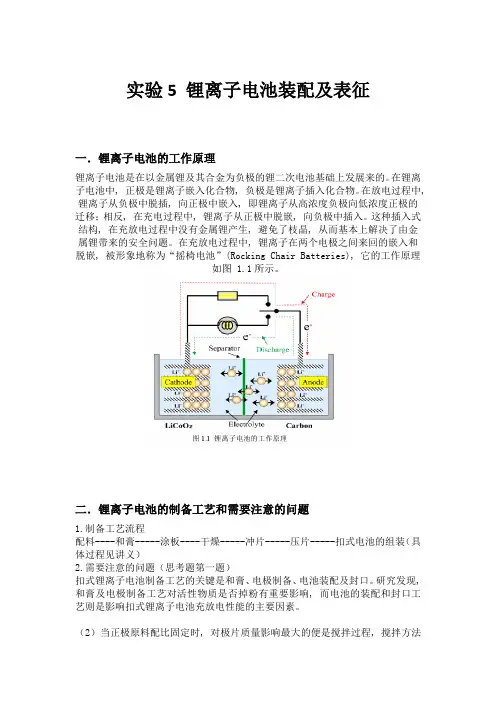
实验5 锂离子电池装配及表征一.锂离子电池的工作原理锂离子电池是在以金属锂及其合金为负极的锂二次电池基础上发展来的。
在锂离子电池中, 正极是锂离子嵌入化合物, 负极是锂离子插入化合物。
在放电过程中, 锂离子从负极中脱插, 向正极中嵌入, 即锂离子从高浓度负极向低浓度正极的迁移;相反, 在充电过程中, 锂离子从正极中脱嵌, 向负极中插入。
这种插入式结构, 在充放电过程中没有金属锂产生, 避免了枝晶, 从而基本上解决了由金属锂带来的安全问题。
在充放电过程中, 锂离子在两个电极之间来回的嵌入和脱嵌, 被形象地称为“摇椅电池”(Rocking Chair Batteries), 它的工作原理如图 1.1所示。
二.锂离子电池的制备工艺和需要注意的问题1.制备工艺流程配料----和膏-----涂板----干燥-----冲片-----压片-----扣式电池的组装(具体过程见讲义)2.需要注意的问题(思考题第一题)扣式锂离子电池制备工艺的关键是和膏、电极制备、电池装配及封口。
研究发现, 和膏及电极制备工艺对活性物质是否掉粉有重要影响, 而电池的装配和封口工艺则是影响扣式锂离子电池充放电性能的主要因素。
(2)当正极原料配比固定时, 对极片质量影响最大的便是搅拌过程, 搅拌方法选择不好将会导致极片的导电性降低和极片掉粉, 极片掉粉将会直接影响电池容量等。
搅拌方式有超声波搅拌、磁力搅拌、强力搅拌以及手工研磨。
经研究发现采用强力搅拌和超声波搅拌得到的极片质量最好, 而在本实验中我们使用的搅拌效果最差的手工研磨, 这很难得到好的结果。
所以在和膏时要注意搅拌方式的选择。
(3)干燥温度和时间选择不适也会导致极片掉粉, 干燥的目的是为了除去膏体中大量的溶剂NMP 以及在配膏过程中吸收到的水分, 温度和时间都应选择合适。
压片时压力要选择适中, 压片的目的主要有两个: 一是为了消除毛刺, 使极片表面光滑、平整, 防止装配电池时毛刺穿透隔膜引起短路; 二是增强膏和集流体的强度, 减小欧姆电阻。

实验一:锂离子电池制备及性能测试实验学时:6实验类型:综合实验要求:必修一、实验目的(1)了解锂离子二次电池的工作原理;(2)了解电解质溶液的导电机理和锂离子电池电极材料的合成方法;(3)掌握扣式锂离子电池电极的制备工艺及电池的装配过程;(4)掌握锂离子电池电性能测试方法。
二、实验内容扣式锂离子电池电极的制备工艺及电池的装配过程和扣式锂离子电池电化学性能测试。
三、实验原理、方法和手段液态锂离子二次电池通常采用层状复合氧化物为正极,人造石墨或者天然石墨为负极,充放电过程中通过锂离子的移动实现。
以商品化的液态电解质锂离子电池为例,如下图1- 1,正极材料和负极材料分别为LiFePO4和石墨,以LiPF6- EC-DEC为电解液,其电池工作原理如下:锂离子电池实质上是一种锂离子浓差电池,正负电极由两种不同的锂离子嵌入化合物组成。
正极材料是一种嵌锂式化合物,在外界电场作用下化合物中的Li 从晶体中脱出和嵌入。
当电池充电时,Li+离子从正极嵌锂化合物中脱出,经过电解质溶液嵌入负极化合物晶格中,正极活性物处于贫锂状态;电池放电时,Li+则从负极化合物中脱出,经过电解质溶液再嵌入正极化合物中,正极活性物为富锂状态。
为保持电荷平衡,充放电过程中应有相同数量的电子经外电路传递,与Li+一起在正、负极之间来回迁移,使正、负极发生相应的氧化还原反应,保持一定的电位。
工作电位与构成正、负极的可嵌锂化合物的化学性质、Li+离子浓度等有关。
在正常充放电过程中,负极材料的化学结构不变。
因此,从充放电反应的可逆性看,锂离子电池反应是一种理想的可逆反应。
锂离子电池在工作电位与构成电极的插入化合物的化学性质、Li+的浓度有关。
充电:LiFePO4 - xLi+ - xe- →xFePO4 + (1-x)LiFePO4放电:FePO4 + xLi+ + xe- →xLiFePO4 + (1-x)FePO4图1- 1. 锂离子电池工作原理,LiFePO4为正极,石墨为负极.研究表明,Li+的脱嵌过程是一个两相反应,存在着LiFePO4和FePO4两相的转化,充电时,铁离子从FeO6层面间迁移出来,经过电解液进入负极,发生Fe2+→Fe3+的氧化反应,为保持电荷平衡,电子从外电路到达负极。

锂离子电池工艺流程1.步骤一:正负电极材料的制备锂离子电池正负电极的制备是整个工艺流程的第一步。
正极材料一般采用氧化物,如氧化钴、氧化镁等,通过混合、磨碎、干燥等工艺制备成片状电极材料。
负极材料则主要是石墨,通过混合、浆料的制备,涂布在铜箔上制备成片状电极材料。
2.步骤二:电极的装配正负电极分别涂覆在铜箔和铝箔上,并通过辊压等工艺将电极材料均匀地涂覆在箔上,形成电极片。
电极片一般需要经过烘干、压实等工艺处理,以提高电极的密度和稳定性。
3.步骤三:电解液的制备电解液是锂离子电池的重要组成部分,一般由电解质、溶剂和添加剂等组成。
电解质常采用锂盐,如六氟磷酸锂、四氟硼酸锂等,溶剂则多为有机溶剂,如碳酸酯类、醚类等。
添加剂用于调节电解液的性能,提高电池的循环寿命和安全性。
4.步骤四:电池的组装电池的组装是将正负电极片以及电解液进行封装,形成完整的电池单体。
一般电池的正负电极片间隔一定的距离,形成正负极与电解质的电池结构。
电池的组装过程一般包括正负极的叠层,电解液的注入和封装等步骤。
5.步骤五:电池的充放电测试组装完成的电池需要进行充放电测试以验证其电池性能。
充放电测试过程中,需要对电池进行循环充放电,并测试其电压、容量、内阻等参数。
测试结果可以评估电池的性能,例如容量、循环寿命和能量密度等。
6.步骤六:电池的封装电池封装是将测试合格的电池进行进一步封装,以保护电池结构,提高其安全性。
电池封装通常将电池单体与保护电路板、外壳等组装在一起,形成成品电池。
电池封装还需要进行温度、湿度等环境适应性测试,以确保电池在各种使用环境中的可靠性和稳定性。
以上是锂离子电池的工艺流程,其中涵盖了正负电极材料的制备、电极的装配、电解液的制备、电池的组装、电池的充放电测试和电池的封装等关键步骤。
整个工艺流程对于保证锂离子电池的性能和可靠性至关重要。

锂电材料观察实验报告实验目的:比较不同锂电材料的性能差异,并观察其在实验条件下的变化情况。
实验所用材料及仪器:1. 锂离子电池正极材料:锂钴酸锂(LiCoO2)、锂铁磷酸锂(LiFePO4)、锂锰酸锂(LiMn2O4)2. 锂离子电池负极材料:石墨3. 锂离子电解液:锂盐溶液4. 电池外壳5. 外部电源和电压表6. 扫描电子显微镜(SEM)、透射电子显微镜(TEM)等观察仪器实验步骤:1. 制备三个锂电池的正极:将锂钴酸锂、锂铁磷酸锂和锂锰酸锂分别与导电剂和粘结剂混合,并涂覆在导电片上,然后通过烘干固化。
2. 制备三个锂电池的负极:将石墨与导电剂和粘结剂混合,并涂覆在导电片上,然后通过烘干固化。
3. 将正极和负极叠放在一起,并以适当的间隔密封在电池外壳中,形成电池单元。
4. 在实验条件下连接外部电源和电压表,测量电池的电压。
5. 使用扫描电子显微镜(SEM)和透射电子显微镜(TEM)观察锂电池材料的微观结构。
6. 在一定周期内重复第4和第5步骤,观察电池的电压变化和材料结构的演变。
实验结果及分析:根据实验观察,以下是对不同锂电材料性能的比较和分析:1. 锂钴酸锂(LiCoO2):此材料具有较高的充电电压和能量密度,但同时也存在较高的成本、不稳定性和安全性问题。
2. 锂铁磷酸锂(LiFePO4):与锂钴酸锂相比,此材料具有较低的成本、较高的稳定性和安全性。
然而,由于其较低的电导率和较低的放电电压,其能量密度相对较低。
3. 锂锰酸锂(LiMn2O4):此材料在成本和安全性方面都具有优势,但相对于锂钴酸锂和锂铁磷酸锂,其电导率和循环寿命较低。
根据SEM和TEM观察,我们还可以更详细地了解不同锂电材料的微观结构和变化情况。
例如,锂钴酸锂通常呈现出颗粒状结构,而锂铁磷酸锂和锂锰酸锂的结构则更为均匀和紧密。
结论:根据本实验的观察和分析,不同的锂电材料具有不同的性能和特点。
选择合适的锂电材料应考虑成本、能量密度、安全性和循环寿命等方面因素的权衡。

先进锂离子电池材料合成与测试实验报告一、实践目的1、了解并掌握锂离子电池负极材料TiO2的制备及检测方法;2、掌握水热法合成材料的特点和操作方法,并对半纽扣电池的制备流程有初步的认识和实践;3、学习掌握各种仪器的操作及文献资料的调研查阅。
二、实验背景1、溶剂热法的原理及特点溶剂热法是以有机溶剂为反应介质,然后通过反应釜创造一个密闭、高压的反应环境使难溶或者不溶的物质溶解并且重结晶的一种液相反应法。
该方法是水热法的发展,它与水热法的不同之处在于所使用的溶剂为有机溶剂而不是水。
在溶剂热反应中,通过把一种或几种前驱体溶解在非水溶剂,在液相或超临界条件下,反应物分散在溶液中并且变得比较活泼,反应发生,产物缓慢生成。
该过程相对简单而且易于控制,并且在密闭体系中可以有效的防止有毒物质的挥发和制备对空气敏感的前驱体。
物相的形成、粒径的大小、形态也能够控制,而且产物的分散性较好。
在溶剂热条件下,溶剂的性质(密度、粘度、分散作用)相互影响,变化很大,且其性质与通常条件下相差很大,相应的反应物(通常是固体)的溶解、分散性及化学反应活性大大的提高或增强。
这就使得反应能够在较低的温度下发生。
2、TiO2的研究背景二氧化钛是多结晶型结构,自然界中有锐钛矿、金红石和板钛矿三种结构,前面两种都是四方晶系,后者为斜方晶系,板钛矿和锐钛矿可以在700T以上转化为金红石结构,金红石结构是一种热力学稳定相,然而锐钛矿具有较小的表面能,使得纳米量级的锐钛矿结构的TiO2稳定性更高。
图LTiO2的晶型结构(a)金红石结构(b)锐钛矿结构(c)板钛矿结构由于二氧化钛具有开放的晶体结构和钛离子灵活的电子结构,因此可以接受外来电子,并为外来阳离子提供空位,为了保持电中性,电子会伴随着锂离子共同嵌入二氧化钛的晶体结构中。
TiO2中嵌锂反应表达式:xLi++TiO2+xe-=Li x TiO2.随着锂离子的嵌入,TiO2从四方结构的贫锂相转化为正交结构的富锂相,理论容量可以达到330mAh/g,然而实际容量是理论容量的1/2,当嵌锂系数大于0.5后,TiO2结构中的额Li・Li存在相互作用,阻碍了锂离子的进一步嵌入。

实验二 锂离子电池的制备合成及性能测定一.实验目的1.熟悉锂离子电极材料的制备方法,掌握锂离子电极材料工艺路线;2.掌握锂离子电池组装的基本方法;3.掌握锂离子电极材料相关性能的测定方法及原理;4.熟悉相关性能测试结果的分析。
二.实验原理锂离子电池的结构与工作原理:所谓锂离子电池是指分别用二个能可逆地嵌入与脱嵌锂离子的化合物作为正负极构成的二次电池。
人们将这种靠锂离子在正负极之间的转移来完成电池充放电工作的,独特机理的锂离子电池形象地称为“摇椅式电池”,俗称“锂电”。
以LiCoO 2为例:⑴电池充电时,锂离子从正极中脱嵌,在负极中嵌入,放电时反之。
这就需要一个电极在组装前处于嵌锂状态,一般选择相对锂而言电位大于3V 且在空气中稳定的嵌锂过渡金属氧化物做正极,如LiCoO 2、LiNiO 2、LiMn 2O 4、LiFePO 4。
⑵为负极的材料则选择电位尽可能接近锂电位的可嵌入锂化合物,如各种碳材料包括天然石墨、合成石墨、碳纤维、中间相小球碳素等和金属氧化物,包括SnO 、SnO 2、锡复合氧化物SnBxPyOz(x=0.4~0.6,y=0.6~0.4,z=(2+3x +5y)/2)等。
三.实验装置及材料1.实验装置:恒温槽,冰箱,搅拌器,管式电阻炉,真空干燥箱,鼓风干燥箱,铁夹,分液漏斗,研钵,烧杯,pH 试纸,循环水真空泵,漏斗,抽滤瓶,滤纸,玻璃皿,温度计;2.实验材料:乙醇,醋酸镍,醋酸钴,醋酸锰,碳酸钠,去离子水,氨水,乙炔黑,PVDF ,NMP ,LiOH ;四.实验内容及步骤1.样品的制备及准备碳酸盐共沉淀法制备LiNi 1/3Co 1/3Mn 1/3O 2:分别称取摩尔比为1:1:1的醋酸镍(Ni(CH 3COO)2·4H 2O)、醋酸钴 (Co(CH 3COO)2·4H 2O)、醋酸锰 (Mn(CH 3COO)2·4H 2O),用去离子水溶解,溶液金属离子总浓度为1mol ·L -1。
实验⼋锂离⼦电池制备及性能测试实验指导书实验⼀:锂离⼦电池制备及性能测试实验学时:6实验类型:综合实验要求:必修⼀、实验⽬的(1)了解锂离⼦⼆次电池的⼯作原理;(2)了解电解质溶液的导电机理和锂离⼦电池电极材料的合成⽅法;(3)掌握扣式锂离⼦电池电极的制备⼯艺及电池的装配过程;(4)掌握锂离⼦电池电性能测试⽅法。
⼆、实验内容扣式锂离⼦电池电极的制备⼯艺及电池的装配过程和扣式锂离⼦电池电化学性能测试。
三、实验原理、⽅法和⼿段液态锂离⼦⼆次电池通常采⽤层状复合氧化物为正极,⼈造⽯墨或者天然⽯墨为负极,充放电过程中通过锂离⼦的移动实现。
以商品化的液态电解质锂离⼦电池为例,如下图1- 1,正极材料和负极材料分别为LiFePO4和⽯墨,以LiPF6- EC-DEC为电解液,其电池⼯作原理如下:锂离⼦电池实质上是⼀种锂离⼦浓差电池,正负电极由两种不同的锂离⼦嵌⼊化合物组成。
正极材料是⼀种嵌锂式化合物,在外界电场作⽤下化合物中的Li 从晶体中脱出和嵌⼊。
当电池充电时,Li+离⼦从正极嵌锂化合物中脱出,经过电解质溶液嵌⼊负极化合物晶格中,正极活性物处于贫锂状态;电池放电时,Li+则从负极化合物中脱出,经过电解质溶液再嵌⼊正极化合物中,正极活性物为富锂状态。
为保持电荷平衡,充放电过程中应有相同数量的电⼦经外电路传递,与Li+⼀起在正、负极之间来回迁移,使正、负极发⽣相应的氧化还原反应,保持⼀定的电位。
⼯作电位与构成正、负极的可嵌锂化合物的化学性质、Li+离⼦浓度等有关。
在正常充放电过程中,负极材料的化学结构不变。
因此,从充放电反应的可逆性看,锂离⼦电池反应是⼀种理想的可逆反应。
锂离⼦电池在⼯作电位与构成电极的插⼊化合物的化学性质、Li+的浓度有关。
充电:LiFePO4 - xLi+ - xe- →xFePO4 + (1-x)LiFePO4放电:FePO4 + xLi+ + xe- →xLiFePO4 + (1-x)FePO4图1- 1. 锂离⼦电池⼯作原理,LiFePO4为正极,⽯墨为负极.研究表明,Li+的脱嵌过程是⼀个两相反应,存在着LiFePO4和FePO4两相的转化,充电时,铁离⼦从FeO6层⾯间迁移出来,经过电解液进⼊负极,发⽣Fe2+→Fe3+的氧化反应,为保持电荷平衡,电⼦从外电路到达负极。
第一部分:干法电极技术层面深度解析一、干法电极制备技术解析1、干法与湿法的工艺介绍及材料对比传统湿法工艺是将活性物、导电剂、粘接剂按比例混合在溶剂中,并通过狭缝涂布模头按要求涂覆在集流体表面并辊压。
干法工艺是将活性颗粒、导电剂和进行干混均匀后加入粘接剂,在粘接剂原纤化作用下形成自支撑膜,最后辊压覆盖在集流体表面。
2、干法制膜工艺介绍2.1、自支撑膜干法制备工艺干法制膜包括:粘接剂原纤化法和静电喷涂法,其中粘接剂原纤化是主流。
静电喷涂法在后续的可加工性、粘连稳固性、电极柔韧和耐久上表现不如粘接剂原纤化法。
2019年特斯拉收购Maxwell公司,Maxwell主要采用粘接剂原纤化制膜,而特斯拉目前也是采用粘接剂原纤化法制造自支撑膜。
Maxwell在粘接剂原纤化方案上具有专利的领先优势。
美国和日本分别是粘接剂原纤化法和静电喷涂法工艺的领先国家,其中,Maxwell和Toyota各是两种工艺的代表公司。
粘接剂原纤化法是将活性物质粉末与导电剂混合后加入PTFE粘接剂,然后对干混合物施加外部的高剪切力,使PTFE原纤化后粘合电极膜粉末,最终挤压混合物形成自支撑膜。
静电喷涂法是用高压气体预混活性物质、导电剂以及粘接剂颗粒,在静电喷枪的作用下使粉末带负电荷并喷至带有正电荷的金属箔集流体上,然后对载有粘接剂的集流体进行热压,粘接剂融化后会粘连其他粉末并被挤压成自支撑膜。
2.2、原纤化干法工艺技术原理原纤化是在外部剪切力作用下,PTFE变成原纤维的过程。
由于PTFE 范德华力较低,堆积松散,在外部剪切力的作用下会从团聚物变成原纤维,原纤维呈网状粘合电极粉末。
温度、剪切是影响PTFE原纤化的重要因素。
当温度高于19度,PTFE会从三斜晶系转变为六方晶系,分子链会变软,也是形成原纤维的主要原因。
原纤化制膜是极片辊压的前段环节,主流的原纤化制膜机器为:1)气流粉碎机;2)螺杆挤出机;3)开炼机。
在PTFE与活性物质充分混合后,混合物被送入原纤化制膜机,在机器的辊压下混合物会形成自支撑膜。
锂离子电池制备工艺流程
锂离子电池是一种高能量密度、长寿命的电池,广泛应用于移动电力、储能设备、电动工具等领域。
其制备工艺流程主要包括以下几个步骤:
1.正负极材料制备:锂离子电池的正负极材料分别为锂离子富集材料和石墨材料。
制备方法主要包括固态反应、溶剂热法和物理混合等。
2.悬浮液制备:将正负极材料粉末与导电剂、粘合剂、溶剂等混合,在高速分散器中搅拌分散,得到均质的悬浮液。
3.涂布:将悬浮液涂覆到铝箔或铜箔上,形成正负极电极,再在电极表面覆盖一层聚烯烃过滤膜,以防止内部污染。
4.电池组装:在电解液中完全浸泡正负极电极,以建立起离子传输通道,将正负极叠放或卷绕起来,放入电池壳中。
5.密封充电:通过与电极相连的正负极端子,对电池进行密封充电,使电解液中的锂离子逆向迁移,从而形成电池电势。
6.电池测试:通过电容、电阻、电化学等测试手段,检测电池的性能指标如容量、循环寿命、内阻、安全性等。
以上是锂离子电池的制备流程,工艺的精细度和质量控制是确保电池性能及安全的关键。
同时,实现材料开发、制备技术及封装工艺等方面的创新,将有助于提高锂离子电池的性能和应用范围。
锂离子电池电极材料的制备和表征方法锂离子电池是一种重要的可再生能源储存技术,在移动设备、电动汽车、以及对环境敏感的应用领域中得到广泛应用。
而锂离子电池的性能则主要取决于电极材料。
电极材料的制备和表征方法对于改善锂离子电池的性能具有重要意义。
电极材料的制备方法:1、化学合成法化学合成方法是电极材料的重要制备方法之一。
它利用溶液中的化学前体在合成操作过程中聚合形成电极材料,常用的方法有溶胶凝胶法、水热法和共沉淀法。
例如通过溶胶-凝胶法可制备出磷酸铁锂,步骤包括:溶胶浸渍法形成氧化物前体,凝胶化处理,煅烧至相应锂化合物。
2、机械法机械法制备电极材料是利用机械研磨的强机械力将粉末制备成电极材料的方法。
常见的有球磨法、离心磨法和高能球磨法。
例如通过球磨法可制备出锰氧化物材料,步骤包括:将锰氧化物粉末和钴粉末齐放到球磨罐中,加自制钛丝球进行球磨,然后采用液相反应方法形成锂离子电极材料。
3、物理浸渍法物理浸渍法是将溶液中的化学前体浸泡在电极材料表面,经过反应后获得电极材料的方法,常见的有电化学沉积法和热分解法。
例如通过电化学沉积法可制备出氧化镁锂,步骤包括:在电极上不断重复施加潜在的方法下,通过界面反应在电极上沉积氧化镁锂材料。
电极材料的表征方法:1、扫描电子显微镜扫描电子显微镜(SEM)是常用的表征电极材料的方法之一,它可以观察到电极材料的横截面和纵向面,获得其表面形貌、粒径大小和微观结构等信息。
2、热重分析热重分析(TGA)是通过连续升温的方式,测量电极材料的重量变化,获取电极材料热稳定性和热解过程的信息。
3、X射线衍射X射线衍射(XRD)是通过测量电极材料制备后的晶体结构和晶面之间的间距,来确认电极材料的晶体结构、晶格参数和材料重要参量等信息。
4、电化学测试电化学测试是评估锂离子电池性能的核心测试方法,可以测得电池的工作电压、比容量、循环寿命等数据,了解电极材料的储象性能和循环稳定性。
例如通过循环伏安法可测得电极材料的静电电容以及充放电曲线,进而评估电极材料的储存能力和循环寿命。
实验1.3 锂离子电池电极制备
一. 实验目的
1.了解锂离子电池电极的构成
2.了解锂离子电池电极的充放电机理
3.掌握锂离子电池电极制备的关键技术
二. 实验原理
锂离子电池是指正负极为Li+嵌入化合物的二次电池。
正极通常采用过渡金属氧化物Li CoO2、LiNiO2、LiMn2O4或LiFePO4等高氧化还原电势的材料,负极采用石墨、碳、或者Li4Ti5O12、LiTi2(PO4)3等氧化还原电势较低的材料。
电解质为可分为有机电解质和水相电解质两类,有机电解质以LiPF6、LiAsF6或LiClO4等锂盐,混合碳酸酯作为溶剂;水相以硫酸锂、硝酸锂、LiOH溶液作为电解质。
充放电过程中,Li+在正负极之间往返嵌入或脱出,被形象地称为“摇椅式”(rock chair)电池。
实际上,电化学活性材料通常因为导电性差,需要添加石墨导电剂,与其混合,并以聚合物分子作为粘合剂,将活性物质、导电剂均匀混合涂布成薄膜,作为锂离子电池的电极片。
以西门子的电池电极片制备工序为例,介绍电极片的制备流程。
混涂压干切
图1.4.1西门子锂离子电池电极制备工艺示意图
1.混料
将负极材料(碳为主)与导电剂和粘结剂,加极性溶剂经混料机混合成均一的浆料。
目标最大可能分散,注意无活性物质溶解或结构破坏。
正极材料以过渡金属锂氧化
物为活性物质。
2.涂布
正极:铝箔;负极:铜箔。
涂布厚度达到150-300微米,注意厚度偏差1-2微米以
内。
3.压片
在干燥流水线上逐步升温至150℃干燥除去溶剂,减少压片过程中产生的气泡,避免极片产生裂缝。
4.干燥
可在真空干燥箱中进一步干燥除去极片中的水分,达到水分低于0.5%.
5.切片
通过高精度切割技术,有时采用激光切割达到高精度尺寸;避免产生毛刺、碎屑。
图1.4.2电极片制备流程图
三.仪器设备
鼓风干燥箱、真空干燥箱、超声清洗机、电子天平、剪刀、红外灯
四.实验原料
电极材料LiTi
2(PO
4
)
3
、导电剂super P,粘结剂聚偏氟乙烯PVDF,溶剂
NMP, 不锈钢片,玛瑙研钵
五.实验步骤
以得到高导电性的电极片为目的。
1.准备集流片:剪取约3×3 cm2的不锈钢片,依次在去离子水和乙醇中超声波清洗1
0 min,取出50~60 ℃干燥10分钟,并测量质量待用。
2.按质量比80:10:10计算电极活性材料、导电碳黑以及PVDF的质量;
3.称量电极材料进行研磨20分钟;称量导电炭黑、PVDF加到上述电极材料中,继
续研磨30分钟混合;
4.并加少量NMP溶剂作为分散剂,在玛瑙研钵中研磨20分钟调匀,得到黑色墨汁状
混合物。
5.然后在不锈钢片上成膜,
6.将60度下干燥的电极膜在烘箱箱中控温125℃,干燥24小时,
六.注意事项
1.电极片须烘干,不含有机溶剂、水分含量足够低。
2.电极浆料要求能够涂布均匀、平整。
七.实验报告要求
1.实验目的、原理、步骤
2.得到电极片上的活性物质的量:(1)需计算出电极片单位面积上的包含粘合
剂、导电剂和LiTi2(PO4)3的总质量,(2)每片电极片上活性物质LiTi2
(PO4)3的净质量。
3.预估理论容量计算方法:计算出LiTi2(PO4)3的理论充放电容量(每个分子
有2电子可转移,容量以mAh/g表示)。
八.思考题
1.浆料混合、制备电极片有什么需要注意事项?
2.讨论一下研磨混合时添加次序的影响。