芳烃的卤取代反应
- 格式:ppt
- 大小:305.00 KB
- 文档页数:22


本文由恶魔之始贡献 ppt文档可能在WAP端浏览体验不佳。
建议您优先选择TXT,或下载源文件到本机查看。
第三节 定义: 定义: 卤代芳烃 芳烃分子中的一个或几个氢原子被卤原子取代后的化合物称为 卤代芳烃。
卤代芳烃。
分类: 分类: 1.侧链取代的卤代芳烃 1.侧链取代的卤代芳烃 Br 2.芳环上取代的卤代芳烃 2.芳环上取代的卤代芳烃 CH2Cl CH2CH2Cl 一、卤代芳烃的命名 二、卤代芳烃的制法 三、卤代芳烃的物理性质 四、卤代芳烃的化学性质 1.苯环位置对卤原子活泼性的影响 苯环位置对卤原子活泼性的影响 2.芳环上的亲核取代反应 2.芳环上的亲核取代反应 3.芳环上的亲核反应机理 3.芳环上的亲核反应机理 4.与金属作用 . 5. 芳环上的亲电取代反应 一、卤代芳烃的命名 1.卤原子直接与芳环相边连时,以芳烃为母体, 1.卤原子直接与芳环相边连时,以芳烃为母体,卤原子作为取代基 卤原子直接与芳环相边连时 CH3 C2H5 4-氯甲苯 (对氯甲苯) 对氯甲苯) Cl Br Cl 2-氯-4-溴乙苯 2.卤原子与侧链相连时,通常以脂肪烃为母体 卤原子与侧链相连时, 卤原子与侧链相连时 αβ CH=CHBr CHCH2CH2Cl CH3 β-溴代苯乙烯 3-苯基-1-氯丁烷 苯基- 二、卤代芳烃的制法 1.直接卤化法 1.直接卤化法 芳环的直接卤化与芳烃侧链的直接卤化的机理是不同 的。
芳环的直接卤化是通过亲电取代反应,而芳烃侧链 进行的。
的直接卤化是按自由基机理进行的。
由于芳烃侧链的α原子比较活泼,取代反应多发生 由于芳烃侧链的α原子比较活泼, 在α位。
CH3 Cl 2 hv CH2Cl Br2 CH2CH3 CHCH3 Br hv 一般Cl 的活性高于Br 而选择性要小于Br 一般Cl2的活性高于Br2,而选择性要小于Br2。
因此乙苯的溴化得到一种产物; 因此乙苯的溴化得到一种产物;而氯化得到的是 氯代的混合物。


芳烃侧链上的反应教学目标:掌握芳烃侧链上的氧化、卤代等反应教学重点:芳烃侧链α―h原子的氧化及卤代反应教学安排:f10―>g6;30min烷基苯的烷基与苯环相连的碳原子称为α-碳原子,其上的氢称为α-氢。
在分子构造上芳烃侧链的α-氢与烯烃的α-氢相似,受苯环的影响比较活泼。
一、α―氢的卤代反应在光照或加热的条件下,烷基苯的α-h被卤素取代,生成α-卤代烷基苯。
例如:α-h氯代反应机理与烷烃卤代反应机理相同,为自由基型反应:苯基自由基比烷基自由基更稳定,因为苯基自由基的单电子的电子云可以分散到环上:苯氯甲烷可以稳步氯化分解成多卤代产物:其它烷基苯的α―h也能被卤代:溴代反应也可以用n-溴代丁二酰亚胺(nbs)搞溴化试剂,反应缓解,极易掌控:二、α―氢的氧化反应烷基苯比苯难被水解,但通常就是烷基被水解,苯环则比较稳定。
用强氧化剂如kmno4、k2cr2o7、hno3的水解下,或在催化剂的促进作用下,用空气或氧气水解,不含α―h的烷基被水解成羧基,而且不论烷基的碳链长短,通常都分解成苯甲酸。
比如:甲苯的氧化这是因为α-氢原子受到苯环影响比较开朗。
若并无α-氢原子,例如叔烷基苯难于被水解,若猛烈水解时,通常就是苯环被破坏性水解。
用途:工业上催化氧化方法制备苯甲酸、对苯二甲酸、邻苯二甲酸酐和均苯四甲酸二酐等,这些化合物在工业上都有重要用途。
如均苯四甲酸二酐可用作环氧树脂的固化剂以及制造聚酰亚胺树脂等。
异丙苯在碱性条件下,很难被空气氧化分解成氢过氧化异丙苯,后者在稀酸促进作用下,水解为苯酚和丙酮。
这就是生产苯酚的关键工业方法。
其主要优点就是原料价廉养胃,可以已连续化生产,且其交产物丙酮也就是关键的化工原料。
氧化反应是自由基型机理,氢过氧化异丙苯在酸作用下的分解反应主要是正离子的重排机理:同理,间甲基异丙基苯展开水解,再经酸催化水解获得丙酮和间甲酚:三、关键词芳烃,α-氢的水解反应,芳烃α-氢的卤代反应。


3 卤化反应在有机化合物中建立碳-卤键的反应称为卤化反应。
意义:在药物分子中引入卤素可改善其药理活性;卤化物是药物合成重要的中间体,可从卤素进行多种官能团转化;卤素可作为烯烃等官能团的保护基,可提高合成的选择性。
3.1不饱和烃与含卤物种的加成卤化含卤物种主要包括卤素和卤化氢。
3.1.1卤素对不饱和烃的加成反应(1)对烯烃的加成氟与烯烃的加成过于剧烈,产物复杂,实用意义不大;二碘化物对光极为敏感,稳定性差,在药物合成中也不常用。
而氯和溴对烯烃的加成在药物合成上较为重要。
氯和溴对烯烃的加成反应为亲电加成机理,是脂肪族碳碳p键的典型反应之一。
这种加成主要包括两步反应:亲电试剂加成到亲核性的p键上得到一个碳正离子(或环鎓离子);得到的碳正离子(或环鎓离子)与亲核试剂反应。
参与第二步反应的亲核试剂一般是与亲电试剂相关的负离子,比如溴离子、氯离子等,也可以是亲核性的溶剂,如水或乙酸等。
①反应机理碳碳双键上的亲电加成。
②立体化学氯和溴对烯烃的加成反应的立体化学较为复杂, 与底物结构、反应条件和加成物有关。
反式加成:一般情况下,溴对烯烃的亲电加成反应会经过三员环过渡态(中间体),当这种中间体在反应条件下比较稳定时,可发生反式亲电加成。
cis-和trans-2-丁烯的立体专一性反式加成:由于两个溴原子分别从双键的相反方向加成,所以得到立体专一产物。
顺式加成:氯加到双键上有时也可得到顺式加成产物,这类反应一般在非极性溶剂中发生,如茚氯化生成cis-1,2-二氯茚。
有几项因素决定了这个氯化加成的立体化学,其一,反应物是氯而不是溴;其二,底物分子的双键处在芳环的共轭位置;其三,反应在非极性溶剂薪小?lt;/p>氯的原子半径和可极化度都比溴小,因此,形成鎓离子也比溴难;而且,双键的位置导致在氯亲电加成时在苄位形成平面型的碳正离子,在非极性溶剂中,不能溶剂化的碳正离子与氯离子强烈吸引,形成离子对,所以,氯离子留在它最初形成的位置上,而不能像鎓离子机理那样从碳正离子的反面进攻,于是,氯离子就从正面与碳正离子结合,给出顺式加成产物。

卤素取代反应
卤素取代反应是有机化学中的一种常见反应类型,是指在有机化合物中的卤素原子(如氟、氯、溴、碘等)被其他原子或基团取代的过程。
这种反应通常发生在碳氢化合物、醇、酚、醛、酮、羧酸、酯等化合物中。
卤素取代反应通常需要催化剂或高温条件,反应条件的不同会影响反应的速率和选择性。
在有机化学中,卤素取代反应是非常重要的一种反应类型,它可以用于制备各种有机化合物,如医药、农药、染料、高分子材料等。
常见的卤素取代反应包括:
1. 氟取代反应:在碳氢化合物中,氟原子取代了氢原子,形成了一系列具有特殊化学性质的化合物,如氟代烃、氟代烷基、氟代芳烃等。
2. 氯取代反应:在碳氢化合物中,氯原子取代了氢原子,形成了一系列具有不同化学性质的化合物,如氯代烃、氯代烷基、氯代芳烃等。
3. 溴取代反应:在碳氢化合物中,溴原子取代了氢原子,形成了一系列具有不同化学性质的化合物,如溴代烃、溴代烷基、溴代芳烃等。
4. 碘取代反应:在碳氢化合物中,碘原子取代了氢原子,形成了一系列具有不同化学性质的化合物,如碘代烃、碘代
烷基、碘代芳烃等。
卤素取代反应在有机化学中有着广泛的应用,它不仅可以用于制备各种有机化合物,还可以用于分析化学、环境科学、材料科学等领域。

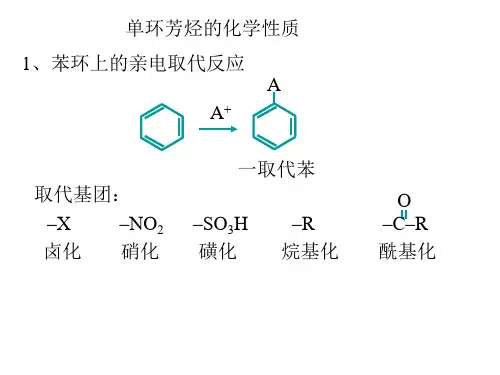


芳香化合物的亲电取代反应方程式汇总芳香化合物的亲电取代反应是有机化学中一种常见的反应类型。
在这类反应中,芳香环上的氢原子被一个亲电试剂取代,产生新的化学物质。
这些反应的方程式可以总结如下:1. 卤代烃的取代反应:芳香环中的一个氢原子被卤素原子取代。
常见的卤素试剂包括溴、氯和碘。
例如,苯和溴反应的方程式为:C6H6 + Br2 → C6H5Br + HBr2. 硝化反应:芳香环中的一个氢原子被亲电的硝酸根离子(NO2-)取代。
这种反应通常在硝化试剂的存在下进行,如浓硝酸或硝酸银。
例如,苯和浓硝酸反应的方程式为:C6H6 + HNO3 → C6H5NO2 + H2O3. 磺化反应:芳香环中的一个氢原子被亲电的磺酸根离子(SO3-)取代。
这种反应需要在磺化试剂的存在下进行,如浓硫酸或磺酸氯。
例如,苯和浓硫酸反应的方程式为:C6H6 + H2SO4 → C6H5SO3H + H2O4. 酯化反应:芳香环中的一个氢原子被亲电的酰氧基(OCOR)取代。
这种反应需要酯化试剂的存在,如醋酸酐。
例如,苯和醋酸酐反应的方程式为:C6H6 + (CH3CO)2O → C6H5COCH3 + CH3COOH5. 酰化反应:芳香环中的一个氢原子被亲电的酰基(COR)取代。
通常在酰化试剂的存在下进行,如乙酰氯。
例如,苯和乙酰氯反应的方程式为:C6H6 + CH3COCl → C6H5COCH3 + HCl除了以上列举的反应类型,还有其他一些亲电取代反应。
芳香化合物的亲电取代反应是有机合成中非常重要的反应之一。
它可以用于合成具有特定功能的化合物,如药物、香料和染料等。
了解这些反应的方程式对于理解有机化学的机理和应用具有十分重要的意义。
总结:本文总结了芳香化合物的亲电取代反应的方程式。
这些反应可以通过不同的亲电试剂实现,如卤素、硝化试剂、磺化试剂、酯化试剂和酰化试剂等。
芳香化合物的亲电取代反应在有机合成中具有重要的应用,在制药、香料和染料等领域中扮演着重要角色。
卤化反应知识点总结一、卤化反应的基本概念1.1 什么是卤化反应卤化反应是指有机化合物中的氢原子被卤素(如氯、溴、碘等)取代的一种反应。
这种反应是一种取代反应,其中一个或多个饱和的氢原子被卤素原子所替代。
卤代烃是一类含有卤素的有机化合物,通常用R-X来表示,其中R代表一个有机基团,X代表卤素原子。
1.2 卤化反应的分类卤化反应可以分为烷基卤化反应和芳香烃的卤化反应两类。
(1)烷基卤化反应:烷烃中的氢被卤素取代的反应称为烷基卤化反应。
烷基卤化反应通常发生在烷烃和卤素(如氯气、溴液等)反应时。
(2)芳香烃的卤化反应:芳香烃的卤化反应是指芳香烃中的氢被卤素取代的反应。
芳香烃的卤化反应通常发生在芳香族化合物和卤素或卤代烃反应时,产生卤代芳烃。
1.3 卤化反应的特点卤化反应具有以下几个特点:(1)反应条件温和,易于操作:卤化反应通常在常温下进行,并且不需要特殊的条件,操作相对较为简单。
(2)生成产物具有良好的化学活性:卤代烃是一种常见的中间体,在有机合成中有很广泛的应用。
(3)取代反应:卤化反应是一种取代反应,即一个或多个氢原子被卤素原子所取代。
(4)反应过程中可能会产生不同的取代产物:在一些情况下,卤化反应可能会得到多种不同的取代产物,需要根据实际情况进行选择。
二、卤化反应的机理2.1 烷基卤化反应的机理烷基卤化反应通常发生在烷烃与卤素反应时,以氯代烷基化反应为例进行说明。
在氯代烷基化反应中,氯气和溴水是两种常用的试剂。
以氯代甲烷的氯化反应为例,反应机理如下:CH4 + Cl2 → CH3Cl + HCl在上述反应中,氯气(Cl2)与甲烷(CH4)反应,其中一个氢原子被氯原子所取代,生成氯代甲烷(CH3Cl)和氢氯酸(HCl)。
当溴水是试剂时,反应机理如下:CH4 + Br2 → CH3Br + HBr在这种情况下,溴水(Br2)与甲烷(CH4)反应,同样是一个氢原子被溴原子所取代,生成溴代甲烷(CH3Br)和氢溴酸(HBr)。
(1)被羟基取代:
卤代烃与水作用可生成醇。
在反应中,卤代烃分子中的卤原子被水分子中的羟基所取代:R—X+HOH—→R—OH+HX.
该反应进行比较缓慢,而且是可逆的。
医学|教育网整理如果用强碱的水溶液来进行水解,这个反应可向右进行,原因是在反应中产生的卤化氢被碱中和掉,而有利于反应向水解方向进行。
R—X+NaOH—→R—OH+NaX.
卤素与苯环相连的卤代芳烃,一般比较难水解。
如氯苯一般需要高温高压条件下才能水解。
(2)被烷氧基取代:
卤代烃与醇钠作用,卤原子被烷氧基(RO—)取代生成醚,这是制取混合醚的方法。
RX+R′ONa—→ROR′+NaX.
例:CH3Br+CH3CH2ONa—→CH3—O—CH2CH3(甲乙醚)+NaBr
(3)被氰基取代:
卤代烃与氰化钠(或氰化钾)的醇溶液共热,卤原子被氰基取代生成腈。
RX+NaCN—→RCN+NaX.
生成的腈分子比原来的卤代烃分子增加了一个碳原子,这在有机合成中作为增长碳链的一种方法。