计算机化系统清单模板
- 格式:xls
- 大小:24.50 KB
- 文档页数:4

附件1计算机化系统第一章范围第一条本附录适用于在药品生产质量管理过程中应用的计算机化系统。
计算机化系统由一系列硬件和软件组成,以满足特定的功能。
第二章原则第二条计算机化系统代替人工操作时,应当确保不对产品的质量、过程控制和其质量保证水平造成负面影响,不增加总体风险。
第三条风险管理应当贯穿计算机化系统的生命周期全过程,应当考虑患者安全、数据完整性和产品质量。
作为质量风险管理的一部分,应当根据书面的风险评估结果确定验证和数据完整性控制的程度。
第四条企业应当针对计算机化系统供应商的管理制定操作规程。
供应商提供产品或服务时(如安装、配置、集成、验证、维护、数据处理等),企业应当与供应商签订正式协议,明确双方责任。
企业应当基于风险评估的结果提供与供应商质量体系和审计信息相关的文件。
第三章人员第五条计算机化系统生命周期中所涉及的各种活动,如验证、使用、维护、管理等,需要各相关的职能部门人员之间的紧密合作。
应当明确所有使用和管理计算机化系统人员的职责和权限,并接受相应的使用和管理培训。
应当确保有适当的专业人员,对计算机化系统的设计、验证、安装和运行等方面进行培训和指导。
第四章验证第六条计算机化系统验证包括应用程序的验证和基础架构的确认,其范围与程度应当基于科学的风险评估。
风险评估应当充分考虑计算机化系统的使用范围和用途。
应当在计算机化系统生命周期中保持其验证状态。
第七条企业应当建立包含药品生产质量管理过程中涉及的所有计算机化系统清单,标明与药品生产质量管理相关的功能。
清单应当及时更新。
第八条企业应当指定专人对通用的商业化计算机软件进行审核,确认其满足用户需求。
在对定制的计算机化系统进行验证时,企业应当建立相应的操作规程,确保在生命周期内评估系统的质量和性能。
第九条数据转换格式或迁移时,应当确认数据的数值及含义没有改变。
第五章系统第十条系统应当安装在适当的位置,以防止外来因素干扰。
第十一条关键系统应当有详细阐述的文件(必要时,要有图纸),并须及时更新。
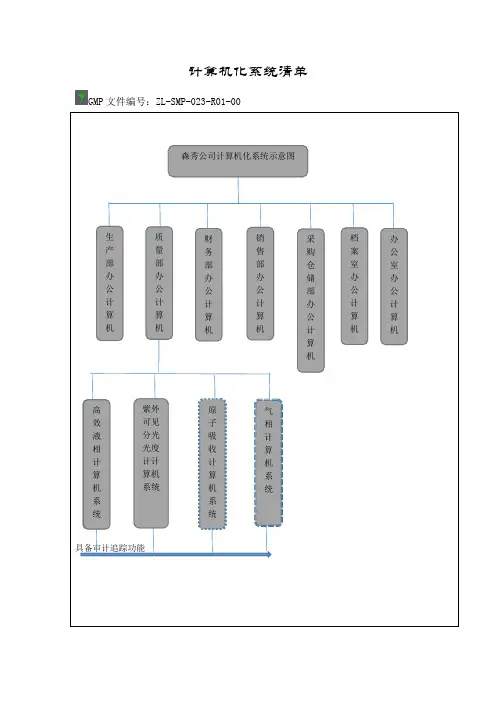
GMP文件编号:ZL-SMP-023-R01-00具备审计追踪功能森秀公司计算机化系统示意图生产部办公计算机质量部办公计算机财务部办公计算机销售部办公计算机采购仓储部办公计算机档案室办公计算机办公室办公计算机高效液相计算机系统气相计算机系统原子吸收计算机系统紫外可见分光光度计计算机系统GMP文件编号:ZL-SMP-023-R01-00序号计算机编号名称安装部门责任人药品生产质量管理相关的功能备注1 JSJ-001 生产部办公计算机生产部初金芝药品生产管理2 JSJ-002 采购仓储部办公计算机采购仓储部侯文华原辅料成品库存3 JSJ-003 财务部办公计算机财务部任晓敏药品财务发票4 JSJ-004 销售部办公计算机销售部侯文华销售发货,召回5 JSJ-005 办公室办公计算机办公室马义人员管理6 JSJ-006 设备部办公计算机生产部郑宏宇设备档案7 JSJ-007 质量部办公计算机质量部齐天宝药品质量管理8 JSJ-008 紫外-可见计算机质控室谢应舟含量测定9 JSJ-009 高效液相计算机质控室谢应舟液相含量检测具审计追踪功能10 JSJ-010 高效气相计算机质控室谢应舟气相含量测定具审计追踪功能11 JSJ-011 原子吸入分光光度计计算机质控室谢应舟含量测定具审计追踪功能计算机系统管理员清单更新日期:年月日。
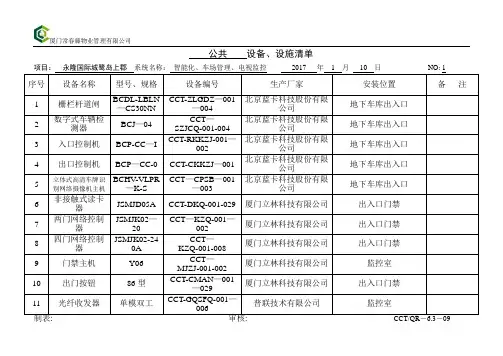
厦门常春藤物业管理有限公司公共设备、设施清单项目:永隆国际城鹭岛上郡系统名称:智能化、车场管理、电视监控2017 年 1 月10 日NO: 1序号设备名称型号、规格设备编号生产厂家安装位置备注1 栅栏杆道闸BCDL-LBLN—CS30NN CCT-ZLGDZ—001—004北京蓝卡科技股份有限公司地下车库出入口2 数字式车辆检测器BCJ—04 CCT—SZJCQ-001-004北京蓝卡科技股份有限公司地下车库出入口3 入口控制机BCP-CC—I CCT-RKKZJ-001—002 北京蓝卡科技股份有限公司地下车库出入口4 出口控制机BCP—CC-0 CCT-CKKZJ—001 北京蓝卡科技股份有限公司地下车库出入口5 立体式高清车牌识别网络摄像机主机BCHV-VLPR—K-SCCT—CPSB—001—003北京蓝卡科技股份有限公司地下车库出入口6 非接触式读卡器JSMJD05A CCT-DKQ-001-029 厦门立林科技有限公司出入口门禁7 两门网络控制器JSMJK02—20CCT—KZQ-001—002 厦门立林科技有限公司出入口门禁8 四门网络控制器JSMJK02-240ACCT—KZQ-001-008 厦门立林科技有限公司出入口门禁9 门禁主机Y06 CCT—MJZJ-001-002 厦门立林科技有限公司监控室10 出门按钮86型CCT-CMAN—001—029厦门立林科技有限公司出入口门禁11 光纤收发器单模双工CCT-GQSFQ-001—006 普联技术有限公司监控室厦门常春藤物业管理有限公司公共设备、设施清单项目:永隆国际城鹭岛上郡系统名称:智能化、车场管理、电视监控2017 年 1 月10 日NO:2序号设备名称型号、规格设备编号生产厂家安装位置备注12 接入层交换机8口CCT—JHJ-001—003 普联技术有限公司监控室13 门禁电源D12V/10A CCT-MJDY—001-012 厦门立林科技有限公司出入口门禁14 彩色可视管理机L8—5003VC—50/1CCT—KSGL—001 厦门立林科技有限公司监控室15 IP转换器L8—5005-5002IP CCT-ZHQ—001-005 厦门立林科技有限公司入户大堂弱电井16 IP转换器电源L8—5001K—160 CCT-ZHQDY——001—005 厦门立林科技有限公司入户大堂弱电井17 接入层交换机24口CCT-JHJ-001 普联技术有限公司监控室18 光纤配线架48口CCT—GQPXJ—001 厦门永锐智能科技有限公司监控室19 单元彩色可视主机L8-5002MGLC-10ISCCT-CSKSZJ-001-006 厦门立林科技有限公司入户大堂门禁20 围墙主机L8-5002MGLWC—10IS CCT-WQZJ—001 厦门立林科技有限公司监控室21 彩色可视分机L8—5004VCW7060CCT-CSKSFJ-001—696 厦门立林科技有限公司楼层住户22 主机开关电源L8—5001K-1260 CCT—ZJKGDY—001—045 厦门立林科技有限公司弱电井厦门常春藤物业管理有限公司公共设备、设施清单项目:永隆国际城鹭岛上郡系统名称:智能化、车场管理、电视监控2017 年 1 月10 日NO:3序号设备名称型号、规格设备编号生产厂家安装位置备注23 分机开关电源L8-5001K—3290 CCT—FJKGDY—001—062 厦门立林科技有限公司弱电井24 二合一控制器L8-5005-5109—D CCT-KZQ-001-174 厦门立林科技有限公司弱电井25 电梯半球摄像机SCD—2010P CCT-DTSXJ-001-012天津三星泰科光电子有限公司电梯轿厢26 20米彩色红外摄像机SCO—1020RPCCT—HWSXJ-001—046天津三星泰科光电子有限公司地下室27 彩色摄像机SCO-3000P CCT-CSSXJ-001—002 天津三星泰科光电子有限公司地下室28 彩色半球摄像机SCD—2022RPCCT-CSBQSXJ-001—007天津三星泰科光电子有限公司入户大堂29 16路视频光端机YHGTDT/R16V1FD—A CCT—GDJ-001-006深圳市宇航光通科技有限公司弱电井30 16路硬盘录像机DH—DVR1604HF-LCCT-LXJ-001—005 浙江大华技术股份有限公司监控室31 22″液晶监视器V A22-L30 CCT—JSQ-001-008 TCL集团股份有限公司监控室32 42″液晶监视器V A42—L11 CCT—JSQ—001 TCL集团股份有限公司监控室33 矩阵控制主机ADT8200-80V12P CCT-JZKZZJ-001 浙江大华技术股份有限公司监控室厦门常春藤物业管理有限公司制表: 审核:CCT/QR-6。

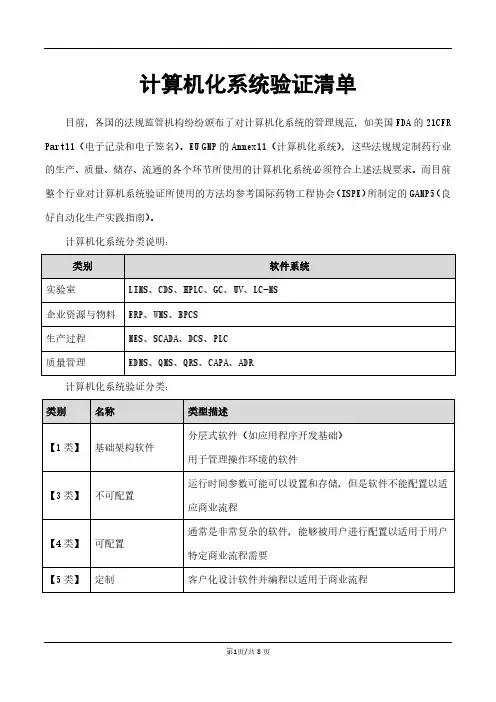
计算机化系统验证清单
目前,各国的法规监管机构纷纷颁布了对计算机化系统的管理规范,如美国FDA的21CFR Part11(电子记录和电子签名)。
EU GMP的Annex11(计算机化系统),这些法规规定制药行业的生产、质量、储存、流通的各个环节所使用的计算机化系统必须符合上述法规要求。
而目前整个行业对计算机系统验证所使用的方法均参考国际药物工程协会(ISPE)所制定的GAMP5(良好自动化生产实践指南)。
计算机化系统分类说明:
计算机化系统验证分类:
1.1计算机化系统验证流程
1.2计算机化系统验证清单
序号验证阶段内容框架类别
【1】计划阶段
01
用户需求说明
(URS)
【编写用户需求】
【审核用户需求】
【批准用户需求】
用户需求(URS)是从用户的角度描述系统的需求。
它应当
根据系统的工艺需求,描述系统所需具备的功能、控制参
数、数据采集、数据存储、数据输出、数据备份、数据还
原、权限控制、电子签名等各项要求,确保系统的功能满
足法规要求及符合预定用途。
用户需求(URS)主要内容:
1、文件的整体介绍,内容包括:
文件内容摘要
目的:阐述写该项目URS的目的。
适用范围:要确定文件用在项目建设中哪个阶段,指导
什么工作。
参考文献:主要列出在描述URS时引用的文献资料名
称、版本、章节等。
2、项目简介、背景
这部分内容应该摘自项目计划书。
3、文件内容,包括:
甲方编写。

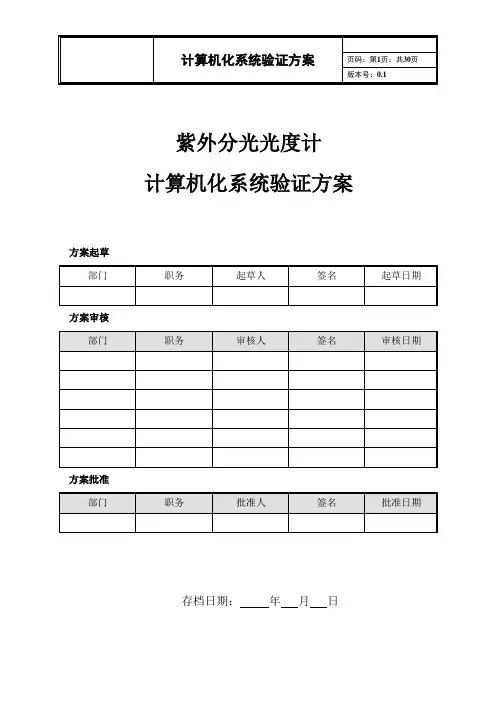
紫外分光光度计计算机化系统验证方案方案起草方案审核方案批准存档日期:年月日目录1 验证目的 (3)2 验证范围 (3)3 职责确认 (3)4 指导文件确认 (3)5 术语缩写 (3)6 验证实施前提条件 (4)7 人员确认 (4)8 风险评估 (4)9 验证时间安排 (5)10 验证内容 (5)11 偏差处理 (12)12 风险的接收与评审 (12)13 确认计划 (12)14 验证谱图编制 (12)15 审核、结论 (13)1 验证目的我司质量检验部现有1台XXX型紫外分光光度计(),与工作站软件、计算机系统及打印机组成色谱仪计算机化系统。
为保证这些系统符合GMP标准,满足使用要求和分析测试需求,保证数据的安全,特制定本验证方案,以进行计算机化系统验证.2 验证范围本次验证范围是我部1套紫外分光光度计计算机化系统,如表1所示。
表1 计算机化系统列表3 职责确认《药品生产质量管理规范》2010 修订版《药品生产质量管理规范》2010 修订版附录:《计算机化系统》《药品生产质量管理规范》2010 修订版附录:《确认与验证》《Cary 60 UV—Vis Specifications》5 术语缩写6。
1 相关人员已经过岗位培训且考核合格,见附件1:人员培训及考核确认记录。
6.2 相关文件系统已编制完成并经过审批,见附件2:验证确认所需文件审核确认记录。
7 人员确认验证小组成员和所有参与测试的人员均经过验证方案的培训,见附件3:验证方案培训签到表。
8 风险评估验证小组人员共同对紫外分光光度计计算机化系统验证进行了风险评估,对存在的质量风险提出了预防和纠正措施建议,具体见下表:当RPN=24~32,风险中等,非关键性风险,建议采取措施降低风险;当RPN>32或S=5时,风险较高,关键性风险,必须采取措施降低风险至中等风险以下。
当RPN<24时,风险较低,可接受的风险,无需采取措施。
9 验证时间安排2018.01.20~2017。
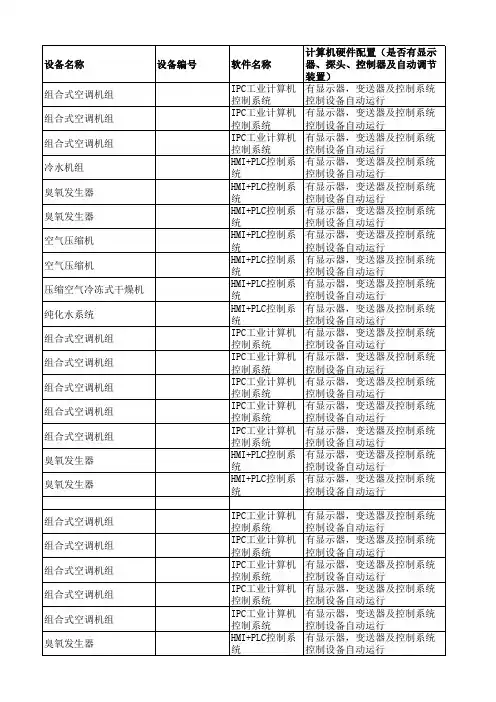

机房网络系统需求清单一、需求描述根据项目应用研究架构,以满足研发数据存储、数据管理、数据应用和系统备份需求,配置应用服务器系统、数据库服务器系统、存储系统、备份系统,以及商用机、核心交换机、路由器、防火墙、UPS电源、KVM切换控制器、精密空调、机柜、办公桌椅等。
本项目服务器系统选择两台国产华为RH2288H,分别作应用服务器、数据库服务器(详见表1);交换机选择华为S5700—28C-SI(详见表2);路由器选择华为AR2220(详见表3);防火墙选择华为USG2210(详见表4);UPS 电源选择美国山特UPS电源;KVM切换控制器选择卓普LZ708(详见表5),机柜选择图腾A3。
6042,以及工作人员办公用台式电脑选用联想扬天R4900D (I7 4790)、笔记本选用ThinkPad L440(i7 4712MQ/8GB/1TB)、微软Surface Pro 3(i5/128GB/windows8。
1/中国版)(详见,表6-8)等。
考虑到经费紧张,本项目暂不考虑存储系统、备份系统、核心交换机、云计算虚拟化系统,以及精密空调等设备。
表1 服务器设备技术规格参数表2 交换机技术规格参数表3 路由器技术规格参数表4 防火墙技术规格参数表5 KVM控制平台技术规格参数表6 台式电脑技术规格参数表7 商用办公笔记本技术规格参数表8 商用办公笔记本(2合1)技术规格参数显示屏支持十点触控;12英寸;显示比例:3:2;屏幕分辨率2160x1440;屏幕技术:LED背光,Retina显示屏,IPS屏幕,Full HD显示屏;显卡核芯显卡;卡芯片IntelGMAHD4400;DirectX 11;多媒体摄像头(前置:500万像素,后置:500万像素);音频系统内置音效芯片; Dolby音效的立体声扬声器;立体声麦克风;网络连接无线网卡:支持802.11a/b/g/n无线协议;支持蓝牙4.0模块;数据接口数据接口:1×USB3。
第一条:本附录适用于在药品生产质量管理过程中应用的计算机化系统,计算机化系统由一系列硬件和软件组成,以满足特定的功能。
解读:1、本规范仅适用于与GMP质量管理相关的计算机化系统;2、计算机化系统的定义,包括硬件和软件,并满足特定功能;和“计算机系统”的区别在于“满足特定功能”上;第二条:计算机化系统代替人工操作时,应当确保不对产品的质量、过程控制和其质量保证水平造成负面影响,不增加总体风险。
解读:1、允许用计算机化系统代替人工操作,因为一切事物的发展都是以新技术的应用作为表现形式,不断的提高社会生产率,降低成本;2、提出一个基本的底线就是新技术的应用,和过去的操作方式相比不能增加整体的风险,所以也就说我们使用新技术和新方法的时,要小心谨慎,并且要有一套科学的程序证明风险可控;3、明确风险的范围,可能是来自最终产品的质量,或者产品生产过程,抑或产品的质量保证体系等;第三条:风险管理应当贯穿计算机化系统的生命周期全过程,应当考虑患者安全、数据完整性和产品质量。
作为质量风险管理的一部分,应当根据书面的风险评估结果确定验证和数据完整性控制的程度。
解读:1、计算机化系统的管理引入风险管理的理念与GMP质量风险管理一脉相承;2、风险管理要求贯穿整个计算机化系统全生命周期,按照时间顺序包括方案规划、项目实施、系统运行、系统升级、系统退役;3、风险管理的目标靶点即风险如果发生可能会导致的后果是什么?应充分考虑的风险包括使用产品的患者安全风险,药品生产质量数据的丢失的风险,产品设计、生产以及最终产品质量风险等;4、计算机化系统风险管理是质量风险管理一部分,应根据风险评估设计系统验证方案和作为系统数据可靠性的依据;第四条:企业应当针对计算机化系统供应商的管理制定操作规程,供应商提供产品或服务时(如安装、配置、集成、验证、维护、数据处理等),企业应当与供应商签订正式协议,明确双方责任。
企业应当基于风险评估的结果,提供与供应商质量体系和审计信息相关的文件。
4、SCADA系统(集团级)
即分布式数据采集和监控系统,它集中了PLC系统的现场测控功能和DCS系统的组网通讯能力两大优点,性价比高,主要用于大系统、大量、甚至远程数据的采集和监控。
三、C类:检验数据处理类计算机
1、实验室设备计算机控制/数据采集处理分析系统
HPLC(液相)、GC(气相)、IR(红外光谱)、UV(紫外)
CDS色谱工作站(普通个人计算机+特定的数据采集系统+检验仪器)与(工业控制计算机+IO接口+输入输出信号)类似
四、D类:办公及管理类计算机
1、个人电脑(生产质量管理、文件记录管理、人员培训管理)
2、LIMS系统:实验室信息管理系统
6、基于互联网的电子商务版ERP。
计算机化系统管理文件体系的建立前几天,有些人一直在问我计算机化系统到底怎么样验证,管理文件怎么弄,他们觉得计算机化系统是如此的另类,必须有单独的《计算机化系统管理规程》、《计算机化系统验证主计划》、《计算机化系统验证SOP》、《计算机化系统变更管理规程》、《计算机化系统偏差管理规程》、《计算机化系统操作管理规程》、《计算机化系统维护管理规程》……,反正,只要别的设备有的,计算机化系统也要有,恨不得为“计算机化系统”另外建立一套完整的GMP体系文件,这真是一个庞大的世纪工程!前面的几期微信中,我一直在说,“计算机硬件”其实就是普通的电气设备、或者主设备和主系统的一个组成部分,我们把它理解为设备的一个关键部件也可以,那么“计算机软件”就是写给计算机系统进行运行的“操作SOP”,计算机硬件按照软件指令进行工作,那么“软件”就和写给人的操作SOP文件没有本质区别。
如果把计算机比作人也可以,我们没必要去研究人的五脏六腑、七情六欲,只要经过适当的培训,他能够按照SOP进行正常的操作,就OK了!如果真的要为计算机化系统建立一些管理规程,我觉得也没必要全部都特别单独建立。
1、质量风险管理计算机系统作为一台设备或者设备的一个部件进行风险管理就可以了,没必要单独写一份计算机化系统的质量风险管理文件,计算机化系统代替人工操作,不应增加风险,风险主要来自于计算机执行的动作和实现的功能对产品质量的影响。
而且风险管理应当贯穿设备的生命周期,当然包括计算机化系统,作为质量风险管理的一部分,就可以了。
2、验证主计划如果非想单独写一份计算机化系统的验证主计划,也可以,随便吧。
制药项目实施阶段可以有项目验证主计划,也可以分车间和QC,当然也可以分计算机和非计算机,正常运行阶段有公司的验证主计划,当然也可以把计算机系统单列,不过我认为没必要。
3、计算机化系统分类清单台账登记,可以把嵌入式计算机系统(比如智能仪表)不单独登记,但是它们肯定也是计算机系统。
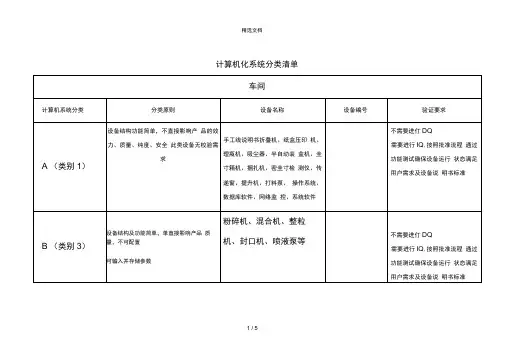
计算机化系统分类清单计算机化系统分类清单车间计算机系统分类分类原则设备名称设备编号验证要求A(类别1)设备结构功能简单,不直接影响产品的效力、质量、纯度、安全此类设备无校验需求手工线说明书折叠机、纸盒压印机、理瓶机、吸尘器、半自动装盒机、封箱机、捆扎机、密封检测仪、传递窗、提升机、打料泵、操作系统、数据库软件、网络监控、系统软件不需要进行DQ需要进行IQ,按照批准流程通过功能测试确保设备运行状态满足用户需求及设备说明书标准B(类别3)设备结构及功能简单,单直接影响产品质量,不可配置可输入并存储参数粉碎机、混合机、整粒机、封口机、喷液泵等不需要进行DQ需要进行IQ,按照批准流程通过功能测试确保设备运行状态满足用户需求及设备说明书标准设备结构、功能相对复杂,对产品质量有一定影响,但非关键中包机、全自动装箱机、纸箱码垛机、检重仪、金属探测器、烘箱、洗衣机、干衣机1.需要进行DQ(成熟品牌的商用设备可通过“URS反馈表”完成设计确认)2.需要进行IQ、OQ,个别设备还应考虑PQC类(类别3)设备结构复杂,可通过对运行中采集参数(信号)的处理实现相应的反馈,并最终实现设备的调整(自动或手动)设备会严重影响到产品的质量、效力、纯度、安全,某些功能的失效会带来法规风险制备罐、贮罐、压片机、胶囊填充机、包衣机、灌封机、计数装瓶机、泡罩包装机、全自动装盒机、贴标机、批号打印装置、照相检测装置、药监码系统、自动清洗机、手套箱等实验室计算机系统分类分类原则设备名称设备编号验证要求A(类别1)没有测量能力或者没有常规校验要求的保准设备氮气发生器、氢气发生器、水蒸气发生器、电子干燥箱、冰箱、显微镜、均质器、超声波清洗机、水浴锅、磁力搅拌器、漩涡搅拌器、离心机、摇床、菌类计数器、微波消解仪等不需要进行DQ需要进行IQ通过功能测试确保设备运行状态满足用户要求及设备说明书标准B(类别1)提供测量值得标准仪器和设备,仪器可通过需要校准的物理参数(如温度、压力或流量)进行控制。