高中化学专题三有机化合物的获得与应用35乙烯的性质导读案无答案苏教版必修2
- 格式:doc
- 大小:30.00 KB
- 文档页数:2

第2课时 石油炼制 乙烯一、石油的炼制 1.石油的分馏(1)原理:根据沸点不同,通过加热汽化,然后冷凝,把石油分成不同沸点范围内的产物。
(2)石油的蒸馏实验(3)分馏产品①特点:各馏分均为混合物。
②产品:石油气、汽油、煤油、柴油、润滑油、重油。
2.石油的裂化(1)目的:为了提高从石油中得到的汽油等轻质油的产量和质量。
(2)原理:用石油分馏产品为原料,在加热、加压和催化剂存在下,使相对分子质量较大、沸点较高的烃断裂为相对分子质量较小、沸点较低的烃。
(3)举例(十六烷的裂化)化学方程式:C 16H 34――→催化剂加热、加压C 8H 18+C 8H 16。
3.石油的裂解(1)原理:以比裂化更高的温度使石油分馏产物中的长链烃断裂为乙烯、丙烯等气态短链烃。
(2)目的:获得乙烯、丙烯等气态短链烃,为石油化工提供原料。
(1)石油的分馏是物理过程,而催化裂化和裂解属于化学过程。
(2)石油裂解是生产乙烯的主要方法。
例1(2019·丽水高一检测)实验室用下列仪器组装一套蒸馏石油的装置,并进行蒸馏得到汽油和煤油。
(1)写出下列仪器的名称:①_____________;②_____________;③_____________。
(2)将以上仪器按从左到右顺序,用字母a、b、c…进行连接:e接( );( )接( );( )接( )接( )。
(3)仪器的A口是________,B口是________。
(4)蒸馏时,温度计水银球应在________(位置)。
(5)在②中注入原油后,加几片碎瓷片的目的是________________________________________________________________________________________________________。
考点石油的炼制题点石油的蒸馏实验答案(1)①冷凝管②蒸馏烧瓶③锥形瓶(2)c d a b f g (3)进水口出水口(4)蒸馏烧瓶支管口处(5)防止暴沸例2下图是石油分馏塔的示意图。
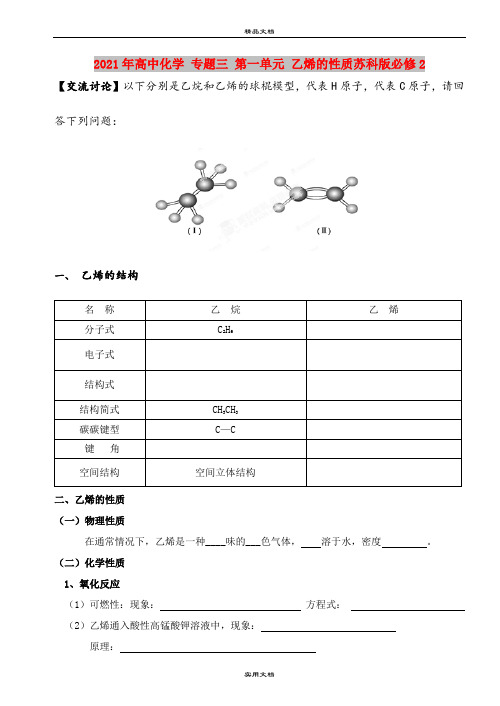
2021年高中化学专题三第一单元乙烯的性质苏科版必修2【交流讨论】以下分别是乙烷和乙烯的球棍模型,代表H原子,代表C原子,请回答下列问题:一、乙烯的结构名称乙烷乙烯分子式C2H6电子式结构式结构简式CH3CH3碳碳键型C—C键角空间结构空间立体结构二、乙烯的性质(一)物理性质在通常情况下,乙烯是一种____味的___色气体,溶于水,密度。
(二)化学性质1、氧化反应(1)可燃性:现象:方程式:(2)乙烯通入酸性高锰酸钾溶液中,现象:原理:OC 、CH 3—C —H + H 2 CH 3—CH 2—OH催化剂D 、CH 3—CH 3+ 2Cl 2 CH 2Cl —CH 2Cl+2HCl催化剂2、加成反应将乙烯通过溴水,现象:方程式:★加成反应定义:有机物分子中 与其他 直接结合生成新的化合物的反应。
加成反应的结构条件:加成反应规律: 【活学活用】CH 2==CH 2 + H 2 CH 2==CH 2 + HCl CH 2==CH 2 + H —OH例1:下列各反应中属于加成反应的是( )A 、CH 2= CH 2 + H —OH CH 3—CH 2—OHB 、H 2 +Cl 2 2HCl例2:由乙烯推测丙烯(CH 2=CH —CH 3)与溴水反应时,对反应产物的叙述正确的A .CH 2Br —CH 2—CH 2BrB .CH 3—CBr 2—CH 3C .CH 3—CH 2—CHBr 2D .CH 3—CHBr —CH 2Br【问题思考】①怎样鉴别乙烷和乙烯两种气体?②如何除去乙烷气体中混有的乙烯,得到纯净的乙烷气体? ③分析比较制取较纯净氯乙烷的两种方法,哪一种更合理?例3:某烯烃与H 2加成后的产物是, 则该烯烃的结构式可 能有( )催化光A.1种B.2种C.3种D.4种3、加聚反应nCH2==CH2▲具有不饱和键的有机化合物通过得到高分子化合物叫反应。
聚乙烯属于,分子式由于不同它属于。
(3) 加聚规律:例4:nCH2==CH—CH 3nCH2==CH—Cl【归纳总结】乙烯型加聚通式:三、乙烯的实验室制法1、原料:2、原理:3、发生装置:4、收集:【交流讨论】(1)浓硫酸的作用是什么?(2)向烧瓶中加试剂时,是先加浓硫酸还是先加乙醇?(3)烧瓶中加入几片碎瓷片的作用是什么?(4)为什么使用温度计?温度计水银球所插的位置与蒸馏时有何区别?(5)已知140℃时,乙醇在浓硫酸催化下会生成乙醚,该实验中要迅速升温至1700C的原因是什么?(6)加热过程中混合液往往变黑,黑色物质是什么?产生的刺激性气味的气体是什么气体?原因是什么?如需制备纯净乙烯如何除去该气体?四、乙烯用途1、乙烯是石油化工最重要的基础原料,是衡量一个国家化工水平的标志,用于制涤纶、橡胶等。

苏教版化学必修二专题三第一单元第2节乙烯【教材剖析】本节课的内容位于化学必修2专题三的第一单元——化石燃料与有机化合物。
教材介绍了乙烯是一种重要的基本化工原料,它的产量能够用来权衡一个国家的石油化工发展水平,从乙烯用途的角度激发学生的学习兴趣,侧重介绍乙烯分子的构成和构造,乙烯的性质和重要的有机反响——加成反响。
乙烯的分子构造是掌握乙烯化学性质的基础,乙烯性质的要点放在化学性质上。
而在讲解乙烯的性质时,又牢牢环绕乙烯的构造睁开,重申乙烯分子中碳碳双键有一个键简单断裂的特色,所以本节课在展望并考证了乙烯的化学性质以后,要点从乙烯分子构造下手,分析乙烯的化学性质,使学生更深刻地理解物质的构造决定物质的性质。
【学情剖析】在本节课以前,学生已经学习了以甲烷为代表的简单烷烃的构造、性质(要点是代替反响)以及构造式、电子式、构造简式表示有机物机构等基础知识,学生也掌握了碳的四价理论,这为本节课的学习确立了基础。
【教课目的】知识与技术:认识乙烯的构造特色。
认识乙烯的主要物理性质和化学性质。
认识乙烯在生产生活中的应用。
过程与方法:提高学生剖析、类比、迁徙以及归纳的能力。
认识有机化合物的存在—构造—性质—用途的主线。
培育学生抽象、归纳形成规律性认识的能力。
深入学习详细物质的科学方法。
感情态度与价值观:经过有机化学中构造决定性质,反响条件决定产物的思想,意会内外因的辩证关系;联合加成反响加强对化学反响实质的辩证认识。
经过乙烯性质实验培养学生谨慎务实的科学态度和研究创新质量。
【教课要点和难点】乙烯的构造特色和主要性质。
乙烯的加成反响。
【教课策略】自主学习、合作学习、实验议论、对照归纳。
【教课过程】教课教师活动学生活动设计企图环节课题【引入】视频“能够吃的矿泉水瓶”学生思虑,明确本节让学生明确本节课的学引入作为引入。
学习任务。
习任务。
经过视觉、听觉【设疑】为何要发明这类能够吃冲击,感觉乙烯在社会生1展望考证化学性质的矿泉水瓶?产生活中的重要价值,激【剖析】塑料难以降解,简单造成发他们的兴趣和学习的白色污染,塑料的成分之一就是聚主动性。



2019-2020年高中化学《乙烯》导学案苏教版必修2【学习目标】1.掌握乙烯的结构和化学性质,2.掌握加成反应的概念,对比取代反应和加成反应【学习重点】乙烯的加成反应【学习过程】(一)自主学习2.根据乙烯和乙烷分子的空间构型推测乙烯和乙烷的化学性质是否相似。
3.观看乙烯的制备和性质实验写出乙烯物理性质常温下为色、味的气体,比空气,溶于水。
化学性质4.乙烯不仅可以与Br2发生加成反应,在一定条件下还可以与H2、Cl2、H2O、HCl等物质发生加成反应。
写出有关反应的化学方程式:(二)合作探究加成反应和取代反应的区别?(三)当堂巩固1.关于乙烯的叙述中不正确的是()A.乙烯的化学性质比乙烷的活泼B.乙烯燃烧时火焰明亮,同时伴有黑烟C.乙烯可做香蕉等水果的催熟剂D.乙烯双键中的一个键可以断裂,容易发生加成反应和取代反应2、不能用于鉴别甲烷和乙烯的试剂是 ( )A、溴的四氯化碳溶液B、酸性高锰酸钾溶液C、NaOH溶液D、溴水3、乙烯发生的反应中,不属于加成反应的是( )A、与H2反应生成乙烷B、与水反应生成乙醇C、与溴水反应使之褪色D、与O2反应生成CO2和水4.下列物质不能使酸性高锰酸钾褪色的是( )A.二氧化硫B.甲烷C.二氧化碳D.乙烯5.既可以用来鉴别乙烯和乙烷,又可以用来除去乙烷中的乙烯得到纯净乙烷的方法是 ( )A、通过足量的氢氧化钠溶液B、通过足量的KMnO4酸性溶液C、通过足量的Br2水D、在Ni催化加热条件下,通入氢气【学习反思】当堂训练班级姓名一.选择题1.(xx年江苏省普通高中学业水平测试)下列化学用语表示正确的是A.氯化钙的化学式 CaCl B.HCl分子的电子式 C.乙烯的结构简式 CH2CH2 D.氯原子的结构示意图2.(xx年江苏省普通高中学业水平测试)下列有机物中,含有碳碳双键的是A.甲烷 B.乙烯 C.苯 D.乙酸3.关于乙烯的叙述中不正确的是()A.乙烯的化学性质比乙烷的活泼B.乙烯燃烧时火焰明亮,同时伴有黑烟C.乙烯可做香蕉等水果的催熟剂D.乙烯双键中的一个键可以断裂,容易发生加成反应和取代反应二、填空题4.现有A、B、C三种烃,其球棍模型如下图:(1)写出分子式: A B C(2)写出结构简式:A B C(3)A、B、C三种烃,发生取代反应的是_______________发生氧化反应的是_____________发生加成反应的是_______________5.完成化学方程式:(1)乙烯使溴的四氯化碳溶液褪色(2)乙烯与水的加成反应(3)乙烯与氢气反应(4)乙烯与溴化氢反应。
第三课时乙烯整体设计三维目标1.知识与技能使学生知道乙烯的分子结构,了解乙烯的工业制法和主要性质.了解乙烯的可燃性、加成反应和加聚反应及主要用途。
通过比较乙烯和乙烷的结构及相关实验现象,培养学生观察和类比的思维能力。
2。
过程与方法本课时主要采用实验探究法和提问、启发式教学.3。
情感态度与价值观通过对乙烯性质和用途的介绍,引导学生了解乙烯的重要应用。
培养学生热爱化学的情感。
教学重点乙烯的化学性质.教学难点乙烯的加成反应、加聚反应。
课前准备药品:酸性高锰酸钾溶液、溴的四氯化碳溶液、乙烯气体、甲烷气体。
仪器:试管、贮气瓶、导管、火柴。
教具:乙烷、乙烯的球棍模型.教学过程知识回顾前面我们学习了石油的组成和炼制方法。
石油的成分:(1)组成元素:主要为碳和氢;(2)组成物质:各种烷烃和芳香烃.石油的分馏:通过给石油加热,使低沸点的烃首先汽化,再经过冷凝,使石油分成不同沸点范围的蒸馏产物的方法。
裂化目的:提高轻质油的产量。
裂化原理:在一定条件下,将相对分子质量较大、沸点较高的烃断裂为相对分子质量较小、沸点较低的烃的过程.裂解目的:获得更多乙烯、丙烯等基本有机化工原料.裂解原理:比裂化更高的温度,使长链烃断裂成为乙烯、丙烯等气态短链烃。
导入新课工业上可以从石油产品中得到大量的乙烯,它的产量通常是用来衡量一个国家石油化工发展水平的标志。
乙烯有很多用途,例如,过去南方的水果在北方很难吃到。
交通不便是其中的原因之一,主要是因为一些水果(如香蕉)成熟后难以长时间保存,乙烯应用于水果的催熟解决了这一难题。
现在,人们可以把接近成熟的香蕉摘下来,运送到各地,然后在香蕉上喷洒催熟剂乙烯利(学名:2氯乙基磷酸)。
乙烯利能被作物吸收并在植物体内分解释放出乙烯。
使植物呼吸旺盛、代谢速度加快,促进作物的成熟。
这样,硬而青的香蕉在喷洒了乙烯利后,一夜之间就会泛黄、变软,散发出诱人的清香.今天,我们就来学习这神奇的乙烯。
推进新课[思考] 前面我们学习过乙烷,请大家观察乙烷和乙烯的球棍模型,分析它们组成和结构上的差别。
乙烯的性质1.教学内容分析本节内容选自高中新课程标准教科书(苏教版)必修2第一单元化石燃料与有机化合物中“石油炼制乙烯”的第二课时。
乙烯是烯烃的代表物,本节内容的安排与原人教版教材相比有较大不同,教材内容特别强调从实验、学生生活实际和已有知识出发,回避类别性质的归纳。
根据探究实验----乙烯与酸性高锰酸钾溶液、溴水的反应现象推断乙烯与烷烃分子结构上的不同之处。
根据物质结构的初步知识,从结构角度适度深化学生对甲烷、乙烯的认识,建立有机物“结构(组成)-性质-用途”的认识关系,使学生了解学习和研究有机化合物的一般思维方法,养成一定的分析解决问题的能力。
2.学生情况分析在初中化学的学习中,学生对有机物、化学燃料、淀粉、维生素、油脂、蛋白质等有了非常粗浅的了解,但对乙烯和不饱和烃是初次接触,学习兴趣较高。
本节内容不要求学生系统地学习有机化学知识,不强调按官能团分类学习有机化合物的知识。
教学的关键是让学生在学习乙烯的有关知识的同时,体会化学源自生活,体验自主合作探究学习的过程。
3.设计思想本节课采用“实验探究”、“小组讨论”、“教师启发”、“阅读自学”、“课堂练习”等的教学方式组织教学活动,给学生动手实验、表达和交流的机会,提高学生的教学参与度,帮助学生了解乙烯的主要性质。
通过引导学生“玩”乙烷、乙烯的球棍模型,使他们形象直观地了解乙烷、乙烯结构的区别。
再通过讨论、分析、归纳,让学生认识饱和烃与不饱和烃成键特点的不同。
以“活动与探究”实验,让学生认识:乙烯能被酸性高锰酸钾溶液氧化,能溴发生加成反应。
从动手书写乙烯与溴加成反应的化学方程式,理解、抽象出加成反应的概念。
通过和乙烯的类比,认识乙炔的结构特点,了解乙炔与溴、氯化氢的加成反应,从而加深对加成反应的认识。
4.教学目标知识与技能:(1)了解饱和烃与不饱和烃概念。
(2)了解乙烯分子的组成、结构式和乙烯的主要化学性质。
(3)了解加成反应的概念。
(4)认识乙炔的性质。
乙烯(第一课时)
一、课标要求
认识乙烯的分子组成,结构特征、主要化学性质
二、研读目标
1、知道乙烯的分子式、结构式、结构简式
2、掌握乙烯的化学性质
3、理解加成反应
三、研读要求
研读教材P63到P64页
四、导读设计
(一)知识回顾:
甲烷的代表性质是能发生反应,写出甲烷与氯气生成一氯甲烷的化学方程式。
(二)导读设计:
1、乙烯的结构
乙烯的分子式,结构式,
电子式,结构简式
2、乙烯的化学性质
⑴可以燃烧(写化学方程式)
⑵可以使酸性高锰酸钾溶液退色
⑶发生加成反应
写出乙烯与溴反应的化学方程式
写出乙烯与水反应的化学方程式
五、质疑问难
六、考题链接
1、下列各反应中属于加成反应的是()
A.CH4+2O2⑩CO2+2H2O B.CH2═CH2+H-OH→CH3—CH2OH 乙醇(酒精)
C. CH4+Cl2⑩CH3Cl+HCl
D.HCl+AgNO3=AgCl +HNO3
2.下列物质在催化剂作用下和氢气加成不能得到2-甲基戊烷的是()
A .3223CH CHCH C )(CH =
B .233)CHCH(CH CH CH =
C . 3233CH CH )C(CH CH CH =
七、课后作业
1、 2-甲基丁烷和氯气反应,可能生成一氯取代产物的同分异构体有 ( )
A .3 种
B .2 种
C .5 种
D .4种
2、下列质量相同的烃完全燃烧时消耗氧气的量由多到少的顺序是 ( ) ①CH 4 ②C 2H 4 ③C 3H 4 ④C 2H 6 ⑤C 6H 6
A 、②①④③⑤
B 、①②③⑤④
C 、⑤③④②①
D 、①④②③⑤
3、有①CH 4 ②NH 3 ③P 4 ④CHCl 3 ⑤CCl 4 ⑥CO 2分子,其中不是正四面体构型是 ( )
A .①③
B .③⑤
C .①⑤
D .②④⑥
4、下列5种烃的沸点按由高到低的顺序排列正确的是 ( )
① 2—甲基丁烷 ②2,2—二甲基丙烷 ③丙烷 ④戊烷 ⑤2—甲基丙烷
A 、①②③④⑤
B 、②③④⑤①
C 、⑤②①③④
D 、④①②⑤③
5、 在戊烷的各种同分异构体中, 的一氯代物只有一种结构。
6、烃A 与含氢量最高的烃B 属于同系物,在光照下1体积A 最多能与6体积氯气完全反应(同温同压),则A 的结构简式是 。
7、碳原子在10个以内的烷烃中,它们与卤素发生取代反应,只能得到一种一卤代烷,这些烷烃的结构简式是: 。
8、 3.2克某有机物在纯氧中完全燃烧,生成4.4克CO 2和3.6克H 2O ,通过计算,确定该化合物由哪些元素组成?
(写出计算过程与最后的结论)。