s区和p区元素总结
- 格式:ppt
- 大小:757.00 KB
- 文档页数:36

s区元素的单质均为金属晶体;p区元素的中间部分,其单质的晶体结构较为复杂,有的为原子晶体,有的是过渡型(链状或层状)晶体,有的为分子晶体。
周期系最右方的非金属和稀有气体则全部为分子晶体。
总的来看,同一周期元素的单质,从左到右,一般由典型的金属晶体经过原子晶体、层状晶体或链状晶体等,最后过渡到分子晶体。
同一族元素单质由上而下,常由分子晶体或原子晶体过渡到金属晶体。
副族元素单质均为金属晶体.表9-5 主族及零族元素单质的晶体类型ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 零一H2分子晶体He分子晶体二Li金属晶体Be金属晶体B原子晶体C金刚石原子晶体石墨片状结构晶体富勒烯碳原子簇分子晶体N2分子晶体O2分子晶体F2分子晶体Ne分子晶体三Na金属晶体Mg金属晶体Al金属晶体Si原子晶体P白磷为分子晶体黑磷为层状结构晶体S斜方硫、单斜硫为分子晶体弹性硫为链状结构晶体Cl2分子晶体Ar分子晶体四K金属晶体Ca金属晶体Ga金属晶体Ge原子晶体As黑砷为分子晶体灰砷为层状结构晶体Se红硒为分子晶体灰硒为链状结构晶体Br2分子晶体Kr分子晶体五Rb金属晶体Sr金属晶体In金属晶体Sn灰锡为原子晶体白锡为金属结构晶体Sb黑锑为分子晶体灰锑为层状结构晶体Te灰碲链状结构晶体I2分子晶体Xe分子晶体六Cs金属晶体Ba金属晶体Tl金属晶体Pb金属晶体Bi层状结构晶体(近于金属晶体)Po金属晶体At金属晶体(具有某些金属性)Rn分子晶体单质的晶体结构和物理性质表9-5列出了主族及零族元素单质的晶体类型。
可以看出:s区元素的单质均为金属晶体;p区元素的中间部分,其单质的晶体结构较为复杂,有的为原子晶体,有的是过渡型(链状或层状)晶体,有的为分子晶体。
周期系最右方的非金属和稀有气体则全部为分子晶体。
总的来看,同一周期元素的单质,从左到右,一般由典型的金属晶体经过原子晶体、层状晶体或链状晶体等,最后过渡到分子晶体。
同一族元素单质由上而下,常由分子晶体或原子晶体过渡到金属晶体。

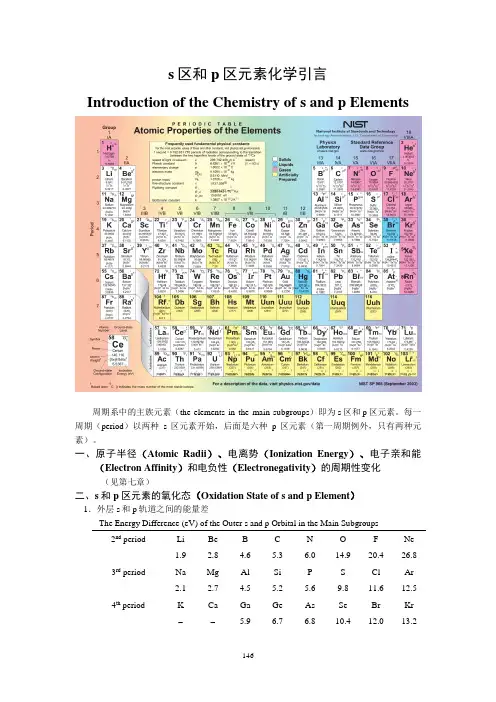
s区和p区元素化学引言Introduction of the Chemistry of s and p Elements周期系中的主族元素(the elements in the main subgroups)即为s区和p区元素。
每一周期(period)以两种s区元素开始,后面是六种p区元素(第一周期例外,只有两种元素)。
一、原子半径(Atomic Radii)、电离势(Ionization Energy)、电子亲和能(Electron Affinity)和电负性(Electronegativity)的周期性变化(见第七章)二、s和p区元素的氧化态(Oxidation State of s and p Element)1.外层s和p轨道之间的能量差The Energy Difference (eV) of the Outer s and p Orbital in the Main Subgroups 2nd period Li Be B C N O F Ne1.92.8 4.6 5.3 6.0 14.9 20.4 26.83rd period Na Mg Al Si P S Cl Ar2.1 2.7 4.5 5.2 5.6 9.8 11.6 12.54th period K Ca Ga Ge As Se Br Kr-- 5.9 6.7 6.8 10.4 12.0 13.25th periodIn Sn Sb Te I Xe 5.2 5.8 6.6 8.8 10.1 - 6th periodTl Pb Bi Po At Rn(7)(9)(10)(12)(16)-(1) 同一周期元素的最高氧化态的稳定性从左到右降低,这是由于s 和p 轨道之间的能级差增大,因此失去n s 2电子的机会减少,例如第三周期:ΔE 3s ~3p :Si(5.2eV),P(5.6eV),S(9.8eV),Cl(11.6eV)∴ ----4243444ClO SO O P SiO 、、、的稳定性从左到右降低(2) ΔE 3s ~3p <ΔE 4s ~4p >ΔE 5s ~5p 可以解释实验上发现如下稳定性序列:PCl 5>AsCl 5<SbCl 5,SF 6>SeF 6<TeF 6,-4ClO >-4BrO <-4IO(3) ΔE 6s ~6p 的值特别大,所以6s 2电子很难参与形成化学键,这种效应称为“6s 2惰性电子对效应”(inert 6s pair effect )2.通常周期系中奇数族元素的氧化数为奇数,偶数族元素的氧化数为偶数+3+5+7+1, 1En sn pEn sn p+4+6+2, 2三、s 和p 区元素的配位数(Coordination Numbers of s and p Elements )1.Fluoro and oxy complexes of selected elements) 2nd period -24BeF-4BF4CF +4NF3rd period -36AlF -26SiF -6PF 6SF+6ClF4th period -36GaF -26GeF-6AsF6SeF2nd period -33BO-23CO -3NO3rd period -44SiO -34PO-24SO-4ClO4th period -44GeO -34AsO -24SeO -4BrO5th period-86SnO-76SbO-66TeO-56IO-46XeO主族元素从上到下,配位数增大;同种元素与不同配体配位,配体体积越小,配位数越大。







元素化学总复习s 区元素元素 同一族自上而下,原子半径增大,电离能、电负性减小,金属性、还原性增强。
单质 物理性质:轻、软、低(看一下保存方法)化合物 氢化物 制备 性质 水解放氢气(做生氢剂)氧化物:在空气中燃烧直接形成的相应的氧化物Li2O Na2O2 KO2 RbO2 CsO2BeO MgO CaO SrO BaO2制备方程式: 性质方程式:氢氧化物 LiOH NaOH KOH RbOH CsOH 中强 强 强 强 强Be(OH)2 Mg(OH)2 Ca(OH)2 Sr(OH)2 Ba(OH)2两性 中强 强 强 强同一族自上而下,碱性增强,溶解度增大盐 碱金属硝酸盐加热时易分解碱土金属碳酸盐的稳定性随金属离子半径的增大而增强。
BeCO3 MgCO3 CaCO3 SrCO3 BaCO3T 分 /℃ <100 540 900 1290 1360对角线规则Li 与Mg ,Be 与Al 的相似性p 区元素概述:惰性电子对效应:同一族元素这种自上而下低氧化值化合物比高氧化值化合物变得更稳定的现象。
(IIIA ~VA )p 区元素性质的特征(四个通性):(原因:d 区和f 区元素的插入) ①第二周期元素具有反常性②第四周期元素表现出异样性 溴酸、高溴酸氧化性分别比其二次周期性 他卤酸(HClO3 ,HIO3)、高卤酸(HClO4,H5IO6)强。
③最后三个元素性质缓慢地递变④ 第五、六周期两种元素性质有些相似。
(镧系收缩))(CaH 2Li/NaH ΔH 2Li/Na/Ca 22−→−+2222222H M(OH)O 2H MH H MOH O H MH +−→−++−→−+O 2Na 2Na O Na 222−→−+223N O 6K 10K 2KNO +−→−+222O Na O 2Na −→−+22KO O K −→−+22222O H 2NaOH O 2H O Na +−→−+22222O O H 2KOH O 2H 2KO ++−→−+)g (O CO 2Na 2CO O 2Na 232222+−→−+)(g 3O CO 2K 2CO 4KO 23222+−→−+2O22KNO 67032KNO 2O2NaNO273032NaNO 2O 24NO O 22Li 70034LiNO +−−→−+−−→−++−−→−硼族元素缺电子化合物:成键电子对数<价层轨道数 如:BF3,H3BO3但HBF4不是缺电子化合物硼的化合物:乙硼烷B2H6 B 利用sp3杂化轨道,与氢形成三中心两电子键。

S区、P区和D区的划分标准主要来自于化学中的价电子构型理论。
1. S区(Segregation Zone):这是由于元素在化学反应中,其外层电子的分布情况不同,导致其在化学反应中的行为也不同。
S区的元素通常是那些外层电子数较少,易于失去电子形成阳离子的元素,如碱金属和碱土金属。
2. P区(Transition Zone):这是由于元素在化学反应中,其外层电子的分布情况介于S区和D区之间,因此其化学反应性也介于两者之间。
P区的元素通常是那些外层电子数较多,易于接受电子形成阴离子的元素,如过渡金属。
3. D区(Diffusion Zone):这是由于元素在化学反应中,其外层电子的分布情况与S区和P 区都不同,因此其化学反应性也与S区和P区都不同。
D区的元素通常是那些外层电子数较多,难以失去或接受电子形成阳离子或阴离子的元素,如非金属元素。
以上是理论上的划分,实际上,元素的化学反应性还会受到其他因素的影响,如原子半径、电负性等。
物质结构与性质知识点总结专题一了解测定物质组成和结构的常用仪器(常识性了解)。
专题二第一单元1.认识卢瑟福和玻尔的原子结构模型。
2.了解原子核外电子的运动状态,了解电子云的概念。
3.了解电子层、原子轨道的概念。
4.知道原子核外电子排布的轨道能级顺序。
知道原子核外电子在一定条件下会发生跃迁。
5.了解能量最低原理、泡利不相容原理、洪特规则,能用电子排布式、轨道表示式表示1-36号元素原子的核外电子排布。
第二单元1.理解元素周期律,了解元素周期律的应用。
2.知道根据原子外围电子排布特征,可把元素周期表分为不同的区。
3.了解元素第一电离能、电负性的概念及其周期性变化规律。
(不要求用电负性差值判断共价键还是离子键)4.了解第一电离能和电负性的简单应用。
专题三第一单元1.了解金属晶体模型和金属键的本质。
2.能用金属键理论解释金属的有关物理性质。
了解金属原子化热的概念。
3.知道影响金属键强弱的主要因素。
认识金属物理性质的共性。
4.认识合金的性质及应用。
注:金属晶体晶胞及三种堆积方式不作要求。
第二单元1.认识氯化钠、氯化铯晶体。
2.知道晶格能的概念,知道离子晶体的熔沸点高低、硬度大小与晶格能大小的关系。
3.知道影响晶格能大小的主要因素。
4.离子晶体中离子的配位数不作要求。
第三单元1.认识共价键的本质,了解共价键的方向性和饱和性。
2.能用电子式表示共价分子及其形成过程。
认识共价键形成时,原子轨道重叠程度与共价键键能的关系。
3.知道σ键和π键的形成条件,了解极性键、非极性键、配位键的概念,能对一些常见简单分子中键的类型作出判断。
注:大π键不作要求4.了解键能的概念,认识影响键能的主要因素,理解键能与化学反应热之间的关系。
5.了解原子晶体的特征,知道金刚石、二氧化硅等常见原子晶体的结构与性质的关系。
第四单元1.知道范德华力和氢键是两种最常见的分子间作用力。
2.了解影响范德华力的主要因素,知道范德华力对物质性质的影响。
s区元素蓝色代表s区元素,氦也属于s区元素。
s区元素主要包括元素周期表中IA族元素和IIA族元素,IA族元素包括氢、锂、钠、钾、铷、铯、鍅七种元素,由于钠和钾的氢氧化物是典型的碱,因此除氢外的这六种元素又称碱金属,IIA族元素包括铍、镁、钙、锶、钡、镭六种元素,由于钙,锶,钡的氧化物之性质介于碱金属与稀土元素之间,因此又称碱土金属。
由于氦的电子排布为1s2,故被分为S区元素。
钫和镭都是放射性元素。
锂最重要的矿石是锂辉石(LiAlSi2O6)。
钠主要以氯化钠溶液的形式存在于海洋,盐湖及岩石中。
钾的主要矿物是钾石盐(2KCl·MgCl2·6H2O)。
铍的主要矿物是绿柱石(3BeO·Al2O3·6SiO2)。
镁的主要矿石是菱镁矿(MgCO3)及白云石。
另外,钙,锶,钡则主要以碳酸盐及硫酸盐的形式存在,如方解石(碳酸钙),石膏(二水合硫酸钙),天青石(硫酸锶),重晶石(硫酸钡)。
在本区元素中同一主族从上到下、同一周期从左至右性质的变化都呈现明显的规律性。
p区元素p区元素包括元素周期表中IIIA族元素~VIIIA族元素。
IIIA族元素又称为硼族元素,包括硼、铝、镓、铟、铊等元素;IVA族元素又称作碳族元素,包括碳、硅、锗、锡、铅等元素;VA族元素又称作氮族元素,包括氮、磷、砷、锑、铋等元素;VIA族元素又称为氧族元素,包括氧、硫、硒、碲、钋等元素;VIIA族元素又称卤素,包括氟、氯、溴、碘、砹等元素;VIIIA族元素或0族元素,又称为稀有气体或惰性气体,包括氦、氖、氩、氪、氙、氡等元素。
d区元素d区元素是元素周期表中的副族元素,即第3至第12族元素。
这些元素中具有最高能量的电子是填在d轨道上的。
这些元素有时也被称作过渡金属。
D区的D来自英语的“diffuse”。
ds区元素ds区元素是指元素周期表中的ⅠB、ⅡB两族元素,包括铜、银、金、锌、镉、汞6种自然形成的金属元素和錀、鎶2种人工合成元素。