药品经营企业质量管理工作流程图
- 格式:doc
- 大小:102.50 KB
- 文档页数:14
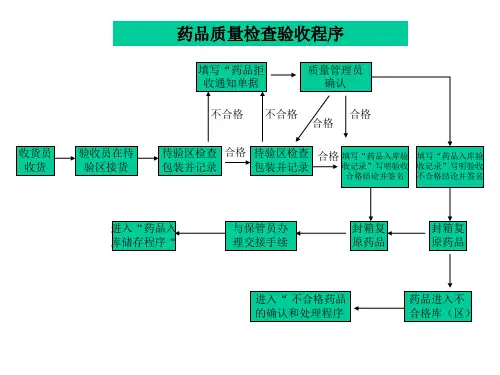
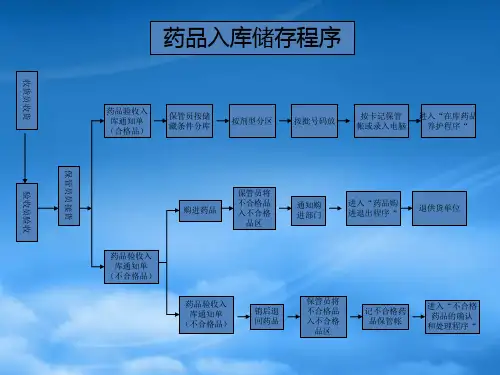


操作规程目录1、质量文件管理程序2、药品采购操作规程3、药品收货操作规程4、药品验收操作规程5、药品销售操作程序6、处方审核、调配、核对操作规程7、药品拆零销售操作规定8、含特殊药品的复方制剂销售操作规程9、营业场所药品陈列操作规程10、营业场所药品陈列检查操作规程11、营业场所冷藏药品的存放操作规程12、计算机系统的操作和管理操作规程制度1:质量文件管理程序一、目的:对质量活动进行预防、控制和改进,确保企业所经营药品安全有效和质量管理体系正常有效地运行,规范质量管理文件的起草、审核、批准、执行、存档等操作程序。
二、适用范围:适用于企业经营质量管理过程中的质量管理制度、工作程序等文件。
责任:质量负责人、质量管理员对本程序的实施负责。
三、内容:(一)文件的起草1、文件应由门店质量负责人依据有关规定和实际工作的需要,提出起草申请,报公司质量负责人。
2、公司质量负责人接到申请后,应对文件的题目进行审核,并确定文件编号,然后指定有关人员起草。
3、文件一般应由门店质量负责人起草,如有特殊情况可指定熟悉法律法规、药品经营质量管理和企业实际情况的人员起草。
4、如有特殊情况可指定熟悉法律法规、药品经营质量管理和企业实际情况的人员起草。
起草人、起草日期、审核人、审核日期、批准人、批准日期、执行日期、分发人员、目的、依据、适用范围和内容。
5、岗位职责还应有质量责任、主要考核指标和任职资格。
6、文件编号规则:(1)形式:企业代码-文件类别代码-顺序号(2)企业代码:由本企业名称前两个字的第一个拼音大写代表。
(3)文件类别代码:质量管理制度(代码为ZD );岗位职责(代码为GZ );操作程序(代码为CX )。
(4)顺序号按文件类别分别用2位阿拉伯数字,从“01”开始顺序编号。
7、文件起草时应依据文件的合法性、实用性、合理性、指令性、可操作性、可检查考核性等六个方面进行制定。
(二)文件的审核和批准:1、公行审核。
2、审核的要点:(1)是否与现行的法律法规相矛盾。
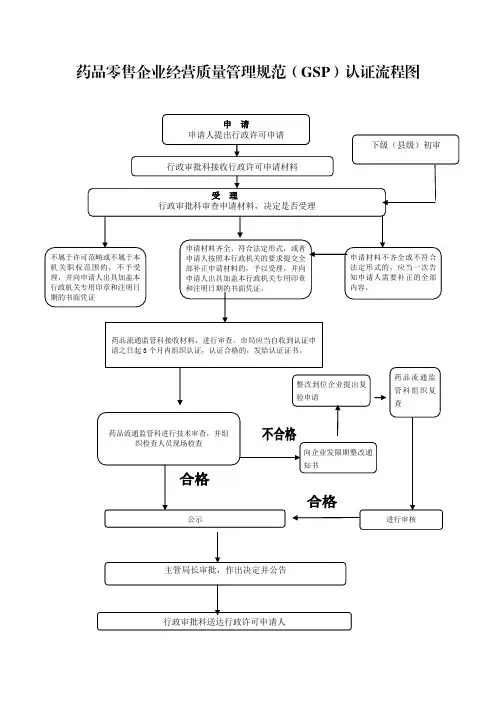
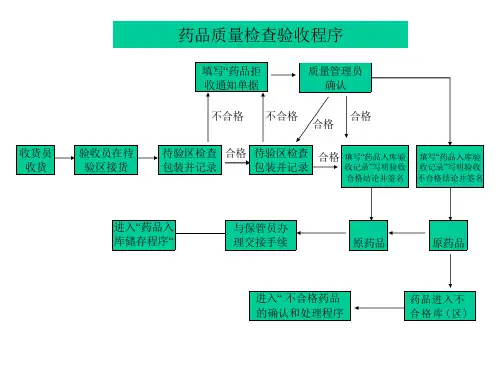

质量管理工作程序、流程图质量工作程序目录1、质量管理制度控制程序--------------------------------------------(1)2、质量管理体系内部审核程序----------------------------------------(2)3、药品进货控制程序------------------------------------------------(5)4、药品购销合同评审程序--------------------------------------------(9)5、药品质量检查验收程序-------------------------------------------(10)6、药品入库储存程序----------------------------------------------(13)7、药品在库养护程序---------------------------------------------(15)8、药品出库复核程序----------------------------------------------(17)9、销后退回、进货通出药品管理程序--------------------------------(19)10、不合格药品的确认和处理程序-----------------------------------(20)11、拆零和拼装发货操作方法--------------------------------------(22)12、药品验收抽样程序----------------------------------------------(23)13、质量记录控制程序----------------------------------------------(25)14、药品储位及条形码编码规程-------------------------------------(26)15、中药饮片养护操作方法-----------------------------------------(28)16、中药饮片零货称取操作方法-------------------------------------(29)17、验收养护仪器操作规程-----------------------------------------(29)14、附录:流程图(1—15)------------------------------------------(36)(4)由办公室统一销毁作废文件。
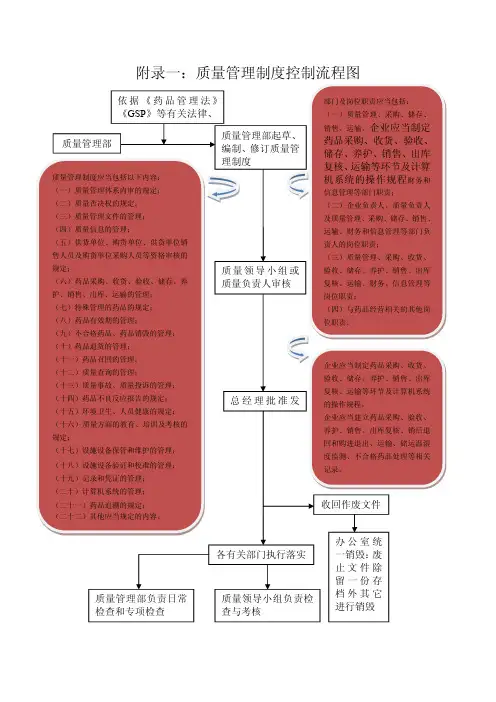
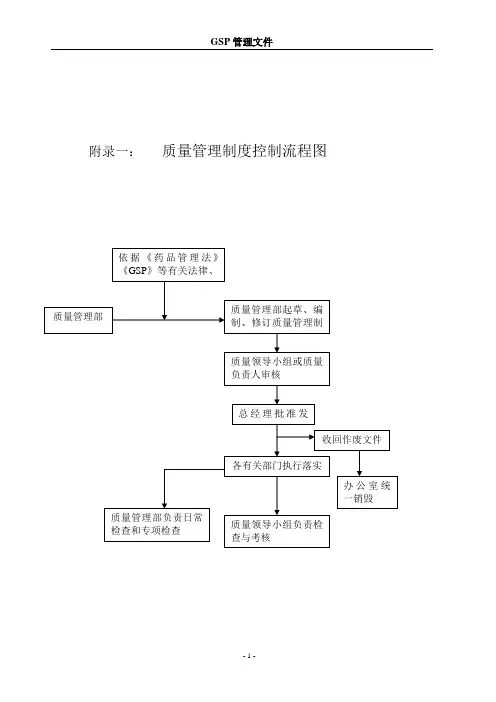

药品经营企业全套业务流程图药品采购管理程序包括首营企业、供货方、采购部、质量管理部和储运部等部门。
首营企业负责收集供货方的经营资格、质量信誉和履行合同能力等资料,并填写“首营企业审批表”进行审核。
同时,采购部对供货商销售人员的资格进行审查,包括委托授权书、身份证复印件和上岗证书复印件等。
质量管理部审核并建立合格供应商档案,包括生产批件或新药证书、质量标准或检验方法、包装、标签、说明书实样、药品检验报告单、药品批件、物价资料、样品等。
同时,质量管理部负责建立和归档药品质量档案,并签订质量保证协议,形成合格采购品种目录。
对于其他合格经营品种,采购部需要索取加盖供方质管机构原印章的《进品药品注册证》或《医药产品注册证》和《进口药品检验报告单》或《进口药品通关单》等相关文件。
在采购计划中,采购部需要制定采购计划,并与财务部进行付款协商,签订合同和采购订单,生成药品收货单。
储运部负责收货,验收员在待验区内进行品种、数量、批号、效期和外包装检查和质量抽验。
收货员需要检查来货运输条件、药品外观,核对药品收货单和来货随货同行单,并按随货同行单核对来货药品品种、批号、数量。
如果不符合质量问题、品种不符或效期违约等情况,需要拒收。
如果符合数量不符,采购部需要通知供货商确认并修改采购记录、随货同行单,按修改后的单据收货。
如果供货商不予确认,需要拒收。
如果经过质管部复查不合格,需要填写封箱复原并盖上“已抽验”,确认验收项目,生成验收入库单,并凭验收入库单与保管员办理入库交接手续。
验收记录需要注明不合格项目结论,并填写《拒收报告单》。
如果供货方质量违约,需要委托销毁或放入不合格品库。
对于不合格品,需要进行购进退出管理程序和不合格品管理程序。
药品入库储存管理程序需要保管员将药品按照入库通知单要求置入合格品区、冷库、阴凉库、常温库、不合格品区或退货区内。
同时,需要对服药品和外用药品进行信息编码、定位录入系统管理,以便进行药品在库养护管理程序。