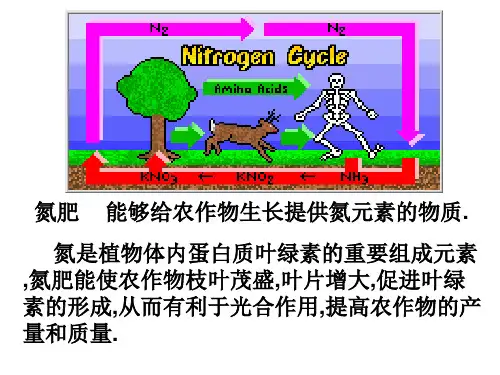
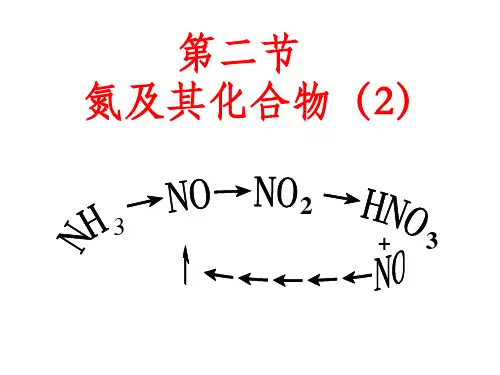
二、铵盐 1.物理性质:铵盐都是易溶于水的白色晶体。 2.化学性质
3.
NH
4
的检验__色,则证明含
NH
4
。
【自主探索】
(1)加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结,能说明 NH4Cl固体可以升华吗? 提示:NH4Cl固体不能升华,受热分解,遇冷重新冷凝成固体。
(2)(思维升华) 用于检验氯气是否泄漏的原理,如图,室温下将过量的氨推入试 管,预测试管中可能出现的现象有哪些?你能写出反应过程的化学方程式吗?(宏 观辨识与微观探析)
(3)(情境应用)与图甲所示装置对比,只提供如图乙所示装置也引发喷泉。在图 丙所示装置的锥形瓶中加入酒精,将锥形瓶置于一水槽中,向水槽中加入冷水后, 再加入浓硫酸、NaOH等物质也能产生喷泉。利用图丙所示装置,在锥形瓶中分 别加入足量的能反应的物质,反应后也可能产生喷泉。
【自主探索】
(1)1 mol·L-1氨水,则该溶液中NH3·H2O浓度是1 mol·L-1吗?该氨水中的溶质 通常认为是什么?
提示:不是。溶液中NH3、
NH
4
、NH3·H2O的浓度和为1
mol·L-1。表示氨水的浓
度时,通常认为氨水中的溶质是NH3。
(2)(前后串联)氨水易挥发,盐酸、硝酸也均易挥发。蘸有浓硝酸的玻璃棒与蘸
【易错提醒】
①NO2溶于水也能形成喷泉,但溶液不能充满烧瓶。 ②NO2和O2的混合气体(体积比4∶1)也能形成喷泉,溶液充满烧瓶。 ③NO和O2的混合气体(体积比4∶3)也能形成喷泉,溶液充满烧瓶。
3.
NH
4
的检验
(1)原理
(2)方法
【规律方法】 1.氨的四“个性” (1)氨是中学阶段学习的唯一溶于水,其水溶液显碱性的气体。 (2)氨水的浓度越大,密度越小。