四川大学 有机及物理化学真题
- 格式:pdf
- 大小:426.46 KB
- 文档页数:4

1.四川大学材料科学与工程学院有机化学(材料学、应用化学等)2000试题资料下载2.四川大学材料科学与工程学院有机化学(材料学、应用化学等)2003试题资料下载3.四川大学材料科学与工程学院有机化学(材料学、应用化学等)2001试题资料下载4.四川大学材料科学与工程学院有机化学(无机化学、分析化学、有机化学、物理化学、高分子化学与物理)2002试题资料下载5.四川大学材料科学与工程学院有机化学(生化与分子生物学、药物化学、药物分析学、微生物与生化药学)2003试题资料下载6.四川大学材料科学与工程学院有机化学(材料学、应用化学等)2005试题资料下载7.四川大学材料科学与工程学院有机化学(生物化学与分子生物学)2000试题资料下载8.四川大学材料科学与工程学院有机化学(材料学、应用化学等)2002试题资料下载9.四川大学材料科学与工程学院有机化学(生物化学与分子生物学)2001试题资料下载10.四川大学材料科学与工程学院有机化学(材料学、应用化学等)2004试题资料下载11.四川大学材料科学与工程学院有机化学(生物化学与分子生物学)2002试题资料下载12.四川大学材料科学与工程学院材料科学基础(1)2005试题资料下载13.四川大学材料科学与工程学院材料科学基础(2)2005试题资料下载14.四川大学材料科学与工程学院电子技术基础2002试题资料下载15.四川大学材料科学与工程学院计算机技术2005试题资料下载16.四川大学材料科学与工程学院金属学(材料学)2001-2002试题资料下载17.四川大学材料科学与工程学院金属学(材料加工工程)2002试题资料下载18.四川大学材料科学与工程学院计算机技术2002试题资料下载19.四川大学材料科学与工程学院高分子化学与物理2002试题资料下载20.四川大学材料科学与工程学院金属材料学2002试题资料下载21.四川大学材料科学与工程学院高分子化学及物理(材料学)2003试题资料下载22.四川大学材料科学与工程学院高分子化学及物理(材料加工工程)2002试题资料下载23.四川大学材料科学与工程学院高分子化学及物理(材料学、化学工程、生物医学工程)2002试题资料下载24.四川大学材料科学与工程学院高分子化学与物理(含高分子物化)2001试题资料下载25.四川大学材料科学与工程学院金属材料学2001试题资料下载26.四川大学材料科学与工程学院高分子化学及物理(材料学、化学工程、生物医学工程)2005试题资料下载27.四川大学材料科学与工程学院高分子物理及化学(材料加工工程)2005试题资料下载28.四川大学水利水电学院土力学及地基基础2005试题资料下载29.四川大学材料科学与工程学院高分子化学与物理(含高分子物化)2000试题资料下载30.四川大学法学院刑法学2000试题资料下载31.四川大学法学院刑事诉讼法2002试题资料下载32.四川大学水利水电学院水力学2005试题资料下载33.四川大学法学院刑事诉讼法2001试题资料下载34.四川大学法学院刑法学2003试题资料下载35.四川大学法学院刑事诉讼法2000试题资料下载36.四川大学法学院刑法学2002试题资料下载37.四川大学法学院刑法学2001试题资料下载38.四川大学法学院宪法学与行政法学(宪法、行政法学)2005试题资料下载39.四川大学法学院刑法学2005试题资料下载40.四川大学法学院宪法学2004试题资料下载41.四川大学法学院刑法学2004试题资料下载42.四川大学法学院化学(诉讼法学专业)2000试题资料下载43.四川大学法学院民事诉讼法学2000试题资料下载44.四川大学法学院民事法学(民法学、民事诉讼法学) 2004试题资料下载45.四川大学法学院民事诉讼法学2002试题资料下载46.四川大学法学院民商法学(民法学、知识产权法、婚姻继承法)2005试题资料下载47.四川大学法学院民事法学(民法学、民事诉讼法学) 2003试题资料下载48.四川大学法学院民事诉讼法学2001试题资料下载49.四川大学法学院民法学2003试题资料下载50.四川大学法学院民法学2000试题资料下载51.四川大学法学院民法学2001试题资料下载52.四川大学法学院法理学2004试题资料下载53.四川大学法学院法学综合(法理学、宪法学、法律逻辑)2005试题资料下载54.四川大学法学院民法学2004试题资料下载55.四川大学法学院民法学2002试题资料下载56.四川大学法学院法理学(含宪法学、中外法制史)2001试题资料下载57.四川大学法学院法理学(含宪法学、中外法制史)2000试题资料下载58.四川大学法学院法理学(含宪法学、中外法制史)2004试题资料下载59.四川大学法学院法理学(含宪法学、中外法制史)2003试题资料下载60.四川大学法学院经济法学(经济法、商法)2004试题资料下载61.四川大学法学院法理学(含宪法学、中外法制史)2002试题资料下载62.四川大学法学院综合考试(法理学、民法学、刑法总则) 2004试题资料下载63.四川大学法学院综合考试(含法理、刑法、民法)2001试题资料下载64.四川大学法学院综合考试(含法理、刑法、民法)2000试题资料下载65.四川大学法学院综合(中外法制史、中西法律思想史)2004试题资料下载66.四川大学法学院诉讼法学(刑事诉讼、行政诉讼)2002试题资料下载67.四川大学法学院诉讼法学(刑事诉讼、行政诉讼)2000试题资料下载68.四川大学法学院诉讼法学(刑法、民法、刑事诉讼法、民事诉讼法)2005试题资料下载69.四川大学法学院综合考试(含法理、刑法、民法)2002试题资料下载70.四川大学法学院综合(法理、法制史、宪法、行政法学)2004试题资料下载71.四川大学法学院诉讼法学(刑事诉讼、行政诉讼)2001试题资料下载72.四川大学物理科学与技术学院光学2000试题资料下载73.四川大学物理科学与技术学院光学2003试题资料下载74.四川大学物理科学与技术学院半导体器件2003试题资料下载75.四川大学物理科学与技术学院半导体物理2003试题资料下载76.四川大学物理科学与技术学院半导体物理2002试题资料下载77.四川大学物理科学与技术学院半导体物理2004试题资料下载78.四川大学物理科学与技术学院光学2002试题资料下载79.四川大学物理科学与技术学院光学2001试题资料下载80.四川大学物理科学与技术学院半导体物理及器件基础2005试题资料下载81.四川大学物理科学与技术学院半导体器件2002试题资料下载82.四川大学物理科学与技术学院原子核物理2002试题资料下载83.四川大学物理科学与技术学院固体物理2002试题资料下载84.四川大学物理科学与技术学院固体物理2003试题资料下载85.四川大学物理科学与技术学院大学物理2002试题资料下载86.四川大学物理科学与技术学院大学物理(热、电、光)2003试题资料下载87.四川大学物理科学与技术学院固体物理2004试题资料下载88.四川大学物理科学与技术学院原子核物理2003试题资料下载89.四川大学物理科学与技术学院固体物理2005试题资料下载90.四川大学物理科学与技术学院大学物理(力、电、学)2004试题资料下载91.四川大学物理科学与技术学院大学物理(电磁学)2004试题资料下载92.四川大学物理科学与技术学院大学物理(电学、光学)2005试题资料下载93.四川大学物理科学与技术学院大学物理(热、电、光)2005试题资料下载94.四川大学物理科学与技术学院数学(无线电物理)2000试题资料下载95.四川大学物理科学与技术学院普通物理(凝聚态物理、光学)2003试题资料下载96.四川大学物理科学与技术学院普通物理(力学、电学、光学)(光学、无线电物理专业)2001试题资料下载97.四川大学物理科学与技术学院普通物理(力学、电学、光学)(理论物理、粒子物理与原子核物理专业)2001试题资料下载98.四川大学物理科学与技术学院普通物理(凝聚态物理、光学)2004试题资料下载99.四川大学物理科学与技术学院普通物理(力学、电学、光学)(光学、无线电物理专业)2000试题资料下载100.四川大学物理科学与技术学院普通物理(力学、电学、光学)(理论物理、粒子物理与原子核物理专业)2002试题资料下载101.四川大学物理科学与技术学院普通物理(力学、电学、光学)(光学、无线电物理专业)2002试题资料下载102.四川大学物理科学与技术学院普通物理(电磁学、光学)2003试题资料下载103.四川大学物理科学与技术学院普通物理(力学、电学、光学)(理论物理、粒子物理与原子核物理专业)2003试题资料下载104.四川大学物理科学与技术学院有机化学及物理化学2005试题资料下载105.四川大学物理科学与技术学院普通物理(电磁学、光学)2004试题资料下载106.四川大学物理科学与技术学院普通物理(电磁学、光学)2005试题资料下载107.四川大学物理科学与技术学院高等数学(微积分、常微分方程、级数)2005试题资料下载108.四川大学物理科学与技术学院有机化学及物理化学2004试题资料下载109.四川大学物理科学与技术学院高等数学(微积分、常微分方程、级数)2004试题资料下载110.四川大学物理科学与技术学院高等数学(微积分、级数、线性代数)2003试题资料下载111.四川大学物理科学与技术学院高等数学(微积分、常微分方程、级数)2003试题资料下载112.四川大学物理科学与技术学院高等数学(微积分、级数)2001试题资料下载113.四川大学物理科学与技术学院高等数学(微积分、级数)2005试题资料下载114.四川大学物理科学与技术学院高等数学(微积分、级数)2002试题资料下载115.四川大学物理科学与技术学院高等数学(微积分、级数、线性代数)2004试题资料下载116.四川大学生命科学学院动物学2001试题资料下载117.四川大学生命科学学院动物学2003试题资料下载118.四川大学生命科学学院动物学2000试题资料下载119.四川大学生命科学学院动物学2002试题资料下载120.四川大学物理科学与技术学院高等数学(微积分、级数)2004试题资料下载121.四川大学生命科学学院微生物学2000试题资料下载122.四川大学生命科学学院动物学2004试题资料下载123.四川大学生命科学学院微生物学2001试题资料下载124.四川大学生命科学学院微生物学2002试题资料下载125.四川大学生命科学学院微生物学1998试题资料下载126.四川大学生命科学学院微生物学2004试题资料下载127.四川大学生命科学学院微生物学2003试题资料下载128.四川大学生命科学学院微生物学2005试题资料下载129.四川大学生命科学学院植物学2001试题资料下载130.四川大学生命科学学院普通生物学2002试题资料下载131.四川大学生命科学学院植物学2000试题资料下载132.四川大学生命科学学院普通生物学2001试题资料下载133.四川大学生命科学学院植物学2002试题资料下载134.四川大学生命科学学院植物学2003试题资料下载135.四川大学生命科学学院生态学2000试题资料下载136.四川大学生命科学学院植物生理学2004试题资料下载137.四川大学生命科学学院生态学2002试题资料下载138.四川大学生命科学学院生态学2003试题资料下载139.四川大学生命科学学院生态学2001试题资料下载140.四川大学生命科学学院植物学2005试题资料下载141.四川大学生命科学学院生物学2000试题资料下载142.四川大学生命科学学院植物学2004试题资料下载143.四川大学生命科学学院植物生理学2005试题资料下载144.四川大学生命科学学院生物综合2005试题资料下载145.四川大学生命科学学院细胞生物学2000试题资料下载146.四川大学生命科学学院生物综合2003试题资料下载147.四川大学生命科学学院生物学2003试题资料下载148.四川大学生命科学学院生物学2005试题资料下载149.四川大学生命科学学院生物学2004试题资料下载150.四川大学生命科学学院细胞生物学2003试题资料下载。




四川大学工科物理化学考试题A 卷(2007-2008第1期)一、选择题:(每小题2分,共30分,每小题只能选择一个答案) 1、体系经绝热不可逆膨胀ΔS > 0,经绝热不可逆压缩则体系的A. ΔS > 0B. ΔS = 0C. ΔS < 0D. ΔS 的值无法确定 2、1mol 理想气体绝热向真空膨胀,何种扩大1倍,则此过程A. ΔS 体系 +ΔS 环境 = 0,ΔS 环境 < 0B. ΔS 体系 +ΔS 环境 > 0,ΔS 环境 = 0C. ΔS 体系 +ΔS 环境 < 0,ΔS 环境 = 0D. ΔS 体系 +ΔS 环境 = 0,ΔS 环境 > 03、某体系经历一不可逆循环后,下列关系式中不成立的是A. W=0B. ΔC p = 0C. ΔU=0D. ΔT=04、已知反应C(s)+O 2(g)=CO 2(g)的Or m H (298.15K)=-393.51kJ.mol -1,若此反应在一绝热钢瓶中进行,则此过程的A. ΔT =0,ΔU=0,ΔH<0B. ΔT >0,ΔU>0,ΔH=0C. ΔT >0,ΔU=0,ΔH<0D. ΔT >0,ΔU=0,ΔH>05、某均相化学反应A+B →C 经如下两个途径①在恒压,绝热,非体积功为零的条件下进行,系统的温度,由T 1升高到T 2,此过程的焓变为ΔH 1;②在恒温、恒压、非体积功为零的条件下进行,此过程的焓变为ΔH 2,则有A. ΔH 1>0, ΔH 2>0B. ΔH 1=0, ΔH 2=0C. ΔH 1=0, ΔH 2<0D. ΔH 1=0, ΔH 2>06、当某溶质溶解于某溶剂形成一定浓度的溶液时,若采用不同的浓标,则下列描述溶质的说法中正确的是A. 浓度数据相同B. 活度数据相同C. 活度系数相同D. 化学势相同 7、下列偏导数中,( )不是化学势。

复习必备川大工科物理化学考试试题A 卷(2007-2008年2学期) 川大学子专用一 选择题 每小题2分,共40分。
1、在一抽空的器中放入过量的NH 4HCO 3(S ),加热时反应NH 4HCO 3(S )=NH3(g )+NH 3(g)+H 2O(g)+CO 2(g)达到平衡,则该系统的独立组分数C 和自由度数F 为,A .1,2B .2,1C .2,2 D1,12、物质A 与B 可形成低共沸混合物E 。
已知纯A 的沸点小于纯B 的沸点。
若将任意比例的A+B 混合物在一个精馏,在塔顶的馏出物是A .纯AB .纯BC .低共沸混合物D .都有可能3、二元液系相图中,共沸点的自由度数F 为A .0 B.1 C.2 D.34、当克拉佩龙-克劳修斯方程应用与液相变为气相时,则A .P 必随T 的升高而减小 B.P 不随T 的升高而改变C .P 必随T 的升高而变大 D.P 随T 的升高可变大或减小5、组分A 和B 可以形成以下几种化合物:A 2B (s )、AB (s )、AB 2(s )和AB 3(s ),则此A-B 系统的低共点最多有A .2个 B.3个 C.4个 D.5个6、电池在恒温、恒压下可逆放电2F 与以一定的电压放电2F ,二者相比不同的有:A .电池反应的r m H ∆B .电池反应的r m G ∆C .电池反应的r m S ∆D .对环境作的电功W7、已知Ti ++e →Ti 的3(1)0.34,3E V Ti e Ti θ+=-+→的(2)0.72E V θ=则32Ti e Ti +++→的(3)E θ是A .2.50VB .1.25VC .1.06VD .0.38V8、下列哪组电极的组合可计算AgC1的标准摩尔生成吉布斯函数?A .Ag +/Ag 和C1-/AgC1/AgB .Ag +/Ag 和Cl 2/C1-C .C1-/AgC1/Ag 和Cl 2/C1-D .三者都不可以9.已知121()50.1110,x x m m Na Sm mol OH Sm mol +-+∧=⨯∧=⨯ ()NaOH t OH ∞在无限稀的溶液是A .0.202 B. 0.253 C .0.798 D. 110.在下述电池中,电池电动势与氯离子活度无关的是:A 。

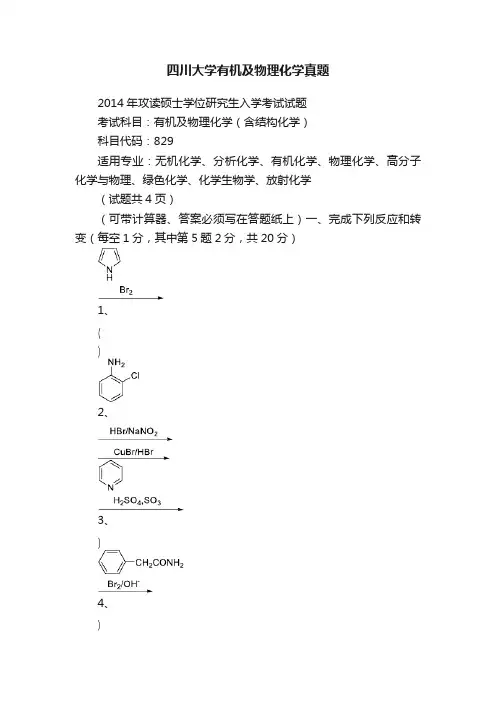
四川大学有机及物理化学真题2014年攻读硕士学位研究生入学考试试题考试科目:有机及物理化学(含结构化学)科目代码:829适用专业:无机化学、分析化学、有机化学、物理化学、高分子化学与物理、绿色化学、化学生物学、放射化学(试题共4页)(可带计算器、答案必须写在答题纸上)一、完成下列反应和转变(每空1分,其中第5题2分,共20分)1、2、3、4、5、6、7、8、9、10、111213、14二、(23分)由制定原料和必要试剂完成下列转变1、由苯出发合成1,3,5-三溴苯2、由苯胺制备对溴苯胺3、由β-甲基吡啶合成β-氨基吡啶4、由正溴丁烷为原料合成正丁胺,要求不含其它胺5、三、(10分)用化学方法鉴别下列物质,写出鉴别过程、现象1、D-麦芽糖,D-果糖,蔗糖,淀粉2、苯胺,苯酚,环己胺四、(10分)推测反应机理1、2、五、(10分)推测结构1、某化合物A 分子式为C 10H 15N 能溶于稀盐酸,与亚硝酸作用放出氮气得B ,B 与浓硫酸共热得C ,C 进行臭氧化得乙醛和一残留物D ,化合物D 在红外图谱的1900~1650cm -1范围内有一强特征吸收峰,且能发生碘仿反应,得苯甲酸。
写出A,B,C,D 的结构式,并用反应式说明推断过程。
2、两个具有旋光性的化合物A 和B ,与苯肼作用生成相同的糖脎。
A ,B 用硝酸氧化后,A 和B 都生成含有四个碳原子的二元酸,但A 氧化后得到的二元酸有旋光性,B 氧化后得到的二元酸没有旋光性,写出A ,B 的结构式,并用反应式说明推断过程。
六、(9分)如下图所示的绝热容器,用销钉固定的绝热隔板将容器分为两部分,隔板两边装有理想气体He 和N 2,初始状态如图。
若将隔板换成一块铝板(销钉仍保持固定),体系最终将达热平衡,求此过程的?U 、?H 和?S ,并判断过程是否自发?七、(14分)H 2O(A)-NaI(B)体系的固液平衡相图如右图所示:(1)、标出各区域的相态(2)、试绘出物系a 、b 冷却过程中的步冷曲线(3)、以0o C 纯水为标准态,求10%的NaI 水溶液温度降低至-10.7o C (此时冰与饱和溶液平衡共存)饱和溶液中水的活度,已知水的凝固热为-600.8-?1J mol八、(10分)298K 时测定0.001-?3mol dm 24Na SO 溶液的电导率κ--=??211 2.610S m ,已知∞+--Λ=321m (Na ) 5.010S m mol ,∞+--Λ=2321m 1(Ca ) 6.010S m mol 2,以上溶液可视为无限稀释。

目 录
2014年四川大学890有机化学考研真题(试题不全)2013年四川大学890有机化学考研真题
2012年四川大学890有机化学考研真题
2010年四川大学890有机化学考研真题
2009年四川大学890有机化学考研真题
2008年四川大学890有机化学考研真题
2007年四川大学890有机化学考研真题
2006年四川大学886有机化学考研真题
2005年四川大学886有机化学考研真题
2004年四川大学886有机化学考研真题
2003年四川大学855有机化学考研真题
2002年四川大学471有机化学考研真题
2001年四川大学471有机化学考研真题
2000年四川大学471有机化学考研真题
2014年四川大学890有机化学考研真题(试
题不全)。


四川大学下期工科物理化学考试试题A卷一、选择题:1.对复杂反应中的中间物应用近似稳态法的条件是(A)中间物不活泼,浓度很大且浓度变化很大。
(B)中间物不活泼,浓度很小且浓度变化很小。
(C)中间物很活泼,浓度很小且浓度变化很小。
(D)中间物很活泼,浓度很大且浓度变化很大。
2.表观速率方程中的反应级数是一个实验结果,它的取值(A)只能是正数。
(B)只能是负数。
(C)只能是小数。
(D)可能是任何值。
3.利用微分法确定反应级数的依据是(A)在不同时刻,系统的反应速率不同。
(B)反应级数不随反应物初浓度改变。
(C)反应速率不随反应时间改变。
(D)在不同时刻,系统的反应速率之比等于反应物浓度的幂函数之比。
4.在室温和无催化剂存在时,N2和H2可视为不起反应的。
今在一容器中任意充入N2,H2和NH3三种气体,则该物系中物种数S和组分数C将是(A)S=3,C=1(B)S=3,C=2(C)S=3,C=3(D)S=2,C=35.在抽空密闭容器中加热NH4Cl(s),有一部分分解成NH3(g)和HCl(g),当物系建立平衡时,其组分数C和自由度F是(A)C=1,F=1(B)C=2,F=2(C)C=3,F=3(D)C=2,F=16.在克拉配龙方程dp/dT=⊿H/T⊿V中(A)⊿H和⊿V的符号可相同或不同。
(B)⊿H和⊿V的符号必定是相同的。
(C)⊿H和⊿V的符号必定是不同的。
(D)⊿H和⊿V的数值必定相等。
7.当克拉配龙-克劳修斯方程应用于液相转变为气相时,则(A)p必随T的升高而减小。
(B)p不随T的升高而变(C)p必随T的升高而变大。
(D)p随T的升高可变大或减小。
8.在-20℃,101.325KPa条件下,1mol水结冰,则系统,环境和总熵变为(A)⊿S(系)<0,⊿S(环)<0,⊿S(总)<0。
(B)⊿S(系)>0,⊿S(环)>0,⊿S(总)>0。
(C)⊿S(系)<0,⊿S(环)>0,⊿S(总)<0。
(D)⊿S(系)<0,⊿S(环)>0,⊿S(总)>0。
第一章热力学第一定律练习题一、判断题(说法对否):1.道尔顿分压定律,对理想气体和实际混合气体来说关系式P B =n B (RT/V)都成立。
2.在两个封闭的容器中,装有同一种理想气体,若两个容器中压力、体积相同,那么温度也相同。
3.物质的温度越高,则热量越多;天气预报:天气很热。
其热的概念与热力学相同。
4.恒压过程也就是恒外压过程,恒外压过程也就是恒压过程。
5.实际气体在恒温膨胀时所做的功绝对值等于所吸收的热。
6.凡是温度升高的过程体系一定吸热;而恒温过程体系不吸热也不放热。
7.当系统的状态一定时,所有的状态函数都有一定的数值。
当系统的状态发生变化时,所有的状态函数的数值也随之发生变化。
8.在P ө、100℃下有lmol 的水和水蒸气共存的系统,该系统的状态完全确定。
9.一定量的理想气体,当热力学能与温度确定之后,则所有的状态函数也完全确定。
10.从同一始态经不同的过程到达同一终态,则Q 和W 的值一般不同,Q +W 的值一般也不相同。
11.因Q P =ΔH ,Q V =ΔU ,所以Q P 与Q V 都是状态函数。
12.封闭系统在压力恒定的过程中吸收的热等于该系统的焓。
13.对于一定量的理想气体,当温度一定时热力学能与焓的值一定,其差值也一定。
14.在101.325kPa 下,1mol l00℃的水等温蒸发为100℃的水蒸气。
若水蒸气可视为理想气体,那么由于过程等温,所以该过程ΔU =0。
15.1mol ,80.1℃、101.325kPa 的液态苯向真空蒸发为80.1℃、101.325kPa 的气态苯。
已知该过程的焓变为30.87kJ ,所以此过程的Q =30.87kJ 。
16.1mol 水在l01.325kPa 下由25℃升温至120℃,其ΔH =∑C P ,m d T 。
17.因焓是温度、压力的函数,即H =f (T ,p ),所以在恒温、恒压下发生相变时,由于d T =0,d p =0,故可得ΔH =0。
四川大学有机化学试卷班级姓名分数一、选择题( 共32题64分)1. 2 分(0037)0037CH3CH2CH2CH2+(I),CH3CH+CH2CH3(II),(CH3)3C+(Ⅲ)三种碳正离子稳定性顺序如何(A) I>II>III (B) III>II>I (C) II>I>III (D) II>III>I2. 2 分(0038)0038HBr与3,3-二甲基-1-丁烯加成生成2,3-二甲基-2-溴丁烷的反应机理是什么(A)碳正离子重排(B) 自由基反应(C) 碳负离子重排(D) 1,3-迁移3. 2 分(0039)0039环己烯加氢变为环己烷的热效应如何(A) 吸热反应(B) 放热反应(C) 热效应很小(D) 不可能发生4. 2 分(0040)0040下列化合物中哪些可能有E,Z异构体(A)2-甲基-2-丁烯(B) 2,3-二甲基-2-丁烯(C) 2-甲基-1-丁烯(D) 2-戊烯5. 2 分(0041)0041下列化合物中哪些可能有顺反异构体(A) CHCl=CHCl (B) CH2=CCl2(C) 1-戊烯(D) 2-甲基-2-丁烯6. 2 分(0042)0042烯烃加I2的反应不能进行,原因是:(A) I─I太牢固不易断裂(B) C─I不易生成(C) I+不易生成(D) 加成过程中C─C键易断裂7. 2 分(0043)0043实验室中常用Br2的CCl4溶液鉴定烯键,其反应历程是:(A)亲电加成反应(B) 自由基加成(C) 协同反应(D) 亲电取代反应8. 2 分(0044)0044测定油脂的不饱和度常用碘值来表示,测定时所用试剂为:(A) I2(B) I2 + Cl2(C) ICl (D) KI9. 2 分(0045)0045烯烃与卤素在高温或光照下进行反应,卤素进攻的主要位置是:(A)双键C原子(B) 双键的α-C原子(C) 双键的β-C原子(D) 叔C原子*. 2 分(0046)0046实验室制备丙烯最好的方法是:(A)石油气裂解(B) 丙醇脱水(C) 氯丙烷脱卤化氢(D) Wittig反应11. 2 分(0049)0049CH3CH=CH2 + Cl2 + H2O :(A) CH3CHClCH2Cl + CH3CHClCH2OH (B) CH3CHOHCH2Cl + CH3CHClCH2Cl (C) CH3CHClCH3 + CH3CHClCH2OH (D) CH3CHClCH2Cl12. 2 分(0052)0052某烯烃经臭氧化和还原水解后只得CH3COCH3,该烯烃为:(A) (CH3)2C=CHCH3(B) CH3CH=CH2(C) (CH3)2C=C(CH3)2(D) (CH3)2C=CH213. 2 分(0053)0053CH3CH=CHCH2CH=CHCF3 + Br2 (1 mol) 主要产物为:(A) CH3CHBrCHBrCH2CH=CHCF3(B) CH3CH=CHCH2CHBrCHBrCF3 (C) CH3CHBrCH=CHCH2CHBrCF3(D) CH3CHBrCH=CHCHBrCH2CF314. 2 分(0054)0054CH2=CHCOOCH=CH2 + Br2 (1 mol) 主要产物为:(A) CH2BrCHBrCOOCH=CH2(B) CH2=CHCOOCHBrCH2Br (C) CH2BrCOOCH=CHCH2Br (D) CH2BrCH=CHCOOCH2Br15. 2 分(0055)0055ROCH=CH2 + HI 主要产物为:(A) ROCH2CH2I (B) ROCHICH3(C) ROH + CH2=CH2(D) RCH=CH2 +HOI16. 2 分(0056)0056CF3CH=CHCl + HI 主要产物为:(A) CF3CH2CHClI (B) CF3CHICH2Cl(C) CF3I + CH2=CHCl (D) CF3Cl + CH2=CHI17. 2 分(0057)0057(CH3)2C=CCl2 +HI 主要产物为:(A) (CH3)2CH―CCl2I (B) (CH3)2CI―CHCl2(C) CH3CH=CCl2 + CH3I (D) (CH3)2C=CClI + HCl18. 2 分(0061)0061分子式为C7H14的化合物G与高锰酸钾溶液反应生成4-甲基戊酸,并有一种气体逸出, G 的结构式是:(A) (CH3)2CHCH2CH2CH=CH2(B) (CH3)3CCH=CHCH3(C) (CH3)2CHCH=C(CH3)2(D) CH3CH2CH=CHCH(CH3)219. 2 分(0066)00661-甲基环己烯+ HBr 反应的主要产物是:(A) 1-甲基-1-溴代环己烷(B) 顺-2-甲基溴代环己烷(C) 反-2-甲基溴代环己烷(D) 1-甲基-3-溴环己烷20. 2 分(0068)0068由CH3CH2CH2Br 3CHBrCH3,应采取的方法是:(A) ①KOH,醇;②HBr,过氧化物(B) ①HOH,H+;②HBr(C) ①HOH,H+;②HBr,过氧化物(D) ①KOH,醇;②HBr21. 2 分(0071)00713-甲基-1-丁烯与HBr反应的主要产物是什么(A) 2-甲基-3-溴丁烷与2-甲基-2-溴丁烷(B) 3-甲基-2-溴丁烷与3-甲基-1-溴丁烷(C) 3-甲基-1-溴丁烷(D) 3-甲基-2-溴丁烷22. 2 分(0076)0076烃C6H12能使溴溶液褪色,能溶于浓硫酸,催化氢化得正己烷,用酸性KMnO4氧化得二种羧酸,则该烃是:(A) CH3CH2CH=CHCH2CH3(B) (CH3)2CHCH=CHCH3(C) CH3CH2CH2CH=CHCH3(D) CH3CH2CH2CH2CH=CH223. 2 分(0077)0077在碳烯(carbene)与烯烃的加成反应中,三线态比单线态的立体定向性差的原因是什么(A) 三线态能量高,易发生副反应(B) 三线态能量低,不易起反应(C) 三线态易转化为单线态(D) 三线态的双价自由基分步进行加成24. 2 分(0078)0078下列哪种化合物进行催化氢化后不能得到丁烷(A) 1-丁烯(B) (Z)-2-丁烯(C) (E)-2-丁烯(D) 2-甲基-2-丁烯25. 2 分(0079)0079卤化氢HCl(I),HBr(II),HI(III)与烯烃加成时,其活性顺序为:(A)I>II>III (B) III>II>I(C) II>I>III (D) II>III>I26. 2 分(0080)00802-甲基-2-丁烯与HI加成的主要产物是:(A) (CH3)2CICH2CH3(B) (CH3)2CHCHICH3(C) (CH3)2CHCH2CH2I (D) (CH3)2CHCH=CH227. 2 分(0081)00811-戊烯与HBr加成的主要产物是:(A) CH3CH2CH2CH2CH2Br (B) CH3CH2CH=CHCH3(C) CH3CH2CH2CHBrCH3(D) CH3CH2CHBrCH2CH328. 2 分(0082)0082丙烯与HBr加成,有过氧化物存在时,其主要产物是:(A)CH3CH2CH2Br (B) CH3CH2BrCH3(C) CH2BrCH=CH2(D)( B), (C) 各一半29. 2 分(0084)0084用下列哪种方法可由1-烯烃制得伯醇(A)H2O (B) 浓H2SO4,水解(C) ①B2H6;②H2O2,OH-(D) 冷、稀KMnO430. 2 分(0085)0085某烯烃经酸性KMnO4氧化,得到CH3COCH3和(CH3)2CHCOOH,则该烯烃结构是: (A) (CH3)2C=C(CH3)2(B) (CH3)2C=CHCH(CH3)2(C) (CH3)2CHCH=CH2(D) (CH3)2CHCH=CHCH(CH3)231. 2 分(0086)0086某烯烃经臭氧化和水解后生成等物质的量的丙酮和乙醛,则该化合物是: (A) (CH3)2C=C(CH3)2(B) CH3CH=CHCH3(C) (CH3)2C=CHCH3(D) (CH3)2C=C=CH232. 2 分 (0177)0177CH 3CH =CHCH 3与CH 3CH 2CH =CH 2是什么异构体 (A) 碳架异构 (B) 位置异构(C) 官能团异构 (D) 互变异构二、填空题 ( 共18题 36分 ) 33. 2 分 (1413)1413化合物(E )-3,4-二甲基-2-戊烯的结构式是:34. 2 分 (1414)1414化合物(E)-4,4-二甲基-2-戊烯的结构式是:35. 2 分 (1415)1415化合物(Z )-3-甲基-4-异丙基-3-庚烯的结构式是:36. 2 分 (1342) 1342写出下列反应的主要有机产物或所需之原料和试剂(如有立体化学问题请注明)。
2014年攻读硕士学位研究生入学考试试题
考试科目:有机及物理化学(含结构化学)
科目代码:829
适用专业:无机化学、分析化学、有机化学、物理化学、高分子化学与物理、绿色化学、化学生物学、放射化学
(试题共4页)
(可带计算器、答案必须写在答题纸上)一、完成下列反应和转变(每空1分,其中第5题2分,共20分)
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11
12
13、
14
二、(23分)由制定原料和必要试剂完成下列转变
1、由苯出发合成1,3,5-三溴苯
2、由苯胺制备对溴苯胺
3、由β-甲基吡啶合成β-氨基吡啶
4、由正溴丁烷为原料合成正丁胺,要求不含其它胺
5、
三、(10分)用化学方法鉴别下列物质,写出鉴别过程、现象
1、D-麦芽糖,D-果糖,蔗糖,淀粉
2、苯胺,苯酚,环己胺
四、(10分)推测反应机理
1、
2、
五、(10分)推测结构
1、某化合物A 分子式为C 10H 15N 能溶于稀盐酸,与亚硝酸作用放出氮气得B ,B 与浓硫酸共热得C ,C 进行臭氧化得乙醛和一残留物D ,化合物D 在红外图谱的1900~1650cm -1范围内有一强特征吸收峰,且能发生碘仿反应,得苯甲酸。
写出A,B,C,D 的结构式,并用反应式说明推断过程。
2、两个具有旋光性的化合物A 和B ,与苯肼作用生成相同的糖脎。
A ,B 用硝酸氧化后,A 和B 都生成含有四个碳原子的二元酸,但A 氧化后得到的二元酸有旋光性,B 氧化后得到的二元酸没有旋光性,写出A ,B 的结构式,并用反应式说明推断过程。
六、(9分)如下图所示的绝热容器,用销钉固定的绝热隔板将容器分为两部分,隔板两边装有理想气体He 和N 2,初始状态如图。
若将隔板换成一块铝板(销钉仍保持固定),体系最终将达热平衡,求此过程的∆U 、∆H 和∆S ,并判断过程是否自发?
七、(14分)H 2O(A)-NaI(B)体系的固液平衡相图如右图所示: (1)、标出各区域的相态 (2)、试绘出物系a 、b 冷却过程中的步冷曲线 (3)、以0o C 纯水为标准态,求10%的NaI 水溶液温度降低至-10.7o C (此时冰与饱和溶液平衡共存)饱和溶液中水的活度,已知水的凝固热为-600.8-⋅1J mol
八、(10分)298K 时测定0.001-⋅3mol dm 24Na SO 溶液的电导率κ--=⨯⋅211 2.610S m ,
已知∞+--Λ=⨯⋅⋅321m (Na ) 5.010S m mol ,∞+--Λ=⨯⋅⋅2321m 1(Ca ) 6.010S m mol 2
,以上溶液可
视为无限稀释。
(1)、求298K 时的∞
Λm 24(Na SO ),λ∞-2m 4(SO )和∞Λm 4(CaSO ); (2)、该溶液饱和了4CaSO 后电导率κ--=⨯⋅2127.010S m ,求难溶盐4CaSO 的活度积常数ΘK ,说明标准态浓度Θc 的取值。
1mol He(g) 200K, 1mol N 2(g) 300K,
-40
-20 0 20 40 60 80 100
0 20 40 60 80 100 H 2O NaI A B
BA 5 BA 2
6 a b 1 2 3 4
5
7 8
九、(12分)在300K 研究反应+→+2A 2B 2C 2D ,假设其速率方程为β=2[A ][B]r k (1)、当2A 、B 的初始浓度分别为0.0100-⋅3mol dm 和0.0200-⋅3mol dm 时,测得反应物B 在不同时刻的浓度数据如下:
t/s 0
90 268 [B]/-⋅3mol dm
0.0200
0.0100
0.0050
求该反应的总级数,以及反应的速率常数k 。
(2)、320K 时研究上述反应,当2A 、B 的初始浓度均为0.020-⋅3mol dm 时,实验测定初始反应速率0,2r 为实验(1)中测定初始反应速率0,1r 的5倍,求反应的活化能a E 。
(3)、假设反应机理为:
+→+→12
2
3
k 22k k 2k 2快速平衡 慢平衡(i)A B
A B
(ii)A B 2C
(iii)A B B 2 D
快反应
2A B 是中间物,试推导反应速率方程表达式。
十、(15分)世界卫生组织规定,汞蒸气在31m 空气中最高允许含量为-⨯51.0010g 。
已知
M(Hg)=0.2006-⋅1kg mol ,-∆=⋅g *1l m 60.668kJ mol
H ,=(Hg,298K)0.160Pa p ,蒸气中汞为单原子,设汞蒸气为理想气体,298K 时热力学数据如下:
Hg(l) S(s) HsS(s) Θ
-∆⋅1f m /kJ mol H
0 0 -58.16 Θ-⋅⋅1-1m /J mol K S
76.02
31.8
82.4
(1)、303K ,Hg(l)与其蒸气呈平衡,求算空气中Hg 的含量是否超过所规定的最高允许含
量。
(2)、298K 时,学生在使用汞时不小心将汞撒在桌面上,用过量的硫磺粉来清除残留的Hg ,设反应为:+=Hg(l)S(s)HgS(s),请从热力学角度说明能否清除尽?
(3)、298K 时,把HCl 的水溶液与Hg 和HgO 混合,溶液中生成22Hg Cl ,摇动达平衡时,---=⨯⋅23[Cl ]9.98410mol dm ,---=⨯⋅43[OH ] 1.40910mol dm ,求298K 时水的w K 。
已知298K 时电池:
ΘΘ
==2212222(i)Pt|H (g)|KOH(aq)|H O(s)|Hg(l)
0.9264V
(ii)Pt|H (g)|KCl(aq)|Hg Cl (s)|Hg(l)0.2676V
E E
十一、(15分)在酶的作用下,人体内会产生超氧离子-
2O 、羟基自由基⋅OH 、过氧化氢22H O 及单线态12O 等活性氧物种。
这些活性氧物种若在体内积聚过多,有使人衰老,患炎症甚至癌变等不良影响。
(1)、写出22H O 的结构式,确定分子中各原子的氧化数。
(3分) (2)、判断两种分子22H O 和2O 所属点群。
(4分)
(3)、写出⋅OH 、-2O 及12O 的电子组态,计算键级,确定化学键,HOMO ,LUMO 及磁性
质,比较他们化学活泼性大小。
(8分)。