滴定分析法
- 格式:ppt
- 大小:319.00 KB
- 文档页数:76


滴定分析法百科名片滴定分析法,是化学分析法的一种,将一种已知其准确浓度的试剂溶液(称为标准溶被)滴加到被测物质的溶液中,直到化学反应完全时为止,然后根据所用试剂溶液的浓度和体积可以求得被测组分的含量,这种方法称为滴定分析法(或称容量分析法)。
目录[隐藏]简介特点分类原理简介特点分类原理[编辑本段]简介滴定分析法,又叫容量分析法,将已知准确浓度的标准溶液,滴加到被测溶液中(或者将被测溶液滴加到标准溶液中),直到所加的标准溶液与被测物质按化学计量关系定量反应为止,然后测量标准溶液消耗的体积,根据标准溶液的浓度和所消耗的体积,算出待测物质的含量。
这种定量分析的方法称为滴定分析法,它是一种简便、快速和应用广泛的定量分析方法,在常量分析中有较高的准确度。
[编辑本段]特点1. 加入标准溶液物质的量与被测物质的量恰好是化学计量关系;2. 此法适于组分含量在1%以上各种物质的测定;3. 该法快速、准确、仪器设备简单、操作简便;4.用途广泛。
[编辑本段]分类根据标准溶液和待测组分间的反应类型的不同,分为四类1. 酸碱滴定法——以质子传递反应为基础的一种滴定分析方法2. 配位滴定法——以配位反应为基础的一种滴定分析方法3. 氧化还原滴定法——以氧化还原反应为基础的一种滴定分析方法4. 沉淀滴定法——以沉淀反应为基础的一种滴定分析方法[编辑本段]原理滴定滴定分析法是将一种已知准确浓度的试剂溶液,滴加到被测物质的溶液中,直到所加的试剂与被测物质按化学计量定量反应为止,根据试剂溶液的浓度和消耗的体积,计算被测物质的含量。
这种已知准确浓度的试剂溶液称为滴定液。
将滴定液从滴定管中加到被测物质溶液中的过程叫做滴定。
当加入滴定液中物质的量与被测物质的量按化学计量定量反应完成时,反应达到了计量点。
在滴定过程中,指示剂发生颜色变化的转变点称为滴定终点。
滴定终点与计量点不一定恰恰符合,由此所造成分析的误差叫做滴定误差。
具备条件适合滴定分析的化学反应应该具备以下几个条件:(1)反应必须按方程式定量地完成,通常要求在99.9%以上,这是定量计算的基础。

滴定分析法3.2滴定分析法3.2.1 滴定分析法的特点与分类滴定分析法是将一种已知准确浓度的试剂溶液,通过滴定管滴加到被测物质的溶液中,获奖被测物质的溶液滴加到已知准确浓度的溶液中,直到所加的试剂溶液与被测物质按化学计量关系完全反应为止,根据所用试剂溶液的浓度和消耗的体积,计算被测物质含量的方法。
这种分析方法的操作手段主要是滴定,因此称为滴定分析法。
又因这一类分析方法是以测量容积为基础的分析方法,所以又称容量分析法。
已知准确浓度的试剂融液称为标准溶液(又称为滴定剂或滴定液)。
将标准溶液从滴定管中滴加到被测物质溶液中的操作过程称为滴定。
当加入的标准溶液中物质的量与被测组分物质的量恰好符合化学反应时所表示的化学计量关系时,称为反应达到化学计量点,亦称等量点或等当点。
许多滴定反应在到达化学计量点时外观上没有明显的变化,为了确定化学计量点的到达,在实际滴定操作时,常在被测物质的溶液中加入一种辅助试剂,借助于其颜色变化作为化学计量点到达的标志,这种能通过颜色变化指示剂到达化学计量点的辅助试剂称为指示剂。
在滴定过程中,指示剂发生颜色变化的转变点成为滴定终点。
化学计量点是根据化学反应的计量关系求得的理论值,而滴定终点是实际滴定时的测量值,只有在理想情况下滴定终点才能完全一致。
在实际测定中,指示剂往往不是恰好在到达化学计量点的一瞬间变色,两者不一定完全符合,这种由滴定终点与化学计量点不一定恰好符合而造成的分析误差称为终点误差或滴定误差。
它的大小取决于化学反应的完全程度和指示剂的选择是否恰当。
因此,为了减小终点误差,应选择合适的指示剂,使滴定终点尽可能接近化学计量点。
滴定分析法通常适用于被测组分的含量在1%以上的常量组分的分析,具有操作简便、快速、所用仪器简单、准确、价格便宜的特点。
一般情况下相对平均偏差在0.2%以下。
各测量值及分析结果的有效数字位数为四位。
根据标准溶液与被测物质间所发生的化学反应类型不同,将滴定分析法分为酸碱滴定法(又称中和法)、沉淀滴定法、配位滴定法和氧化还原滴定法四大类。


滴定分析的分析方法滴定分析是一种常用的分析方法,它通过溶液中的酸碱反应进行定量分析。
滴定分析的基本原理是根据酸碱中和反应的化学方程式和定量关系,通过滴定液的加入,确定滴定点的位置,从而计算出待测溶液中溶质的浓度或化学计量数。
滴定分析的基本步骤包括:准确量取待测溶液,加入适当的指示剂,利用滴定管从滴定瓶中加入滴定液,当待测溶液中的溶质已与滴定液发生完全反应时,滴定反应到达终点,在滴定瓶中滴加过量的滴定液,直至指示剂颜色发生明显变化。
通过滴定液的用量(滴定体积)和滴定液的浓度,可以计算出待测溶液中溶质的浓度或化学计量数。
滴定分析可以分为酸碱滴定、氧化还原滴定、络合滴定和沉淀滴定等不同的类型。
下面将分别介绍这些类型的滴定分析方法。
1. 酸碱滴定:酸碱滴定是最常见的滴定分析方法,用于测定待测溶液中的酸或碱的浓度。
常用的滴定酸碱对有酸钠溶液对标准酸和碳酸钠溶液对标准碱。
滴定结束时,滴定液与待测溶液达到化学计量比例,pH值发生明显变化。
2. 氧化还原滴定:氧化还原滴定是利用氧化还原反应进行定量分析的方法。
常见的氧化还原滴定有碘量法、亚铁量法和过氧化氢量法等。
滴定过程中,滴定剂与待测溶液发生氧化还原反应,溶液颜色或电位发生明显变化。
3. 络合滴定:络合滴定是利用配位化学中金属离子与配体的配位反应进行定量分析的方法。
常见的络合滴定有硬络合滴定、铁计法和EDTA滴定等。
滴定时,滴定剂与待测溶液中的金属离子或配体形成稳定的络合物,滴定剂与待测溶液达到化学计量比例后,化学指示剂的颜色发生明显变化。
4. 沉淀滴定:沉淀滴定是利用沉淀反应进行定量分析的方法。
常见的沉淀滴定有氯化银沉淀滴定和氯化钡沉淀滴定等。
滴定时,滴定剂与待测溶液中的阳离子或阴离子发生反应,生成可见的沉淀物,从而判断滴定结束的标志。
在进行滴定分析时,有一些基本的实验技巧需要注意。
首先,需要准确量取待测溶液和滴定液,使用准确的量杯或容量瓶,并控制好温度和湿度。

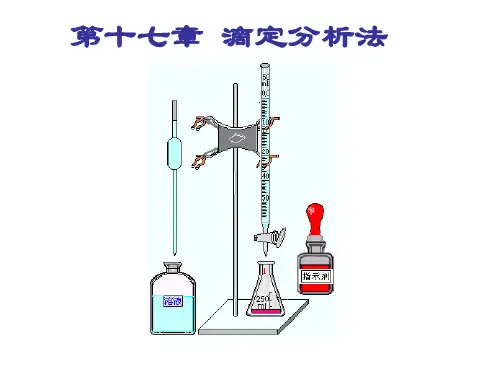

分析化学四大滴定总结滴定分析法又称为容量分析法,是一种简便、快速和应用广泛的定量分析方法,在常量分析中有较高的准确度。
这其中又有重要的四大滴定方法。
以下是店铺整理的分析化学四大滴定总结,欢迎查看。
一、酸碱滴定原理:利用酸和碱在水中以质子转移反应为基础的滴定分析方法。
可用于测定酸、碱和两性物质。
其基本反应为H﹢+OH﹣=H2O也称中和法,是一种利用酸碱反应进行容量分析的方法。
用酸作滴定剂可以测定碱,用碱作滴定剂可以测定酸,这是一种用途极为广泛的分析方法。
最常用的酸标准溶液是盐酸,有时也用硝酸和硫酸。
标定它们的基准物质是碳酸钠Na2CO3。
方法简介:最常用的碱标准溶液是氢氧化钠,有时也用氢氧化钾或氢氧化钡,标定它们的基准物质是邻苯二甲酸氢钾KHC8H4O6或草酸H2C2O·2H2O:OH+HC8H4O6ˉ→C8H4O6ˉ+H2O如果酸、碱不太弱,就可以在水溶液中用酸、碱标准溶液滴定。
离解常数 A和Kb是酸和碱的强度标志。
当酸或碱的浓度为0.1M,而且A或Kb大于10-7时,就可以准确地滴定,一般可准确至0.2%。
多元酸或多元碱是分步离解的,如果相邻的离解常数相差较大,即大于104,就可以进行分步滴定,这种情况下准精确度不高,误差约为1%。
盐酸滴定碳酸钠分两步进行:﹢ˉCO32-+H→HCO3HCO3ˉ+H﹢→CO2↑+H2O相应的滴定曲线上有两个等当点,因此可用盐酸来测定混合物中碳酸钠和碳酸氢钠的含量,先以酚酞(最好用甲酚红-百里酚蓝混合指示剂)为指示剂,用盐酸滴定碳酸钠至碳酸氢钠,再加入甲基橙指示剂,继续用盐酸滴定碳酸氢钠为二氧化碳,由前后消耗的盐酸的体积差可计算出碳酸氢钠的含量。
某些有机酸或有机碱太弱,或者它们在水中的溶解度小,因而无法确定终点时,可选择有机溶剂为介质,情况就大为改善。
这就是在非水介质中进行的酸碱滴定。
有的非酸或非碱物质经过适当处理可以转化为酸或碱。
然后也可以用酸碱滴定法测定之。

滴定分析法名词解释
滴定分析法是一种常用于测定物质含量的分析手段。
它通过加入一种已知浓度的试剂(称为滴定剂)来与待测物质进行反应,从而确定待测物质的含量。
在滴定分析法中,试样通常以溶液的形式存在。
首先,需要取适量的试样加入反应容器中。
然后,使用滴定管将滴定剂滴入试样溶液中,滴定过程中需要进行颜色指示。
当滴定剂与试样中的物质反应完全时,颜色发生突变,这时需要统计记录滴定剂的用量,从而确定试样中物质的含量。
滴定分析法有多种类型,其中最常见的是酸碱滴定法。
在酸碱滴定中,酸溶液的酸度可以通过滴定一定浓度的碱溶液来测定;同样地,碱溶液的碱度也可以通过滴定一定浓度的酸溶液来测定。
此外,氧化还原滴定法和络合滴定法也是常用的滴定分析方法。
滴定分析法的精确度主要依赖于滴定剂的浓度和试样的准确配制。
因此,在实际操作中需要注意滴定剂和试样的溶解度、匀浆度和温度等因素,以提高滴定分析的准确性。
滴定分析法广泛应用于化学、生物、医药等领域。
它可以用于分析酸碱度、氧化还原性质以及配位络合等方面的问题。
例如,在药学领域中,滴定分析法可用于测定药物的含量;在环境监测领域中,滴定分析法可以测定水样中各种污染物的含量。
总之,滴定分析法是一种常用且有效的分析手段,通过滴定剂
与试样反应的完全性来测定物质的含量。
滴定分析法准确度高,广泛应用于各个领域。
