[精品]2019年中考化学总复习 第五单元 化学方程式训练
- 格式:doc
- 大小:674.19 KB
- 文档页数:8
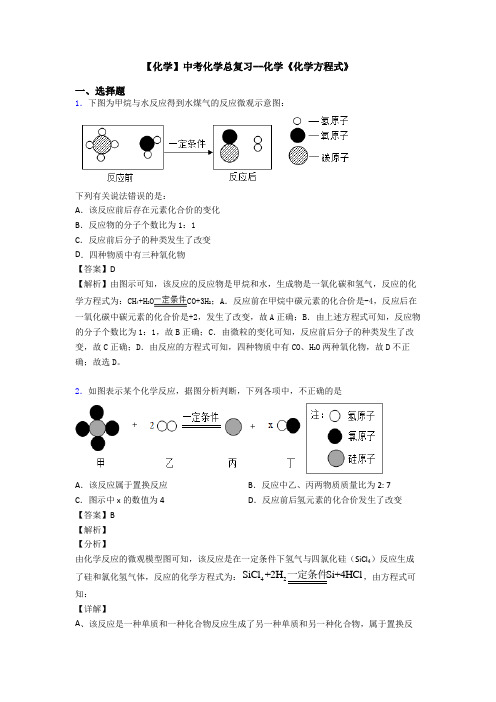
【化学】中考化学总复习--化学《化学方程式》一、选择题1.下图为甲烷与水反应得到水煤气的反应微观示意图:下列有关说法错误的是:A .该反应前后存在元素化合价的变化B .反应物的分子个数比为1:1C .反应前后分子的种类发生了改变D .四种物质中有三种氧化物【答案】D【解析】由图示可知,该反应的反应物是甲烷和水,生成物是一氧化碳和氢气,反应的化学方程式为:CH 4+H 2O CO+3H 2;A .反应前在甲烷中碳元素的化合价是-4,反应后在一氧化碳中碳元素的化合价是+2,发生了改变,故A 正确;B .由上述方程式可知,反应物的分子个数比为1:1,故B 正确;C .由微粒的变化可知,反应前后分子的种类发生了改变,故C 正确;D .由反应的方程式可知,四种物质中有CO 、H 2O 两种氧化物,故D 不正确;故选D 。
2.如图表示某个化学反应,据图分析判断,下列各项中,不正确的是A .该反应属于置换反应B .反应中乙、丙两物质质量比为2: 7C .图示中x 的数值为4D .反应前后氢元素的化合价发生了改变【答案】B【解析】【分析】 由化学反应的微观模型图可知,该反应是在一定条件下氢气与四氯化硅(SiCl 4)反应生成了硅和氯化氢气体,反应的化学方程式为:42SiCl +2H Si+4HCl 一定条件,由方程式可知:【详解】A 、该反应是一种单质和一种化合物反应生成了另一种单质和另一种化合物,属于置换反应,故A 正确;B 、反应中乙、丙两物质质量比就是氢气和硅的质量比为:(2×1×2):28=1:7,故B 不正确;C 、由方程式可知,图示中x 的数值为4,故C 正确;D 、由方程式可知,氢元素的化合价由0价变成了+1价,故D 正确。
故选B 。
3.某物质在空气中燃烧的化学方程式为2222X+3O 2CO +4H O 点燃,下列说法正确的是( )A .O 2中氧元素的化合价为﹣2B .该反应属于置换反应C .X 属于有机物D .CO 2中碳、氧元素的质量比为1:2【答案】C【解析】【详解】A 、单质中元素的化合价为零,错误;B 、该反应的生成物均为化合物,不属于置换反应,错误;C 、由2X+3O 22CO 2+4H 2O 可知,反应后碳原子是2个,反应前应该是2个,包含在2X 中;反应后氧原子是8个,反应前应该是8个,其中2个包含在2X 中;反应后氢原子是8个,反应前应该是8个,包含在2X 中;由分析可知,每个X 中含有1个碳原子、1个氧原子和4个氢原子,化学式是CH 4O ,为有机物,正确;D 、CO 2中碳、氧元素的质量比为:12:(16×2)=3:8,错误。


中考化学《第五单元化学方程式》巩固复习题(含详细答案解析)中考化学巩固复习-第五单元化学方程式(含详细答案解析)一、单选题1.下列图像的对应关系表示正确的是()A. 图甲表示电解水实验从开始到断开电源后这一过程中,产生的气体体积与反应时间的关系(不考虑气体在水中的溶解情况)B. 图乙表示两份完全相同的双氧水在有无MnO2的情况下,产生的O2质量m与反应时间t的关系C. 图丙表示碳在密闭容器内燃烧,容器内物质总质量m与反应时间t的关系D. 图丁表示加热一定质量的高锰酸钾,产生氧气质量m与加热时间t的关系2.如果用“”和“”分别表示氢原子和氧原子,则下列图中表示混合物的是( )A. B. C.D. 3.下列图像能正确反映其对应操作中某物质质量变化关系的是( )A. 加热氯酸钾和二氧化锰的混合固体B. 将一定质量的红磷放在盛有氧气的密闭容器中燃烧C. 将一定量的镁片和铝片分别和等质量、等溶质质量分数的稀硫酸混合D. 向氢氧化钠和氯化钡的混合溶液中滴加过量的稀硫酸 4.对下列事实解释正确的是()选项事实解释A水银温度计受热液柱升髙汞原子受热体积变大B食盐加入水中,水变咸了NaCl分子不断运动的结果C稀HCl、H2SO4都能使紫色石蕊试液变红溶液中都含有H+D金刚石和石墨的性质不同原子结构不同A. AB. BC. CD. D5.对以下三个化学反应的分析正确的是()C+O2CO24P+5O22P2O5CH4+O2CO2+H2O.A. 都属于化合反应 B. 反应温度都需达到着火点 C. 生成物均是气体 D. 反应时均产生蓝色火焰6.向质量为m克的CaCO3和KHCO3的混合物中,加入质量分数为a%的稀盐酸n克,恰好完全反应后,得到二氧化碳的质量是w克.(已知:KHCO3+HCl═KCl+H2O+CO2↑)下列说法正确的是()A. 混合物中CaCO3和KHCO3的质量比一定是1:1B. 混合物充分反应后,所得溶液的质量是(m+n某a%﹣w)克C. 混合物中CaCO3和KHCO3无论以任何比例混合,消耗稀盐酸的总质量均为n克D. 混合物中CaCO3和KHCO3无论以任何比例混合,生成二氧化碳的总质量均为w克7.在一个密闭容器中,充入a个CO分子和b个O2分子,在一定条件下充分反应后,容器内碳原子个数和氧原子个数之比是()A.B.C.D. 8.根据化学方程式4NH3+5O2 =“=“4某+6H2O,可推断某的化学式是( )A. NOB. NO2C.N2O3D. NH39.将6.96g铁的某种氧化物在高温下与足量的一氧化碳充分反应,生成5.28g二氧化碳,则这种铁的氧化物应该为()A. FeOB. Fe2O3C. Fe3O4D. 无法确定二、多选题10.如图四个图象中能正确反应其对应实验操作的是()A. 向等质量的铝粉和镁粉中分别滴入质量分数相同的足量的稀盐酸 B. 向一定量的氢氧化钡溶液中不断加入稀硫酸C. 等质量的块状石灰石和粉末状石灰石分别与质量分数相同的足量的稀盐酸反应 D. 碳和氧化铜的固体混合物在高温条件下反应11.在等质量的锌、铁中分别滴加等质量分数的稀硫酸至过量,产生氢气的质量随硫酸的质量变化曲线如图。


【化学】中考化学总复习∶化学方程式(提高)知识讲解及答案(word)一、化学方程式选择题1.火药是我国的四大发明之一。
已知某配方火药燃烧的化学方程式为S+2KNO3+3C K2S+N2↑+3X↑,则X的化学式为()A.CO B.NO C.CO2 D.SO2【答案】C【解析】【详解】反应物中硫、钾、氮、氧、碳原子的个数分别是1,4,2,6,3,生成物中硫、钾、氮、氧、碳原子的个数分别是1,2,2,0,0,故3X中含有6个氧原子,3个碳原子,故X中含有1个碳原子,2个氧原子,故X的化学式为CO2,故选C。
2.食盐不仅可以做调味品,还是一种重要的化工原料。
电解饱和食盐水,不可能得到的产物是()A.H2B.Cl2C.NaOH D.Na2CO3【答案】D【解析】【分析】根据化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和,是因为化学反应前后,元素的种类不变,原子的种类、总个数不变进行分析。
【详解】饱和食盐水中不含有碳元素,所以电解饱和食盐水不可能得到碳酸钠,故选D。
3.油画上的白色含铅颜料经过一段时间会变为黑色的硫化铅(PbS)。
使其恢复为白色的方法是蘸涂双氧水(H2O2),发生如下反应:PbS+4H2O2X+4H2O,其中X的化学式是( ) A.PbSO4B.PbSO2C.PbSO3D.PbHSO3【答案】A【解析】试题分析∶油画上的白色含铅颜料经过一段时间会变为黑色的硫化铅(PbS)。
使其恢复为白色的方法是蘸涂双氧水(H2O2),发生如下反应:PbS+4H2O2=X+4H2O,其中X的化学式是A.PbSO4考点∶考查质量守恒定律的应用。
4.已知:Ca(HCO3)2ΔCaCO3+CO2↑+H2O.下列图象表示一定质量的 Ca(HCO3)2受热过程中某些量随时间的变化趋势(该过程的 CaCO3不分解),其中不正确的是()A.B.C.D.【答案】C【解析】【分析】A、C、D选项根据碳酸氢该受热分解后生成碳酸钙、二氧化碳和水,固体质量减少分析;B选项根据质量守恒定律分析。

【化学】中考化学总复习--《化学方程式》一、选择题1.下图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子。
下列说法错误的是A.此反应有单质生成B.原子在化学变化中是不可分的C.图中生成物全部是化合物D.参加反应的两种分子的个数比为1∶1【答案】C【解析】【分析】【详解】A、反应后生成了一种由同种原子构成的单质分子,因此此反应有单质生成;故A正确;B、反应前共有三种原子,而反应后仍然是这三种原子,说明反应中原子不变,可推断得出化学变化中原子不可分;故B正确;C、反应的生成物为一种单质的分子和一种化合物的分子,生成物一种为化合物一种为单质;故C不正确;D、反应前的两种分子各有2个分子参加反应,因此参加反应的两种分子的个数比为1:1,故D正确。
故选C。
2.某有机物在空气中完全燃烧,测得生成物中含有二氧化碳、水蒸气、二氧化硫,下列对该有机物的组成推断正确的是()A.一定含碳、氢、硫元素B.一定含有碳、氢、氧元素C.只含碳、氢元素D.一定含碳、氢、氧元素,可能含有硫元素【答案】A【解析】【分析】【详解】物质+氧气 = 二氧化碳+水蒸气+二氧化硫,根据元素守恒,物质中一定含有碳、氢、硫元素,可能含氧元素,故选A。
3.氯气是一种有毒的气体,实验室制取氯气时,可以用氢氧化钠溶液来吸收尾气,其反应原理为Cl2 + 2NaOH = X + NaClO + H2O, 则X 的化学式为A.H2B.NaCl C.HCl D.HClO【答案】B【解析】【分析】【详解】书写化学式的时候应该遵循质量守恒定律,等号两侧每一种元素的原子总数应该相等。
反应物中一共有2个l C原子,2个Na原子,2个O原子,2个H原子;生成物中一共有1个Na原子,1个l C原子,2个H原子,2个O原子,相比反应物少1个Na原子和1个NaC,故B正确。
l C原子,所以X的化学式为l故选B。
4.将一定量xFeSO4•y(NH4)2SO4•6H2O晶体加入到过量NaOH溶液中,加热生成NH30.85g(假如生成NH3的全部逸出),过滤、洗涤、灼烧,得Fe2O3固体2.0g.则x,y 的关系正确的是()A.x:y=1:1 B.x:y=1:2 C.x:y=1:4 D.x:y=2:1【答案】A【解析】【分析】【详解】据质量守恒定律可以知道,晶体中的氮元素和氨气中的氮元素的质量相等,而晶体中的铁元素的质量和生成的氧化铁中的铁元素的质量相等,即:56x:(14×2)y=(2.0g××100%):(0.85g××100%)解得:x:y=1:1,故选A.5.在一个密闭容器内有四种物质,一定条件下充分反应后,测得反应前后各物质的质量如表,下列推理正确的是物质X Y Z Q反应前质量/g410121反应后质量/g01215待测A.反应物是X和Y,成物是Q和ZB.参加反应的Y和Q的质量比是1∶1C.参加反应的X与Q的质量比是1∶3D.反应后生成15 g Z【答案】C【解析】由表中数据分析可知,反应前后X的质量减少了4 g﹣0 g=4 g,故X是反应物,参加反应的X的质量为4 g;反应前后Y的质量增加了12 g﹣10 g=2 g,故Y是生成物;同理确定Z 是生成物,生成的Z的质量为15 g﹣1 g=14 g;由质量守恒定律,Q应是反应物,且参加反应的Q的质量为14 g+2 g﹣4 g=12 g,故待测的数值为21g﹣12 g=9 g。
【化学】中考化学总复习--化学《化学方程式》一、选择题1.科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置,如图是该反应的微观示意图,下列说法错误的是( )A.化学反应前后原子的种类、个数、质量均保持不变B.W中碳元素的质量分数为75%C.参加反应的X、Y两物质的粒子个数比为3︰4D.化学反应前后元素的种类发生了变化【答案】D【解析】由反应的微观示意图和质量受守恒律可知,该反应是碳和氨气在一定条件下反应生成了氮气和甲烷,反应的方程式是:3C+4NH3催化剂高温2N2+3CH4。
A、由微粒的变化可知,化学反应前后原子的种类、个数、质量均保持不变,故A正确;B、由图示可知,W为甲烷,碳元素的质量分数为:1216×100%=75%,故B正确;C、由上述方程式可知,参加反应的X、Y两物质的粒子个数比为3:4,故C正确;D、化学反应前后元素的种类不变,故D错误;故选D。
点睛:根据反应的微观示意图和质量受守恒律,分析反应物、生成物,写出化学式、方程式,根据其意义分析判断有关的问题;根据微粒的变化,分析分子、原子的变化等。
2.浓盐酸跟二氧化锰混合加热会产生一种黄绿色的有毒气体,该气体可能是A.Cl2B.H2C.NH3D.HCl【答案】A【解析】【详解】浓盐酸跟二氧化锰混合加热会产生一种黄绿色的有毒气体,根据质量守恒定律,反应前后,元素种类不变,该气体可能是氯气,氢气为无色的无毒气体;反应物中不含氮元素,不可能生成氨气;氯化氢气体无色,不可能是氯化氢。
故选A。
3.图反映了某个化学反应各物质质量与时间的关系。
下列描述正确的是A.该反应是化合反应B.甲的相对分子质量大于乙C.丙是反应物,甲和乙是生成物D.t1时,丙的质量一定等于甲、乙的质量之和【答案】C【解析】【分析】【详解】A、由图知从0到t1时间内丙物质逐渐减少,甲乙两物质逐渐增加。
所以,丙为反应物,甲、乙为生成物,该反应分解反应,描述错误;B、甲的生成量比乙多,但分子个数不知,相对分子质量甲不一定比乙大,描述错误;C、丙是反应物,甲和乙是生成物,描述正确;D、t1时,参加反应的丙质量一定等于甲、乙的质量之和,描述错误。
第1页(共11页)2023年中考化学总复习:第五单元化学方程式(二)一、 单项选择题(共10小题)1.(2022·全国·九年级课时练习)下列关于2CO+O 2 点燃2CO 2的说法不正确...的是( ) A .表示一氧化碳与氧气在点燃条件下反应生成二氧化碳B .参加反应的一氧化碳与氧气的质量比为7:8C .反应前后碳原子、氧原子的个数均保持不变D .参加反应的一氧化碳与生成的二氧化碳的分子个数比为1:12.(2022·上海嘉定·九年级期中)北京冬奥会火种灯使用X 作燃料,其反应的化学方程式为:X+5O 2点燃3CO 2+4H 2O ,推断X 的化学式是( )A .CH 4B .C 2H 6OC .C 3H 8D .C 3H 6O 2 3.(2022·湖南长沙·九年级单元测试)下列反应的化学方程式书写正确的是( )A .铁在氧气中燃烧: 4Fe+3O 2Fe O 点燃B .实验室用过氧化氢溶液制氧气:222222H O 2O H n O M ↑+↑ C .镁条在空气中燃烧:22Mg+O 2MgO 点燃 D .红磷在空气中燃烧: 2254P+5O 2P O 点燃4.(2022·湖南长沙·九年级单元测试)红磷在空气中燃烧化学方程式中2P+5O 2点燃P 2O 5指出其中错误是( )A .反应条件应改为燃烧B .氧气应改为“↑”C .没有配平化学方程式D .五氧化二磷应改为“↓” 5.(2022·全国·九年级课时练习)下列关于化学反应2X+Y==2Z 的叙述,错误的是( )A .Z 一定是化合物B .在反应中X 、Y 、Z 三种物质的粒子数目比为2:1:2C .若X 和Y 的相对分子质量分别为M 和N ,则Z 的相对分子质量为(M+N )D .若ag X 完全反应生成bgZ ,则同时消耗(b-a )gY.。
第五单元化学方程式姓名:________ 班级:________ 限时:______分钟一、选择题1.(2018·威海)在化学变化中,下列说法正确的是( )①原子的种类、元素的种类、分子的种类均不变②原子的数目、分子的数目均不变③原子的质量、元素的质量、物质的总质量均不变④原子核的种类、数量、质量均不变A.①② B.①③ C.③④ D.②④2.(2019·改编题)质量守恒定律是自然界基本的规律之一,下列装置及实验(天平未画出)能用来验证质量守恒定律的是( )3.(2018·荆州)根据化学方程式不能获得的信息有( )A.化学反应发生的条件B.化学反应的快慢C.反应物和生成物的质量比D.化学反应的反应物和生成物4.(2018·河南)过氧化钠(Na2O2)可作呼吸面具中氧气的来源,它与二氧化碳反应后的生成物为( )A.Na2CO3和H2B.Na2O和O2C.NaOH和O2D.Na2CO3和O25.(2015·曲靖)下列物质能发生反应,且化学方程式书写正确的是( )A.2Fe+6HCl=== 2FeCl3+3H2↑B .NaOH +KCl=== NaCl +KOHC .Cu +H 2SO 4=== CuSO 4+H 2↑D .AgNO 3+NaCl=== AgCl↓+NaNO 36.(2018·山西)生活中的自来水通常用氯气(Cl 2)进行杀菌消毒处理,发生反应的化学方程式是Cl 2+H 2O=== X +HClO 。
则X 的化学式为 ( ) A .H 2 B .ClH C .HClD .ClO 27.(2018·广西)关于化学方程式4P +5O 2=====点燃2P 2O 5的理解,正确的是( ) A .反应前后分子总数保持不变 B .该反应的反应物是五氧化二磷C .每四份质量的磷和五份质量的氧气完全反应D .在点燃的条件下,磷和氧气反应生成五氧化二磷8.(2018·昆明五华区一模)下列化学方程式不能正确表示所述内容的是( ) A .铁丝在氧气中燃烧:4Fe +3O 2=====点燃2Fe 2O 3 B .高温煅烧石灰石:CaCO 3=====高温CaO +CO 2↑ C .盐酸除铁锈:Fe 2O 3+6HCl=== 2FeCl 3+3H 2O D .实验室制取氢气:Zn +H 2SO 4=== ZnSO 4+H 2↑9.(2018·海南)我国古代典籍中有“银针试毒”的记载,其反应原理之一是4Ag +2H 2S +O 2=== 2X +2H 2O ,下列有关该反应的说法不正确的是( ) A .X 的化学式是Ag 2S B .H 2S 中S 元素为-2价 C .反应前后元素的种类不变 D .H 2S 是无毒的10.(2017·省卷)如图为甲和乙在一定条件下反应生成丙和丁的微观示意图,下列结论错误的是( )A .该反应属于置换反应B .参加反应的甲和乙的质量比为22∶3C .图中的甲和丁属于氧化物D .生成的丙和丁的分子个数比为1∶111.(2018·西山区二模)下列说法正确的是( )A .D 分子可以保持水的化学性质B .C 物质是由碳原子和氢分子构成 C .图中A 、B 、C 均为化石燃料D .此反应的方程式为:CO +H 2=====催化剂CH 4+H 2O12.(2018·罗平县三模)2017年5月,中国科学家取得了将二氧化碳在一定条件下转化为化工原料的重大突破,二氧化碳和氢气反应制取乙烯,其反应的微观过程如下图所示,下列说法正确的是( )A .生成物分子数之比是1∶2∶4B .乙烯的化学式为C 2H 4C .反应前后分子种类、数目均不变D .无机物不能转化为有机物13.(2018·绵阳)镍氢充电电池有着广泛应用,镍(Ni)及其化合物能发生下列反应: ①Ni+2HCl=== NiCl 2+H 2↑ ②NiO+2HCl=== NiCl 2+H 2O③NiO 2+4HCl=== NiCl 2+Cl 2↑+2H 2O 对上述反应的分析判断错误的是( ) A .镍能与氯化铜溶液发生置换反应 B .NiCl 2能与NaOH 溶液发生复分解反应 C .反应②和③都是复分解反应D .反应①、③中Ni 的化合价都发生了变化14.(2018·黄冈)一定条件下,甲、乙混合后发生化学反应,测得反应前后各物质的质量变化如下表所示。
下列说法中,不正确的是( )A.X的值等于0.5B.甲一定是化合物C.丙和丁的变化比为8∶1D.该反应是化合反应15.(2018·衡阳)甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )A.参加反应的甲和乙质量比为2∶7B.丙可能是该反应的催化剂C.丁一定是化合物D.x的值是716.(2018·南京)在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前及反应过程中的两个时刻各物质的质量分数如图所示。
图中a、b、c、d分别表示相应物质的质量分数。
下列数据正确的是( )A.a=56% B.b=6%C.c=17% D.d=8%二、填空与简答17.(2018·苏州)根据下列反应事实写出相应的化学方程式。
(1)稀硫酸与锌粒反应制氢气:_____________________________________。
(2)金属铝与氧气反应生成氧化膜:_________________________________。
(3)碳酸钙在高温下分解:_________________________________________。
(4)石灰水与硫酸铜溶液反应:_____________________________________。
(5)甲烷在足量氧气中充分燃烧:___________________________________。
18.(2019·改编题)化学发展经历了从定性到定量,从宏观到微观的过程。
(1)图1是某同学验证质量守恒定律的实验装置。
①反应的化学方程式为___________________________________________;②该实验方案设计不合理的原因是_________________________________;③若保持装置不变,改变药品即可验证。
他用的一组药品是________________________________________。
(2)水分解的微观过程,可用以下三幅模型图表示。
①模型图排列顺序正确的是__________(填标号)。
②反应前后保持不变的是__________________(填具体微粒名称)。
三、实验与探究19.(2019·经典题)在测定质量守恒定律时,某同学设计了如图A、B两个实验,根据质量守恒定律回答下列问题:(1)通过实验知道,实验A中反应前后质量总和相等,在该实验中气球变化的现象是____________________,实验B中测得反应前后质量减小了,质量减小的原因是________________________________________,若要使该实验测得的质量相等,需要进行如何改进________________________________________。
(2)以上两个实验中,满足质量守恒定律的是______。
(3)某学生在课外研究性学习活动课上用如图C所示的装置做实验,瓶内放了足量的稀硫酸,气球内放有一定量的镁粉将它紧紧栓在瓶口上,放在托盘天平上称量,质量为W1,然后将气球内的镁粉全部倒入瓶内,反应的化学方程式为Mg+H2SO4=== MgSO4+H2↑,观察到立即产生大量的气泡,气球逐渐胀大,充分反应后最终再次称量,质量为W2,结果W1>W2。
(装置不漏气)反应后称得质量减小的原因是________________________________________________________。
四、分析与计算20.(2017·省卷)用47.8 g氢氧化钠溶液充分吸收二氧化碳气体,得到50.0 g碳酸钠溶液,请计算:(温馨提示:CO2+2NaOH=== Na2CO3+H2O)(1)参加反应的二氧化碳气体的质量是__________g。
(2)反应后溶液中溶质的质量分数是多少?(计算结果精确到0.1%)1.(2018·昆明一中适应性考试2)某有机物在空气中完全燃烧,测得生成物中含有二氧化碳、水蒸气、二氧化硫,下列对该有机物的推断正确的是( )A.一定含有碳、氢、硫元素B.一定含有碳、氢、氧元素C.只含有碳、氢元素D.一定含有碳、氢、氧,可能含有硫元素2.(2018·天津)在反应A+3B=== 2C+2D中,已知A和B的相对分子质量之比为7∶8,当2.8 g A与一定量B恰好完全反应后,生成3.6 g D,则生成C的质量为( )A.9.6 g B.8.8 g C.6.8 g D.4.4 g3.(2019·改编题)四种物质在一定条件下充分混合反应,测得反应前后各物质的质量分数如图所示,则有关说法中正确的( )A.丙一定是化合物B.该反应可能是水的电解C .乙一定是该反应的催化剂D .参加反应或生成的甲和丙的质量比为19∶414.(2019·易错题)如图表示混合均一质量的KClO 3和MnO 2固体在受热过程中各物质质量随时间的变化趋势。
下列说法不正确的是( )A .a 是氯酸钾B .b 是氧气C .d 是二氧化锰D .t 1时反应开始参考答案夯基过关1.C 2.A 3.B 4.D 5.D 6.C 7.D 8.A 9.D 10.A 11.A 12.B 13.C 14.D 15.A 16.A 17.(1)Zn +H 2SO 4=== ZnSO 4+H 2↑ (2)4Al +3O 2=== 2Al 2O 3 (3)CaCO 3=====高温CaO +CO 2↑(4)Ca(OH)2+CuSO 4=== CaSO 4+Cu(OH)2↓ (5)CH 4+2O 2=====点燃CO 2+2H 2O18.(1)①2H 2O 2=====MnO 22H 2O +O 2↑ ②反应生成的氧气逸散到空气中,使锥形瓶中物质的质量减小,天平不再平衡 ③氢氧化钠溶液与硫酸铜溶液(合理即可) (2)①cab ②氢原子、氧原子19.(1)气球先变大后变小 反应生成的二氧化碳气体逸散到了空气中 将碳酸钠与稀盐酸放在密闭的容器中反应 (2)A (3)生成的氢气密度比空气小,会产生向上的浮力,使称得的质量减小20.(1)2.2(2)解:设反应生成碳酸钠的质量为x,CO2+2NaOH=== Na2CO3+H2O,44 1062.2 g x44 2.2 g =106xx=5.3 g反应后溶液中溶质的质量分数为5.3 g50.0 g×100%=10.6% 答:反应后溶液中溶质的质量分数是10.6%。