凝集反应
- 格式:ppt
- 大小:43.50 KB
- 文档页数:18


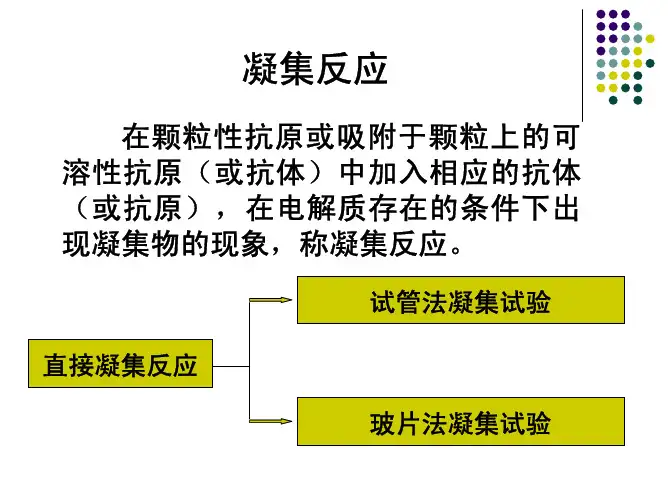
第四章凝集反应内容一、玻片凝集反应二、试管凝集反应三、血型鉴定当颗粒性抗原与其相应抗体混合时,在电解质存在的环境下,相应的抗原抗体结合产生大小不等的凝集块,这种现象称为凝集。
凝集反应有直接与间接凝集两种。
直接凝集反应是颗粒性抗原与相应抗体直接结合出现的凝集现象;间接凝集反应是指将可溶性抗原吸附于一类与免疫无关的载体微球上,形成人工的免疫微球(或致敏载体),再与相应抗体结合出现的凝集现象。
在操作方法上,凝集反应又可分为玻片凝集与试管凝集。
一、玻片凝集反应将已知的抗体与未知的颗粒性抗原物质(如细菌、钩端螺旋体或细胞等)混悬于载玻片上,摇匀后经数分钟出现可见的凝集颗粒为阳性反应。
该法为定性试验,常用于细菌的种类及分型鉴定、血型鉴定等。
【材料】1、抗体:1∶10稀释伤寒杆菌抗血清。
2、抗原:伤寒杆菌菌液、大肠杆菌菌液。
3、生理盐水。
4、蜡笔、载玻片,毛细血管,吸头或吸球等。
【方法】1、取洁净载玻片一张,用蜡笔分为三格,并在边上标明1、2、3。
2、用毛细吸管于第1、3格内各加1滴伤寒杆菌菌液,第2格加1滴大肠杆菌菌液。
3、用毛细吸管于第1、2格内各加1滴1∶10倍稀释的伤寒杆菌抗血清,第3格加生理盐水1滴作为对照。
4、轻摇动玻片,数分钟后观察结果。
如果不够清晰,可将玻片放于低倍镜下观察。
【结果观察与判定】若上述混合悬液由均匀状变为澄清透明,并出现大小不等的乳白色凝集块者即为阳性,若混合物仍呈均匀混浊状则为阴性。
二、试管凝集反应该法常用已知的颗粒性抗原来检测未知抗体及其相对含量,属定量(半定量)试验。
方法是用生理盐水将待测血清在试管中作倍比稀释,然后于各管中加入等量的已知抗原悬液,37℃恒温箱过夜或56℃水浴2h后,观察有无凝集,并根据凝结情况判定血清抗体的效价。
临床上主要用于诊断伤寒与副伤寒(如肥达反应)、斑疹伤寒及恙虫病(如外斐反应)等。
【材料】1、血清:抗伤寒杆菌H血清或病人血清。
2、抗原:伤寒杆菌H菌液。

凝集反应的操作方法凝集反应是一种常见的化学反应,它能够将分散的物质聚集在一起形成较大的聚集体。
在实际的操作过程中,我们需要遵循一定的步骤和条件来完成凝集反应。
下面将介绍凝集反应的操作方法。
1. 准备实验器材和试剂在进行凝集反应之前,首先需要准备好实验所需的器材和试剂。
一般来说,我们需要玻璃容器、搅拌棒、移液管等基本的实验器材,以及所需的化学试剂。
2. 调节溶液的pH值pH值是影响凝集反应的重要因素之一。
在进行凝集反应之前,需要调节溶液的pH值,使其处于适宜的范围。
通常情况下,pH值的调节可以通过加入酸或碱来实现。
3. 加入凝集剂凝集剂是促使物质发生凝集反应的关键。
在操作过程中,我们需要将凝集剂逐渐加入溶液中,并进行充分的搅拌,以确保凝集剂均匀分散在溶液中。
4. 控制搅拌速度和时间搅拌速度和时间的控制对凝集反应的效果有着重要的影响。
一般来说,适当增加搅拌速度和延长搅拌时间可以增加凝集的程度,但过高的搅拌速度和过长的搅拌时间可能会导致溶液的不稳定性。
5. 控制温度温度是影响凝集反应速率的因素之一。
在操作过程中,我们需要根据具体的反应条件来控制反应体系的温度。
一般来说,提高温度可以加快凝集反应的进行,但过高的温度可能会导致反应失控或产生副反应。
6. 观察和记录反应结果在进行凝集反应的过程中,我们需要仔细观察和记录反应的结果。
这包括观察凝集物的形态、颜色和大小等方面的变化,并记录下来以备后续分析和研究。
7. 分离和纯化凝集物在凝集反应完成后,我们需要对凝集物进行分离和纯化。
这可以通过离心、过滤、洗涤等方法来实现。
分离和纯化的目的是获取纯净的凝集物,并进一步进行后续的分析和应用。
总结:凝集反应是一种重要的化学反应,它能够将分散的物质聚集在一起形成较大的聚集体。
在进行凝集反应的操作过程中,我们需要准备实验器材和试剂,调节溶液的pH值,加入凝集剂,控制搅拌速度和时间,控制温度,观察和记录反应结果,以及分离和纯化凝集物。

凝集反应的操作方法凝集反应是一种化学反应,通过凝结剂将分散的物质聚集在一起形成凝胶或固体的过程。
它在许多领域中都有着广泛的应用,如制备材料、制药、环境保护等。
本文将介绍凝集反应的操作方法。
凝集反应的操作方法可以分为溶液法和凝胶法两种。
溶液法是最常见的凝集反应方法之一。
在这种方法中,首先需要将反应物溶解在溶剂中,形成均匀的溶液。
然后,加入凝集剂,通过凝集剂的作用使溶液中的分散物聚集在一起,形成凝胶或固体。
溶液法中,选择合适的溶剂对于凝集反应的成功至关重要。
溶剂的选择应考虑溶剂与反应物的相容性、反应速率以及后续处理的便利性等因素。
常用的溶剂有水、有机溶剂(如乙醇、二甲基亚砜等)以及混合溶剂。
根据反应物的特性,可以选择单一溶剂或混合溶剂进行反应。
凝胶法是另一种常用的凝集反应方法。
在这种方法中,首先需要将反应物悬浮在溶剂中,形成均匀的悬浮液。
然后,加入凝胶剂,通过凝胶剂的作用使悬浮液中的颗粒聚集在一起,形成凝胶或固体。
凝胶法中,选择合适的凝胶剂对于凝集反应的成功同样很重要。
凝胶剂的选择应考虑凝胶剂与反应物的相容性、凝胶速率以及后续处理的便利性等因素。
常用的凝胶剂有硅酸盐、聚合物凝胶剂等。
根据反应物的特性,可以选择适合的凝胶剂进行反应。
在凝集反应中,温度、pH值、反应时间等因素也会对反应结果产生影响。
合理调控这些因素,可以控制凝集反应的速率和产物的性质。
温度的选择应根据反应物的热稳定性和反应速率来确定。
pH值的调节可以通过加入酸碱或缓冲溶液来实现。
反应时间的控制可以通过调整反应物的浓度和反应条件来实现。
为了提高凝集反应的效率和产物的纯度,常常会采取一些辅助措施。
例如,可以采用搅拌、超声波处理等方法来促进反应物的混合和凝集过程。
还可以通过过滤、离心、干燥等方法对产物进行后处理,得到所需的固体产物。
总结起来,凝集反应是一种将分散物聚集成固体的化学反应。
在操作上,可以采用溶液法或凝胶法进行。
溶液法是将反应物溶解在溶剂中,加入凝集剂使其凝结。

直接凝集试验(试管法)本法是一种半定量的凝集反应。
常用已知抗原测定受检血清中有无相应抗体及其含量,以辅助临床诊断或供流行病学调查分析,传染病诊断中常用的肥达反应、布氏凝集反应和外斐反应等均属此类。
本试验以 1% 绵羊红细胞(抗原)与羊溶血素(抗体)为例进行试管凝集试验操作实践。
材料1. 1%SRBC 悬液。
2. 1 : 10 稀释(据血清效价决定起始稀释度)的绵羊红细胞抗体(羊红细胞凝集素)。
3. 试管、吸管、生理盐水、试管架等。
方法排列 7 支小试管于管架上,其中 1~6 管为实验管,第七管为盐水对照管,作好标记。
1. 稀释血清:以 1ml 吸管向第 1 管内加生理盐水 0.9ml ,第 2~7 管各加 0.5ml 。
然后取绵羊红细胞溶血素0.1ml 加入第 1 管,连续吹吸三次,使血清与盐水充分混匀成 10 倍稀释(注意勿吹起气泡,勿使液体外溢),然后吸取 0.5ml 注入第 2 管,同上法混匀后,取 0.5ml 注入第 3 管,以下依次以 2 倍稀释法稀释至第 6 管,第 6 管混匀后,吸取 0.5ml 弃去。
各管血清的稀释度分别为 1 : 10 、 1 : 20 、 1 : 40 、 1 : 80 、 1 :160 、 1 : 320 ,第 7 管为对照管不加血清(图 12-16 )。
2. 加抗原:另取一支 1ml 吸管吸取摇匀的 1% 绵羊红细胞悬液分别加入 1~7 管内,每管 0.5ml 。
此时各管血清稀释度又增加一倍,即 1 : 20 、 1 : 40 、 1 : 80 、 1 : 160 、 1 : 320 、 1 : 640 。
3 . 双手举起试管架,振荡混匀各管内容,置 37?C 温箱,次日观察结果。
结果结果观察要点:1. 观察对照管:对照管应无凝集,即上层液基本清澈透亮,管底可见红细胞沉积物,呈圆形,边缘整齐,轻轻振摇试管后,可见红细胞浮起又分散仍呈悬液。
2. 观察各试验管:从第 1 管看起。


凝集反应名词解释凝集反应是一种集聚反应,是一种微生物学上重要的反应,主要是描述一种由特定蛋白质结合在一起形成类聚体的物理现象,或者用于控制多个分子之间的相互作用。
该反应可以激活或增强特定的生物反应,如催化、促肥、保护等,广泛存在于生命系统中,为多种生物活动提供稳定的支持。
当有适当的分子存在于液体中,这种分子将通过结合和细胞膜受体的作用形成簇,且会表现特定的物理和化学行为,这种结合称为凝集反应。
凝集反应可以用于控制多个分子之间的相互作用,以构建分子簇,例如一些活性核酸分子在液体中称为聚合物,它们的聚合可以增强其生物活性和受体结合性。
此外,凝集反应还可以控制具有有害作用的分子的聚集,从而作用于抑制特定的病原体的生长。
此外,凝集反应还可以通过调节液体的通量来维持细胞的酸碱平衡,并促进细胞内外的活性物质的交换,从而使细胞能够适应某种环境条件,从而保证细胞的生存机制。
另外,凝集反应还能够增强生物反应物的发挥功效,例如促肥、催化、保护等,广泛用于细胞水解、脱氢反应、抗病毒感染反应等。
凝集反应在生物学上具有十分重要的意义,凝集反应能够维持细胞内环境的稳定性,有效地促进受体的配体结合及识别,并可以调控特定的生物反应,如催化、促肥、保护等,使生物活动有效而稳定。
凝集反应的发生也能够控制病原体的聚集,从而阻止细菌病发生,以保护细胞。
因此,凝集反应是一种十分重要的生命现象,为生物系统的正常运作提供了稳定的支持。
从化学的角度来看,凝集反应是一种基于氢键的原子、分子或集聚都能发生的结合反应,可以用来制备均质的类聚体,代替反应溶液中的分子组装。
凝集反应伴随着质子的转移或共价键的构建,它们构建或破坏分子之间的双氧水网络,从而控制分子簇的大小、组成和活性,进而能够影响分子间的相互作用。
总之,凝集反应是一种重要的反应,它在生物学和化学上都有着广泛的应用,其中一个重要的用途是控制细胞内外环境的稳定,通过氢键的发生维持质子的转移,能够发挥催化、保护、促肥等特性,在细胞水解,脱氢,病原体的抗感染反应等过程中都起着至关重要的作用,为细胞活动提供了有效和稳定的支持。

凝集反应形成的反应现象一、引言凝集反应是指在溶液中加入一种特定的试剂后,原本分散在溶液中的细小颗粒会凝聚成较大的团块或沉淀物的现象。
凝集反应广泛应用于生物学、化学、医学等领域,具有重要的理论和实际意义。
本文将从凝集反应的定义、机制以及形成的反应现象等方面进行详细阐述。
二、凝集反应的定义与机制凝集反应是一种由于各种原因导致溶液中颗粒聚集成较大团块或沉淀物的现象。
这些颗粒可以是悬浮在溶液中的固体颗粒、胶体颗粒,也可以是悬浮在溶液中的细胞等生物体。
凝集反应通常是由于两个或多个颗粒之间发生相互作用力而引起的。
凝集反应可以通过两种主要机制进行解释:电解质效应和非电解质效应。
1.电解质效应:当一个电解质被加入到溶液中时,它会与溶液中的其他电解质发生反应,形成离子对或离子复合物。
这些离子对或离子复合物可以与溶液中的颗粒表面发生吸附作用,使颗粒之间的相互斥力减小,从而促进颗粒的聚集。
2.非电解质效应:非电解质通常是指分子量较大、不带电荷的化合物。
当非电解质加入到溶液中时,它们可以通过溶剂分子与颗粒表面发生吸附作用,从而改变颗粒之间的相互作用力。
这种改变可以使颗粒之间的斥力减小,促进颗粒的聚集。
三、凝集反应形成的反应现象凝集反应形成的反应现象主要包括沉淀形成、胶体稳定性改变和细胞凝集等。
1.沉淀形成:当两种或多种溶液中的离子在一定条件下结合形成不溶性盐时,会发生沉淀反应。
这些沉淀物通常呈现出比原始溶液中颗粒更大、更明显的团块状。
常见的沉淀反应有氯化银与硝酸钠反应生成氯化钠和硝酸银沉淀。
2.胶体稳定性改变:胶体是由微小颗粒或分子悬浮在介质中形成的分散系统。
当溶液中的胶体颗粒发生凝聚时,胶体的稳定性会发生改变。
凝聚会使胶体颗粒更大、更容易沉积,从而导致胶体系统的失稳。
3.细胞凝集:在生物学研究中,细胞凝集是一种重要的现象。
细胞表面通常存在一些特异性受体或配体,当这些受体与配体结合时,会引发细胞间的凝聚反应。
细胞凝集可以用于细胞分离、免疫学研究等领域。


实验一凝集反应凝集反应是指细菌和红细胞等颗粒性抗原或表面包被可溶性抗原(或抗体)的颗粒性载体与相应抗体(或抗原)发生特异性结合后,在适当电解质存在下,出现肉眼可见的凝集现象。
凝集反应分为两类:直接凝集反应和间接凝集反应。
直接凝集反应是颗粒性抗原直接与抗体结合,在电解质的作用下,出现肉眼可见凝集现象。
间接凝集反应是小分子可溶性抗原吸附到颗粒载体(红细胞、药用炭和乳胶等)表面,再与相应抗体结合,出现肉眼可见的凝集现象。
凝集反应常用的实验方法:玻片法和试管法。
(一)试管凝集试验-血清抗体效价测定实验目的:了解试管凝集反应方法;掌握凝集效价的判定及其意义。
实验原理:试管凝集试验为半定量试验方法,常用已知红细胞(微生物中常用细菌)作为抗原液与一系列稀释的受检血清混合,保温后观察每管内抗原凝集程度,通常以产生明显凝集现象的最高稀释度作为血清中抗体的效价,亦称为滴度。
在试验中,由于电解质浓度和pH不适当等原因,可引起抗原的非特异性凝集,出现假阳性反应,因此必须设不加抗体的稀释液作对照组。
临床上常用的直接试管凝集试验为肥达试验(Widal test)和外斐试验(Weil-Felix test)。
在输血时也常用于受体和供体两者的红细胞和血清的交互配血试验。
实验材料:试管、吸管、试管架、记号笔;生理盐水、鸡红细胞、待检血清、温箱等。
37℃恒温培养箱等。
实验方法:①取洁净试管七支,依次编号;②用玻璃吸管在每管内都加NS0.5ml;③将第1试管内加入1:10待检血清0.5ml,液体吸注混匀3次以上,从中取出0.5ml加入第2个试管内,然后再吸注混匀3次取出0.5ml加入第3个试管内,依此类推,直到第6个试管取出0.5ml弃掉,不加入第7个试管,将第7个试管设为阴性对照管;④每管内都加鸡红细胞0.5ml;⑤混匀后放入37°C恒温箱内1.5h,观察结果表1-1 试管凝集实验方法试管号 1 2 3 4 5 6 7 (对照)生理盐水(ml)0.9 0.5 0.5 0.5 0.5 0.5 0.5待检血清(ml)0.1 0.5 0.5 0.5 0.5 (弃0.5) -红细胞(ml)0.5 0.5 0.5 0.5 0.5 0.5 0.5血清稀释度1:20 1:40 1:80 1:160 1:320 1:640 -37℃30 分钟结果判定++++ ++++ +++ ++ + - -实验结果:先观察生理盐水对照管(第7管),应不发生凝集,液体混浊,管底沉淀呈圆形,边缘整齐。
凝集反应是一种免疫学实验技术,广泛应用于临床诊断和研究领域。
它是通过抗原与抗体的特异结合来发生凝聚现象,从而实现对特定抗原的检测和定量。
凝集反应的原理是基于抗原与抗体相互结合后形成免疫复合物,使得溶液中的物质发生可见的沉淀或凝聚现象。
这种凝聚现象可以通过肉眼观察或者光学仪器来进行定性或定量分析。
凝集反应主要包括直接凝集反应、间接凝集反应和双重凝集反应等类型:1. 直接凝集反应直接凝集反应是指抗原与抗体直接结合形成凝集物质的反应。
在这种反应中,抗原与抗体的结合是直接发生的,不需要其他介质的参与。
该反应通常用于检测红细胞凝集抗体、细菌抗原等。
2. 间接凝集反应间接凝集反应是指抗原与抗体先间接结合,再与介体结合形成凝集物质的反应。
在这种反应中,介体起到传递抗原-抗体复合物的作用,使得凝集反应能够进行下去。
间接凝集反应通常用于检测病毒抗体、梅毒螺旋体抗体等。
3. 双重凝集反应双重凝集反应是指两种抗体与抗原之间分别发生凝集反应,最后抗原-抗体复合物之间再发生凝集现象的反应。
这种反应在研究免疫球蛋白结构和功能、检测致病微生物等方面具有重要意义。
凝集反应的类型多种多样,各自在临床诊断和免疫学研究中发挥着重要作用。
通过对不同类型凝集反应的原理和特点的深入研究,可以更好地理解免疫学的基本原理,提高临床诊断的准确性和敏感性。
凝集反应也为药物研发和免疫治疗提供了重要依据和支持。
希望未来能有更多的科研人员投入到凝集反应领域的研究中,推动该领域的发展,为人类健康做出更大的贡献。
凝集反应是一种免疫学实验技术,广泛应用于临床诊断和研究领域。
它是通过抗原与抗体的特异结合来发生凝聚现象,从而实现对特定抗原的检测和定量。
凝集反应的原理是基于抗原与抗体相互结合后形成免疫复合物,使得溶液中的物质发生可见的沉淀或凝聚现象。
这种凝聚现象可以通过肉眼观察或者光学仪器来进行定性或定量分析。
凝集反应主要包括直接凝集反应、间接凝集反应和双重凝集反应等类型。
凝集反应的概念
凝集反应是指在化学反应中,两个或多个独立的分子(或原子)通过强化学吸引力相互结合,形成更大的聚集体或团簇的过程。
在这种反应中,分子之间的结合是通过原子间的化学键形成的。
凝集反应可以发生在气态、液态或固态中。
在气态中,分子通过碰撞和相互作用形成较大的团簇。
在液态中,溶剂(如水)中的分子可以通过范德华力或离子间相互作用结合在一起。
在固态中,离子间的相互作用和晶体结构能够促使分子或原子形成更大的团簇。
凝集反应在自然界中广泛存在,例如水的结冰过程、气溶胶颗粒的形成、晶体的生长过程等。
此外,凝集反应也是很多化学合成和制备材料的重要步骤,例如合成纳米粒子、合成高分子材料等。
凝集反应的驱动力可以是热力学上的获得更低能量状态,或者是动力学上的提高反应速率。
它可以受到许多因素的影响,包括温度、浓度、压力、溶剂性质等。
总之,凝集反应是指通过强化学吸引力使分子或原子相互结合形成更大的聚集体或团簇的化学反应过程。
凝集反应的操作方法凝集反应操作方法凝集反应是一种将分散的颗粒聚集在一起形成团块的化学反应过程。
这种反应在生物学、材料科学和环境科学等领域具有重要应用。
本文将介绍凝集反应的操作方法,包括溶液制备、实验装置搭建以及反应过程的控制。
一、溶液制备1. 选择合适的溶液体系。
根据所需的反应类型和目标颗粒的特性,选择适当的溶剂和溶质。
溶剂的选择应能够溶解溶质,并具有适当的黏度和表面张力。
溶质的选择应能够在反应中发生聚集反应,并具有一定的稳定性。
2. 确定溶液浓度。
根据实验要求和目标颗粒的大小范围,确定溶液的浓度。
通常情况下,较低的浓度可以产生较小的颗粒,而较高的浓度可以产生较大的颗粒。
3. 调节pH值。
根据所需的反应类型和目标颗粒的表面电荷特性,调节溶液的pH值。
通常情况下,酸性条件下颗粒具有正电荷,碱性条件下颗粒具有负电荷。
二、实验装置搭建1. 准备反应容器。
选择适当的容器,如玻璃烧杯或试管,并确保其表面清洁干净,无杂质。
根据实验要求和目标颗粒的大小范围,选择合适的容器尺寸。
2. 安装搅拌装置。
根据实验要求,选择合适的搅拌方式,如磁力搅拌器或机械搅拌器,并将其安装在反应容器中。
搅拌的目的是促进溶液中颗粒的分散和混合,以实现凝聚反应。
3. 控制温度。
根据实验要求,选择合适的温度控制装置,如水浴或恒温箱,并将其设置在反应容器周围。
温度的选择应使溶液保持稳定,并促进颗粒的凝聚。
三、反应过程控制1. 混合溶液。
将溶剂和溶质按照预定比例加入反应容器中,并进行充分混合。
可以使用搅拌装置或轻轻摇晃容器来实现混合。
2. 控制反应时间。
根据实验要求和目标颗粒的大小范围,确定合适的反应时间。
一般情况下,较短的反应时间可以产生较小的颗粒,而较长的反应时间可以产生较大的颗粒。
3. 观察反应过程。
通过肉眼或显微镜观察反应过程,并注意颗粒的形态和大小变化。
根据观察结果,可以调整反应条件,如溶液浓度、pH值和温度,以控制颗粒的聚集程度和尺寸分布。
凝集反应原理
凝集反应是一种在化学反应中形成或聚集更大分子或物质的过程。
在这种反应中,小分子或物质通过化学键的重组,结合在一起形成较大的分子或物质。
这种过程通常涉及到原子或分子之间的电子转移或共享。
凝集反应在化学合成、生物学和材料科学中起着重要的作用。
凝集反应通常需要特定条件下的加热或提供适当的催化剂。
在加热的过程中,分子或物质之间的能量增加,使得它们更容易发生结合和聚集。
催化剂则可以提供一个合适的环境,使得反应更加迅速和高效。
凝集反应在有机化学中被广泛应用。
例如,酸催化的酯化反应就是一种凝集反应。
在这个反应中,酸催化剂将醇和酸酐反应,生成酯这个较大的分子。
另一个例子是烯烃的聚合反应,其中烯烃单体分子通过共享电子键连接在一起形成高分子聚合物。
生物学中的凝集反应常常涉及蛋白质或多肽之间的结合。
例如,抗体和抗原之间的结合就是一种凝集反应。
在相应的条件下,抗原和抗体可以通过电子转移或共享来形成一个稳定的复合物。
材料科学中的凝集反应可以用于制备纳米颗粒、薄膜或其他复杂结构。
例如,溶胶-凝胶法可以通过控制溶胶粒子的凝结过
程来制备高质量的纳米颗粒或薄膜。
总而言之,凝集反应是一种常见的化学过程,通过将小分子或
物质结合在一起形成较大分子或物质。
这种反应在化学合成、生物学和材料科学中具有广泛应用。