河南化学专题复习:专题二原子结构示意图和元素周期
- 格式:pdf
- 大小:3.97 MB
- 文档页数:20


2020-2021高考化学压轴题专题复习—原子结构与元素周期表的综合附答案一、原子结构与元素周期表练习题(含详细答案解析)1.锌在工业中有重要作用,也是人体必需的微量元素。
回答下列问题:(1)Zn 原子核外电子排布式为__________洪特规则内容_____________泡利不相容原理内容______________________(2)黄铜是人类最早使用的合金之一,主要由Zn 和Cu 组成。
第一电离能I 1(Zn)__________I 1(Cu)(填“大于”或“小于”)。
原因是__________(3)ZnF 2具有较高的熔点(872℃ ),其化学键类型是__________;ZnF 2不溶于有机溶剂而ZnCl 2、ZnBr 2、ZnI 2能够溶于乙醇、乙醚等有机溶剂,原因是__________(4)金属Zn 晶体中的原子堆积方式如图所示,这种堆积方式称为__________,配位数为____六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为N A ,Zn 的密度为__________g·cm -3(列出计算式)。
【答案】1s 22s 22p 63s 23p 63d 104s 2或[Ar ]3d 104s 2 原子核外电子在能量相同的各个轨道上排布时,电子尽可能分占不同的原子轨道,且自旋状态相同,这样整个原子的能量最低 每个原子轨道上最多只能容纳两个自旋状态不同的电子 大于 Zn 核外电子排布为全满稳定结构,较难失电子 离子键 ZnF 2为离子化合物,ZnCl 2、ZnBr 2、ZnI 2的化学键以共价键为主、极性较小 六方最密堆积(A 3型2A 3N 6a c ⨯⨯⨯ 【解析】【分析】【详解】(1)Zn 原子核外有30个电子,分别分布在1s 、2s 、2p 、3s 、3p 、3d 、4s 能级上,其核外电子排布式为1s 22s 22p 63s 23p 63d 104s 2或[Ar]3d 104s 2,洪特规则是指原子核外电子在能量相同的各个轨道上排布时,电子尽可能分占不同的原子轨道,且自旋状态相同,这样整个原子的能量最低,而泡利原理是指每个原子轨道上最多只能容纳两个自旋状态不同的电子,故答案为:1s 22s 22p 63s 23p 63d 104s 2或[Ar]3d 104s 2;原子核外电子在能量相同的各个轨道上排布时,电子尽可能分占不同的原子轨道,且自旋状态相同,这样整个原子的能量最低;每个原子轨道上最多只能容纳两个自旋状态不同的电子;(2)轨道中电子处于全满、全空、半满时较稳定,失去电子需要的能量较大,Zn 原子轨道中电子处于全满状态,Cu 失去一个电子内层电子达到全充满稳定状态,所以Cu 较Zn 易失电子,则第一电离能Cu <Zn ,故答案为:大于;Zn 核外电子排布为全满稳定结构,较难失电子;(3)离子晶体熔沸点较高,熔沸点较高ZnF 2,为离子晶体,离子晶体中含有离子键;根据相似相溶原理知,极性分子的溶质易溶于极性分子的溶剂,ZnF 2属于离子化合物而ZnCl 2、ZnBr 2、ZnI 2为共价化合物,ZnCl 2、ZnBr 2、ZnI 2分子极性较小,乙醇、乙醚等有机溶剂属于分子晶体极性较小,所以互溶,故答案为:离子键;ZnF 2为离子化合物,ZnCl 2、ZnBr 2、ZnI 2的化学键以共价键为主,极性较小;(4)金属锌的这种堆积方式称为六方最密堆积,Zn 原子的配位数为12,该晶胞中Zn 原子个数=12×16+2×12+3=6,六棱柱底边边长为acm ,高为ccm ,六棱柱体积=[(6×23a )×3×c]cm 3,晶胞密度=2A m V 3N 6a c =⨯⨯⨯,故答案为:六方最密堆积(A 3型);12;2A 3N 6a c ⨯⨯⨯。

一、选择题1.下图为元素周期表部分内容和两种微观粒子的结构示意图。
结合图示信息判断,下列说法中正确的是A.钠原子核内有11个质子B.氖的相对原子质量为20.18gC.氖原子与钠原子的电子层数相同D.氖原子与钠原子的化学性质相似2.据《自然》杂志报道,科学家研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如图所示,下列说法错误的是A.x为29B.B.锶原子最外层电子数为2C.锶原子核外有5个电子层D.锶原子在化学变化中易失电子3.下列是五种微粒的结构示意图,有关说法正确的是A.他们表示五种元素的不同粒子B.微粒③③的化学性质相似C.微粒③在化学反应中易得到电子形成阴离子D.微粒③所表示的元素位于元素周期表中的第二周期4.硒有防癌、抗癌作用。
如图为硒的原子结构示意图,下列说法不正确的是A.图中x的值为8B.硒原子的质子数为34C.硒原子核外有四个电子层D.硒在反应中易得电子5.“天为棋盘星作子,中国北斗耀太空”,铷原子钟被称为北斗卫星的心脏。
如图是铷元素在元素周期表中的信息及其原子结构示意图。
下列有关铷原子的说法错误的是A.铷元素属于金属元素B.铷原子核内有37个中子微专题离子、原子结构示意图(二)十分钟练习C.铷元素在元素周期表的第五周期D.铷原子在化学反应中容易失去电子形成阳离子,离子符号为Rb+6.如图为钪在元素周期表中的相关信息及其原子结构示意图。
下列说法不正确的是A.钪元素位于元素周期表第四周期B.原子结构示意图中x的数值为9C.钪原子易得电子而形成钪离子D.钪原子的相对原子质量是44.967.氯原子、碘原子结构示意图如下图所示。
下列说法不正确...的是A.氯元素和碘元素的化学性质相似B.符号“2I-”可表示2个碘原子C.圆圈中“+”表示两种原子核均带正电荷D.氯原子在化学反应中易得到1个电子8.如图是砷元素在元素周期表中的信息及原子结构示意图。
下列说法错误的是A.砷属于非金属元素B.砷原子的质子数为33C.砷原子的相对原子质量为74.92gD.x=5,砷与磷元素化学性质相似9.高精度地磁监测系统可实现“震前”预报,该仪器的材料中含有金属钴,钴原子的结构示意图如图所示,下列有关说法正确的是A.x的数值为8B.钴元素属于金属元素C.钴在化学反应中容易得到电子D.钴原子的中子数为2710.氮化镓(GaN)是生产通信芯片的关键材料,氮的原子结构示意图及其在元素周期表中的信息如图,下列说法正确的是A.x=3B.氮的相对原子质量为14.01gC.氮原子在化学反应中容易失去电子D.氮元素位于元素周期表的第二周期11.国产C919大型客机使用了第三代铝锂合金。

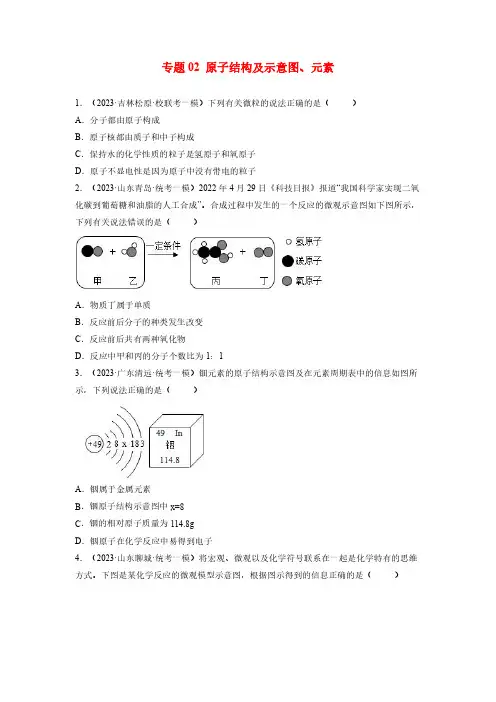
专题02原子结构及示意图、元素1.(2023·吉林松原·校联考一模)下列有关微粒的说法正确的是()A.分子都由原子构成B.原子核都由质子和中子构成C.保持水的化学性质的粒子是氢原子和氧原子D.原子不显电性是因为原子中没有带电的粒子2.(2023·山东青岛·统考一模)2022年4月29日《科技日报》报道“我国科学家实现二氧化碳到葡萄糖和油脂的人工合成”。
合成过程中发生的一个反应的微观示意图如下图所示,下列有关说法错误的是()A.物质丁属于单质B.反应前后分子的种类发生改变C.反应前后共有两种氧化物D.反应中甲和丙的分子个数比为1:13.(2023·广东清远·统考一模)钿元素的原子结构示意图及在元素周期表中的信息如图所示,下列说法正确的是()A.铟属于金属元素B.铟原子结构示意图中x=8C.铟的相对原子质量为114.8gD.铟原子在化学反应中易得到电子4.(2023·山东聊城·统考一模)将宏观、微观以及化学符号联系在一起是化学特有的思维方式。
下图是某化学反应的微观模型示意图,根据图示得到的信息正确的是()A.参加反应的甲、乙两物质的质量之和一定等于生成丙和丁的质量之和B.该反应类型属于置换反应C.反应前后原子的种类和数目发生了改变D.参加反应的甲、乙两物质的分子个数比为1:15.(2023·山东聊城·统考一模)2023年3月4日聊城市人民医院成功完成我市首例“人工心脏”植入术,“人工心脏”是由纯钛制作。
钛的原子结构示意图和钛元素在元素周期表中的信息如图所示,下列说法不正确的是()A.钛属于金属元素B.钛排列在元素周期表中第四周期C.钛的相对原子质量为47.87D.钛原子的化学性质与氦原子的化学性质相似6.(2023·新疆克拉玛依·统考一模)在“宏观一微观一符号”之间建立联系是化学学科特有的思维方式。


专题(二)原子结构示意图及元素周期表1.2【2018山东泰安】全球近140个国家将根据签署的《国际防治汞污染公约》,在2020年前禁止生产和出口含汞产品,如电池、荧光灯、化妆品、温度计、血压计等。
汞元素部分信息如图所示,下列说法不正确的是(A)A.汞为非金属元素B.汞原子的核外电子数是80C.汞原子的质子数为80D.汞的相对原子质量为200.63 4 56.【2018年广州市】下图为某粒子的结构示意图,下列说法正确的是( A )A.该粒子有12个质子B.该粒子有2个电子层C.该粒子属于非金属元素D.该粒子已达到相对稳定结构7..如图是某元素的原子结构示意图和该元素在元素周期表中的单元格,下列说法不正确的是(D)A.该元素属于金属元素B.该原子在化学变化中容易失去电子C.该原子的大小主要决定于核外电子的运动空间D.该原子的质量由构成其原子的质子和电子决定8有一种粒子的结构示意图为,下列说法不正确的是(D)A.该粒子具有稳定结构B.该元素是一种金属元素C.该粒子是一种阳离子D.该元素的原子核外有两个电子层9从如图所示的两种微粒结构示意图中,所获取信息不正确的是(A)A.它们属于同种元素B.它们的核外电子层数相同C.它们的核外电子数相同D.①表示阴离子,②表示原子第9题图10.根据右表判断,下列说法正确的是(C)A.铝的相对原子质量是13B.钠离子核外有三个电子层C.第二、三周期元素的原子从左至右最外层电子数逐渐增多D.在化学变化中镁元素容易失去最外层2个电子形成镁离子1112.13.1415.【2018四川巴中】根据下列粒子结构示意图,回答问题:(1)A、B、C、D所示粒子共表示三种元素。
(2)D所示粒子在化学反应中容易_得到(选填“得到”或“失去”)电子。
16【2018年四川省乐山市】元素周期表是学习和研究化学的重要工具。
下面是元素周期表的部分信息:认真分析信息,回答:(1)地壳中含量最多的元素的原子序数是___8__;(2)分析上表规律可推知,表中X=__17_;(3)表示的是(写粒子符号)__ Ca2+_;17.【2018年四川省达州市】图甲是铝元素在元素周期表中的相关信息,图乙是几种微粒的结构示意图,仔细分析答题:(1)图甲中,铝元素的信息有处错误,请加以改正_Al;(2)铝原子的相对原子质量_ 26.98 _ ;(3)图乙中,属于稳定结构的原子是_AD___(填序号,下同);(4)图乙中,与铝不属于同一周期元素的是___A__。

元素周期表各原子结构示意图第1周期[1] K 氢1[2] He 氦2第2周期[3] Li 锂2 1[4] Be 铍2 2[5] B 硼2 3[6] C 碳2 4[8] O 氧2 6[9] F 氟2 7[10]Ne 氖2 8第3周期[11]Na 钠2 8 1[12]Mg 镁2 8 2[13]Al 铝2 8 3[14]Si 硅2 8 4[15] P 磷2 8 5[16] S 硫2 8 6[17]Cl 氯2 8 7[18]Ar 氩2 8 8第4周期[19]K 钾2 8 8 1[20]Ca 钙2 8 8 2[21]Sc 钪2 8 9 2[22]Ti 钛2 8 10 2[23]V 钒2 8 11 2[24]Cr 铬2 8 13 1[25]Mn 锰2 8 13 2[26]Fe 铁2 8 14 2[27]Co 钴2 8 15 2[28]Ni 镍2 8 16 2[29]Cu 铜2 8 18 1[30]Zn 锌2 8 18 2[31]Ga 镓2 8 18 3[32]Ge 锗2 8 18 4[33]As 砷2 8 18 5[34]Se 硒2 8 18 6[35]Br 溴2 8 18 7[36]Kr 氪2 8 18 8第5周期[37]Rb 铷2 8 18 8 1[38]Sr 锶2 8 18 8 2[40]Zr 锆2 8 18 10 2[41]Nb 铌2 8 18 12 1[42]Mo 钼2 8 18 13 1[43]Tc 锝2 8 18 13 2[44]Ru 钌2 8 18 15 1[45]Rh 铑2 8 18 16 1[46]Pd 钯2 8 18 18[47]Ag 银2 8 18 18 1[48]Cd 镉2 8 18 18 2[49]In 铟2 8 18 18 3[50]Sn 锡2 8 18 18 4[51]Sb 锑2 8 18 18 5[52]Te 碲2 8 18 18 6[53]I 碘2 8 18 18 7[54]Xe 氙2 8 18 18 8第6周期[55]Cs 铯2 8 18 18 8 1[56]Ba 钡2 8 18 18 8 2[57]La 镧2 8 18 18 9 2[58]Ce 铈2 8 18 19 9 2[59]Pr 镨2 8 18 21 8 2[60]Nd 钕2 8 18 22 8 2[61]Pm 钷2 8 18 23 8 2[62]Sm 钐2 8 18 24 8 2[63]Eu 铕2 8 18 25 8 2[64]Gd 钆2 8 18 25 9 2[65]Tb 铽2 8 18 27 8 2[66]Dy 镝2 8 18 28 8 2[67]Ho 钬2 8 18 29 8 2[68]Er 铒2 8 18 30 8 2[69]Tm 铥2 8 18 31 8 2[70]Yb 镱2 8 18 32 8 2[71]Lu 镥2 8 18 32 9 2[72]Hf 铪2 8 18 32 10 2[73]Ta 钽2 8 18 32 11 2[74]W 钨2 8 18 32 12 2[75]Re 铼2 8 18 32 13 2[76]Os 锇2 8 18 32 14 2[77]Ir 铱2 8 18 32 15 2[78]Pt 铂2 8 18 32 17 1[79]Au 金2 8 18 32 18 1[81]Tl 铊2 8 18 32 18 3[82]Pb 铅2 8 18 32 18 4[83]Bi 铋2 8 18 32 18 5[84]Po 钋2 8 18 32 18 6[85]A 砹2 8 18 32 18 7[86]Rn 氡2 8 18 32 18 8第7周期[87]Pr 钫2 8 18 32 18 8 1[88]Ra 镭2 8 18 32 18 8 2[89]Ac 锕2 8 18 32 18 9 2[90]Th 钍2 8 18 32 18 102[91]Pa 镤2 8 18 32 20 9 2[92]U 铀2 8 18 32 21 92[93]Np 镎2 8 18 32 22 92[94]Pu 钚2 8 18 32 24 82[95]Am 镅*2 8 18 32 25 82[96]Cm 锔*2 8 18 32 25 92[97]Bk 锫*2 8 18 32 27 82[98]Cf 锎*2 8 18 32 28 82[99]Es 锿*2 8 18 32 29 82[100]Fm 镄* 2 8 18 32 308 2[101]Md 钔* 2 8 18 32 318 2[102]No 锘* 2 8 18 32 328 2[103]Lr 铹* 2 8 18 32 329 2[104]Rf*[105]Db*[106]Sg*[107]Bh*[108]Hs*[109]Mt*[110]Ds*[111]Rg*[112]Uub*104-112号暂未列出57-71号为镧系元素89-103号为锕系元素红色(深红色)为放射性元素带*号为人造元素。

2023届高考化学一轮专题训练——元素或物质推断题1.(2022秋·河南郑州·高三巩义二中校考期末)有四种短周期元素,相关信息如下表。
请根据表中信息回答:(1)A 在周期表中位于第_______周期第_______族。
(2)用电子式表示B 与C 形成化合物的过程:_______。
(3)在元素C 与D 的最高价氧化物对应的水化物中,酸性较强的是_______(填化学式)。
(4)已知硒(Se)与D 同主族,且位于D 下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______。
a .其单质在常温下呈固态 b .2SeO 既有氧化性又有还原性c .最高价氧化物对应的水化物的化学式为23H SeOd .非金属性比Cl 元素的强2.(2022秋·辽宁沈阳·高三沈阳二中校考期末)请回答下列问题 I 、(1)请用下列10种物质的序号填空:①2O ②2H ③43NH NO ④22K O ⑤()2Ba OH ⑥4CH ⑦2CO ⑧NaF ⑨3NH ⑩2I其中既含离子键又含非极性键的是___________(填序号,下同);既含离子键又含极性键的是___________。
(2)X 、Y 两种主族元素能形成2XY 型化合物,已知2XY 中共有38个电子,若XY 2为常见元素形成的离子化合物,其电子式为___________;若2XY 为共价化合物时且每个原子都满足最外层8电子稳定结构,其结构式为___________。
II、下表为元素周期表的一部分,请回答下列有关问题(3)已知元素⑩的一种核素,其中子数为45,用原子符号表示该核素为___________。
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是___________(用离子符号表示),元素⑨的最高价氧化物对应水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为___________。
(5)元素的非金属性⑩___________⑧(填“>”或“<”);下列事实不能证明上述结论的是___________。

2020-2021高考化学综合题专题复习【原子结构与元素周期表】专题解析含详细答案一、原子结构与元素周期表练习题(含详细答案解析)1.硅是构成矿物和岩石的主要成分,单质硅及其化合物具有广泛的用途。
完成下列填空: I.某些硅酸盐具有筛选分子的功能,一种硅酸盐的组成为:M 2O·R 2O 3·2SiO 2·nH 2O ,已知元素M 、R 均位于元素周期表的第3周期。
两元素原子的质子数之和为24。
(1)该硅酸盐中同周期元素原子半径由大到小的顺序为________________; (2)写出M 原子核外能量最高的电子的电子排布式:__________________; (3)常温下,不能与R 单质发生反应的是___________(选填序号);a .CuCl 2溶液b .Fe 2O 3c .浓硫酸d .Na 2CO 3溶液(4)写出M 、R 两种元素的最高价氧化物对应的水化物反应的离子方程式:____________________________________________。
II.氮化硅(Si 3N 4)陶瓷材料硬度大、熔点高。
可由下列反应制得:SiO 2+C+N 2−−−→高温Si 3N 4+CO(5)Si 3N 4晶体中只有极性共价键,则氮原子的化合价为______,被还原的元素为______________。
(6)C 3N 4的结构与Si 3N 4相似。
请比较二者熔点高低。
并说明理由:_____________________。
(7)配平上述反应的化学方程式,并标出电子转移的数目和方向。
_________________ (8)如果上述反应在10L 的密闭容器中进行,一段时间后测得气体密度增加了2.8g/L ,则制得的Si 3N 4质量为_____________。
【答案】Na >Al>Si 3s 1 bd ()-23-2Al OH +OH =lO +H A O -3 N 2中氮元素 两者均为原子晶体,碳原子半径小于硅原子半径,因此C 3N 4中碳原子与氮原子形成的共价键键长较Si 3N 4中硅原子与氮原子形成的共价键键长小,键能较大,熔点较高35g【解析】【分析】【详解】I .(1)化合物的化合价代数和为0,因此M 呈+1价,R 呈+3价,M 、R 均位于元素周期表的第3周期,两元素原子的质子数之和为24,则M 为Na ,R 为Al ,该硅酸盐中Na 、Al 、Si 为同周期元素,元素序数越大,其半径越小,因此半径大小关系为:Na >Al>Si ; (2)M 原子核外能量最高的电子位于第三能层,第三能层上只有1个电子,其电子排布式为:3s 1;(3)常温下,Al 与CuCl 2溶液反应能将铜置换出来;Al 与Fe 2O 3在高温反应;Al 与浓硫酸发生钝化;Al 与Na 2CO 3溶液在常温下不发生反应;故答案为:bd ;(4)Na 、Al 两种元素的最高价氧化物对应的水化物分别为:NaOH 、Al(OH)3,二者反应的离子方程式为:()-23-2Al OH +OH =lO +H A O ; II .(5)非金属性N>Si ,因此Si 3N 4中N 元素化合价为-3价;该反应中N 元素化合价从0价降低至-3价,N 元素被还原;(6)Si 3N 4陶瓷材料硬度大、熔点高,晶体中只有极性共价键,说明Si 3N 4为原子晶体,C 3N 4的结构与Si 3N 4相似,说明C 3N 4为原子晶体,两者均为原子晶体,碳原子半径小于硅原子半径,因此C 3N 4中碳原子与氮原子形成的共价键键长较Si 3N 4中硅原子与氮原子形成的共价键键长小,键能较大,熔点较高;(7)该反应中Si 元素化合价不变,N 元素化合价从0价降低至-3价,C 元素化合价从0价升高至+2价,根据得失电子关系以及原子守恒配平方程式以及单线桥为:;(8)气体密度增加了2.8g/L ,说明气体质量增加了2.8g/L ×10L=28g ,2234=3SiO +6C +2N Si N +6CO 140g 112g28gm∆高温气体质量变化 因此生成的Si 3N 4质量为28g 140g 112g⨯=35g 。
高中化学专题复习五原子结构与周期表一、核外电子排布1.元素:含有相同质子数的同一类原子的总称。
核素:含有一定数目质子和中子的原子。
同位素:含有同质子数,不同中子数的同一种元素的不同原子之间的互称。
质量数:质子数与中子数之和。
2.核外电子排布规律:①最外电子层最多只能容纳8个电子(氢原子是1个,氦原子是2个);②次外电子层最多只能容纳18个电子;③倒数第三电子层最多只能容纳32个电子;④每个电子层最多只能容纳2n2个电子。
注意:电子总是先排布在能量最低的电子层里。
3.1~18号元素的原子结构示意图:略。
4.元素周期律:元素的性质随着原子核电荷数的递增而呈现周期性变化的规律。
元素周期律是元素核外电子排布随元素核电荷数的递增的必然结果。
(1)随着原子核电荷数的递增原子的最外层电子排布呈现周期性变化。
除1、2号元素外,最外层电子层上的电子重复出现1递增到8的变化。
(2)随着原子核电荷数的递增原子半径呈现周期性变化。
同周期元素,从左到右,原子半径减小,如:Na Mg Al Si P S Cl;C N O F同主族元素,从上到下,原子半径增大。
(3)随着原子核电荷数的递增元素的主要化合价呈现周期性变化。
同周期最高正化合价从左到右逐渐增加,最低负价的绝对值逐渐减小元素的最高正化合价==原子的最外层电子数;最高正化合价与负化合价的绝对值之和=8。
(4)随着原子核电荷数的递增元素的金属性和非金属性呈现周期性变化同周期,从左到右,元素的金属性逐渐减弱,元素的非金属性逐渐增强Na Mg Al Si P S Cl 金属性:Na>Mg>Al 金属性逐渐减弱非金属性逐渐增强非金属性:Cl>S>P>Si,(5)①元素的金属性越强,最高价氧化物对应的水化物(氢氧化物)的碱性越强,反之也如此。
如:金属性:Na>Mg>Al,氢氧化物碱性强弱为:NaOH>Mg(OH)2>Al(OH)3。
②元素的非金属性越强,最高价氧化物对应的水化物(含氧酸)的酸性越强,反之也如此。