普通物理学第五版第6章气体动理论答案(精品课件)
- 格式:ppt
- 大小:1.54 MB
- 文档页数:60


十万种考研考证电子书、题库视频学习平台圣才电子书 第6章热力学基础一、选择题1.一定量的理想气体,分别进行如图6-1所示的两个卡诺循环abcda 和a′b′c′d′a′,若在PV 图上这两个循环曲线所围面积相等,则可以由此得知这两个循环()。
图6-1A.效率相等B.由高温热源处吸收的热量相等C.由低温热源处放出的热量相等D.在每次循环中对外作的净功相等【答案】D【解析】循环曲线所围面积就是循环过程做的净功。
2.如图6-2所示,和为两条等温线。
若ab 为一绝热压缩过程,则理想气体由状态c 经cb 过程被压缩到b 状态,在该过程中气体的热容C 为()。
A.C>0B.C<0十万种考研考证电子书、题库视频学习平台圣才电子书 C.C=0D.不能确定图6-2【答案】B3.关于可逆过程和不可逆过程有以下几种说法,正确的是().(1)可逆过程一定是准静态过程;(2)准静态过程一定是可逆过程;(3)对不可逆过程,一定找不到另一过程使系统和外界同时复原;(4)非静态过程一定是不可逆过程。
A.(1),(2),(3)B.(2),(3),(4)C.(1),(3),(4)D.(1),(2),(3),(4)【答案】C4.图6-3示四个循环过程中,从理论上看能够实现的循环过程是图()。
图6-3【答案】(a)二、填空题1.一台理想热机按卡诺循环工作,每一个循环做功,高温热源温度T1=100℃,低温热源温度T2=0℃,则该热机的效率为______,热机每一循环从热源吸收的热量为______J,每一循环向低温处排出的热量是______J。
【答案】0.268;2.73×105;2.008×105【解析】由卡诺循环的效率公式,有热机每一个循环从热源吸收的热量为每一个循环向低温热源排出热量是2.质量为1kg的氧气,其温度由300K升高到350K。
若温度升高是在下列三种不同情况下发生的:(1)体积不变;(2)压强不变;(3)绝热。

第5章气体动理论一、选择题1.两种不同的理想气体,若它们的最概然速率相等,则它们的()。
A.平均速率相等,方均根速率相等B.平均速率相等,方均根速率不相等C.平均速率不相等,方均根速率相等D.平均速率不相等,方均根速率不相等【答案】A【解析】因为平均速率、方均根速率与最概然速率一样,都与成正比,成反比。
2.范德瓦耳斯方程中()。
A.实际测得的压强是,体积是VB.实际测得的压强是p,体积是VC.实际测得的压强是p,V是1mol范氏气体的体积D.实际测得的压强是;1mol范氏气体的体积是(V-b)【答案】C3.1mol单原子分子理想气体从状态A变为状态B,如果不知是什么气体,变化过程也不知道,但A、B两态的压强、体积和温度都知道,则可以求出()。
A.气体所做的功B.气体内能的变化C.气体传给外界的热量D.气体的质量【答案】B【解析】单原子分子的自由度i=3,摩尔数ν=1,内能是状态量,只取决于状态(温度);内能的变化只与始末状态有关,与是什么气体,经历什么变化过程无关。
4.按照经典的能均分定理,由刚性双原子分子组成的理想气体的定体摩尔热容量是理想气体常数R的()。
A.1倍B.1.5倍C.2倍D.2.5倍【答案】D【解析】刚性双原子分子的自由度是i=5,其定体摩尔热容量。
5.质量为m,摩尔质量为M的理想气体,经历了一个等压过程,温度增量为ΔT,则内能增量为()。
A.B.C.D.【答案】B二、填空题1.在平衡态下,已知理想气体分子的麦克斯韦速率分布函数为f(υ)、分子质量为m、最概然速率为υp,试说明下列各式的物理意义:(1)表示______;(2)表示______。
【答案】(1)分布在0~∞速率区间的分子数占总分子数的百分比;(2)分子平动动能的平均值。
2.某种刚性双原子分子理想气体,处于温度为T的平衡态,则其分子的平均平动动能为______,平均转动动能为______,平均总能量为______,lmol气体的内能为______。



第5章 气体动理论本章提要1. 气体的微观图像与宏观性质·气体是由大量分子组成的,1mol 气体所包含的分子数为2310023.6⨯。
分子之间存在相互作用力。
分子在做永不停息的无规则的运动,其运动程度与温度有关。
·在分子层次上,理想气体满足如下条件:(1)分子本身的大小与分子之间平均距离相比可以忽略不计,分子可看作质点。
(2)除碰撞的瞬间以外,分子之间的相互作用力可以忽略不计,分子所受的重力也忽略不计。
(3)气体分子间的碰撞以及分子与器壁之间的碰撞为完全弹性碰撞。
2. 理想气体压强与温度·理想气体的压强公式εn v nm p 32312==其中, 221v m =ε,称分子平均平动动能,它表征了分子运动的剧烈程度。
·理想气体的温度公式32kT ε=温度公式表明,温度是大量分子热运动剧烈程度的标志。
3. 阿伏伽德罗定律在相同的温度和压强下,各种气体在相同体积内所包含的分子数相同。
4. 道尔顿分压定律混合气体的压强等于各种气体的分压强之和。
5. 麦克斯韦速率分布·在平衡态下,气体分子服从如下麦克斯韦速率分布规律23222d 4d 2mv kTN m ev v N kT ππ-⎛⎫= ⎪⎝⎭·麦克斯韦速率分布函数23222d ()4d 2mv kTN m f v ev N v kT ππ-⎛⎫== ⎪⎝⎭其表征了处于起点速率为v 的单位速率区间内的分子数占总分子数的百分比。
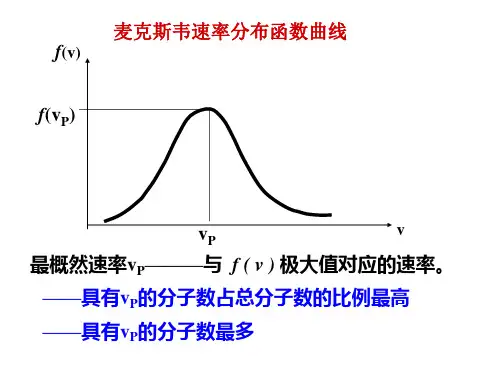
6. 分子速率的三种统计值从麦克斯韦速率分布规律可以导出分子速率的三种统计值 ·最概然速率P v =P v 表明气体分子速率并非从小到大平均分配,速率太大或太小的分子数很少,速率在P v 附近的分子数最多。
·平均速率v =平均速率v 是描述分子运动状况的重要参量,为所有分子的速率之和除以总分子数。
·方均根速率=7. 能量均分定理·描述一个物体空间位置所需的独立坐标数称该物体的自由度。

物理答案第六章⽓体动理论答案-ZSH第六章⽓体动理论6-1 处于平衡状态的⼀瓶氦⽓和⼀瓶氮⽓的分⼦数密度相同,分⼦的平均平动动能也相同,则它们( C ) (A)温度、压强均不相同.(B)温度相同,但氦⽓压强⼤于氮⽓压强. (C)温度、压强都相同.(D)温度相同,但氦⽓压强⼩于氮⽓压强.6-2 三容器A 、B 、C 中装有同种理想⽓体,其分⼦数密度 n 相同,⽽⽅均根速率之⽐为4:2:1)(:)(:)(212212212=CBAv v v ,则其压强之⽐C B A P P P :: 为( C )(A) 4:2:1 (B) 8:4:1 (C) 16:4:1 (D) 1:2:46-3 在⼀个体积不变的容器中,储有⼀定量的某种理想⽓体,温度为0T 时,⽓体分⼦的平均速率为0v ,分⼦平均碰撞次数为0Z ,平均⾃由程为0λ,当⽓体温度升⾼为04T 时,⽓体分⼦的平均速率为v ,分⼦平均碰撞次数为Z ,平均⾃由程为λ分别为( B ) (A) 04v v =,04Z Z =,04λλ= (B) 02v v =,02Z Z =,0λλ= (C) 02v v =,02Z Z =,04= (D) 04v v =,02Z Z =,0=6-4 已知n 为单位体积的分⼦数,)(v f 为麦克斯韦速率分布函数,则dv v nf )(表⽰()(A) 速率v 附近,d v 区间内的分⼦数(B) 单位体积内速率在v ~ v +d v 区间内的分⼦数 (C) 速率v 附近d v 区间内分⼦数占总分⼦数⽐率(D) 单位时间内碰到单位器壁上速率在v ~ v +d v 区间内的分⼦数6-5 温度为0℃和100℃时理想⽓体分⼦的平均平动动能各为多少?欲使分⼦的平均平动动能等于1eV,⽓体的温度需多⾼?解:=1ε231kT =5.65×2110-J=2ε232kT =7.72×2110-J 由于1eV=1.6×1910-J , 所以理想⽓体对应的温度为:T=2ε/3k =7.73×310 K6-6 ⼀容器中储有氧⽓,其压强为0.1个标准⼤⽓压,温度为27℃,求:(1)氧⽓分⼦的数密度n ;(2)氧⽓密度ρ;(3)氧⽓分⼦的平均平动动能k ε?解: (1)由⽓体状态⽅程nkT p =得,242351045.23001038.110013.11.0?===-kT p n 3m - (2)由⽓体状态⽅程RT M MpV mol= (M ,mol M 分别为氧⽓质量和摩尔质量) 得氧⽓密度:13.030031.810013.11.0032.05mol ====RT p M V Mρ 3m kg -? (3) 氧⽓分⼦的平均平动动能21231021.63001038.12323--?===kT k ε6-7 在容积为2.0×33m 10-的容器中,有内能为6.75×210J 的刚性双原⼦理想⽓体分⼦,求(1)⽓体的压强;(2)设分⼦总数5.4×2210个,求⽓体温度;(3)⽓体分⼦的平均平动动能?解:(1)由2iRT M m =ε以及RT M mpV =可得⽓体压强 p =iVε2=1.35×510 Pa (2)分⼦数密度V Nn =, 得该⽓体的温度62.3===NkpV nk p T ×210K (3)⽓体分⼦的平均平动动能为=ε23kT =7.49×2110-J6-8 2100.2-?kg 氢⽓装在3100.4-?m 3的容器内,当容器内的压强为51090.3?Pa 时,氢⽓分⼦的平均平动动能为多⼤?解:由RT M m pV =得 mR MpV T = 所以221089.32323-?=?==mRMpVk kT εJ6-9 1mol 刚性双原⼦⽓体分⼦氢⽓,其温度为27℃,求其对应的平动动能、转动动能和内能各是多少?(求内能时可不考虑原⼦间势能)解:理想⽓体分⼦的能量为RT in E 2=,所以氢⽓对应的平动动能为(3=t ) 5.373930031.8231==t J转动动能为(2=r ) 249330031.8221==r εJ内能5=i 5.623230031.8251==i ε J6-10 设有N 个粒⼦的系统,其速率分布如图所⽰,求:(1)分布函数)(v f 的表达式; (2)速度在1.50v 到2.00v 之间的粒⼦数;(3) N 个粒⼦的平均速率;解:(1)从上图所给条件得:≥=≤≤=≤≤=)2(0)()2()()0(/)(00000v v v Nf v v v a v Nf v v v av v Nf 由此可得分布函数表达式为:≥≤≤≤≤=)2(0)2(/)0(/)(00000v v v v v Na v v Nv av v f 类似于概率密度的归⼀化条件,故)(v f 满⾜?+∞∞-1d )(=v v f ,即=+00020,1d d v v v v a v v av 计算得032v Na =,带⼊上式得分布函数)(v f 为:≥≤≤≤≤=)2(0)2(32)0(3/2)(0000020v v v v v v v v v v v f (2)该区间对应的)(v f 为常数32v N,所以可通过计算矩形⾯积得该区间粒⼦数为: N v v v N N 31)5.12(32000=-=(3) N 个粒⼦平均速率+===∞∞+∞-00020202d 32d 32d )(d )(v v v v v v v v v v v vf v v vf v 0911v = 6-11 设N 个粒⼦系统在各速率区间对应的粒⼦数变化率为:Kdv dN = (为常量K v V ,0>>),0=dN (V v >)(1)画出速率分布函数图;(2)⽤N 和V 表⽰常量K ;(3)⽤V 表⽰出平均速率和⽅均根速率。


第6单元 气体动理论 序号 学号 姓名 专业、班级一 选择题[ C ]1.在标准状态下, 若氧气(视为刚性双原子分子的理想气体)和氦气的体积比2121=V V ,则其内能之比21/E E 为: (A) 1/2 (B) 5/3 (C) 5/6 (D) 3/10[ B ]2.若理想气体的体积为V ,压强为p ,温度为T ,一个分子的质量为m ,k 为玻耳兹曼常量,R 为摩尔气体常量,则该理想气体的分子数为(A) pV/m (B) pV/(kT)(C) pV/(RT) (D) pV/(mT)[ D ]3.若)(v f 为气体分子速率分布函数,N 为分子总数,m 为分子质量,则 )(21221v Nf mv v v ⎰ d v 的物理意义是 (A) 速率为v 2的各分子的总平均动能与速率为v 1的各分子的总平均动能之差。
(B) 速率为v 2的各分子的总平动动能与速率为v 1的各分子的总平动动能之和。
(C) 速率处在速率间隔v 1~ v 2之内的分子的平均平动动能。
(D) 速率处在速率间隔v 1~ v 2之内的分子平动动能之和。
[ D ]4.在一密闭容器中,储有A 、B 、C 三种理想气体,处于平衡状态,A 种气体的分子数密度为 1n ,它产生的压强为 1p ,B 种气体的分子数密度为 12n ,C 种气体的分子数密度为3n 1,则混合气体的压强p 为(A)31p (B)41p(C)51p (D)61p二 填空题1.在定压下加热一定量的理想气体,若使其温度升高1K 时,它的体积增加了0.005倍,则气体原来的温度是_________200k__________。
2.用总分子数N 、气体分子速率v 和速率分布函数f(v),表示下列各量:(1)速率大于0v 的分子数= ⎰∞0)(v dv v Nf ;(2)速率大于0v 的那些分子的平均速率=⎰⎰∞∞00)()(v v dv v f dv v vf ;(3)多次观察某一分子的速率,发现其速率大于0v 的概率=⎰∞0)(v dv v f 。

第六章 相平衡6.1 指出下列平衡系统中的组分数C ,相数P 及自由度F 。
(1) I 2(s)与其蒸气成平衡;(2) CaCO 3(s)与其分解产物CaO(s)和CO 2(g)成平衡;(3) NH 4HS(s)放入一抽空的容器中,并与其分解产物NH 3(g)和H 2S(g)成平衡; (4) 取任意量的NH 3(g)和H 2S(g)与NH 4HS(s)成平衡。
(5) I 2作为溶质在两不互溶液体H 2O 和CCl 4中达到分配平衡(凝聚系统)。
解: (1)C = 1, P = 2, F = C – P + 2 = 1–2 + 2 = 1.(2)C = 3–1 = 2, P = 3, F = C –P + 2 = 2–3 + 2 = 1. (3)C = 3–1–1 = 1, P = 2, F = C –P + 2 = 1–2 + 2 = 1. (4)C = 3–1 = 2, P = 2, F = C –P + 2 = 2–2 + 2 = 2. (5)C = 3, P = 2, F = C –P + 1 = 3–2 + 1 = 2.6.2 已知液体甲苯(A )和液体苯(B )在90℃时的饱和蒸气压分别为=和。
两者可形成理想液态混合物。
今有系统组成为的甲苯-苯混合物5 mol ,在90 ℃下成气-液两相平衡,若气相组成为求:(1) 平衡时液相组成及系统的压力p 。
(2) 平衡时气、液两相的物质的量解:(1)对于理想液态混合物,每个组分服从拉乌尔定律,因此(2)系统代表点,根据杠杆原理mol.n mol .n n )..(n )..(.n n n )x x (n )x y (l g l g g l l l ,B o ,B g o ,B g ,B 7843216125030304556050==-=-=+-=-6.3 单组分系统的相图示意如右图。
试用相律分析图中各点、线、面的相平衡关系及自由度。
6.4 已知甲苯、苯在90℃下纯液体的饱和蒸气压分别为54.22 kPa和136.12 kPa。
第六章 静电场中的导体与电介质6 -1 将一个带正电的带电体A 从远处移到一个不带电的导体B 附近,则导体B 的电势将( )(A ) 升高 (B ) 降低 (C ) 不会发生变化 (D ) 无法确定分析与解 不带电的导体B 相对无穷远处为零电势。
由于带正电的带电体A 移到不带电的导体B 附近时,在导体B 的近端感应负电荷;在远端感应正电荷,不带电导体的电势将高于无穷远处,因而正确答案为(A )。
6 -2 将一带负电的物体M 靠近一不带电的导体N ,在N 的左端感应出正电荷,右端感应出负电荷。
若将导体N 的左端接地(如图所示),则( ) (A ) N 上的负电荷入地 (B )N 上的正电荷入地 (C ) N 上的所有电荷入地 (D )N 上所有的感应电荷入地分析与解 导体N 接地表明导体N 为零电势,即与无穷远处等电势,这与导体N 在哪一端接地无关。
因而正确答案为(A )。
6 -3 如图所示将一个电量为q 的点电荷放在一个半径为R 的不带电的导体球附近,点电荷距导体球球心为d ,参见附图。
设无穷远处为零电势,则在导体球球心O 点有( ) (A )dεqV E 0π4,0== (B )d εqV d εq E 020π4,π4==(C )0,0==V E (D )RεqV d εq E 020π4,π4==分析与解 达到静电平衡时导体内处处各点电场强度为零。
点电荷q 在导 体球表面感应等量异号的感应电荷±q′,导体球表面的感应电荷±q′在球心O 点激发的电势为零,O 点的电势等于点电荷q 在该处激发的电势。
因而正确答案为(A )。
6 -4 根据电介质中的高斯定理,在电介质中电位移矢量沿任意一个闭合曲面的积分等于这个曲面所包围自由电荷的代数和。
下列推论正确的是( )(A)若电位移矢量沿任意一个闭合曲面的积分等于零,曲面内一定没有自由电荷(B)若电位移矢量沿任意一个闭合曲面的积分等于零,曲面内电荷的代数和一定等于零(C)若电位移矢量沿任意一个闭合曲面的积分不等于零,曲面内一定有极化电荷(D)介质中的高斯定律表明电位移矢量仅仅与自由电荷的分布有关(E)介质中的电位移矢量与自由电荷和极化电荷的分布有关分析与解电位移矢量沿任意一个闭合曲面的通量积分等于零,表明曲面内自由电荷的代数和等于零;由于电介质会改变自由电荷的空间分布,介质中的电位移矢量与自由电荷与位移电荷的分布有关。
大学物理(气体动理论)习题答案8-1 目前可获得的极限真空为Pa 1033.111-⨯,,求此真空度下3cm 1体积内有多少个分子?(设温度为27℃)[解] 由理想气体状态方程nkT P =得 kT V NP =,kT PV N =故 323611102133001038110110331⨯=⨯⨯⨯⨯⨯=---...N (个)8-2 使一定质量的理想气体的状态按V p -图中的曲线沿箭头所示的方向发生变化,图线的BC 段是以横轴和纵轴为渐近线的双曲线。
(1)已知气体在状态A 时的温度是K 300=A T ,求气体在B 、C 、D 时的温度。
(2)将上述状态变化过程在 T V -图(T 为横轴)中画出来,并标出状态变化的方向。
[解] (1)由理想气体状态方程PV /T =恒量,可得:由A →B 这一等压过程中BBA A T V T V = 则 6003001020=⋅=⋅=A AB B T V V T (K) 因BC 段为等轴双曲线,所以B →C 为等温过程,则==B C T T 600 (K)C →D 为等压过程,则CCD D T V T V = 3006004020=⋅=⋅=C CD D T V V T (K) (2)8-3 有容积为V 的容器,中间用隔板分成体积相等的两部分,两部分分别装有质量为m 的分子1N 和2N 个, 它们的方均根速率都是0υ,求: (1)两部分的分子数密度和压强各是多少?(2)取出隔板平衡后最终的分子数密度和压强是多少?010203040[解] (1) 分子数密度 VNV N n VN V N n 2222111122====由压强公式:231V nm P =, 可得两部分气体的压强为 VV mN V m n P VV mN V m n P 3231323120220222012011====(2) 取出隔板达到平衡后,气体分子数密度为 VN N V N n 21+==混合后的气体,由于温度和摩尔质量不变,所以方均根速率不变,于是压强为:VV m N N V nm P 3)(31202120+==8-4 在容积为33m 105.2-⨯的容器中,储有15101⨯个氧分子,15104⨯个氮分子,g 103.37-⨯氢分子混合气体,试求混合气体在K 433时的压强。
第六章 气体动理论1、 水银气压计中混进了一个气泡,因此它的读数比实际气体小些,当精确的气压计的水银柱为0.768m 时,它的水银柱只有0.748m 高,此时管中水银面到管顶距离为0.08m,试问此气压计的水银柱为0.734m 高时,实际的气压是多少?(把空气当作理想气体,并设温度不变)。
解:设第一次测得的空气泡的压强和体积汞汞汞(d 02.0d )748.0768.0hd P 1=−=Δ= s 08.0V 1=(s 为截面积)第二次测得空气泡的压强和体积s 094.0s )08.0734.0748.0(V 2=+−=汞汞d 017.0s094.0s 08.0d 02.0V V P P 2112=×== 实际压强)Pa (10999.01033.1751.0d 017.0d 734.0'P 552×=××=+=汞汞2、可用下面方法测定气体的摩尔质量。
先在容积为V的容器内装入被测量的气体,测出其压强为P 1,温度为T,并称出容器连同气体的质量为m 1。
然后放掉一部分气体,这时压强降到P 2,再称出容器连同气体的质量为m 2,假定温度保持不变,试求该气体的摩尔质量。
解:设容器的质量为m开始时)1(T V P R M m m 11=− 放气后 )2(TV P R M m m 22=− 解得 2121P P m m V RT M −−⋅=3、某容器内分子数密度为1026m -3,每个分子的质量为3×10-27kg,设其中1/6分子数以速率v=200ms -1垂直地向容器的一壁运动,而其余5/6分子或者离开此壁,或者平行此壁方向运动,且分子与容器壁的碰撞为完全弹性。
问:(1)每个分子作用于器壁 的冲量为多少?(2)每秒碰在器壁单位面积上的分子数n 0为多少?(3)作用在器壁上的压强为多少?解:(1) (kg m/s )2427102.12001032v 2P I −−×=×××=μ=Δ= (2) s m 10316110200vn 61n 228260⋅×=××==个 (3) Pa 104102.11031P n P 324280×=×××=Δ⋅=−4、有一容积为10cm 3的电子管,当温度为300k的时候,用真空泵把管内空气抽成压强为5×10-6mmHg的高真空,问此时管内有多少个空气分子?此空气分子的平均平动动能的总和是多少?平均转动动能的总和是多少?平动动能的总和是多少?(1mmHg=133.3Pa 空气分子可认为是刚性双原子分子)解:由理想气体状态方程RT PV ν=知空气的摩尔数RTPV =ν 1)个122366A A 1061.13001038.1101032.133105kT PV N RT PV N N ×=××××××===ν=−−− 2)J 1000.13001038.1231061.1kT 23N 82312k −−×=×××××==ε平总 3)J 1067.63001038.11061.1NkT 92312k −−×=××××==ε转总4)J 1067.18k k k −×=ε+ε=ε转总平总总5、一能量为1012eV的宇宙射线粒子,射入一氖管中,氖管中含有氖气0.1mol。
第五章 气体动理论练 习 一一. 选择题1. 一个容器内贮有1摩尔氢气和1摩尔氦气,若两种气体各自对器壁产生的压强分别为1p 和2p ,则两者的大小关系是( C )(A ) 21p p >; (B ) 21p p <; (C ) 21p p =; (D ) 不确定的。
2. 一定量的理想气体贮于某一容器中,温度为T ,气体分子的质量为m. 根据理想气体的分子模型和统计假设,分子速度在x 方向的分量平方的平均值为( D )(A ) 2x v =m kT 3; (B ) 2x v = (1/3)m kT 3 ; (C ) 2x v = 3kT /m ; (D ) 2x v = kT/m 。
3. 设M 为气体的质量,m 为气体分子质量,N 为气体分子总数目,n 为气体分子数密度,0N 为阿伏伽德罗常数,下列各式中哪一式表示气体分子的平均平动动能( A )(A )pV Mm ⋅23; (B )pV M M mol ⋅23; (C ) npV 23; (D ) 023N pV M M mol ⋅。
4. 关于温度的意义,有下列几种说法,错误的是( B ) (A ) 气体的温度是分子平动动能的量度;(B ) 气体的温度是大量气体分子热运动的集体表现,具有统计意义; (C ) 温度的高低反映物质内部分子运动剧烈程度的不同; (D ) 从微观上看,气体的温度表示每个气体分子的冷热程度。
二.填空题1. 在容积为10-2m 3的容器中,装有质量100g 的气体,若气体分子的方均根速率为200m/s ,则气体的压强为ap 51034⨯。
2. 如图1所示,两个容器容积相等,分别储有相同质量的N 2和O 2气体,它们用光滑细管相连通,管子中置一小滴水银,两边的温度差为30K ,当水银滴在正中不动时,N 2和O 2的温度为2N T = 210k ,2O T = 240k 。
( N 2的摩尔质量为28×10-3kg/mol,O 2的摩尔质量为32×10-3kg/mol)3.分子物理学是研究大量微观粒子的集体运动的统计表现的学科, 它应用的方法是 统计学 方法。
第六章 气体动理论6-1 一束分子垂直射向真空室的一平板,设分子束的定向速度为v ,单位体积分子数为n ,分子的质量为m ,求分子与平板碰撞产生的压强.分析 器壁单位面积所受的正压力称为气体的压强.由于压强是大量气体分子与器壁碰撞产生的平均效果,所以推导压强公式时,应计算器壁单位面积在单位时间内受到气体分子碰撞的平均冲力.解 以面积为S 的平板面为底面,取长度等于分子束定向速度v 的柱体如图6-1所示,单位时间内与平板碰撞的分子都在此柱体内.柱体内的分子数为nSv .每个分子与平板碰撞时,作用在平板上的冲力为2mv ,单位时间内平板所受到的冲力为v v nS m F ⋅=2根据压强的定义,分子与平板碰撞产生的压强为22v nm SFp ==6-2 一球形容器,直径为2R ,内盛理想气体,分子数密度为n ,每个分子的质量为m ,(1)若某分子速率为v i ,与器壁法向成θ角射向器壁进行完全弹性碰撞,问该分子在连续两次碰撞间运动了多长的距离?(2)该分子每秒钟撞击容器多少次?(3)每一次给予器壁的冲量是多大?(4)由上结果导出气体的压强公式.分析 任一时刻容器中气体分子的速率各不相同,运动方向也不相同,由于压强是大量气体分子与器壁碰撞产生的平均效果,气体压强公式的推导过程为:首先任意选取某一速率和运动方向的分子,计算单位时间内它与器壁碰撞给予器壁的冲力,再对容器中所有分子统计求和.v图6-1解 (1)如图6-2所示,速率为v i 的分子以θ角与器壁碰撞,因入射角与反射角都相同,连续两次碰撞间运动的距离都是同样的弦长,为θcos 2R AB =(2)该分子每秒钟撞击容器次数为θcos 2R AB ii v v =(3)每一次撞击给予器壁的冲量为θcos 2i m v(4)该分子每秒钟给予器壁的冲力为Rm R m i i i 2cos 2cos 2v v v =θθ由于结果与该分子的运动方向无关,只与速率有关,因此可得容器中所有分子每秒钟给予器壁的冲量为21212222221v v v v v v v RmN N N R m R m R m R m R m R m N i i N i i N i ===+++++∑∑== 其中n R N 334π=.根据压强的定义,分子与器壁碰撞产生的压强为W n m n nm R R m Np 3221323142222=⎪⎭⎫ ⎝⎛===v v vπ 其中W 为分子的平均平动动能.6-3 容积为10 L 的容器内有1 mol CO 2气体,其方均根速率为1440 km/h ,求CO 2气体的压强(CO 2的摩尔质量为31044-⨯kg/mol ).分析 在常温常压下可以将气体视为理想气体,理想气体压强公式中引入了统计平均量----方均根速率2v 和分子数密度n ,1 mol 的气体中分子数为阿伏图6-2伽德罗常量N A ,根据这些关系可求出压强.解 容积为V 的容器中有1 mol CO 2气体,则分子总数为N A ,摩尔质量为M ,则分子数密度为V N A ,分子质量为A N M,因此由气体压强公式得22A A 2313131v v v VM N M V N nm p ===代入数字得Pa 102.35Pa 3600101440101010443131523332⨯=⎪⎪⎭⎫ ⎝⎛⨯⨯⨯⨯⨯==--v V M p 6-4 在实验室中能够获得的最佳真空相当于大约Pa 10013.19-⨯,试问在室温(273K )下在这样的“真空”中每立方厘米内有多少个分子?分析 引入玻尔兹曼常量k 和分子数密度n 后,理想气体状态方程可以表示为nkT p =.解 由理想气体状态方程nkT p =得3-113-239m 1069.2m 2731038.110013.1⨯=⨯⨯⨯==--kT p n 6-5 已知气体密度为1 kg/m 3,压强为Pa 10013.15⨯,(1)求气体分子的方均根速率;(2)设气体为氧,求温度.分析 气体密度ρ是单位体积中气体的质量,因此与分子数密度n 和分子质量m 的关系为nm =ρ.解 压强公式可写为 223131v v ρ==nm p(1)分子的方均根速率m/s 551m/s 110013.13352=⨯⨯==ρpv(2)氧的摩尔质量M =31032-⨯kg/mol ,由定义MRT32=v ,则 K 390K 31.8310325513322=⨯⨯⨯==-R M T v6-6 体积为10-3 m 3,压强为Pa 10013.15⨯的气体,所有分子的平均平动动能的总和是多少?分析 气体动理论的能量公式给出了微观量气体分子的平均平动动能和宏观量气体温度之间的关系.分子的平均平动动能是大量分子的统计平均值,是每个分子平均占有的平动动能量值.解 由气体动理论的能量公式,分子的平均平动动能为kT m 23212=v 容器中分子数nV N =,又由压强公式nkT p =,可得容器中所有分子的平均平动动能的总和为J152J 1010013.123232321352=⨯⨯⨯===-pV kT nV m Nv6-7 一容器内贮有氧气,其压强为Pa 10013.15⨯=p ,温度T =C 27︒,求(1)单位体积内的分子数;(2)氧气的密度;(3)氧分子的质量;(4)分子间的平均距离;(5)分子的平均平动动能;(6)若容器是边长为0.30 m 的立方体,当一个分子下降的高度等于容壁的边长时,其重力势能改变多少?并将重力势能的改变与其平均平动动能相比较.分析 常温和常压下,氧气可视为理想气体.从宏观的角度,可以认为气体是空间均匀分布的,因此分子间的平均距离的立方就是每个分子平均占有的体积.通过本题的计算,可以得到气体动理论中常用到的物理量的量级概念.解 (1) 由理想气体的状态方程nkT p =,可得单位体积内的分子数为3-253-235m 1045.2m 3001038.110013.1⨯=⨯⨯⨯==-kT p n (2) 利用理想气体的状态方程RT MmpV =,氧气的密度为 3335kg/m 3.1kg/m 30031.8103210013.1=⨯⨯⨯⨯===-RT pM V m ρ(3) 氧分子的质量为kg 105.3kg 1045.23.126-25⨯=⨯==nm ρ(4) 分子平均占有的空间开方等于分子间的平均距离m 10443m 1045.21193253.n d -⨯=⨯== (5) 分子的平均平动动能J 10.216J 3001038.123232121-232⨯=⨯⨯⨯==-kT m v(6) 一个氧分子下降的高度等于容壁的边长时,其重力势能改变为J 101.56J 30.08.9103.5-2526⨯=⨯⨯⨯=-mgh与分子平均平动动能相比较,有4252121098.31056.11021.621⨯=⨯⨯=--mgh m v 6-8 在什么温度时,气体分子的平均平动动能等于一个电子由静止通过1 V 电位差的加速作用所得到的动能(即1eV 的能量).解 根据题意,气体分子的平均平动动能J 10260.1eV 12321192-⨯===kT m v 则 K 7739K 1038.1310602.122319=⨯⨯⨯⨯=--T 6-9 1 mol 氢气,在温度C 27︒时,求(1)具有若干平动动能;(2)具有若干转动动能;(3)温度每升高C 1︒时增加的总动能是多少?分析 氢气是双原子分子气体,如果作为刚性分子看待,就具有3个平动自由度和2个转动自由度,根据能量按自由度均分原则可以求出平均平动动能和平均转动动能.解 (1) 1 mol 氢气的平动动能为J 10.743J 30031.82323233A⨯=⨯⨯==RT kT N(2) 1 mol 氢气的转动动能为J 10.492J 30031.8223A⨯=⨯==RT kT N(3) 温度每升高C 1︒,1 mol 氢气增加的总动能为J 8.02J 131.8252525A=⨯⨯=∆=∆T R T k N 6-10 1 mol 单原子理想气体和1 mol 双原子理想气体,温度升高C 1︒时,其内能各增加多少?1 g 氧气和1 g 氢气温度升高C 1︒时,其内能各增加多少?分析 一定量理想气体的内能T R iM m E ∆=2,对于单原子理想气体3=i ,对于双原子理想气体5=i ,对于1 mol 理想气体1=Mm.氧气和氢气都是双原子气体,氧气的摩尔质量kg/mol 10323-⨯=M .解 1 mol 单原子理想气体温度升高C 1︒,内能增量为J 5.12J 131.8232=⨯⨯=∆T R i1 mol 双原子理想气体温度升高C 1︒,内能增量为J 8.02J 131.8252=⨯⨯=∆T R i1 g 氧气温度升高C 1︒,内能增量为J 65.0J 131.8251032101233=⨯⨯⨯⨯⨯=∆--T R i M m 1 g 氢气温度升高C 1︒,内能增量为J 4.01J 131.825102101233=⨯⨯⨯⨯⨯=∆⋅--T R i M m 6-11 计算:(1)氧分子在C 0︒时的平均平动动能和平均转动动能;(2)在此温度下,4 g 氧的内能.分析 氧气是双原子分子气体,如果作为刚性分子看待,就具有3个平动自由度和2个转动自由度,5=i .解 (1) 氧分子在C 0︒时的平均平动动能为J 10.655J 2731038.1232321-23⨯=⨯⨯⨯=-kT 平均转动动能为J 10.773J 2731038.12221-23⨯=⨯⨯==-kT kT(2) 4 g 氧在C 0︒时的内能为J 709J 27331.8251032104233=⨯⨯⨯⨯⨯=⋅--RT i M m 6-12 有40个粒子速率分布如下表所示 (其中速率单位为m/s):速率区间100以下100~200 200~300 300~400 400~500 500~600 600~700 700~800 800~900 900以上粒子数 1 4 6 8 6 5 4 3 2 1若以各区间的中值速率标志处于该区间内的粒子速率值,试求这40个粒子的平均速率v 、方均根速率2v 和最概然速率p v ,并计算出p v 所在区间的粒子数占总粒子数的百分率.分析 为了更深入地理解麦克斯韦速率分布律以及气体动理论中引入的平均速率v 、方均根速率2v 和最概然速率p v 的统计意义,有必要通过实际例子,经过计算,体验速率分布规律和统计方法.解 这40个粒子分成了10个速率区间,若取1000 m/s 为粒子速率在900 m/s 以上的速率区间的中值速率,则根据定义,其平均速率v 为m/s448.75 m/s )1100028503750465055506450 835062504150150(4011101=⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯⨯==∑=i i i N N v v 方均根速率2v 为m/s 499.9 m/s )]1100028503750465055506450 835062504150150(401[121222222222210122=⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯+⨯⨯==∑=i i i N Nv v 最概然速率m/s 350p =v .p v 所在区间的粒子数占总粒子数的百分率为%20%100408p =⨯=∆NN 6-13上题所给分布情况,若以200m/s 为间隔作重新统计,列出分布情况表,计算出相应的v 、2v 和p v ,以及p v 所在区间的粒子数占总粒子数的百分率,并与上题结果进行比较.分析 通过本题和上题计算结果可以看出,在某一速率区间中的分子数和所计算的三种速率不但与速率区间位置有关,还与速率区间的宽度有关.只有当所统计的分子总数足够大,划分的速率区间足够小时,才可能获得处于平衡状态的气体分子速率的一个确定的分布函数,三种速率也才有确定值.解 以200m/s 为间隔对上题粒子速率作重新统计,速率分布情况为(其中速率单位为m/s):速率区间 200以下 200~400 400~600 600~800 800以上 粒子数 5 14 11 7 3这40个粒子分成了5个速率区间,若取900 m/s 为粒子速率在800 m/s 以上的速率区间的中值速率,则根据定义,其平均速率v 为m/s445 m/s)3900770011500143005100(401151=⨯+⨯+⨯+⨯+⨯⨯==∑=i i i N N v v 方均根速率2v 为498m/sm/s )]39007700 11500143005100(401[121222225122=⨯+⨯+⨯+⨯+⨯⨯==∑=i i iN Nvv最概然速率m/s 300p =v .p v 所在区间的粒子数占总粒子数的百分率为%35%1004014p =⨯=∆NN 6-14 N 个假想的气体分子,速率分布如图6-14所示.(1)用N 和v 0表示出a 的值;(2)求最概然速率p v ;(3)以v 0为间隔等分为三个速率区间求各区间中分子数占总分子数的百分率.分析 速率分布函数)(v f 表示气体分子速率在v 值附近单位速率区间内的分子数占总分子数的百分率.本题给出了一个特殊的分布情况,通过计算,理解速率分布函数和最概然速率的物理意义,以及各速率区间中分子数占总分子数的百分率的计算方法.解 (1) 由图6-14可见,分布函数与气体分子总数N 的乘积曲线下的总面积应等于气体分子总数N ,即000302322121d )(0v v v v v v a a a f N =⋅+==⎰则 032v Na =Nf (v )a0 v 0 2 v 0 3 v 0 v图6-14(2) 最概然速率 0p v v =(3) 以v 0为间隔等分为三个速率区间,分子数占总分子数的百分率分别为%3.3331211d )(10010==⋅==⎰v v v v a N f N N N %5021431d )(10220==⋅==⎰v v v v v a N f N N N %7.1661411d )(103230==⋅==⎰v v v v v a N f NN N *6-15在速率区间1v ~2v 内麦克斯韦速率分布曲线下的面积等于分布在此区间内的分子数的百分率.应用(6-17)式和麦克斯韦速率分布函数表示式(6-18)式,求在速率区间v p ~1.01v p 内的气体分子数占总分子数的比率.分析 麦克斯韦速率分布律表明,由速率分布函数)(v f 可得气体分子速率在v ~v v ∆+速率区间内的分子数占分子总数的百分率为v v ∆=∆)(f NN. 解 麦克斯韦速率分布函数22232e24)(v v v kT m kT m f -⎪⎭⎫ ⎝⎛=ππ,因mkT2p =v ,则分布函数可写为1p 2p223p2p22p2e4e4)(----==v v v v v v v v v v ππππf 速率区间v p ~1.01v p 内的气体分子数占总分子数的比率为%83.001.01e 4e4e 4)(1p 2p223p 2p22p2=⨯⨯⨯=∆=∆=∆=∆----πππv v v v v v v v v v v v v f N N *6-16应用平均速率表示式(6-20)*式、麦克斯韦速率分布函数表示式(6-18)式以及积分公式bb 21d e23=-∞⎰v v v 求v 的值.分析 这里采用的是数学中加权求某量值的平均值的方法,权重就是麦克斯韦速率分布函数)(v f .如果要计算方均根速率2v ,可先求速率平方的平均值,只需将积分式中的v 改为2v ,即v v)v v d 022⎰∞=f(,再将积分结果开方.解 麦克斯韦速率分布函数表示式(6-18)式和平均速率表示式(6-20)*式给出v v v v)v v v d e24d 0322302⎰⎰∞-∞⎪⎭⎫⎝⎛==kTm kT m f(ππ利用积分公式bb 21d e 23=-∞⎰v v v 得 mkTkT m kT m f(πππ822124d 2230=⎪⎭⎫ ⎝⎛⎪⎭⎫⎝⎛==⎰∞v v)v v *6-17 试由麦克斯韦速率分布律推出相应的平动动能分布律,并求出最概然能量E p ,它是否就等于2p 21v m .分析 要找出分子按平动动能的分布规律,即求出分布在平动动能区间E k ~E k +d E k 中的分子数占总分子数的百分率.解 速率为v 的分子的平动动能为E k = 221v m ,则v v d d k m E =,麦克斯韦速率分布律可改写为kk k k 232212232223d )(d e12 d e 2112 d e 24d )(d k 22E E f E E kT m m kT kT m f N N kTE kT m kT m =⎪⎭⎫ ⎝⎛=⋅⎪⎭⎫ ⎝⎛⋅⎪⎭⎫ ⎝⎛=⎪⎭⎫ ⎝⎛==---ππππv v v v v v v v v即分子按平动动能分布律,其中分布函数kTE E kT E f k e12)(k 23k -⎪⎭⎫⎝⎛=π参考最概然速率的定义,令0d )(d kk =E E f ,由上式得最概然动能 kT E 21k p =因m kT 2p =v ,则 k p 2p 221E kT m ==v 6-18 飞机起飞前机舱中的压强计指示为Pa 10013.15⨯,温度为C 27︒.起飞后压强计指示为Pa 1010.84⨯,温度仍为C 27︒.试计算飞机此时距地面的高度.解 根据玻尔兹曼分子数密度按高度分布公式kT mgh n n /0e -=和压强公式nkT p =,在高度1h 和2h 的压强分别为1p 和2p ,则有kT h h mg p p /)(2121e --=得m 100.2m 1010.810013.1ln 8.9102930031.8 ln ln 3453212112⨯=⨯⨯⨯⨯⨯⨯==+=-p p Mg RTp p mg kT h h6-19 设地球大气是等温的,温度为C 17︒,海平面上的气压为Pa 100.150⨯=p ,已知某地的海拔高度为h = 2000 m ,空气的摩尔质量kg/m ol 10293-⨯=M ,求该地的气压值.解 根据玻尔兹曼分子数密度按高度分布公式kT mgh n n /0e -=和理想气体状态方程nkT p =,在高度h 处的压强p 为Pa 107.90Pa e100.1e 429031.820008.910295/03⨯=⨯⨯==⨯⨯⨯⨯---RT Mgh p p6-20 在某一粒子加速器中,质子在Pa 10333.14-⨯的压强和273 K 的温度的真空室内沿圆形轨道运动.(1)估计在此压强下每立方厘米内的气体分子数;(2)如果分子有效直径为2.0×10-8 cm .则在此条件下气体分子的平均自由程为多大?分析 由理想气体状态方程nkT p =可得压强和分子数密度的关系,并由此可计算平均自由程.解 (1) 由理想气体状态方程可得3103163234cm 1054.3m 1054.3m 2731038.110333.1----⨯=⨯=⨯⨯⨯==-kT p n (2) 由定义,平均自由程为cm 101.59m )102(1054.32121428102⨯=⨯⨯⨯⨯⨯==-ππλnd6-21设电子管内温度为300 K ,如果要管内分子的平均自由程大于10 cm时,则应将它抽到多大压强?(分子有效直径约为3.0×10-8 cm ).分析 由平均自由程定义和理想气体状态方程可建立压强与平均自由程以及温度之间的关系.解 由平均自由程定义221ndπλ=和理想气体状态方程nkT p =,得Pa 0.1035Pa 1.0)103(23001038.12210232=⨯⨯⨯⨯⨯==--πλπd kT p6-22 计算:(1)在标准状态下,一个氮分子在1 s 内与其它分子的平均碰撞次数;(2)容积为4 L 的容器,贮有标准状况下的氮气,求1 s 内氮分子间的总碰撞次数.(氮分子的有效直径为3.76×10-8 cm .)解 (1) 因平均速率MRTπ8=v ,标准状态下22.4 L 中的分子数为A N ,则平均碰撞次数1-91-32321033-A 22s 1067.7 s 104.2210023.6)1076.3(102827331.816 1022.4162⨯=⨯⨯⨯⨯⨯⨯⨯⨯=⨯==---πππN d M RT n d Z v(2) 4 L 氮的分子数N =A 4.224N ,分子间的总碰撞次数为1321923s 10125.4s 1067.710023.64.2242121-⨯=⨯⨯⨯⨯⨯=-Z N 6-23 假设氦气分子的有效直径为10-10 m ,压强为Pa 10013.15⨯,温度为300 K ,(1)计算氦气分子的平均自由程λ和飞行一个平均自由程所需要的时间τ;(2)如果有一个带基本电荷的氦离子在垂直于电场的方向上运动,电场强度为104 V/m ,试计算氦离子在电场中飞行τ时间内沿电场方向移动的距离s 及s 与λ的比值;(3)气体分子热运动的平均速率与氦离子在电场方向的平均速率的比值;(4)气体分子热运动的平均平动动能与氦离子在电场中飞行一个λ远的距离所获得的能量和它们的比值.解 (1) 由平均自由程定义221ndπλ=和理想气体状态方程nkT p =,得m 1029m 10013.1)10(23001038.1275210232-.pd kT ⨯=⨯⨯⨯⨯⨯==--ππλ 平均速率 m/s 1260m/s 10430031.8883=⨯⨯⨯⨯==-ππM RT v 则 s 107.3s 1260102.910-7⨯=⨯==-v λτ (2) 氦离子质量为A N M m =,沿电场方向受到的电场力为eE ,加速度meE a =,在τ时间内沿电场方向移动的距离为m 106.4m 1042103.710023.610106.1 2218-310234192A 2⨯=⨯⨯⨯⨯⨯⨯⨯⨯===---M eEN a s ττ 14.4104.6102.987=⨯⨯=--s λ(3) 氦离子沿电场方向的平均速率为m/s 87.7m/s 103.7104.6108E =⨯⨯==--τsv 14.4E==s λv v(4) 氦气分子平均平动动能为J 106.21J 3001038.1232321-23⨯=⨯⨯⨯=-kT 氦离子在电场中飞行一个λ远的距离所获得的能量为J 101.472J 102.910106.1-217419⨯=⨯⨯⨯⨯=--λeE二者之比为 22.410472.11021.62121=⨯⨯-- *6-24用范德瓦耳斯方程计算压强为Pa 10013.18⨯,体积为0.050 L 的1 mol氧气的温度,如果用理想气体状态方程计算,将引起怎样的相对误差?已知氧的范德瓦耳斯常数为:225/mol L Pa 10378.1⋅⨯=a ;L/mol 0318.0=b .解 由范德瓦耳斯方程得K 342.6K 10)0318.0050.0(050.010378.110013.131.81 )(13258020=⨯-⨯⎪⎪⎭⎫ ⎝⎛⨯+⨯⨯=-⎪⎪⎭⎫⎝⎛+=-b V V a p R T由理想气体状态方程得K .5609K 31.810050.010013.138=⨯⨯⨯==-R pV T相对误差为%7878.06.3426.3425.609==-*6-25在C 27︒时,2 mol 氮气的体积为0.1 L ,分别用范德瓦耳斯方程及理想气体状态方程计算其压强,并比较结果.已知氮气224/mol L Pa 1039.8⋅⨯=a ,L/mol 1005.32-⨯=b .解 范德瓦耳斯方程)(222RT M m b V V a M m p =-⎪⎪⎭⎫ ⎝⎛+,得Pa 109.43Pa 101039.82Pa 1005.321030031.82 782254222⨯=⨯⨯-⨯⨯-⨯⨯=--=----V a M m bMm V RTM m p 由理想气体状态方程得Pa 104.99Pa 1030031.8274⨯=⨯⨯==-V RT M m p 结果表明由理想气体状态方程计算出的压强小于由范德瓦耳斯方程的计算值.*6-26实验测知C 0︒时氧的粘滞系数1.92×10-4 s)g/(cm ⋅,试用它来求标准状态下氧分子的平均自由程和分子的有效直径.解 粘滞系数 v λρη31= 其中密度Vm=ρ.又由理想气体状态方程 RT Mm pV =平均速率MRTπ8=v ,联立可得m109.49 m 1032827331.810013.11092.138338-355⨯=⨯⨯⨯⨯⨯⨯⨯⨯===--ππηρηλM RT p v 分子的有效直径为m 102.97m 1049.910013.122731038.1 210-8523⨯=⨯⨯⨯⨯⨯⨯⨯==--πλπp kT d*6-27实验测知氮气C 0︒时热传导系数为23.7×10-3 W/(m ·K),定体摩尔热容为20.9 J/(mol ·K),试由此计算氮分子的有效直径.解 热传导系数 λρκv MC mV,31=其中密度A N nM =ρ,平均速率MRTπ8=v ,平均自由程221nd πλ=,则2Am V,132dM RT N C ππκ=m 102.23m 1102827331.810023.6107.2339.202 13210-4343233434Am V,⨯=⨯⨯⋅⨯⨯⨯⨯⨯=⋅=--ππκM RT N C d。