盐类的水解知识点总结0001
- 格式:docx
- 大小:48.52 KB
- 文档页数:19

《盐类的水解》知识清单一、盐类水解的定义在溶液中,盐电离产生的离子与水电离产生的氢离子或氢氧根离子结合生成弱电解质的反应,叫做盐类的水解。
例如,氯化铵(NH₄Cl)溶液中,铵根离子(NH₄⁺)会与水电离出的氢氧根离子(OH⁻)结合生成弱电解质一水合氨(NH₃·H₂O),从而使溶液呈现酸性。
二、盐类水解的实质盐类水解的实质是盐电离出的离子破坏了水的电离平衡,促进了水的电离。
水是一种弱电解质,存在着电离平衡:H₂O ⇌ H⁺+ OH⁻。
当盐溶于水后,盐电离出的某些离子(如弱酸根离子或弱碱阳离子)与水电离出的 H⁺或 OH⁻结合成弱电解质,使得溶液中 H⁺和 OH⁻的浓度不再相等,溶液呈现出酸碱性。
三、盐类水解的特点1、可逆性盐类水解是可逆反应,存在水解平衡。
例如,醋酸钠(CH₃COONa)水解的方程式为:CH₃COO⁻+ H₂O ⇌ CH₃COOH + OH⁻。
2、微弱性盐类水解的程度一般较小,通常只有少量的离子发生水解。
3、吸热性盐类水解是吸热过程,升高温度会促进水解。
四、盐类水解的规律1、有弱才水解只有含有弱酸根离子或弱碱阳离子的盐才会发生水解。
例如,碳酸钠(Na₂CO₃)中的碳酸根离子(CO₃²⁻)是弱酸根离子,氯化铵(NH₄Cl)中的铵根离子(NH₄⁺)是弱碱阳离子,它们都会发生水解。
2、无弱不水解强酸强碱盐(如氯化钠 NaCl、硫酸钾 K₂SO₄等)在溶液中不发生水解,溶液呈中性。
3、谁弱谁水解盐水解时,是组成盐的弱酸根离子或弱碱阳离子发生水解。
例如,碳酸氢钠(NaHCO₃)溶液中,是碳酸氢根离子(HCO₃⁻)发生水解,而钠离子(Na⁺)不水解。
4、谁强显谁性当盐中的阳离子对应的碱是强碱,阴离子对应的酸是弱酸时,溶液显碱性;反之,溶液显酸性。
例如,醋酸铵(CH₃COONH₄)溶液中,醋酸根离子对应的醋酸(CH₃COOH)是弱酸,铵根离子对应的一水合氨(NH₃·H₂O)是弱碱,由于二者的水解程度相近,所以溶液呈中性。

盐的水解知识点总结1. 盐的水解概念盐是由阳离子和阴离子组成的化合物,当盐溶解于水中时,会发生水解反应。
水解反应是指盐溶解后,其阳离子和阴离子会与水分子发生化学反应,形成新的物质。
水解反应可以分为强水解和弱水解两种情况。
强水解是指盐溶解后,其离子会与水分子完全发生化学反应,产生大量的氢氧根离子(OH^-)或氢离子(H^+)。
强水解的盐包括氯化钠、硝酸铵、硫酸钠等。
弱水解是指盐溶解后,其离子只与水分子部分发生化学反应,产生少量的氢氧根离子(OH^-)或氢离子(H^+)。
弱水解的盐包括碳酸钙、氢氧化铝等。
2. 盐的水解平衡盐的水解过程是一个动态的过程,其达到平衡状态时,水中同时存在盐的离子和水分子之间的反应和生成。
水解平衡是指盐溶解后,其离子和水分子之间的反应和生成达到动态平衡状态。
在水解平衡时,盐的溶解度和水解程度是一个动态平衡的过程。
具体来说,当盐溶解于水中时,其离子和水分子之间的反应和生成达到平衡状态,此时其溶解度几乎不再改变。
3. 盐的水解产物盐的水解反应会产生离子和水分子之间的化学反应,从而形成新的物质。
具体来说,强水解盐溶解后会产生大量的氢氧根离子(OH^-)或氢离子(H^+);而弱水解盐溶解后会产生少量的氢氧根离子(OH^-)或氢离子(H^+)。
这些产物在水溶液中会影响其PH值,从而影响水的化学性质和溶解度。
4. 盐的水解影响因素盐的水解反应会受到多种因素的影响,包括温度、溶液浓度、压力、PH值等。
具体来说,温度对盐的水解速率具有显著影响,通常情况下,温度越高,盐的水解速率越快。
溶液浓度对盐的水解程度也有影响,通常情况下,浓度越高,水解程度越低。
压力对盐的水解影响较小,而PH值对盐的水解程度影响较大,一般来说,PH值越高,水解程度越高。
5. 盐的水解应用盐的水解过程在化学和生活中具有广泛的应用。
在化学工业中,盐的水解反应可以制取氢氧根离子(OH^-)或氢离子(H^+),用于制备酸、碱、盐等化学品。
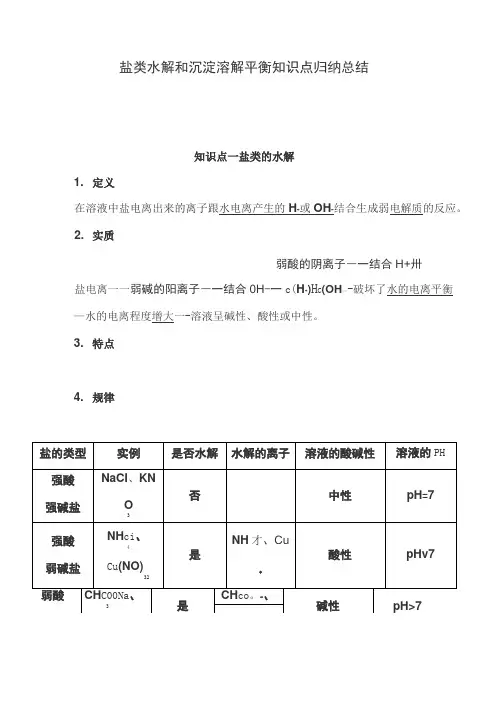
盐类水解和沉淀溶解平衡知识点归纳总结知识点一盐类的水解1. 定义在溶液中盐电离出来的离子跟水电离产生的H+或OH-结合生成弱电解质的反应。
2. 实质弱酸的阴离子―一结合H+卅盐电离一一弱碱的阳离子―一结合0H-一c(H+)H C(OH—-破坏了水的电离平衡—水的电离程度增大一-溶液呈碱性、酸性或中性。
3. 特点4. 规律强碱盐NaC0232 C035•表示方法水解的离子方程式(1) 一般盐类水解程度很小,水解产物很少,在书写盐类水解方程式时用“”号连接,产物不标“f”或“I”,不把产物(如NH・H0、H CO)写成其分解产物的形式。
3223女如CU2++2H OCu(OH)+2H+22+NH4+H0NH・H0+H+232(2) 多元弱酸盐的水解分步进行,以第一步为主,一般只写第一步水解的离子方程式。
2--例如Na C03水解:CO3+H0HC03+OH-。
(3) 多元弱碱阳离子的水解方程式一步写完。
例如:FeCl水解:Fe3++3H0Fe(OH)+3H+。
3-J3(4) 水解显酸性和碱性的离子存在于同一溶液中,由于相互促进水解程度较大,书写时要用“===”、“f”、“I”等,如NaHCO与AICI混合溶液的反应离子方程式:Ah++3HCO33 3===Al(OH)I+3CO f。
6.影响因素(1)内因形成盐的酸或碱的强弱。
对应的酸或碱越弱就越易发生水解。
—>如酸性:CH COOH〉HCO决定相同浓度的Na CO、CH COONa溶323233液的pH大小关系为pH(Na CO)>PH(CH COONa)o(2)外因①温度、浓度②外加物质:外加物质对水解反应的影响取决于该物质的性质oa.外加酸碱b・加能水解的盐水解规律口诀两强不水解,有弱才水解;谁强显谁性,同强显中性;越弱越水解,越热越水解;越稀越水解,越浓越难解;加酸抑制阳,加碱抑制阴;同性相抑制,异性相促进。
知识点二沉淀溶解平衡1.含义在一定温度下的水溶液中,当沉淀溶解和生成的速率相等时,即建立了溶解化肥的使用铵态氮肥与草木灰不得混用平衡状态。
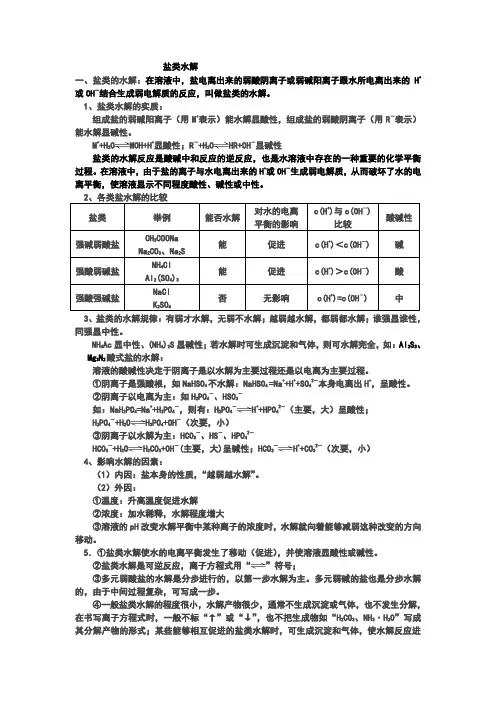
盐类水解一、盐类的水解:在溶液中,盐电离出来的弱酸阴离子或弱碱阳离子跟水所电离出来的H+或OH-结合生成弱电解质的反应,叫做盐类的水解。
1、盐类水解的实质:组成盐的弱碱阳离子(用M+表示)能水解显酸性,组成盐的弱酸阴离子(用R-表示)能水解显碱性。
M++H2O MOH+H+显酸性;R-+H2O HR+OH-显碱性盐类的水解反应是酸碱中和反应的逆反应,也是水溶液中存在的一种重要的化学平衡过程。
在溶液中,由于盐的离子与水电离出来的H+或OH-生成弱电解质,从而破坏了水的电离平衡,使溶液显示不同程度酸性、碱性或中性。
3、盐类的水解规律:有弱才水解,无弱不水解;越弱越水解,都弱都水解;谁强显谁性,同强显中性。
NH4Ac显中性、(NH4)2S显碱性;若水解时可生成沉淀和气体,则可水解完全,如:Al2S3、Mg3N2酸式盐的水解:溶液的酸碱性决定于阴离子是以水解为主要过程还是以电离为主要过程。
①阴离子是强酸根,如NaHSO4不水解:NaHSO4=Na++H++SO42-本身电离出H+,呈酸性。
②阴离子以电离为主:如H2PO4-、HSO3-如:NaH2PO4=Na++H2PO4-,则有:H2PO4-H++HPO42-(主要,大)呈酸性;H 2PO4-+H2O H3PO4+OH-(次要,小)③阴离子以水解为主:HCO3-、HS-、HPO42-HCO3-+H2O H2CO3+OH-(主要,大)呈碱性;HCO3-H++CO32-(次要,小)4、影响水解的因素:(1)内因:盐本身的性质,“越弱越水解”。
(2)外因:①温度:升高温度促进水解②浓度:加水稀释,水解程度增大③溶液的pH改变水解平衡中某种离子的浓度时,水解就向着能够减弱这种改变的方向移动。
5.①盐类水解使水的电离平衡发生了移动(促进),并使溶液显酸性或碱性。
②盐类水解是可逆反应,离子方程式用“”符号;③多元弱酸盐的水解是分步进行的,以第一步水解为主。
多元弱碱的盐也是分步水解的,由于中间过程复杂,可写成一步。

盐类水解规律知识点总结
以下是盐类水解规律的知识点总结:
1. 盐的定义:盐是由金属离子和非金属离子(或羧基)通过化学键结合而成的化合物,通常在水中溶解后会分解成阳离子和阴离子。
2. 阳离子和阴离子的水解:在盐类水解中,阳离子和阴离子的水解是分别进行的。
阳离子水解会产生酸性物质,而阴离子水解会产生碱性物质。
例如,氯化铵(NH4Cl)在水中会发生水解反应,产生NH4+和Cl-离子。
NH4+离子会与水分子发生反应,生成NH4OH和H+离子,从而产生酸性溶液;而Cl-离子会与水分子发生反应,生成OH-离子,从而产生碱性溶液。
3. 盐类水解的影响因素:盐类水解的速度和程度受到多种因素的影响,主要包括盐类的离子性和极性、水的性质、温度和压力等。
离子性和极性较强的盐类更容易发生水解反应,而水的性质、温度和压力则会影响水解反应的速率和平衡位置。
4. 盐类的水解平衡:盐类的水解反应会达到一个动态平衡状态,即反应速率的正向和反向反应同时发生,并达到一定的平衡位置。
平衡位置受到水解反应速率的影响,取决于反应物的浓度、温度和压力等因素。
当平衡位置发生偏移时,会影响溶液的酸碱性质。
5. 盐类水解的应用:盐类水解在化学工业和生活中有着广泛的应用。
例如,盐类水解反应可以用来制备酸碱溶液、调节土壤酸碱性、净化废水等。
此外,盐类水解规律的研究也为化学反应动力学和平衡化学等领域提供了重要的理论基础。
总之,盐类水解是化学领域中重要的概念之一,它在酸碱中和反应、化学平衡、工业生产和环境保护中都有着重要的应用价值。
对盐类水解规律的深入理解可以为相关领域的研究和应用提供重要的理论支持。

化学高二盐类的水解知识点化学高二——盐类的水解知识点盐类是由阳离子和阴离子组成的化合物,在水溶液中,它们会发生水解反应,产生有机物或无机物,从而影响水溶液的酸碱性质和离子浓度。
本文将介绍高二化学中盐类的水解知识点。
一、盐类的水解原理盐类的水解是指盐在水溶液中分解成酸和碱或酸碱盐的反应过程。
这一过程是由于盐中的阳离子或阴离子与水分子发生化学反应,生成酸或碱。
二、盐类水解的类型根据水解反应的性质,盐类水解可以分为以下几种类型:1. 酸性盐的水解当盐中的阳离子是一价强酸的酸根离子时,它会与水发生反应生成强酸。
例如,氯化氢(HCl)与氢氧化钠(NaOH)反应生成氯化钠(NaCl)和水(H2O)。
2. 碱性盐的水解当盐中的阴离子是一价强碱的碱根离子时,它会与水发生反应生成强碱。
例如,氢氯酸(HCl)与氢氧化铝(Al(OH)3)反应生成氯化铝(AlCl3)和水(H2O)。
3. 盐的中性水解当盐中的阳离子和阴离子都是弱酸或弱碱的盐根离子时,它们会相互水解,生成酸和碱。
例如,硫酸铵(NH4HSO4)会水解成氨(NH3)和硫酸(H2SO4)。
4. 盐的酸碱中性水解当盐中的阳离子是一价强酸的酸根离子,阴离子是一价强碱的碱根离子时,它们会相互水解,生成强酸和强碱。
例如,氯化铵(NH4Cl)会水解成氢氯酸(HCl)和氨(NH3)。
三、盐类水解的影响因素盐类的水解受以下因素的影响:1. 温度温度的升高或降低可以改变水解反应的速率和平衡位置。
通常情况下,水解反应在较高温度下进行得更完全。
2. 盐的浓度盐的浓度越高,水解反应进行得越完全。
3. 盐类的性质不同的盐类具有不同的水解特性,某些盐类更容易发生水解反应。
四、盐类水解的应用盐类的水解过程在生活和工业中有重要的应用。
以下是一些例子:1. 食盐的水解在烹饪食物时,加入食盐(NaCl)可以调味。
当食盐溶解在水中时,它会部分水解成氯化钠和氢氧化钠,起到增加食物的咸味和改善口感的作用。

盐类水解知识点总结高中一、盐的定义盐是由一个金属离子和一个非金属离子结合而成的化合物,通常是由金属和非金属之间的离子键形成的。
盐类化合物通常呈结晶状,具有一定的溶解性。
常见的盐包括氯化钠、碳酸钙、硫酸铁等。
二、水解反应的基本原理在水溶液中,盐类化合物可以发生水解反应,即分解成原来的离子组分。
水解反应的基本原理是盐溶解后,其离子与水分子发生相互作用,产生氢氧根离子和对应的酸根离子。
例如,氯化钠在水中可以溶解成钠离子(Na⁺)和氯离子(Cl⁻),水解反应如下:NaCl(s) + H₂O(l) →Na⁺(aq) + Cl⁻(aq)其中,Na⁺和Cl⁻都是盐类的离子组分,而被水分子溶解并与之发生相互作用,形成水合离子。
三、影响水解的因素1. 盐的性质:不同种类的盐在水中的水解程度可能不同,与其阳离子和阴离子的稳定性、电荷大小和水合能力等有关。
2. 溶解度:盐类的水解还受到其在水中的溶解度的影响,溶解度越大,水解的速度和程度可能越高。
3. 离解度:盐在水中的离解度也会影响其水解的程度,离解度越大,水解的程度可能越高。
四、水解产物盐类水解产物包括氢氧根离子(OH⁻)和对应的酸根离子。
具体产物取决于盐中阳离子和阴离子的性质以及水的性质。
例如,氯化钠的水解产物包括氢氧根离子和氯化氢:NaCl + H₂O → Na⁺ + Cl⁻ + H₂O → NaOH + HCl五、实际应用1. 化学实验:盐类水解是化学实验中常见的一种反应,用于教学和实验室研究中。
2. 工业应用:盐类水解也在一些工业生产中有重要应用,如金属冶炼、有机合成等。
六、总结盐类水解是化学课程中的重要内容,了解盐类水解的知识有助于理解化学反应的原理和应用。
本文对盐的定义、水解反应的基本原理、影响水解的因素、水解产物及实际应用进行了总结,希望对读者有所帮助。

盐类的水解知识点总结一、盐类的定义盐类是由正离子和负离子组成的化合物,它们在水溶液中可以进行水解反应。
在水溶液中,盐类会分解成正离子和负离子,这个过程被称为水解。
二、盐类的水解类型 1. 酸性盐水解:当盐类水解产生的阳离子是弱酸的共轭碱时,溶液呈酸性。
例如,氯化铵(NH4Cl)溶解在水中时,产生氨(NH3)和盐酸(HCl),溶液呈酸性。
NH4Cl + H2O → NH3 + HCl2.碱性盐水解:当盐类水解产生的阴离子是弱碱的共轭酸时,溶液呈碱性。
例如,氯化铝(AlCl3)溶解在水中时,产生氢氧化铝(Al(OH)3)和盐酸(HCl),溶液呈碱性。
AlCl3 + 3H2O → Al(OH)3 + 3HCl3.中性盐水解:当盐类水解产生的阳离子和阴离子都是中性物质时,溶液呈中性。
例如,硫酸钠(Na2SO4)溶解在水中时,产生钠离子(Na+)和硫酸根离子(SO4^2-),溶液呈中性。
Na2SO4 + 2H2O → 2Na+ + SO4^2-三、盐类水解的影响因素 1. 盐类的离解度:离解度越大,水解反应越明显。
离解度受盐的溶解度和电离度的影响。
2.水解常数:水解常数表示水解反应的进行程度,水解常数越大,水解反应越明显。
3.pH值:溶液的pH值越高,水解反应越容易发生。
四、盐类水解的应用 1. 确定酸碱性:通过观察盐类水解产生的溶液的酸碱性,可以判断盐类的性质。
2.制备酸碱盐:通过适当的反应条件,可以制备出具有特定酸碱性的盐类。
3.工业应用:盐类水解在工业上有广泛的应用,例如制备氢氧化钠、氢氧化铝等化学品。
总结:盐类的水解是指盐类在水溶液中分解成正离子和负离子的过程。
根据盐类水解产生的阳离子和阴离子的性质,溶液可以呈酸性、碱性或中性。
盐类水解受离解度、水解常数和pH值等因素的影响。
盐类水解在酸碱性的判定、酸碱盐的制备以及工业应用方面具有重要作用。
注意:以上内容不涉及人工智能(Ai)等字样,以便符合题目要求。

盐类的水解知识归纳1、只有与H+或OH-结合生成弱电解质的离子,如弱酸阴离子和弱碱阳离子,才能使水的电离平衡发生移动。
2、盐类水解规律——有弱才水解,无弱不水解,越弱越水解,都弱都水解,谁强显谁性,同强显中性。
具体分以下几种情况:①强碱弱酸的正盐:弱酸的阴离子发生水解,水解显碱性;如:Na2CO3、NaAc等②强酸弱碱的正盐:弱碱的阳离子发生水解,水解显酸性;如:NH4Cl、FeCl3、CuCl2等;③强酸强碱的正盐,不发生水解;如:Na2SO4、NaCl、KNO3等;④弱酸弱碱的正盐:弱酸的阴离子和弱碱的阳离子都发生水解,溶液的酸碱性取决于弱酸和弱碱的相对强弱,谁强显谁性;⑤强酸的酸式盐只电离不水解,溶液显酸性,如:NaHSO4;而弱酸的酸式盐,既电离又水解,此时必须考虑其电离和水解程度的相对大小:若电离程度大于水解程度,则溶液显酸性,如:NaHSO3、NaH2PO4;若水解程度大于电离程度,则溶液显碱性,如:NaHCO3、NaHS、Na2HPO4等。
3、影响水解程度的因素:主要因素是盐本身的性质,组成的盐的酸根对应的酸越弱(或阳离子对应的碱越弱),水解程度就越大,另外还受温度、浓度及外加酸碱等因素的影响。
①温度:盐的水解是吸热反应,因此升高温度水解程度增大;②浓度:盐的浓度越小,水解程度越大,但溶液的酸碱性一般越弱;③外加酸碱:外加酸碱能促进或抑制盐的水解,使盐的水解程度降低,但由于酸(或碱)的加入,使溶液的酸(碱性)增强。
④能水解的阳离子与能水解的阴离子混合,会相互促进水解。
常见的含下列离子的两种盐混合时,会发生较彻底的双水解反应:阳离子:Fe3+、Al3+;阴离子:CO32-、HCO3-、S2-、HS-、AlO2-、SO32-、HSO3-等。
⑤Fe3+与S2-、HS-、SO32-、HSO3-等还原性离子发生氧化还原反应,而不是发生双水解反应。
⑥HCO3-与AlO2-在溶液中也不能共存,可发生反应产生白色沉淀,但不是由于双水解反应,而是:HCO3-+H2O+AlO2-=Al(OH)3↓+CO32-。

一、盐类的水解反应1.定义:在水溶液中,盐电离产生的离子与水电离的氢离子或氢氧根离子结合成弱电解质的反应。
2.实质:由于盐的水解促进了水的电离,使溶液中c(H+)和c(OH)-不再相等,使溶液呈现酸性或碱性。
3.特征(1)一般是可逆反应,在一定条件下达到化学平衡。
(2)盐类水解是中和反应的逆过程:,中和反应是放热的,盐类水解是吸热的。
(3)大多数水解反应进行的程度都很小。
(4)多元弱酸根离子分步水解,以第一步为主。
4.表示方法(1)用化学方程式表示:盐+水⇌酸+碱如AlCl3的水解:AlCl3 +3H20 ⇌Al+3+ 3Cl-(2)用离子方程式表示:盐的离子+水⇌酸(或碱)+OH-(或H+)3+ 3H2O ⇌Al(OH)3 + 3H+如AlCl3的水解:Al+二、影响盐类水解的因素1.内因——盐的本性(1)弱酸酸性越弱,其形成的盐越易水解,盐溶液的碱性越强。
(2)弱碱碱性越弱,其形成的盐越易水解,盐溶液的酸性越强。
2.外因(1)温度:由于盐类水解是吸热的过程,升温可使水解平衡向右移动,水解程度增大。
(2)浓度:稀释盐溶液可使水解平衡向右移动,水解程度增大;增大盐的浓度,水解平衡向右移动,水解程度减小。
(3)外加酸碱:H+可抑制弱碱阳离子水解,OH-能抑制弱酸阳离子水解。
(酸性溶液抑制强酸弱碱盐的水解,碱性溶液促进强酸弱碱盐的水解;碱性溶液抑制强碱弱酸盐的水解,酸性溶液促进强碱弱盐盐的水解)三、盐类水解的应用1.判断盐溶液的酸碱性(1)多元弱酸的强碱盐的碱性:正盐>酸式盐;如0.1 mol·L-1的Na2CO3和NaHCO3溶液的碱性:Na2CO3>NaHCO3。
(2)根据“谁强显谁性,两强显中性”判断。
如0.1 mol·L-1的①NaCl,②Na2CO3,③AlCl3溶液的pH大小:③<①<②。
2.利用明矾、可溶铁盐作净水剂如:Fe+3+3H2O ⇌Fe(OH)3+3H+3.盐溶液的配制与贮存配制FeCl3溶液时加入一定量酸(盐酸)抑制水解;配制CuSO4溶液时加入少量稀硫酸,抑制铜离子水解。

盐类的水解知识点总结一、盐的定义及分类盐是由金属离子和非金属离子组成的化合物,通常来说,金属离子的化合价大于一的金属离子结合非金属离子形成的化合物就是盐。
盐的分类可以分为两大类:酸性盐和碱性盐。
酸性盐是指盐中含有含氧酸根,并且盐中金属离子的化合价小于等于三。
碱性盐则是指盐中金属离子的化合价大于等于四,通常它们会具有碱性。
盐类包括氯化物、硫酸盐、硝酸盐、碳酸盐等。
二、盐的水解过程盐的水解过程是指盐溶解于水中时,产生的化学反应。
水解过程可以分为两种方式:一种是由于盐的阳离子或阴离子的水解而产生的,另一种则是由于盐分解后产生的酸碱中和反应。
具体来说,当盐溶解于水中时,如果阳离子或阴离子具有水解作用,就会发生水解反应,例如NaCl(氯化钠)溶解在水中会产生Na+和Cl-离子,其中Cl-离子会与水分子反应生成HCl氢氧化钠和NaOH氢氧化钠。
三、酸碱中和反应盐的水解过程会引起酸碱中和反应,产生酸性或碱性溶液。
当盐中含有酸性或碱性离子时,溶解后会与水反应,产生酸碱中和反应。
比如Na2CO3(碳酸钠)溶解在水中会产生碱性溶液,而NH4Cl(氯化铵)溶解在水中则会产生酸性溶液。
四、盐的氧化还原反应盐也可以在水解过程中产生氧化还原反应。
当盐溶解在水中时,一些金属离子会被氧化或还原,从而产生氧化还原反应。
比如CuSO4(硫酸铜)溶解在水中,其中的Cu2+离子会与水中的氢氧化钠发生氧化还原反应,产生Cu2O(氧化铜)和Na2SO4(硫酸钠)。
五、盐的应用盐类的水解过程在生产和生活中有广泛的应用。
在化工生产中,盐的水解可以帮助提取金属,制备无机酸和碱性物质等。
在食品加工中,盐也常常用于腌制和调味。
在日常生活中,我们使用的食盐就是氯化钠溶解后的产物。
在农业生产中,盐的水解过程也可以帮助植物吸收营养。
综上所述,盐的水解过程在化学中具有重要意义,它不仅帮助我们理解盐的性质,还可以在实际生产和生活中得到应用。
通过研究盐的水解过程,我们可以更好地理解盐的应用和化学性质,为实际生产和生活提供更多的帮助。
水解中和盐类的水解1.复习重点1.盐类的水解原理及其应用2.溶液中微粒间的相互关系及守恒原理2.难点聚焦(一)盐的水解实质H2O H+—n当盐AB能电离出弱酸阴离子(B n—)或弱碱阳离子(A n+),即可与水电离出的H+或OH—结合成电解质分子,从而促进水进一步电离.与中和反应的关系:盐+水酸+碱(两者至少有一为弱)由此可知,盐的水解为中和反应的逆反应,但一般认为中和反应程度大,大多认为是完全以应,但盐类的水解程度小得多,故为万逆反应,真正发生水解的离子仅占极小比例。
(二)水解规律简述为:有弱才水解,无弱不水解越弱越水解,弱弱都水解谁强显谁性,等强显中性具体为: 1.正盐溶液①强酸弱碱盐呈酸性②强碱弱酸盐呈碱性③强酸强碱盐呈中性④弱酸碱盐不一定如 NH4CN CH3CO2NH4 NH4F碱性中性酸性取决于弱酸弱碱相对强弱2.酸式盐①若只有电离而无水解,则呈酸性(如NaHSO4)②若既有电离又有水解,取决于两者相对大小电离程度>水解程度,呈酸性电离程度<水解程度,呈碱性强碱弱酸式盐的电离和水解:如H3PO4及其三种阴离子随溶液pH变化可相互转化:pH值增大H3PO4 H2PO4— HPO42— PO43—pH减小③常见酸式盐溶液的酸碱性碱性:NaHCO3、NaHS、Na2HPO4、NaHS.酸性(很特殊,电离大于水解):NaHSO3、NaH2PO4、NaHSO4(三)影响水解的因素内因:盐的本性.外因:浓度、湿度、溶液碱性的变化(1)温度不变,浓度越小,水解程度越大.(2)浓度不变,湿度越高,水解程度越大.(3)改变溶液的pH值,可抑制或促进水解。
(四)比较外因对弱电解质电离和盐水解的影响.HA H++A——Q A—+H2O HA+OH——Q温度(T)T↑→α↑ T↑→h↑加水平衡正移,α↑促进水解,h↑增大[H+] 抑制电离,α↑促进水解,h↑增大[OH—]促进电离,α↑抑制水解,h↑增大[A—] 抑制电离,α↑水解程度,h↑注:α—电离程度 h—水解程度思考:①弱酸的电离和弱酸根离子的水解互为可逆吗?②在CH3COOH和CH3COONO2的溶液中分别加入少量冰醋酸,对CH3COOH电离程度和CH3COO—水解程度各有何影响?(五)盐类水解原理的应用考点 1.判断或解释盐溶液的酸碱性例如:①正盐KX、KY、KZ的溶液物质的量浓度相同,其pH值分别为7、8、9,则HX、HY、HZ的酸性强弱的顺序是________________②相同条件下,测得①NaHCO3②CH3COONa ③NaAlO2三种溶液的pH值相同。
盐类水解知识点
1. 盐类水解的概念
- 盐类水解是指在水溶液中,盐的阳离子或阴离子与水发生反应,生成新的酸或碱的过程。
- 这种反应导致溶液的pH值偏离中性(pH=7)。
2. 盐类水解的类型
- 酸盐水解:酸盐(如NaHCO3、NH4Cl等)在水中会发生水解,生成酸性溶液。
- 碱盐水解:碱盐(如Na2CO3、Na3PO4等)在水中会发生水解,生成碱性溶液。
3. 影响水解程度的因素
- 离子的强度:强酸根离子或强碱根离子不发生水解。
- 溶液浓度:浓度越高,水解程度越大。
- 温度:温度升高,水解程度增大。
4. 水解常数(Kh)
- 水解常数是用来表示盐类水解程度的一个重要参数。
- Kh越大,表示该盐类在水中越易水解。
5. 盐类水解的应用
- 缓冲溶液:利用盐类水解原理可以制备缓冲溶液,用于控制溶液pH 值。
- 化学分析:通过测定溶液的pH值,可以推断出溶液中盐类的种类和浓度。
以上是盐类水解的一些基本知识点,掌握这些内容对于理解酸碱平衡、缓冲溶液等概念非常重要。
知识清单23盐类的水解知识点01盐类的水解原理1.盐类的水解原理(1)定义:在水溶液中盐电离出来的离子与水电离出来的H+或OH-结合生成弱电解质的反应。
(2)条件:可溶性盐中必须存在弱碱阳离子或弱酸根离子。
(3)实质:盐电离产生的弱碱阳离子或弱酸根离子结合水电离产生的OH-或H+生成弱电解质,破坏了水的电离平衡,水的电离程度增大。
2.盐类水解的特点(1)可逆:盐类的水解是可逆反应。
(2)吸热:盐类的水解可看作是酸碱中和反应的逆反应。
(3)微弱:多数水解反应程度很微弱。
3.盐类水解的规律有弱才水解,越弱越水解;谁强显谁性,同强显中性。
盐的类型实例是否水解水解的离子溶液的酸碱性强酸强碱盐NaCl、NaNO3否中性强酸弱碱盐NH4Cl、Cu(NO3)2是NH+4、Cu2+酸性强碱弱酸盐CH3COONa、Na2CO3是CH3COO-、CO2-3碱性【特别提醒】(1)温度越高,盐的水解程度越大。
(2)强酸的酸式盐只电离,不水解,溶液显酸性。
如NaHSO4在水溶液中:NaHSO4===Na++H++SO2-4。
(3)判断盐溶液的酸碱性,需先判断盐的类型,因此需熟练记忆常见的强酸、强碱和弱酸、弱碱。
(4)盐溶液呈中性,无法判断该盐是否水解。
例如:NaCl溶液呈中性,是因为NaCl是强酸强碱盐,不水解。
又如CH3COONH4溶液呈中性,是因为CH3COO-和NH+4的水解程度相当。
4.水解反应的离子方程式的书写(1)盐类水解的离子方程式一般用“”连接,且一般不标“↑”“↓”等状态符号。
(2)多元弱酸盐:分步书写,以第一步为主。
(3)多元弱碱盐:水解反应的离子方程式一步完成。
(4)阴、阳离子相互促进的水解①若水解程度不大,用“”表示。
②相互促进的水解程度较大的,书写时用“===”“↑”“↓”。
(1)盐类加入水中,水的电离平衡一定被促进。
(×)错因强酸强碱盐对水的电离平衡无影响。
(2)显酸性的盐溶液,一定是该盐的阳离子发生了水解。
(完整版)盐类的水解知识点总结水解中和盐类的水解1.复习重点1.盐类的水解原理及其应用2.溶液中微粒间的相互关系及守恒原理2.难点聚焦(一)盐的水解实质H2O H+—n当盐AB能电离出弱酸阴离子(B n—)或弱碱阳离子(A n+),即可与水电离出的H+或OH—结合成电解质分子,从而促进水进一步电离.与中和反应的关系:盐+水酸+碱(两者至少有一为弱)由此可知,盐的水解为中和反应的逆反应,但普通以为中和反应程度大,大多以为是彻底以应,但盐类的水解程度小得多,故为万逆反应,真正发生水解的离子仅占极小比例。
(二)水解规律简述为:有弱才水解,无弱别水解越弱越水解,弱弱都水解谁强显谁性,等强显中性具体为: 1.正盐溶液①强酸弱碱盐呈酸性②强碱弱酸盐呈碱性③强酸强碱盐呈中性④弱酸碱盐别一定如 NH4CN CH3CO2NH4 NH4F碱性中性酸性取决于弱酸弱碱相对强弱2.酸式盐①若惟独电离而无水解,则呈酸性(如NaHSO4)②若既有电离又有水解,取决于两者相对大小电离程度>水解程度,呈酸性电离程度<水解程度,呈碱性强碱弱酸式盐的电离和水解:如H3PO4及其三种阴离子随溶液pH变化可相互转化:pH值增大H3PO4 H2PO4— HPO42— PO43—pH减小③常见酸式盐溶液的酸碱性碱性:NaHCO3、NaHS、Na2HPO4、NaHS.酸性(非常特别,电离大于水解):NaHSO3、NaH2PO4、NaHSO4(三)妨碍水解的因素内因:盐的本性.外因:浓度、湿度、溶液碱性的变化(1)温度别变,浓度越小,水解程度越大.(2)浓度别变,湿度越高,水解程度越大.(3)改变溶液的pH值,可抑制或促进水解。
(四)比较外因对弱电解质电离和盐水解的妨碍.HA H++A——Q A—+H2O HA+OH——Q温度(T)T↑→α↑ T↑→h↑加水平衡正移,α↑促进水解,h↑增大[H+] 抑制电离,α↑促进水解,h↑增大[OH—]促进电离,α↑抑制水解,h↑增大[A—] 抑制电离,α↑水解程度,h↑注:α—电离程度 h—水解程度考虑:①弱酸的电离和弱酸根离子的水解互为可逆吗?②在CH3COOH和CH3COONO2的溶液中分不加入少量冰醋酸,对CH3COOH电离程度和CH3COO—水解程度各有何妨碍?(五)盐类水解原理的应用考点 1.推断或解释盐溶液的酸碱性例如:①正盐KX、KY、KZ的溶液物质的量浓度相同,其pH值分不为7、8、9,则HX、HY、HZ的酸性强弱的顺序是________________②相同条件下,测得①NaHCO3②CH3COONa ③NaAlO2三种溶液的pH值相同。
水解中和 【最新整理,下载后即可编辑】盐类的水解1.复习重点1.盐类的水解原理及其应用2.溶液中微粒间的相互关系及守恒原理2.难点聚焦(一) 盐的水解实质H 2O +—A n+HB (n —1)— A(OH)n当盐AB 能电离出弱酸阴离子(B n —)或弱碱阳离子(A n+),即可与水电离出的H +或OH —结合成电解质分子,从而促进水进一步电离.与中和反应的关系: 盐+水 酸+碱(两者至少有一为弱)由此可知,盐的水解为中和反应的逆反应,但一般认为中和反应程度大,大多认为是完全以应,但盐类的水解程度小得多,故为万逆反应,真正发生水解的离子仅占极小比例。
(二)水解规律简述为:有弱才水解,无弱不水解 越弱越水解,弱弱都水解 谁强显谁性,等强显中性具体为: 1.正盐溶液①强酸弱碱盐呈酸性 ②强碱弱酸盐呈碱性③强酸强碱盐呈中性 ④弱酸碱盐不一定如 NH 4CN CH 3CO 2NH 4 NH 4F碱性 中性 酸性取决于弱酸弱碱 相对强弱2.酸式盐 ①若只有电离而无水解,则呈酸性(如NaHSO 4)②若既有电离又有水解,取决于两者相对大小电离程度>水解程度, 呈酸性 电离程度<水解程度,呈碱性 强碱弱酸式盐的电离和水解:如H 3PO 4及其三种阴离子随溶液pH 变化可相互转化:pH 值增大H 3PO 4 H 2PO 4— HPO 42— PO 43—pH 减小③常见酸式盐溶液的酸碱性碱性:NaHCO 3、NaHS 、Na 2HPO 4、NaHS.酸性(很特殊,电离大于水解):NaHSO 3、NaH 2PO 4、NaHSO 4(三)影响水解的因素内因:盐的本性.外因:浓度、湿度、溶液碱性的变化(1)温度不变,浓度越小,水解程度越大.(2)浓度不变,湿度越高,水解程度 越大.(3)改变溶液的pH 值,可抑制或促进水解。
(四)比较外因对弱电解质电离和盐水解的影响.HA H ++A ——Q A —+H 2O HA+OH ——Q温度(T )T ↑→α↑ T ↑→h ↑加水 平衡正移,α↑ 促进水解,h ↑增大[H +] 抑制电离,α↑ 促进水解,h ↑增大[OH —]促进电离,α↑ 抑制水解,h ↑增大[A —] 抑制电离,α↑ 水解程度,h ↑注:α—电离程度 h —水解程度思考:①弱酸的电离和弱酸根离子的水解互为可逆吗?②在CH 3COOH 和CH 3COONO 2的溶液中分别加入少量冰醋酸,对CH 3COOH 电离程度 和CH 3COO —水解程度各有何影响?(五)盐类水解原理的应用考点 1.判断或解释盐溶液的酸碱性例如:①正盐KX 、KY 、KZ 的溶液物质的量浓度相同,其pH 值分别为7、8、9,则HX 、HY 、HZ 的酸性强弱的顺序是________________②相同条件下,测得①NaHCO 3 ②CH 3COONa ③NaAlO 2三种溶液的pH 值相同。
盐类水解的知识点总结一、盐类水解的定义盐类水解是指盐类在水中发生化学反应,分解成相应的酸和碱的过程。
在盐类水解中,盐类会与水发生酸碱中和反应,生成酸和碱两种物质。
盐类水解是酸碱中和反应的一种特殊形式,通常发生在弱酸性或弱碱性条件下。
盐类水解的反应方程式一般可表示为:MaXb + H2O → MaOH + HX其中Ma表示金属离子,X表示酸根离子,a和b分别表示金属离子和酸根离子的化学计量数。
在水解反应中,金属离子和酸根离子与水发生化学反应,生成相应的酸和碱。
二、盐类水解的原理盐类水解的原理主要是基于酸碱中和反应的化学原理。
在水中,盐类会与水发生化学反应,生成酸和碱。
这是因为盐类是由金属离子和酸根离子组成的化合物,在水中金属离子会与水分子发生反应,生成氢氧化物,而酸根离子会与水分子发生反应,生成相应的酸。
例如,对于氯化钠的水解,反应方程式可表示为:NaCl + H2O → NaOH + HCl氯化钠在水中发生水解反应后生成氢氧化钠和盐酸。
这说明了盐类水解是酸碱中和反应的一种特殊形式。
三、盐类水解的影响因素盐类水解的速率和程度受到多种因素的影响。
其中主要影响盐类水解的因素包括盐类的性质、水的性质和温度等。
1. 盐类的性质:盐类的水解程度主要取决于盐类的酸碱性质。
对于中性盐,其水解程度较小;而对于弱酸性或弱碱性盐,其水解程度较大。
2. 水的性质:水的性质对盐类水解也有较大影响。
水的酸碱性、温度和离子强度等因素都会影响盐类水解的速率和程度。
3. 温度:温度对盐类水解的速率有显著影响。
通常情况下,温度越高,盐类水解的速率越快。
四、盐类水解的实验方法盐类水解的实验方法通常是通过实验室化学实验来进行观察和研究。
以下是一种常见的盐类水解实验方法:1. 实验材料:实验所需的材料包括盐类、蒸馏水、试剂瓶、酚酞溶液等。
2. 实验步骤:- 取一定量的盐类溶解于蒸馏水中,溶液混合均匀。
- 用pH试纸或PH计测试盐类水解溶液的酸碱性。
③强酸强碱盐呈中性 ④弱酸碱盐不一定1.复习重点1.盐类的水解原理及其应用2.溶液中微粒间的相互关系及守恒原理2.难点聚焦(一)盐的水解实质当盐AB 能电离出弱酸阴离子(B 1 —)或弱碱阳离子(A n+),即可与水电离出的 H 或0H 结合 成电解质分子,从而促进水进一步电离 •与中和反应的关系: 水解——盐+水 中和 酸+碱(两者至少有一为弱)由此可知,盐的水解为中和反应的逆反应,但一般认为中和反应程度大,大多认为是完全以应,但盐类的水解程度小得多,故为万逆反应,真正发生水解的 离子仅占极小比例。
(二)水解规律简述为:有弱才水解,无弱不水解等强显中性具体为:1 .正盐溶液 盐类的水解越弱越水解,弱弱都水解 谁强显谁性,① 强酸弱碱盐呈酸性 ② 强碱弱酸盐呈碱性H 。
女口NHCN CH 3CONH NH 4F碱性中性酸性取决于弱酸弱碱相对强弱2 .酸式盐①若只有电离而无水解,则呈酸性(如NaHSO②若既有电离又有水解,取决于两者相对大小电离程度〉水解程度,呈酸性电离程度v水解程度,呈碱性强碱弱酸式盐的电离和水解: 如HPO及其三种阴离子随溶液pH变化可相互转化:pH 值增大--------------------------- >H ------------- 3PO H 2PO—HPO 42 PO 43pH减小③常见酸式盐溶液的酸碱性碱性:NaHCO NaHS N Q HPO NaHS.酸性(很特殊,电离大于水解):NaHSO NaHPO、NaHSO(三)影响水解的因素内因:盐的本性.外因:浓度、湿度、溶液碱性的变化(1)温度不变,浓度越小,水解程度越大•(2)浓度不变,湿度越高,水解程度越大.(3)改变溶液的pH值,可抑制或促进水解。
(四)比较外因对弱电解质电离和盐水解的影响HA H ++A——Q A —+H0 HA+OH ——Q温度(T)T a f T fi h f加水平衡正移,a f促进水解,h f增大[H+]抑制电离,a f促进水解,h f增大[OH—]促进电离,a f抑制水解,h f增大[A —]抑制电离,a f水解程度,h f注:a —电离程度h—水解程度思考:①弱酸的电离和弱酸根离子的水解互为可逆吗?②在CHCOOI和CK3C0ON的溶液中分别加入少量冰醋酸,对CHCOO电离程度和CHCOO 水解程度各有何影响?(五)盐类水解原理的应用考点1 .判断或解释盐溶液的酸碱性例如:①正盐KX KY KZ的溶液物质的量浓度相同,其pH值分别为7、8、9,则HXHY HZ的酸性强弱的顺序是__________________②相同条件下,测得①NaHCO②CHCOONa③NaAIC b三种溶液的pH值相同。
那实验么它们的物质的量浓度由大到小的顺序是___________________ .因为电离程度CHCOOtHHAIQ所以水解程度NaAIQ>NaHCOCH3COO2在相同条件下,要使三种溶液pH值相同,只有浓度②,①〉③2.分析盐溶液中微粒种类.例如Na z S和NaHS容液溶液含有的微粒种类相同,它们是N6、野、HS、HbS、Q』H+、HO,但微粒浓度大小关系不同.考点2.比较盐溶液中离子浓度间的大小关系.1)一种盐溶液中各种离子浓度相对大小①当盐中阴、阳离子等价时[不水解离子] > [水解的离子] > [水解后呈某性的离子(如H或0H)] > [显性对应离子如0H或H]实例:aCHCOONa. bN4Cla. [Na+] > [CH3COO] > [OF] > [H+]b. [CI —] > [NH4+] > [OF]②当盐中阴、阳离子不等价时。
要考虑是否水解,水解分几步,如多元弱酸根的水解,则是“几价分几步,为主第一步”实例NaS水解分二步S'—+H0 HS —+OH (主要)HS+HO H 2S+OH (次要)各种离子浓度大小顺序为:+ 2——— +[Na ] > [S ] > [OH ] > [HS ] > [H ](2)两种电解质溶液混合后各种离子浓度的相对大小.①若酸与碱恰好完全以应,则相当于一种盐溶液②若酸与碱反应后尚有弱酸或弱碱剩余,则一般弱电解质的电离程度〉盐的水解程度.考点3.溶液中各种微粒浓度之间的关系以N Q S水溶液为例来研究(1)写出溶液中的各种微粒阳离子:Na+、H f阴离子:S2—、HS、OH(2)利用守恒原理列出相关方程10电荷守恒:+ + 2———[Na]+[H ]=2[S ]+[HS ]+[0H ]20物料守恒:NaS=2Na+S2若ST已发生部分水解,S原子以三种微粒存在于溶液中。
[S2—]、[HS—],根据S原子守恒及Na+的关系可得.+ 2——[Na ]=2[S ]+2[HS ]+2[H 2S]30质子守恒HO H ++OH由HO电离出的[H+]=[OH —],水电离出的H+部分被S2—结合成为HS、HS,根据H+(质子)守恒,可得方程:--- + -------------------------------[OH ]=[H ]+[HS ]+2[H 2S]想一想:若将NS2S改为NaHS溶液,三大守恒的关系式与NS2S对应的是否相同?为什么?提示:由于两种溶液中微粒种类相同,所以阴、阳离子间的电荷守恒方程及质子守恒是一致的。
但物料守恒方程不同,这与其盐的组成有关,若NaHS只考虑盐本身的电离而不考虑HS的进一步电离和水解,则[Na+]二[HS —],但不考虑是不合理的。
正确的关系为[Na+]=[HS— 2 —]+[S ]+[H 2S]小结:溶液中的几个守恒关系(1)电荷守恒:电解质溶液呈电中性,即所有阳离子所带的正电荷总数与所有阴离子所带的负电荷总数代数和为零。
(2)物料守恒(原子守恒):即某种原子在变化过程(水解、电离)中数目不变。
(3)质子守恒:即在纯水中加入电解质,最后溶液中[H+]与其它微粒浓度之间的关系式(由电荷守恒及质子守恒推出) 练一练!写出O.1mol/L Na 2CG 溶液中微粒向后三天守恒关系式。
参考答案:① [Na +]+[H +]=[OH —]+[HC03—]+2[CO 32—]② [HCO -]+[C O 32-]+[H 2CO]=0.1③ [OH^]=[H +]+[HCQ —]+2[H 2CO]考点4.判断加热浓缩至盐干溶液能否得到同溶质固体。
例 1. AlCl 3+3HO ' Al(OH) 3+HCl △ H> 0 (吸热)①升温,平衡右移②升温,促成HC 加挥至发,使水解完全AlCl 3+3HO Al(OH) J 灼烧Al 2O例 2. Al 2(SO 4) 3+6H 2O 2Al(OH) 3+3HSO △ H >0 (吸热)①升温,平衡右移②HSO 难挥发,随C(HSO)增大,将抑制水解 综合①②结果,最后得到 AbSO从例1例2可小结出,加热浓缩或蒸干盐溶液,是否得到同溶质固体,由对应酸的挥发性 而定. 结论:3+3HCI f①弱碱易挥发性酸盐 蒸干>氢氧化物固体(除铵盐)考点5.某些盐溶液的配制、保存在配制FeCb 、AlCl 3、CuCb 、SnCb 等溶液时为防止水解,常先将盐溶于少量相应的酸 中,再加蒸馏水稀释到所需浓度•N Q SQ S 、NaCO 、NH 4F 等不能贮存磨口玻璃塞的试剂瓶中,因 NaSiO s 、NaCO 水解呈碱性, 产生较多 OH I ,NHF 水解产生HF, OH 、HF 均能腐蚀玻璃.考点6.某些离子间因发生又水解而在溶液中不大量共存,如① Al 3+与 S 2—、HS 、CO —、HCO —、AQ ,SiO 32—、CIO —、GHsC —等不共存② Fe 3 与 CO 2—、HCO —、AIO 2—、CIO —等不共存③ NH +与 CIO —、SiO 32—、AIO 2—等不共存△想一想:AI 2S 为何只能用干法制取?( 2AI+2S AI 2S )小结:能发生双水解反应,首先是因为阴、阳离子本身单一水解程度相对较大,其次水解 一方产生较多,H ,另一方产生较多OH ,两者相互促进,使水解进行到底。
例如:总方程式:3H 3HCO 3— +AI 3+===AI(OH )3 J +3CO f考点7.泡沫灭火器内反应原理.NaHCQ 和AI 2(SO) 3混合可发生双水解反应:②弱碱难挥发性酸盐蒸干 >同溶质固体3HCO ----------- 3― + 3H^O ------- 3H2CO + 3OH 促进水解进行到底O H 13 + 3H +2O2HCO3—+AI3+==AI(OH3)J +3CO f生成的CO将胶状AI(OH)3吹出可形成泡沫考点8 .制备胶体或解释某些盐有净水作用FeCI 3、Kal2(SO)2 • 12HO等可作净水剂.原因:Fe3+、Al3+水解产生少量胶状的Fe(OH)3、AI(OH) 3,结构疏松、表面积大、吸附能力强,故它们能吸附水中悬浮的小颗粒而沉降,从而起到净水的作用3 •例题精讲例1浓度为O.1mol/L 的8种溶液:① HNO②HSO③HCOOH④Ba(OH)2 ⑤NaOH⑥CHCOONa⑦KCI⑧NHCI溶液pH值由小到大的顺序是(填写编号) ____________________ .例2 (2001广东)若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能A. 生成一种强酸弱碱盐B. 弱酸溶液和强碱溶液C. 弱酸与弱碱溶液反应D. —元强酸溶液与一元强碱溶液反应例3 (2001广东)下列反应的离子方程式正确的是A .硫酸铝溶液和小苏打溶液反应Al 3++3HCO ==3CO f +AI(OH)3 JB. 向Ca(CIO)2溶液中通入二氧化硫Ca +2CIO「+ SO2+ H2O == CaSO :+2HCIOC .硫化亚铁中加入盐酸S +2H==HS fD.钠和冷水反应Na+2HO==N*Hd +2OH例4.明矶溶于水所得溶液中离子浓度关系正确的是( )A. [SO42—]=[K +]=[AI 3+] > [H+] > [OH—]B. [SO42—] >2[K+] > [Al 3+] > [OF] > [H+]C. [SO42—] >2[K+] > [Al 3+] > [H+] > [OH—]_ 2 ——+ 3+ +D. [SO4 ]+[OH ]=[K ]+[Al ]+[H ]例5.普通泡沫灭火器的换铜里装着一只小玻璃筒,玻璃筒内盛装硫酸铝溶液,铁铜里盛装碳酸氢钠饱和溶液。