第四章 红外分光光光度法(书后习题参考答案)
- 格式:doc
- 大小:115.00 KB
- 文档页数:3

红外吸收光谱法一.填空题1.一般将多原子分子的振动类型分为伸缩振动和变形振动,前者又可分为对称伸缩振动和反对称伸缩振动,后者可分为面内剪式振动(δ)、面内摇摆振动(ρ) 和面外摇摆振动(ω)、面外扭曲振动(τ) 。
2.红外光区在可见光区和微波光区之间,习惯上又将其分为三个区: 远红外区,中红外区和近红外区,其中中红外区的应用最广。
3.红外光谱法主要研究振动中有偶极矩变化的化合物,因此,除了单原子和同核分子等外,几乎所有的化合物在红外光区均有吸收.4.在红外光谱中,将基团在振动过程中有偶极矩变化的称为红外活性,相反则称为红外非活性的 .一般来说,前者在红外光谱图上出现吸收峰。
5.红外分光光度计的光源主要有能斯特灯和硅碳棒 .6.基团一OH、一NH;==CH的一CH的伸缩振动频率范围分别出现在3750—3000 cm-1, 3300-3000 cm—1,3000-2700 cm-1。
7.基团一C≡C、一C≡N ;-C==O;一C=N,一C=C—的伸缩振动频率范围分别出现在2400—2100 cm-1,1900-1650 cm—1,1650—1500 cm-1。
8.4000-1300 cm—1 区域的峰是由伸缩振动产生的,基团的特征吸收一般位于此范围,它是鉴最有价值的区域,称为官能团区;1300—600 cm-1 区域中,当分子结构稍有不同时,该区的吸收就有细微的不同,犹如人的指纹一样,故称为指纹区。
二、选择题1.二氧化碳分子的平动、转动和振动自由度的数目分别(A)A. 3,2,4B. 2,3,4 C。
3,4,2 D。
4,2,32.乙炔分子的平动、转动和振动自由度的数目分别为(C)A。
2,3,3 B. 3,2,8 C. 3,2,7 D. 2,3,74.下列数据中,哪一组数据所涉及的红外光谱区能够包括CH3CH2COH的吸收带?(D)A. 3000-2700cm—1,1675—1500cm-1,1475-1300cm一1.B. 3300—3010cm—1,1675-1500cm—1,1475-1300cm-1.C。
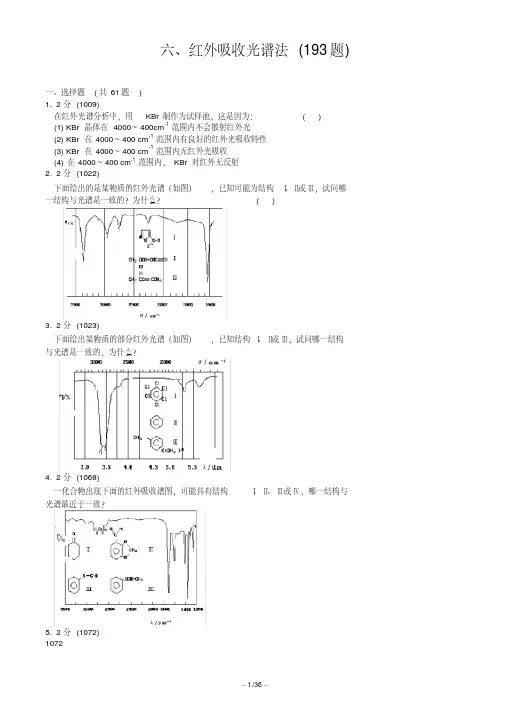
六、红外吸收光谱法(193题)一、选择题( 共61题)1. 2 分(1009)在红外光谱分析中,用 KBr制作为试样池,这是因为: ( )(1) KBr 晶体在 4000~400cm-1范围内不会散射红外光(2) KBr 在 4000~400 cm-1范围内有良好的红外光吸收特性(3) KBr 在 4000~400 cm-1范围内无红外光吸收(4) 在 4000~400 cm-1范围内,KBr 对红外无反射2. 2 分(1022)下面给出的是某物质的红外光谱(如图),已知可能为结构Ⅰ、Ⅱ或Ⅲ,试问哪一结构与光谱是一致的?为什么? ( )3. 2 分(1023)下面给出某物质的部分红外光谱(如图),已知结构Ⅰ、Ⅱ或Ⅲ,试问哪一结构与光谱是一致的,为什么?4. 2 分(1068)一化合物出现下面的红外吸收谱图,可能具有结构Ⅰ、Ⅱ、Ⅲ或Ⅳ,哪一结构与光谱最近于一致?5. 2 分(1072)1072羰基化合物中,C = O 伸缩振动频率出现最低者为 ( )(1) I (2) II (3) III (4) IV6. 2 分(1075)一种能作为色散型红外光谱仪色散元件的材料为 ( )(1) 玻璃 (2) 石英 (3) 卤化物晶体 (4) 有机玻璃7. 2 分(1088)并不是所有的分子振动形式其相应的红外谱带都能被观察到,这是因为 ( )(1) 分子既有振动运动,又有转动运动,太复杂(2) 分子中有些振动能量是简并的(3) 因为分子中有 C、H、O 以外的原子存在(4) 分子某些振动能量相互抵消了8. 2 分(1097)下列四组数据中,哪一组数据所涉及的红外光谱区能够包括CH3- CH2-CH = O的吸收带( )9. 2 分(1104)请回答下列化合物中哪个吸收峰的频率最高? ( )10. 2 分(1114)在下列不同溶剂中,测定羧酸的红外光谱时,C=O 伸缩振动频率出现最高者为( )(1) 气体 (2) 正构烷烃 (3) 乙醚 (4) 乙醇11. 2 分(1179)水分子有几个红外谱带,波数最高的谱带对应于何种振动 ? ( )(1) 2 个,不对称伸缩 (2) 4 个,弯曲(3) 3 个,不对称伸缩 (4) 2 个,对称伸缩12. 2 分(1180)CO2的如下振动中,何种属于非红外活性振动 ? ( )(1) ←→ (2) →←→ (3)↑↑ (4 )O=C=O O = C =O O = C =O O = C = O↓13. 2 分(1181)苯分子的振动自由度为 ( )(1) 18 (2) 12 (3) 30 (4) 3114. 2 分(1182)双原子分子在如下转动情况下 (如图),转动不形成转动自由度的是 ( )15. 2 分(1183)任何两个振动能级间的能量差为 ( )(1) 1/2 h (2) 3/2 h (3) h (4) 2/3 h16. 2 分(1184)在以下三种分子式中 C=C 双键的红外吸收哪一种最强? ( )(a) CH3- CH = CH2(b) CH3- CH = CH - CH3(顺式)(c) CH3- CH = CH - CH3(反式)(1) a 最强 (2) b 最强 (3) c 最强 (4) 强度相同17. 2 分(1206)在含羰基的分子中,增加羰基的极性会使分子中该键的红外吸收带 ( )(1) 向高波数方向移动 (2) 向低波数方向移动(3) 不移动 (4) 稍有振动18. 2 分(1234)以下四种气体不吸收红外光的是 ( )(1)H2O (2)CO2 (3)HCl (4)N219. 2 分(1678)某化合物的相对分子质量M r=72,红外光谱指出,该化合物含羰基,则该化合物可能的分子式为 ( )(1) C4H8O (2) C3H4O2 (3) C3H6NO (4) (1)或(2)20. 2 分(1679)红外吸收光谱的产生是由于 ( )(1) 分子外层电子、振动、转动能级的跃迁(2) 原子外层电子、振动、转动能级的跃迁(3) 分子振动-转动能级的跃迁(4) 分子外层电子的能级跃迁21. 1 分(1680)乙炔分子振动自由度是 ( )(1) 5 (2) 6 (3) 7 (4) 822. 1 分(1681)甲烷分子振动自由度是 ( )(1) 5 (2) 6 (3) 9 (4) 1023. 1 分(1682)Cl2分子基本振动数目为 ( )(1) 0 (2) 1 (3) 2 (4) 324. 2 分(1683)Cl2分子在红外光谱图上基频吸收峰的数目为 ( )(1) 0 (2) 1 (3) 2 (4) 325. 2 分(1684)红外光谱法试样可以是 ( )(1) 水溶液 (2) 含游离水 (3) 含结晶水 (4) 不含水26. 2 分(1685)能与气相色谱仪联用的红外光谱仪为 ( )(1) 色散型红外分光光度计 (2) 双光束红外分光光度计(3) 傅里叶变换红外分光光度计 (4) 快扫描红外分光光度计27. 2 分(1686)下列化合物在红外光谱图上1675~1500cm-1处有吸收峰的是 ( )28. 2 分(1687)某化合物的红外光谱在3500~3100cm-1处有吸收谱带, 该化合物可能是 ( ) (1) CH3CH2CN(4) CH3CO-N(CH3)229. 2 分(1688)试比较同一周期内下列情况的伸缩振动(不考虑费米共振与生成氢键)产生的红外吸收峰, 频率最小的是 ( )(1) C-H (2) N-H (3) O-H (4) F-H30. 2 分(1689)已知下列单键伸缩振动中C-C C-N C-O键力常数k/(N·cm-1) 4.5 5.8 5.0吸收峰波长λ/μm 6 6.46 6.85问C-C, C-N, C-O键振动能级之差⊿E顺序为 ( )(1) C-C > C-N > C-O (2) C-N > C-O > C-C(3) C-C > C-O > C-N (4) C-O > C-N > C-C31. 2 分(1690)下列化合物中, C=O伸缩振动频率最高者为 ( )32. 2 分(1691)下列化合物中, 在稀溶液里, C=O伸缩振动频率最低者为 ( )33. 2 分(1692)羰基化合物中, C=O伸缩振动频率最高者为 ( )34. 2 分(1693)1693下列的几种醛中, C=O伸缩振动频率哪一个最低? ( )(1) RCHO(2) R-CH=CH-CHO(3) R-CH=CH-CH=CH-CHO35. 2 分(1694)丁二烯分子中C=C键伸缩振动如下:A. ←→←→CH2=CH-CH=CH2B. ←→→←CH2=CH-CH=CH2有红外活性的振动为 ( )(1) A (2) B (3) A, B都有 (4) A, B都没有36. 2 分(1695)下列有环外双键的烯烃中, C=C伸缩振动频率最高的是哪个? ( )37. 2 分(1696)一个含氧化合物的红外光谱图在3600~3200cm-1有吸收峰, 下列化合物最可能的是 ( )(1) CH3-CHO (2) CH3-CO-CH3(3) CH3-CHOH-CH3 (4) CH3-O-CH2-CH338. 2 分(1697)某化合物的红外光谱在3040-3010cm-1和1670-1620cm-1处有吸收带, 该化合物可能是 ( )39. 2 分(1698)红外光谱法, 试样状态可以是 ( )(1) 气体状态 (2) 固体状态(3) 固体, 液体状态 (4) 气体, 液体, 固体状态都可以40. 2 分(1699)用红外吸收光谱法测定有机物结构时, 试样应该是 ( )(1) 单质 (2) 纯物质(3) 混合物 (4) 任何试样41. 2 分(1700)试比较同一周期内下列情况的伸缩振动(不考虑费米共振与生成氢键)产生的红外吸收峰强度最大的是 ( )(1) C-H (2) N-H (3) O-H (4) F-H42. 2 分(1701)一个有机化合物的红外光谱图上在3000cm-1附近只有2930cm-1和2702cm-1处各有一个吸收峰, 可能的有机化合物是 ( )(2) CH3─CHO(4) CH2= CH-CHO43. 2 分(1702)羰基化合物中, C=O伸缩振动频率最低者是 ( )(1) CH3COCH344. 2 分(1703)色散型红外分光光度计检测器多用 ( )(1) 电子倍增器 (2) 光电倍增管(3) 高真空热电偶 (4) 无线电线圈45. 2 分(1704)红外光谱仪光源使用 ( )(1) 空心阴级灯 (2) 能斯特灯(3) 氘灯 (4) 碘钨灯46. 2 分(1705)某物质能吸收红外光波, 产生红外吸收谱图, 其分子结构必然是 ( )(1) 具有不饱和键 (2) 具有共轭体系(3) 发生偶极矩的净变化 (4) 具有对称性47. 3 分(1714)下列化合物的红外谱中σ(C=O)从低波数到高波数的顺序应为 ( )(1) a b c d (2) d a b c (3) a d b c (4) c b a d48. 1 分(1715)对于含n个原子的非线性分子, 其红外谱 ( )(1) 有3n-6个基频峰 (2) 有3n-6个吸收峰(3) 有少于或等于3n-6个基频峰 (4) 有少于或等于3n-6个吸收峰49. 2 分(1725)下列关于分子振动的红外活性的叙述中正确的是 ( )(1)凡极性分子的各种振动都是红外活性的, 非极性分子的各种振动都不是红外活性的(2) 极性键的伸缩和变形振动都是红外活性的(3) 分子的偶极矩在振动时周期地变化, 即为红外活性振动(4) 分子的偶极矩的大小在振动时周期地变化, 必为红外活性振动, 反之则不是50. 2 分(1790)某一化合物以水或乙醇作溶剂, 在UV光区204nm处有一弱吸收带, 在红外光谱的官能团区有如下吸收峰:3300~2500cm-1(宽而强); 1710cm-1, 则该化合物可能是 ( )(1) 醛 (2) 酮 (3) 羧酸 (4) 酯51. 3 分(1791)某一化合物以水作溶剂, 在UV光区214nm处有一弱吸收带, 在红外光谱的官能团区有如下吸收峰:3540~3480cm-1和3420~3380cm-1双峰;1690cm-1强吸收。

红外吸收光谱作业(IR)一、判断题1.红外光谱不仅包括振动能级的跃迁,也包括转动能级的跃迁,故又称为振转光谱。
(√)2.由于振动能级受分子中其他振动的影响,因此红外光谱中出现振动偶合谱带。
(√)3.确定某一化合物骨架结构的合理方法是红外光谱分析法。
(×)4.对称分子结构,如H2O分子,没有红外活性。
(×)5.分子中必须具有红外活性振动是分子产生红外吸收的必备条件之一。
(√)6.红外光谱中,不同化合物中相同基团的特征频率总是在特定波长范围内出现,故可以根据红外光谱中的特征频率峰来确定化合物中该基团的存在。
(√)7.不考虑其他因素的影响,下列羰基化合物的大小顺序为:酰卤>酰胺>酸>醛>酯。
(×)8.傅里叶变换型红外光谱仪与色散型红外光谱仪的主要差别在于它有干涉仪和计算机部件。
(√)9.当分子受到红外光激发,其振动能级发生跃迁时,化学键越强吸收的光子数目越多。
(√)10.游离有机酸C=O伸缩振动v C=O频率一般出现在1760cm-1,但形成多聚体时,吸收频率会向高波数移动。
(×)二、选择题1.化学键的力常数越大,原子的折合质量越小,则化学键的振动频率(B)A.越低;B.越高;C.不变2.在红外吸收光谱中,乙烯分子的C-H非对称伸缩振动具有(A)A.红外活性;B.非红外活性;C.视实验条件3.在醇类化合物中,O-H伸缩振动随溶液浓度的增大向低波数移动的原因是(C)A.诱导效应;B.溶液极性增大;C.形成分子间氢键;D.振动耦合4.分子的C-H对称伸缩振动的红外吸收带频率比弯曲振动的(A)A.高;B.低;C.相当5.在红外吸收光谱中,C=O和C=C基,两者的吸收强度的大小关系是(B)A.前者<后者;B.前者>后者.C.两者相等6.用于测量红外辐射的检测器是(D)。
A.光电池;B.光电管;C.热导池;D.热电偶7.应用红外光谱解析分子结构的主要参数是(B)A.质荷比;B.波数;C.偶合常数;D.保留值。


仪器分析课后习题答案第二章光学分析法导论(书后习题参考答案)1. 已知1电子伏特=1. 602×10-19J ,试计算下列辐射波长的频率(以兆赫为单位),波数(以cm -1为单位)及每个光子的能量(以电子伏特为单位):(1)波长为900pm 的单色X 射线;(2)589.0nm 的钠D 线;(3)12.6μm 的红外吸收峰;(4)波长为200cm 的微波辐射。
解:已知1eV=1.602×10-19J, h =6.626×10-34J·s, c =3.0×108m·s -1 ①λ=900pm 的X 射线1712810333.310900100.3?=??==-λcv Hz ,即3.333×1011MHz 71010111.11090011?=?==-λσcm -11617341008.210333.310626.6--?===hv E J用eV 表示,则319161910378.110602.11008.210602.1?=??=?=---hv E eV②589.0nm 的钠D 线149810093.5100.589100.3?=??==-λcv Hz ,即5.093×108MHz 4710698.1100.58911?=?==-λσcm -119143410375.310093.510626.6--?===hv E J用eV 表示,则107.210602.11075.310602.1191919=??=?=---hv E eV③12.6μm 的红外吸收峰136810381.2106.12100.3?=??==-λcv Hz ,即2.381×107MHz 2410937.7106.1211?=?==-λσcm -120133410578.110381.210626.6--?===hv E J用eV 表示,则219201910850.910602.110578.110602.1----?=??=?=hv E eV④波长为200cm 的微波辐射8281050.110200100.3?=??==-λcv Hz ,即1.50×102MHz 31000.520011-?===λσcm -12683410939.91050.110626.6--?===hv E J用eV 表示,则719261910204.610602.110939.910602.1----?=??=?=hv E eV2. 一个体系包含三个能级,如果这三个能级的统计权重相同,体系在300K温度下达到平衡时,试计算在各能级上的相对分布(N i /N ).能级的相对能量如下。

光谱概论习题一、单项选择题1.下列表达式表述关系正确的是()。
A.B.C.D.2.下述哪种性质可以说明电磁辐射的微粒性()。
A.波长B.频率C.波数D.能量3.光量子的能量正比于辐射的()A.频率和波长B.波长和波数C.频率和波数D.频率、波长和波数4.下面四个电磁波谱区中波长最短的是()A.X射线B.红外光区C.紫外和可见光区D.无线电波5.下列四种电磁辐射中能量最小的是()。
A.微波B.X射线C.无线电波D.g 射线二、简答题1.简述下列术语的含义:(1)电磁波谱(2)发射光谱(3)吸收光谱(4)荧光光谱2.请按照波长和能量递减的顺序排列下列常见的电磁辐射区:紫外光、红外光、可见光、X射线、无线电波。
3.常见的光学分析法有哪些类型?光谱概论习题答案A 2.D 3.C 4.A 5.C紫外-可见分光光度法习题一、单项选择题1.分子的紫外-可见吸收光谱呈带状光谱,其原因是()A.分子中价电子运动的离域性质B.分子中价电子能级的相互作用C.分子振动能级的跃迁伴随着转动能级的跃迁D.分子中电子能级的跃迁伴随着振动、转动能级的跃迁2.在紫外-可见分光光度分析中,极性溶剂会使被测物的吸收峰()A.消失B.精细结构更明显C.位移D.分裂3.在紫外-可见分光光度法中,某有色物质在某浓度下测得其透光率为T;若浓度增大1倍,则透光率为()A.T/2 B.T2 C.T1/2 D.2T4.用分光光度计测量有色化合物的浓度,相对标准偏差最小时的吸光度为()A.0.334 B.0.343 C.0.434 D.0.4435.下列表达正确的是()A.吸收光谱曲线表明吸光物质的吸光度随波长的变化而变化B.吸收光谱曲线以波长为纵坐标、吸光度为横坐标C.吸收光谱曲线中,最大吸收处的波长不一定为最大吸收波长D.吸收光谱曲线不能表明吸光物质的光吸收特性6.在紫外分光光度法中,参比溶液的选择原则是().通常选用蒸馏水A.B.根据加入试剂和被测试液的颜色、性质来选择C.通常选用试剂溶液D.通常选用褪色溶液7.下列四种化合物中,在紫外区出现两个吸收带的是()A.乙醛B.乙烯C.1, 5-己二烯D.2-丁烯醛8.助色团能使谱带()A.波长变短B.波长变长C.波长不变D.蓝移9.不能用作紫外-可见分光光度法的定性参数是()A.吸光度B.最大吸收波长C.吸收光谱的形状D.吸收峰的数目10.以下四种化合物,能同时产生B吸收带、K吸收带和R吸收带的是()A.B.C.D.11.紫外可见分光光度法测定中,使用参比溶液的作用是()A. 消除试剂等非测定物质的影响B. 吸收入射光中测定所需要的光波C. 调节入射光的光强度D. 调节仪器透光率的零点12. 扫描K2Cr2O7硫酸溶液的紫外-可见吸收光谱时,一般选作参比溶液的是()A. 蒸馏水B. H2SO4溶液C. K2Cr2O7的水溶液D. K2Cr2O7的硫酸溶液13.在比色法中,显色反应的显色剂选择原则错误的是()A. 显色反应产物的e值愈大愈好B. 显色剂的e值愈大愈好C. 显色剂的e值愈小愈好D. 显色反应产物和显色剂,在同一光波下的e值相差愈大愈好14.某分析工作者,在光度法测定前用参比溶液调节仪器时,只调至透光率为95.0%,测得某有色溶液的透光率为35.2%,此时溶液的真正透光率为()A. 40.2%B. 37.1%C. 35.1%D. 30.2%15. 下列化合物中,不适合作为紫外分光光度法测定用的溶剂是()A.水B.苯C.乙腈D.甲醇二、简答题1.电子跃迁的类型有哪几种?2.具有何种结构的化合物能产生紫外吸收光谱?3.为什么邻二氮杂菲分光光度法测定微量铁时要加入盐酸羟胺溶液?4.在没有干扰的条件下,紫外分光光度法为什么总是选择在λmax处进行吸光度的测量?5.举例说明紫外分光光度法如何检查物质纯度。

紫外-可见分光光度和红外光谱法习题及参考答案一、 填空题1、分子内部的运动方式有三种,即: 、和 ,相应于这三种不同的运动形式,分子具有 能级、 能级和能级。
2、折射率是指光线在 速度与在 速度的比值。
当温度、光波波长固定后,有机化合物折射率主要决定于物质的和 。
通过折射率可以测定出、 以及 等。
3、饱和碳氢化合物分子中只有 键,只在 产生吸收,在200-1000nm范围内不产生吸收峰,故此类化合物在紫外吸收光谱中常用来做 。
4、在中红外光区中,一般把4000-1350cm-1区域叫做 ,而把1350-650区域叫做 。
5、在有机化合物中,常常因取代基的变更或溶剂的改变,使其吸收带的最大吸收波长发生移动,向长波方向移动称为___________,向短波方向移动称为___________。
6、在朗伯—比尔定律I/I o= 10-abc中, I o是入射光的强度, I是透射光的强度, a是吸光系数, b是光通过透明物的距离,即吸收池的厚度, c是被测物的浓度,则透射比T =_________,百分透过率T% =______,吸光度A与透射比T的关系为__________________。
7、在单色器的线色散率为0.5mm/nm的条件下用原子吸收分析法测定铁时,要求通带宽度为0.1nm,狭缝宽度要调到 。
8、紫外吸收光谱分析可用来进行在紫外区范围有吸收峰的物质的________及________分析。
9、在紫外光谱中,随溶剂极性增加,R带_____移,K带_______移10、某单色器的线色散率为0.5mm/nm,当出射狭缝宽度为0.1mm时,则单色仪的光谱通带宽度为 。
11、对于紫外及可见分光光度计,在可见光区可以用玻璃吸收池,而紫外光区则用________吸收池进行测量。
12、、红外光谱是由于分子振动能级的跃迁而产生,当用红外光照射分子时,要使分子产生红外吸收,则要满足两个条件:(1)________________________________________________,(2)_______________________________________________。

红外分光光度法(通则0402)培训试题及答案2018 62018.6姓名:成绩:一、单选题(每题4分,共20分)1、FTIR检测时的环境条件是:。
(A)A、环境温度:15〜30℃,相对湿度:乏70%B、环境温度:10〜30℃,相对湿度:乏70%C、环境温度:15〜40℃,相对湿度:乏70%D、环境温度:15〜30℃,相对湿度:乏75%2、红外分光光度法属于:。
(B)A、原子光谱法B、分子光谱法C、电子光谱法D、离子光谱法3、在FTIR性能验证的波数示值误差中:。
(C)A、在3027cm-1, 2851cm-1处的波数示值误差为±1cm-1B、在3027cm-1, 2851cm-1处的波数示值误差为±2cm-1C、在3027cm-1, 2851cm-1处的波数示值误差为±5cm-1D、在3027cm-1, 2851cm-1处的波数示值误差为±6cm-14、固体样品制备方法不包括:。
(A)A、液体池法B、压片法C、糊法D、溶液法5、在FTIR性能验证的100%线的平直度中:。
(C)A、在3200〜2800cm-1内100%线的平直度不大于5%B、在3200〜2800cm-1内100%线的平直度不大于4%C、在3200〜2800cm-1内100%线的平直度不大于1%D、在3200〜2800cm-1内100%线的平直度不大于3%二、多选题(每题4分,共20分)1、FTIR的结构组成包括:。
(ABCD)A、光源、单色器B、样品室C、检测器D、计算机系统2、红外光谱仪的检测器主要分为:。
(BC)A、荧光检测器B、热检测器C、量子检测器D、二极管阵列检测器3、FTIR红外分光光度计具有如下优点:。
(ABCD)A、分辨率高、波数精度高B、灵敏度高C、光谱范围宽D、扫描速度快4、在使用红外光谱法进行定量分析时,为减小误差,分析峰的选择应遵循下列原则:。
(ABD)A、各组分的分析峰应不受其他组分吸收峰的干扰B、峰形尖锐,背景吸收平坦C、透光率为100%时线性好D、强度中等,通常透光率为30%〜70%时线性比较好5、红外光区分为:。

红外吸收光谱法一.填空题1.一般将多原子分子的振动类型分为伸缩振动和变形振动,前者又可分为对称伸缩振动和反对称伸缩振动,后者可分为面内剪式振动(δ)、面内摇摆振动(ρ) 和面外摇摆振动(ω)、面外扭曲振动(τ) . 2.红外光区在可见光区和微波光区之间,习惯上又将其分为三个区:远红外区,中红外区和近红外区,其中中红外区的应用最广。
3.红外光谱法主要研究振动中有偶极矩变化的化合物,因此,除了单原子和同核分子等外,几乎所有的化合物在红外光区均有吸收。
4.在红外光谱中,将基团在振动过程中有偶极矩变化的称为红外活性,相反则称为红外非活性的。
一般来说,前者在红外光谱图上出现吸收峰。
5.红外分光光度计的光源主要有能斯特灯和硅碳棒 .6.基团一OH、一NH;==CH的一CH的伸缩振动频率范围分别出现在3750—3000 cm-1, 3300—3000 cm—1,3000—2700 cm—1。
7.基团一C≡C、一C≡N ;—C==O;一C=N, 一C=C—的伸缩振动频率范围分别出现在2400—2100 cm-1,1900-1650 cm-1, 1650—1500 cm—1.8.4000-1300 cm—1 区域的峰是由伸缩振动产生的,基团的特征吸收一般位于此范围,它是鉴最有价值的区域,称为官能团区;1300—600 cm-1 区域中,当分子结构稍有不同时,该区的吸收就有细微的不同,犹如人的指纹一样,故称为指纹区。
二、选择题1.二氧化碳分子的平动、转动和振动自由度的数目分别(A)A。
3,2,4 B. 2,3,4 C。
3,4,2 D。
4,2,32.乙炔分子的平动、转动和振动自由度的数目分别为(C)A。
2,3,3 B. 3,2,8 C。
3,2,7 D. 2,3,74.下列数据中,哪一组数据所涉及的红外光谱区能够包括CH3CH2COH的吸收带?(D)A。
3000—2700cm—1,1675-1500cm—1,1475—1300cm一1。

红外吸光度习题及答案思考与练习一一、选择题1.并不是所有的分子振动形式其相应的红外谱带都能被观察到,这是因为( )A.分子既有振动运动,又有转动运动,太复杂B.分子中有些振动能量是简并的C.因为分子中有C、H、O 以外的原子存在D.分子某些振动能量相互抵消了2.水分子有几个红外谱带,波数最高的谱带对应于何种振动( )A.2个,不对称伸缩B.4个,弯曲C.3个,不对称伸缩D.2个,对称伸缩3.红外吸收光谱的产生是由于( )A.分子外层电子、振动、转动能级的跃迁B.原子外层电子、振动、转动能级的跃迁C.分子振动-转动能级的跃迁D.分子外层电子的能级跃迁4.一个含氧化合物的红外光谱图在3600~3200cm-1有吸收峰, 下列化合物最可能的是( )A.CH3-CHOB.CH3-CO-CH3C.CH3-CHOH-CH3D.CH3-O-CH2-CH35.在红外光谱分析中,用KBr制作为试样池,这是因为KBr晶体在4000~400 cm-1 范围内:( )A.不会散射红外光B.对红外无反射C.无红外光吸收D.有良好的红外光吸收特性6.下列关于分子振动的红外活性的叙述中正确的是( )A.分子的偶极矩在振动时周期地变化, 即为红外活性振动B.分子的偶极矩的大小在振动时周期地变化, 必为红外活性振动, 反之则不是C.极性键的伸缩和变形振动都是红外活性的D.凡极性分子的各种振动都是红外活性的, 非极性分子的各种振动都不是红外活性的7. 以下四种气体不吸收红外光的是 ( )A.H2OB.CO2C.HClD.N28. 红外光谱法, 试样状态可以是 ( )A.气体状态B.固体状态C.固体, 液体状态D.气体, 液体, 固体状态都可以二、填空题1. 一般的红外吸收光谱主要指,波数在之间。
2. 区域的峰是由伸缩振动产生的吸收带。
由于基团的特征吸收峰一般位于高频范围,并且在该区域内,吸收峰比较,因此,它是基团鉴定工作最有价值的区域,称为。
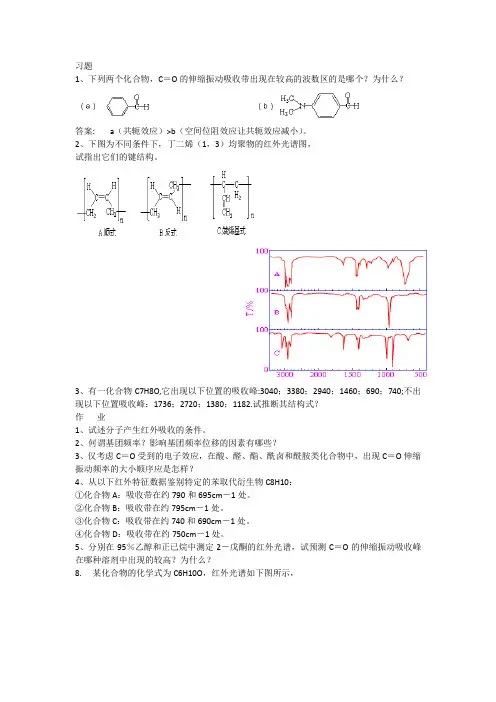
习题1、下列两个化合物,C=O的伸缩振动吸收带出现在较高的波数区的是哪个?为什么?答案: a(共轭效应)>b(空间位阻效应让共轭效应减小)。
2、下图为不同条件下,丁二烯(1,3)均聚物的红外光谱图,试指出它们的键结构。
3、有一化合物C7H8O,它出现以下位置的吸收峰:3040;3380;2940;1460;690;740;不出现以下位置吸收峰:1736;2720;1380;1182.试推断其结构式?作业1、试述分子产生红外吸收的条件。
2、何谓基团频率?影响基团频率位移的因素有哪些?3、仅考虑C=O受到的电子效应,在酸、醛、酯、酰卤和酰胺类化合物中,出现C=O伸缩振动频率的大小顺序应是怎样?4、从以下红外特征数据鉴别特定的苯取代衍生物C8H10:①化合物A:吸收带在约790和695cm-1处。
②化合物B:吸收带在约795cm-1处。
③化合物C:吸收带在约740和690cm-1处。
④化合物D:吸收带在约750cm-1处。
5、分别在95%乙醇和正已烷中测定2-戊酮的红外光谱,试预测C=O的伸缩振动吸收峰在哪种溶剂中出现的较高?为什么?8. 某化合物的化学式为C6H10O,红外光谱如下图所示,试推断其结构式。
答案: μ=1+6-5=2说明可能是不饱和烃3000以上无小尖峰,说明双键不在端碳上1680-羰基1715连接双键导致共轭移到低波位1618-碳碳双键1461-CH-1380、1360-分裂说明异丙基存在1215、1175-双峰强度相仿验证双甲基在端碳816-三取代呈链状。
9. 某化合物的化学式为C8H14O3,红外光谱如下图所示,试推断其结构式。
答案: μ=1+8-7=23000以上无小尖峰,1370峰没分裂,说明没有cc双键1810、1740-羰基分裂成双峰说明有两个羰基,并且直接连接只有基团数少于2(两个不饱和度已满,其他为饱和键)-1465-CH21370-甲基1040-与1740验证呈酸酐,共轭使峰位降低,755以下没有峰-说明连接-(CH)-个数少于42。
第三章紫外可见吸收光谱法一、选择题1、人眼能感觉到的可见光的波长范围是()。
A、400nm~760nmB、200nm~400nmC、200nm~600nmD、360nm~800nm2、在分光光度法中,透射光强度(I)与入射光强度(I0)之比I/I0称为( )。
A、吸光度B、吸光系数C、透光度D、百分透光度3、符合朗伯-比尔定律的有色溶液在被适当稀释时,其最大吸收峰的波长位置( )。
A、向长波方向移动B、向短波方向移动C、不移动D、移动方向不确定4、对于符合朗伯-比尔定律的有色溶液,其浓度为c0时的透光度为T0;如果其浓度增大1倍,则此溶液透光度的对数为( )。
A、T0/2B、2T0C、2lgT0D、0.5lgT05、在光度分析中,某有色物质在某浓度下测得其透光度为T;若浓度增大1倍,则透光度为( )。
A、T2B、T/2C、2TD、T1/26、某物质的摩尔吸光系数很大,则表明( )。
A、该物质溶液的浓度很大B、光通过该物质溶液的光程长C、该物质对某波长的光的吸收能力很强D、用紫外-可见光分光光度法测定该物质时其检出下限很低7、在用分光光度法测定某有色物质的浓度时,下列操作中错误的是( )。
A、比色皿外壁有水珠B、待测溶液注到比色皿的2/3高度处C、光度计没有调零D、将比色皿透光面置于光路中8、下列说法正确的是( )。
A、透光率与浓度成正比B、吸光度与浓度成正比C、摩尔吸光系数随波长而改变D、玻璃棱镜适用于紫外光区9、在分光光度分析中,常出现工作曲线不过原点的情况。
与这一现象无关的情况有( )。
A、试液和参比溶液所用吸收池不匹配B、参比溶液选择不当C、显色反应的灵敏度太低D、被测物质摩尔吸光系数太大10、质量相等的A、B两物质,其摩尔质量M A>M B。
经相同方式发色后,在某一波长下测得其吸光度相等,则在该波长下它们的摩尔吸光系数的关系是( )。
A、εA>εBB、εA<εBC、εA=εBD、2εA>εB11、影响吸光物质摩尔吸光系数的因素是( )。
六、红外吸收光谱法(193题)一、选择题( 共61题)1. 2 分(1009)在红外光谱分析中,用 KBr制作为试样池,这是因为: ( )(1) KBr 晶体在 4000~400cm-1范围内不会散射红外光(2) KBr 在 4000~400 cm-1范围内有良好的红外光吸收特性(3) KBr 在 4000~400 cm-1范围内无红外光吸收(4) 在 4000~400 cm-1范围内,KBr 对红外无反射2. 2 分(1022)下面给出的是某物质的红外光谱(如图),已知可能为结构Ⅰ、Ⅱ或Ⅲ,试问哪一结构与光谱是一致的?为什么? ( )3. 2 分(1023)下面给出某物质的部分红外光谱(如图),已知结构Ⅰ、Ⅱ或Ⅲ,试问哪一结构与光谱是一致的,为什么?4. 2 分(1068)一化合物出现下面的红外吸收谱图,可能具有结构Ⅰ、Ⅱ、Ⅲ或Ⅳ,哪一结构与光谱最近于一致?5. 2 分(1072)1072羰基化合物中,C = O 伸缩振动频率出现最低者为 ( )(1) I (2) II (3) III (4) IV6. 2 分(1075)一种能作为色散型红外光谱仪色散元件的材料为 ( )(1) 玻璃 (2) 石英 (3) 卤化物晶体 (4) 有机玻璃7. 2 分(1088)并不是所有的分子振动形式其相应的红外谱带都能被观察到,这是因为 ( )(1) 分子既有振动运动,又有转动运动,太复杂(2) 分子中有些振动能量是简并的(3) 因为分子中有 C、H、O 以外的原子存在(4) 分子某些振动能量相互抵消了8. 2 分(1097)下列四组数据中,哪一组数据所涉及的红外光谱区能够包括CH3- CH2-CH = O的吸收带( )9. 2 分(1104)请回答下列化合物中哪个吸收峰的频率最高? ( )10. 2 分(1114)在下列不同溶剂中,测定羧酸的红外光谱时,C=O 伸缩振动频率出现最高者为( )(1) 气体 (2) 正构烷烃 (3) 乙醚 (4) 乙醇11. 2 分(1179)水分子有几个红外谱带,波数最高的谱带对应于何种振动 ? ( )(1) 2 个,不对称伸缩 (2) 4 个,弯曲(3) 3 个,不对称伸缩 (4) 2 个,对称伸缩12. 2 分(1180)CO2的如下振动中,何种属于非红外活性振动 ? ( )(1) ←→ (2) →←→ (3)↑↑ (4 )O=C=O O = C =O O = C =O O = C = O↓13. 2 分(1181)苯分子的振动自由度为 ( )(1) 18 (2) 12 (3) 30 (4) 3114. 2 分(1182)双原子分子在如下转动情况下 (如图),转动不形成转动自由度的是 ( )15. 2 分(1183)任何两个振动能级间的能量差为 ( )(1) 1/2 h (2) 3/2 h (3) h (4) 2/3 h16. 2 分(1184)在以下三种分子式中 C=C 双键的红外吸收哪一种最强? ( )(a) CH3- CH = CH2(b) CH3- CH = CH - CH3(顺式)(c) CH3- CH = CH - CH3(反式)(1) a 最强 (2) b 最强 (3) c 最强 (4) 强度相同17. 2 分(1206)在含羰基的分子中,增加羰基的极性会使分子中该键的红外吸收带 ( )(1) 向高波数方向移动 (2) 向低波数方向移动(3) 不移动 (4) 稍有振动18. 2 分(1234)以下四种气体不吸收红外光的是 ( )(1)H2O (2)CO2 (3)HCl (4)N219. 2 分(1678)某化合物的相对分子质量M r=72,红外光谱指出,该化合物含羰基,则该化合物可能的分子式为 ( )(1) C4H8O (2) C3H4O2 (3) C3H6NO (4) (1)或(2)20. 2 分(1679)红外吸收光谱的产生是由于 ( )(1) 分子外层电子、振动、转动能级的跃迁(2) 原子外层电子、振动、转动能级的跃迁(3) 分子振动-转动能级的跃迁(4) 分子外层电子的能级跃迁21. 1 分(1680)乙炔分子振动自由度是 ( )(1) 5 (2) 6 (3) 7 (4) 822. 1 分(1681)甲烷分子振动自由度是 ( )(1) 5 (2) 6 (3) 9 (4) 1023. 1 分(1682)Cl2分子基本振动数目为 ( )(1) 0 (2) 1 (3) 2 (4) 324. 2 分(1683)Cl2分子在红外光谱图上基频吸收峰的数目为 ( )(1) 0 (2) 1 (3) 2 (4) 325. 2 分(1684)红外光谱法试样可以是 ( )(1) 水溶液 (2) 含游离水 (3) 含结晶水 (4) 不含水26. 2 分(1685)能与气相色谱仪联用的红外光谱仪为 ( )(1) 色散型红外分光光度计 (2) 双光束红外分光光度计(3) 傅里叶变换红外分光光度计 (4) 快扫描红外分光光度计27. 2 分(1686)下列化合物在红外光谱图上1675~1500cm-1处有吸收峰的是 ( )28. 2 分(1687)某化合物的红外光谱在3500~3100cm-1处有吸收谱带, 该化合物可能是 ( ) (1) CH3CH2CN(4) CH3CO-N(CH3)229. 2 分(1688)试比较同一周期内下列情况的伸缩振动(不考虑费米共振与生成氢键)产生的红外吸收峰, 频率最小的是 ( )(1) C-H (2) N-H (3) O-H (4) F-H30. 2 分(1689)已知下列单键伸缩振动中C-C C-N C-O键力常数k/(N·cm-1) 4.5 5.8 5.0吸收峰波长λ/μm 6 6.46 6.85问C-C, C-N, C-O键振动能级之差⊿E顺序为 ( )(1) C-C > C-N > C-O (2) C-N > C-O > C-C(3) C-C > C-O > C-N (4) C-O > C-N > C-C31. 2 分(1690)下列化合物中, C=O伸缩振动频率最高者为 ( )32. 2 分(1691)下列化合物中, 在稀溶液里, C=O伸缩振动频率最低者为 ( )33. 2 分(1692)羰基化合物中, C=O伸缩振动频率最高者为 ( )34. 2 分(1693)1693下列的几种醛中, C=O伸缩振动频率哪一个最低? ( )(1) RCHO(2) R-CH=CH-CHO(3) R-CH=CH-CH=CH-CHO35. 2 分(1694)丁二烯分子中C=C键伸缩振动如下:A. ←→←→CH2=CH-CH=CH2B. ←→→←CH2=CH-CH=CH2有红外活性的振动为 ( )(1) A (2) B (3) A, B都有 (4) A, B都没有36. 2 分(1695)下列有环外双键的烯烃中, C=C伸缩振动频率最高的是哪个? ( )37. 2 分(1696)一个含氧化合物的红外光谱图在3600~3200cm-1有吸收峰, 下列化合物最可能的是 ( )(1) CH3-CHO (2) CH3-CO-CH3(3) CH3-CHOH-CH3 (4) CH3-O-CH2-CH338. 2 分(1697)某化合物的红外光谱在3040-3010cm-1和1670-1620cm-1处有吸收带, 该化合物可能是 ( )39. 2 分(1698)红外光谱法, 试样状态可以是 ( )(1) 气体状态 (2) 固体状态(3) 固体, 液体状态 (4) 气体, 液体, 固体状态都可以40. 2 分(1699)用红外吸收光谱法测定有机物结构时, 试样应该是 ( )(1) 单质 (2) 纯物质(3) 混合物 (4) 任何试样41. 2 分(1700)试比较同一周期内下列情况的伸缩振动(不考虑费米共振与生成氢键)产生的红外吸收峰强度最大的是 ( )(1) C-H (2) N-H (3) O-H (4) F-H42. 2 分(1701)一个有机化合物的红外光谱图上在3000cm-1附近只有2930cm-1和2702cm-1处各有一个吸收峰, 可能的有机化合物是 ( )(2) CH3─CHO(4) CH2= CH-CHO43. 2 分(1702)羰基化合物中, C=O伸缩振动频率最低者是 ( )(1) CH3COCH344. 2 分(1703)色散型红外分光光度计检测器多用 ( )(1) 电子倍增器 (2) 光电倍增管(3) 高真空热电偶 (4) 无线电线圈45. 2 分(1704)红外光谱仪光源使用 ( )(1) 空心阴级灯 (2) 能斯特灯(3) 氘灯 (4) 碘钨灯46. 2 分(1705)某物质能吸收红外光波, 产生红外吸收谱图, 其分子结构必然是 ( )(1) 具有不饱和键 (2) 具有共轭体系(3) 发生偶极矩的净变化 (4) 具有对称性47. 3 分(1714)下列化合物的红外谱中σ(C=O)从低波数到高波数的顺序应为 ( )(1) a b c d (2) d a b c (3) a d b c (4) c b a d48. 1 分(1715)对于含n个原子的非线性分子, 其红外谱 ( )(1) 有3n-6个基频峰 (2) 有3n-6个吸收峰(3) 有少于或等于3n-6个基频峰 (4) 有少于或等于3n-6个吸收峰49. 2 分(1725)下列关于分子振动的红外活性的叙述中正确的是 ( )(1)凡极性分子的各种振动都是红外活性的, 非极性分子的各种振动都不是红外活性的(2) 极性键的伸缩和变形振动都是红外活性的(3) 分子的偶极矩在振动时周期地变化, 即为红外活性振动(4) 分子的偶极矩的大小在振动时周期地变化, 必为红外活性振动, 反之则不是50. 2 分(1790)某一化合物以水或乙醇作溶剂, 在UV光区204nm处有一弱吸收带, 在红外光谱的官能团区有如下吸收峰:3300~2500cm-1(宽而强); 1710cm-1, 则该化合物可能是 ( )(1) 醛 (2) 酮 (3) 羧酸 (4) 酯51. 3 分(1791)某一化合物以水作溶剂, 在UV光区214nm处有一弱吸收带, 在红外光谱的官能团区有如下吸收峰:3540~3480cm-1和3420~3380cm-1双峰;1690cm-1强吸收。
红外吸收光谱法一.填空题1.一般将多原子分子的振动类型分为伸缩振动和变形振动,前者又可分为对称伸缩振动和反对称伸缩振动,后者可分为面内剪式振动(δ)、面内摇摆振动(ρ) 和面外摇摆振动(ω)、面外扭曲振动(τ) 。
2.红外光区在可见光区和微波光区之间,习惯上又将其分为三个区: 远红外区,中红外区和近红外区,其中中红外区的应用最广。
3.红外光谱法主要研究振动中有偶极矩变化的化合物,因此,除了单原子和同核分子等外,几乎所有的化合物在红外光区均有吸收。
4.在红外光谱中,将基团在振动过程中有偶极矩变化的称为红外活性,相反则称为红外非活性的。
一般来说,前者在红外光谱图上出现吸收峰。
5.红外分光光度计的光源主要有能斯特灯和硅碳棒。
6.基团一OH、一NH;==CH的一CH的伸缩振动频率范围分别出现在3750—3000 cm-1, 3300—3000 cm-1, 3000—2700 cm-1。
7.基团一C≡C、一C≡N ;—C==O;一C=N,一C=C—的伸缩振动频率范围分别出现在2400—2100 cm-1, 1900—1650 cm-1, 1650—1500 cm-1。
8.4000—1300 cm-1 区域的峰是由伸缩振动产生的,基团的特征吸收一般位于此范围,它是鉴最有价值的区域,称为官能团区;1300—600 cm-1 区域中,当分子结构稍有不同时,该区的吸收就有细微的不同,犹如人的指纹一样,故称为指纹区。
二、选择题1.二氧化碳分子的平动、转动和振动自由度的数目分别(A)A. 3,2,4B. 2,3,4C. 3,4,2D. 4,2,32.乙炔分子的平动、转动和振动自由度的数目分别为(C)A. 2,3,3B. 3,2,8C. 3,2,7D. 2,3,74.下列数据中,哪一组数据所涉及的红外光谱区能够包括CH3CH2COH的吸收带?(D)A. 3000—2700cm-1,1675—1500cm-1,1475—1300cm一1。
第四章光谱分析技术及相关仪器习题参考答案一、名词解释1.激发光谱:将激发光的光源用单色器分光,连续改变激发光波长,固定荧光发射波长,测定不同波长的激发光照射下,物质溶液发射的荧光强度的变化,以激发光波长为横坐标,荧光强度为纵坐标作图,即可得到荧光物质的激发光谱。
从激发光谱图上可找出发生荧光强度最强的激发波长λex。
2.荧光光谱:选择λex作激发光源,并固定强度,而让物质发射的荧光通过单色器分光,测定不同波长的荧光强度。
以荧光波长作横坐标,荧光强度为纵坐标作图,便得荧光光谱。
荧光光谱中荧光强度最强的波长为λem 。
荧光物质的最大激发波长(λex)和最大荧光波长(λem)是鉴定物质的根据,也是定量测定中所选用的最灵敏的波长。
3.光谱分析:对物质发射辐射能的能谱分析或对辐射能与物质相互作用引起的能谱改变的分析均称为光谱分析。
4.吸收光谱:光照射到物质时,一部分光会被物质吸收。
在连续光谱中某些波长的光被物质吸收后产生的光谱被称作吸收光谱。
每一种物质都有其特定的吸收光谱,因此可根据物质的吸收光谱来分析物质的结构和含量。
5.发射光谱:一部分物质分子或原子吸收了外来的能量后,可以发生分子或原子间的能级跃迁,所产生的光谱称为发射光谱,包括线状光谱、带状光谱及连续光谱。
通过测定物质发射光谱可以分析物质的结构和含量。
6.摩尔吸光系数(ε):摩尔吸光系数表示在一定波长下测得的液层厚度为1cm, 溶液浓度c为1mol/L时的稀溶液吸光度值。
吸光系数与入射光波长、溶液温度、溶剂性质及吸收物质的性质等多种因素有关。
当其它因素固定不变时,吸光系数只与吸收物质的性质有关,可作为该物质吸光能力大小的特征数据。
7.分光光度计:能从含有各种波长的混合光中将每一单色光分离出来并测量其强度的仪器称为分光光度计。
它具有分析精密度高、测量范围广、分析速度快和样品用量少等优点。
根据所使用的波长范围不同可分为紫外光区、可见光区、红外光区以及万用(全波段)分光光度计等。
红外分光光度法课后答案1.分子吸收红外光能级跃迁,必须满足什么条件?答:①分子吸收的红外辐射应具有刚好满足分子振动跃迁所需的能量。
②分子振动只有使偶极矩发生变化的振动形式才能吸收红外辐射。
2.何为红外非活性振动?答:分子发生能级跃迁需要产生偶极矩的变化,如果只振动而无偶极矩变化,那么红外光谱上无吸收曲线。
3.乙酰乙酸乙酯存在酮式和烯醇式两种互变异构体,二者的红外光谱有何区别?答:烯醇式红外吸收中的羰基和羟基振动频率因为其内部形成氢键而向短波移动。
4.苯甲酸乙酯和苯乙酸甲酯可否用红外光谱区别?为什么?答:能;①苯乙酸甲酯的乙基因为和苯环的大π键形成p-π共轭,其振动频率向短频方向移动。
②苯甲酸乙酯的羰基因为和苯环形成π-π共轭,其振动频率向短频方向移动。
5.试推测分子式为C9H6O2的化合物结构。
答该红外图谱中有关炔基的振动频率并未标出,但图上可以明显的看见其特征吸收峰。
另在920cm处的吸收峰为苯的芳氢面内伸缩振动引起的。
6.一化合物为无色可燃液体,有果子香味,沸点为77.1,微溶于水,易溶于有机溶剂。
其分子式为C4H8O2,推测其结构式。
答:Ω=2+2x4-8/2=1,故含有双键。
842cm处的吸收属于乙基的面内摇摆振动频率。
9.一白色粉末,有特殊气味,熔点为76.5,稍溶于水,溶于乙醇和乙醚。
质谱分析,确定分子式为C8H8O2.试推测其结构式。
答:Ω=2+2x8-8/2=5,故含有苯环或为芳香化合物。
927cm处为芳氢的面内振动引起的。
1690处的吸收峰为高强吸收峰,无干扰峰,可确认为羧基的羰基基团。
8.某未知物的分子式为C10H12O.推断其结构式。
答:Ω=2+2x10-12/2=5,故含有苯环或为芳香化合物。
1390、1365cm处的两个峰,分裂峰,吸收强度几乎相同,说明含有偕二甲基(异丙基)。
830cm的吸收峰说明苯环上含有对位取代。
2820、2720cm处的特征吸收峰则表示分子结构中含有醛基。
第四章 红外分光光光度法(书后习题参考答案)
1.CO 的红外光谱在2 170cm -1处有一振动吸收峰.问
(1)CO 键的力常数是多少?
(2)14CO 的对应峰应在多少波数处发生吸收? 解:碳原子的质量2323100.210022.612--⨯=⨯=
C m g
氧原子的质量2323106.210022.616--⨯=⨯=O m g (1) σ =2071cm -1
O C O C m m m m k c ⋅+=
)(21πσ 2346
210210)6.22(106.22)217010314.32()2(--⨯+⨯⨯⨯⨯⨯⨯⨯=+=O C O C m m m m c k σπ =18.6×105 dyn·cm -1=18.6N·cm -1(厘米克秒制)
(2)14CO 2323103.210022.614-⨯=⨯=C m g
2071106.23.210)6.23.2(106.1810314.3214623
510≈⨯⨯⨯+⨯⨯⨯⨯⨯⨯=--σcm -1
或O C O C O C O C m m m m m m m m +⋅⨯⋅+=1212141412σσ σ =2080cm -1
2.已知C―H 键的力常数为5N/cm ,试计算C―H 键伸展振动的吸收峰在何波数?若将氘(D )置换H ,C―D 键的振动吸收峰为多少波数.
解:C-H 键:k =5N·cm -1=5.0×105dyn·cm -1
碳原子的质量:m C =2.0×10-23g, 氢原子的质量:23
231017.010022.61--⨯=⨯=
H m g
氘原子的质量: 23231034.010022.62--⨯=⨯=D m g 依2121)(21m m m m k c ⋅+=
πσ得
29961017.00.210)17.00.2(10510314.3214623
510≈⨯⨯⨯+⨯⨯⨯⨯⨯⨯=--σcm -1
21991034.00.210)34.00.2(10510314.3214623
510≈⨯⨯⨯+⨯⨯⨯⨯⨯⨯=--σcm -1
3.指出以下振动在红外光谱中是活性的还是非活性的
分 子 振 动
(1)CH 3一CH 3 C―C 伸缩振动
(2)CH 3一CC13 C―C 伸缩振动
(3)SO 2 对称伸缩振动
(4)CH 2=CH 2 C―H 伸缩振动
C C
H H
(5)CH 2=CH 2 C―H 伸缩振动
C C
H H
(6)CH 2=CH 2 CH 2
摆动 C C
H
H H
(7)CH 2=CH 2 CH 2扭曲振动
C C
H
H H H
解:非红外活性:(1), (5), (7)
红外活性:(2), (4), (6), (8)
4.下面三个图形(图4-20)分别为二甲苯的三种异构体的红外光谱图。
请说明各个图形分别属于何种异构体(邻、间、对位)?并指明图中主要吸收峰的来源。
解:分别为间二甲苯、对二甲苯、邻二甲苯
主要吸收峰来源:苯环骨架振动,1700cm -1~2000cm -1
C-H 面外弯曲振动,650~900cm -1
5.有一种苯的氯化物在900~660cm -1区域没有吸收峰,它的可能结构是什么? 答:C 6Cl 6 (六六六)
6.图4-21是由组成为C 3H 6O 的纯液体获得的红外谱图,试推断这种化合物的结构。
答:丙酮 O
CH 3-C-CH 3
7.下面两个化合物的红外光谱有何不同?
(a )CH 2-NH 2 (b) CH 3--N(CH 3)2O
答:红外光谱不同点:
(a)3300cm -1,N-H 伸缩振动(宽且强),CH 2-伸缩振动峰,
苯环骨架振动峰(1600cm -1附近),一取代指纹峰(770~730, 710~690cm -1)
(b)1680cm -1, C=O 强伸缩振动峰,甲基的伸缩振动峰(2928cm -1)
8.某化合物分子式为C 5H 8O ,有下面的红外吸收带:3 020 ,2 900,1 690和1 620 cm -1;在紫外区,它的吸收峰在227nm 处( =104)。
试提出一个结构,并说明它是否是唯一可能的结构。
答:O
CH 3-C-CH=CH-CH 3,否.
9. 下面两个化合物中哪一个νC=O 吸收带出现在较高频率,为什么?
(a)
CHO (b) CHO -(CH 3)2N 答:(a)化合物的羰基吸收带出现在较高频率.
N 原子提供孤对电子,与苯环、C=O 形成大π键,中介效应.
10. 举例说明分子的基本振动形式。
答:
CO2和H2O的振动模式
11. 试说明产生红外吸收的条件是什么?
答:(1)必要条件:振动或转动时会引起偶极矩净变化的分子.
(2)辐射的频率与分子的固有振动频率相匹配.
12. 试说明什么是基团频率和“指纹区”?各有什么特点和作用?
答:组成分子的各种原子基团都有自己的特征红外吸收的频率范围和吸收峰,称这些能用于鉴定原子基团存在并有较高强度的吸收峰为特征峰,其相应的频率称为特征频率或基团频率。
“指纹区”:在1300 cm-1~600 cm-1(7.7μm~16.7μm)范围的光谱区,分子构型和结构的微小差别,都可引起吸收峰分布的明显改变。
这一区域内的光谱对于分子来说就好像“指纹”对人一样,具有各自独特的特征。
基团频率:有一定的范围,吸收峰较强,用于鉴定原子基团的存在.
指纹区:分子构型和结构的微小差别,会引起吸收峰分布的明显改变,可用于区分化合物的精细结构.
13. 什么是拉曼散射,Stokes线和反Stokes线。
答:一束单色光作用于透明介质时,在透射和反射方向以外出现的光称为散射光。
当散射的粒子为分子大小时,发生与入射光频率相同的瑞利(Rayleigh)散射光,另外在其两侧对称分布有强度较弱的频率不同于入射光的散射光,称之为拉曼(Raman)光。
这种现象称为拉曼散射.其中频率较低的称为斯托克斯(Stokes)线,频率较高的称为反斯托克斯线(anti-Stokes)。
14. 下述分子的振动各具有什么活性(红外、拉曼、或两者均有)
(1)O2的对称伸缩振动;(2)CO2的不对称伸缩振动;
(3)H2O的弯曲振动;(4)C2H4的弯曲振动。
答:红外活性拉曼活性备注
(1)O2的对称伸缩振动非是
(2)CO2的不对称伸缩振动是非
(3)H2O的弯曲振动是是
(4)C2H4的扭曲(或弯曲)振动非非。